草鱼粉中4种磺胺类药物残留基体标准物质的研制
2022-10-06王新新封腾望王慧姣李晋成孙慧武
王新新,封腾望,王慧姣,李晋成,孙慧武,刘 欢
(1.上海海洋大学水产与生命学院,上海 201306;2.中国水产科学研究院,农业农村部水产品质量安全控制重点实验室,北京100141)
磺胺类药物(sulfonamides,SAs)是一类以对位氨基苯磺酰胺为基本结构的衍生物,磺酰胺基上的氢,可被不同杂环取代,形成不同种类的磺胺类药物。磺胺类药物因具有抗菌谱广、化学性质稳定、低毒性等优点被广泛应用于水产养殖业,主要用于预防和治疗细菌感染性疾病。我国发布《食品安全国家标准 食品中兽药最大残留限量》中规定磺胺类药物最大残留限量总量为100 μg/kg。不按规定使用、不遵守养殖使用休药期规定则会导致其在水产品中残留,进而影响人类健康。根据农业农村部、国家市场监管总局等发布的关于水产品监督抽检情况的通告,水产品中磺胺类药物残留共检出19批次残留超标样品,其中,磺胺甲噁唑(Sulfamethoxazole,SMZ)、磺胺二甲异噁唑(Sulfaisoxazole,SFZ)、磺胺二甲基嘧啶(sulfamethazine,SM)、磺胺甲基嘧啶(sulfamerazine,SM)是超标的主要参数。
基体标准物质(matrix reference material,MRM)是具备实际样品特性的标准物质,目标物与基体相结合,并且与待测样品具有相同的特性,在分析过程中可有效避免基质效应对目标物造成的干扰。水产品因基质复杂,在药物残留检测分析中基质效应对检测结果的准确性影响较大。因此,如在检测分析中,使用基体标准物质进行校准及质量控制,将可以有效提高检测的准确度。欧盟明确要求对动物源食品进行兽药残留检测必须采用基体标准物质进行校准及过程质量控制。
目前,我国以水产品为基质的磺胺类药物残留分析所用基体标准物质研究成果有限。颜显辉等曾研制了鲤()肌肉中SMZ残留冻干粉标准样品,尹太坤等以鳗鲡()肌肉为基质研制了包含两种磺胺类药物残留的基体标准物质,但尚未有报道以草鱼()为基质研制的包含SMZ、SFZ、SM、SM4种磺胺类药物残留的基体标准物质。本研究以草鱼为基质,研究建立了草鱼粉中SMZ、SFZ、SM、SM药物残留基体标准物质制备方法,以期为水产品基质中磺胺类药物残留基体标准物质的制备提供技术参考。
1 材料与方法
1.1 材料与试剂
鲜活草鱼购自北京市房山区琉璃河镇赵德旺养鱼场(约1 kg/尾),于北京市房山区中国水产科学研究院鲟鱼繁育技术与工程中心养殖池中暂养备用。
SMZ(Sulfamethoxazole,CAS:723-46-6,纯度≥99.8%)、SFZ(Sulfaisoxazole,CAS:127-69-5,纯度≥99.74%)、SM(sulfamethazine,CAS:57-68-1,纯度≥99.8%)、SM(sulfamerazine,CAS:127-79-7,纯度≥99.72%)标准物质均购于德国Dr.Ehrenstorfer 公司;磺胺邻二甲氧嘧啶(sulfadoxine,CAS:2447-57-6,纯度≥99.8%)、磺胺间二甲氧嘧啶(sulfadimethoxine,CAS:122-11-2,纯度≥99.8%)均购于德国Witega公司;SMZ原料药(上海阿达玛斯试剂有限公司,纯度>98%)、SFZ原料药[梯希爱(上海)化成工业发展有限公司,纯度>98%]、SM原料药(上海阿达玛斯试剂有限公司,纯度>99%)、SM原料药[西格玛奥德里奇(上海)贸易有限公司,纯度>98%];乙腈、甲醇、正己烷(色谱纯,美国J.T.Baker公司);乙酸铵、甲酸(质谱级,美国Fisher公司);无水硫酸镁(上海麦克林生化科技有限公司)。
1.2 仪器与设备
QTRAP®5500超高效液相色谱-三重四级杆/复合线性离子阱质谱仪(美国SCIEX公司);MVM-2500多管涡流混合器(上海泰坦科技股份有限公司);MS3 Basic基本型旋涡混匀器(德国IKA公司);SB-5200DTN超声波清洗机(宁波新芝生物科技股份有限公司);PL2002电子天平[Mettler Toledo仪器(上海)有限公司];H-2050R台式高速离心机(湖南湘仪实验室仪器开发有限公司);Buchi R210旋转蒸发仪(瑞士Buchi公司);冷冻干燥机(德国 ZIRBUS公司);药浴池为圆形,规格为直径150 cm,水深25.5 cm。
1.3 实验方法
1.3.1 溶液配置
(1)标准溶液配制:分别准确称取10.02 mg SMZ、10.03 mg SFZ、10.02 mg SM、10.03 mg SM、10.02 mg磺胺邻二甲氧嘧啶及10.02 mg磺胺间二甲氧嘧啶标准品,用甲醇配制成1.0 mg/mL标准储备液;分别移取适量标准储备液置于棕色容量瓶中,用甲醇逐级稀释成浓度为100.0 μg/mL、10.0 μg/mL的SMZ、SFZ、SM、SM外标混合标准中间液和磺胺邻二甲氧嘧啶、磺胺间二甲氧嘧啶内标混合标准中间液;以甲醇为溶剂,移取适量混合标准中间液,配制成1.0 μg/mL、100.0 ng/mL SMZ、SFZ、SM、SM外标混合标准工作液和1.0 μg/mL磺胺邻二甲氧嘧啶、磺胺间二甲氧嘧啶内标混合标准工作液,-20 ℃保存。
(2)药浴液配制:准确称取0.700 g SMZ于100 mL容量瓶,用乙腈配制成7.0 mg/mL药浴液;准确称取0.750 g SFZ于250 mL容量瓶,用乙腈配制成3.0 mg/mL药浴液,超声30 min;准确称取0.250 g SM于100 mL容量瓶,用乙腈配制成2.5 mg/mL药浴液;准确称取0.375 g SM于250 mL容量瓶,用乙腈配制成1.5 mg/mL药浴液,超声10 min。
(3)酸化乙腈配制:99 mL乙腈中加入1 mL甲酸。
1.3.2 4种磺胺类药物残留分析方法
参照农业部1077号公告-1-2008《水产品中17种磺胺类及15种喹诺酮类药物残留量的测定 液相色谱-质谱法》,并进行优化改进,具体方法如下:
(1)样品前处理方法
准确称取1.0 g草鱼粉样品(±0.01 g)于50 mL离心管中,加入4 mL超纯水使其复原,振摇、充分混匀。准确加入0.05 mL内标混合标准工作液,涡旋混合30 s,依次加入15 mL酸化乙腈、4 g无水硫酸镁,涡旋混匀,超声提取10 min,4 500 r/min离心10 min,取上清液于50 mL梨形瓶中。向残渣中加入15 mL酸化乙腈,重复提取一次,合并两次提取液,于40 ℃水浴条件下旋转蒸发至干。加入1.0 mL 20%甲醇水溶液,涡旋溶解残留物,继续加入3.0 mL正己烷涡旋混合30 s,12 000 r/min离心5 min,取下层清液,过0.22 μm滤膜,供液相色谱-串联质谱仪测定。
(2)标准工作曲线的制作
分别准确吸取SMZ、SFZ、SM、SM的混合标准工作液和0.05 mL磺胺邻二甲氧嘧啶、磺胺间二甲氧嘧啶的内标混合标准工作液,加入阴性草鱼肌肉粉基质中,配制成10、20、50、100、200 μg/L系列混合标准工作曲线,按1.3.2样品前处理步骤进行操作后上机检测。以浓度为横坐标,目标物与内标物峰面积的比值为纵坐标,绘制标准曲线。
(3)液相色谱条件
色谱柱:Hypersil GOLD C18柱(150 mm×2.1 mm,5 μm,赛默飞世尔科技有限公司);柱温:40 ℃;进样量:5 μL;流动相A相为 0.1 %甲酸溶液(含5.0 mmol/L醋酸铵),流动相B相为甲醇;梯度洗脱程序见表1。

表1 梯度洗脱条件Tab.1 Conditions of gradient elution
(4)质谱条件
采用电喷雾离子源(ESI),正离子模式下采用多反应监测(MRM)模式采集数据。离子源的详细参数如下:喷雾电压(IS):5 500 V;离子源温度(TEM):550 ℃;气帘气(CUR):206.85 kPa;雾化气(GS1):310.28 kPa;辅助加热气(GS2):55 379.23 kPa;4种磺胺类化合物MRM质谱参数见表2。

表2 4种化合物的主要质谱参数Tab.2 MS/MS parameters of 4 compounds
1.3.3 药浴时间的确定
药浴实验组池中SMZ、SFZ、SM、SM药浴初始浓度分别为2.72、3.75、1.05、2.49 mg/L,水温(23±2) ℃,选择暂养池中经检测后均无SMZ、SFZ、SM、SM药物残留的健康、活泼草鱼,一次放入37尾,每尾规格在900~1 100 g,连续药浴24 h后全量换水。给药后分别在 0.5、1、2、4、6、8、10、12、14、15、24、28、32、48 h采集样品,每个时间点随机捞出草鱼3尾,取其背部肌肉并混匀,于-20 ℃保存用于测定4种磺胺类药物残留量。
1.3.4 样品的制备
根据优化后的药浴时间对草鱼进行药浴,并制备成鱼糜样品。将样品放置于冷冻干燥机中进行干燥处理;随后对冷冻干燥样品进行粉碎、过120目筛后充分混匀。按照每瓶(5.0±0.1) g分装到带有密封内盖的棕色玻璃瓶中,放入-20 ℃冰箱中保存,以考察样品的均匀性和稳定性。
1.3.5 样品的均匀性检验
根据JJF 1343-2012《标准物质定值的通用原则及统计学原理》,对样品进行均匀性检验。本研究按照编号顺序随机抽取11 个包装单元,每个单元取3个平行样品,采用1.3.2确定的分析方法进行样品测定。检测结果采用单因素方差分析法进行统计分析,通过比较检验值与临界值的大小来判断样品的均匀性。
1.3.6 样品的稳定性检验
根据JJF 1343-2012《标准物质定值的通用原则及统计学原理》,对样品进行长期和短期稳定性检验。样品在-20 ℃储存条件下进行长期稳定性考察,考察的时间间隔为1、2、3、4、6个月;短期稳定性检测模拟样品运输条件和极端条件,考察样品在-40、-20、4、25、50 ℃保存条件下在 0、3、7、11、15 d的短期稳定性。每次随机取3个包装单元,平行测定两次,测量方法与均匀性检验方法相同。取三个包装单元测量结果的平均值作为该次稳定性检测结果,采用检验法评定样品的稳定性,判断样品的长期稳定性与短期稳定性。
1.3.7 样品的定值
采用多个实验室合作定值法对样品进行定值测试。由6家通过资质认定的实验室使用1.3.2检测方法对样品进行测定,合作定值实验室进行严格的质量控制,并制定统一的作业指导书。每个实验室随机发放三个样品,测定三个平行。所有检测数据经狄克逊准则与科克伦检验后,数据等精度、无界外值,取平均值定值。
1.3.8 不确定度评定
草鱼粉中4种磺胺类药物残留基体标准物质样品定值结果的不确定度由三部分组成:即标准物质定值引入的不确定度u;标准物质的均匀性引入的不确定度u、标准物质长期稳定性和短期稳定性引入的不确定度u和u。
1.4 数据统计分析
采用Microsoft Excel 2010软件对数据进行统计,结果以平均值的形式表示,并利用origin8.0软件进行分析及绘图。
2 结果
2.1 标准曲线及回收率
4种磺胺类药物的线性回归方程、相关系数见表 3,由表3可知,4种磺胺类药物的相关系数均大于0.998,线性关系良好。SMZ、SFZ、SM、SM回收率和相对标准偏差见表4,由表4可知,4种磺胺类药物的回收率在92.90%~102.84%,批内和批间的相对标准偏差均小于10%。说明该方法的准确度高,重复性好,精密度良好,可满足草鱼粉中SMZ、SFZ、SM、SM残留量的检测要求。

表3 4种磺胺类药物的标准曲线和相关系数Tab.3 Standard curves and correlation coefficients of four sulfonamides

表4 4种磺胺类药物的回收率和精密度(n=6)Tab.4 Recovery and precision of four sulfonamides(n=6)
2.2 药浴时间的确定
草鱼肌肉中4种磺胺类药物的残留量随给药后时间的变化趋势如图1所示。由图1可知,在给药后0~24 h,是草鱼对SMZ、SFZ、SM、SM的药物吸收过程,从总体趋势来看,给药后6~12 h草鱼肌肉中药物残留量变化趋势相对平缓,10 h后药物残留量迅速上升,24 h时草鱼肌肉中药物残留量达到峰值,24 h后药浴池全量换水后,草鱼肌肉中药物残留量随着时间的推移逐渐降低。因此,阳性样本的采集时间范围在用药后的6~12 h,考虑到预期的浓度水平且保证草鱼肌肉中的SMZ、SFZ、SM、SM残留量相对稳定,最终选择药浴后10 h采集阳性样品。
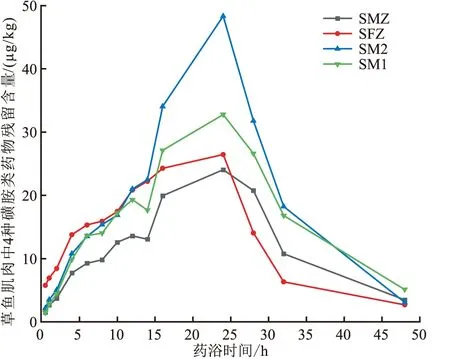
图1 不同药浴时间下草鱼肌肉中SMZ、SFZ、SM2、SM1残留量的变化Fig.1 Changes of SMZ,SFZ,SM2,SM1 residues in muscle of grass carp under different bath time
2.3 均匀性研究
样品的均匀性统计结果见表5。其中,组间自由度为10,组内自由度为22,(10,22)=2.3。由表中数据可知,草鱼粉中的4种磺胺类药物的统计量值均小于(10,22),表明样品间不存在显著性差异,即样品中SMZ、SFZ、SM、SM的含量是均匀的。

表5 均匀性统计结果Tab.5 Statistical analysis results of homogeneity testing
2.4 稳定性研究
2.4.1 短期稳定性
样品短期稳定性统计结果见表 6。采用检验法评定样品的稳定性,其中,自由度为3,置信水平0.95,t=3.18。由表中数据可知,|| 表6 短期稳定性统计结果Tab.6 Statistical results of short-term stability 2.4.2 长期稳定性 样品在棕色玻璃瓶包装储存条件下,进行了6个月的长期稳定性考察,统计结果见表7。其中,自由度为3,置信水平0.95,=3.18。由表中数据可知,||<×s(),表明样品在-20 ℃下储存6个月是稳定的。 表7 长期稳定性统计结果Tab.7 Statistical analysis results of long-term stability testing 6家实验室的定值数据经过狄克逊和科克伦检验,数据等精度、无界外值,均符合定值要求,数据都可以保留,统计结果见表8。草鱼粉中SMZ、SFZ、SM、SM药物残留基体标准物质的特性量的多家联合定值结果平均值分别为(22.22±1.90)、(24.04±3.65)、(31.11±3.95)、(28.55±2.26) μg/kg。 表8 定值数据狄克逊与科克伦检验统计检验Tab.8 Fixed value data Dixon and Cochran test statistical test 通过评估协作定值、均匀性和稳定性的不确定度分量,合成得出基体标准物质特性值的标准不确定度,在95%置信水平下,取包含因子=2,得出相对扩展不确定度,不确定度评估结果见表9。草鱼粉中SMZ、SFZ、SM、SM药物残留基体标准物质的特性量由定值的总平均值与合成扩展不确定度组成,详见表10。 表9 不确定度评估结果Tab.9 Evaluation results of uncertainty 表10 基体标准物质定值结果Tab.10 Characterization results of matrix reference materials 通过对草鱼肌肉中的 SMZ、SFZ、SM、SM残留量检测,由消除曲线图可以看出,SMZ、SFZ、SM、SM在肌肉中随着药浴时间的延长而逐渐升高,随后进入缓慢上升阶段,24 h 换水前残留量达到峰值,考虑到预期的浓度水平且保证草鱼肌肉中的药物残留量相对稳定,最终确定药浴时间为10 h。与余孔捷等研究结果较相似,24 h 换水前药物残留都出现峰值,但与本实验有所不同的是,余孔捷实验中换水后第28 h 残留变化相对平缓,而本实验中,换水后4种磺胺类药物都呈现快速下降的现象,结果的差异性可能与实验环境的温度、鱼类品种不同有关,本实验中的药浴水体使用加热棒控制药浴水温为(23±2) ℃,温度越高药物消除速率越快。ZHAO等研究了磺胺嘧啶和磺胺甲噁唑在鲤鱼体内的吸收与残留消除,结果显示,0.006、0.6、6 μg/L三个给药浓度水平下,鲤鱼组织中的2种磺胺类药物浓度随时间而增加,所有剂量组均观察到鱼体快速吸收现象,这与本实验中在换水前草鱼对SMZ、SFZ、SM、SM的吸收情况是一致的。 根据JJF1343-2012《标准物质定值的通用原则及统计学原理》中对标准物质样品均匀性检验的要求,记总体单元数为N,当N≤200时,抽样单元数不少于11个。本研究共研制187个单元,按照编号顺序,使用Microsoft Excel 2010 软件随机抽取11个包装单元,每个单元独立测量3次,结果采用单因素方差分析法进行统计分析。结果显示草鱼粉中的4种磺胺类药物的统计量值均小于(10,22),表明通过本研究中的制备方法所制得的样品含量是均匀的,可以满足基体标准物质制备的均匀性要求。 稳定性检验在均匀性检验之后进行。标准物质的稳定性检验分为两种情况,一是在规定保存条件下,较长周期内定期地进行标准物质特性值的长期稳定性检验;二是不同温度的运输条件下或极限条件下对标准物质特性值的短期稳定性检验,依据样品包装和运输形式,确定短期稳定性评估的温度。在本研究中制备的样品为冻干粉状态,包装形式为棕色玻璃瓶,运输方式为邮政网络运输传递。由2.4分析结果可知,样品在6个月内是稳定的并且样品可采用常温运输,该结论与尹太坤等研制的两种磺胺类基体标准物质的稳定性评估结论是一致的。 标准物质的定值分为以下几种方式:(1)由单一实验室进行单一基准方法测量;(2)由一个或多个实验室用2种或多种独立的标准方法测量;(3)多个实验室使用一种或多种已证明其准确性的方法协作定值;(4)用特定方法测量;(5)利用一级标准物质进行比较定值。在本研究中选择第三种方法进行定值,邀请国内6家具有相关检验资质的权威检验机构合作定值,合作实验室均采用1.3.1中已确定的检测方法进行样品测定。参加联合定值的6家实验室,长期参加全国农产品质量安全例行监测、专项监测等工作,均为国家级或省部级权威实验室,为本研究中草鱼粉中SMZ、SFZ、SM、SM药物残留基体标准物质准确定值提供了可靠保证。 由不确定度评估结果可知,样品由均匀性引入的不确定度分量最小,说明本研究中制备的样品均匀性良好;对4种磺胺类药物的不确定度贡献较大的因素主要为长期稳定性引入的不确定度分量,这表明尽管标准物质的长期稳定性已监测合格,但仍有必要在标准物质长期稳定性方面进一步开展研究,探索更加有效的标准物质储存条件,同时在实际实验操作过程中,尽量规范操作,减少因测量引入的不确定度,从而降低不确定度,提升标准物质品质与检测结果的准确性。 本研究通过药浴养殖的给药方式获得了适合浓度的草鱼自然污染的阳性样品。采用液相色谱-串联质谱法和多家实验室合作定值的方式,制备了一批草鱼粉中SMZ、SFZ、SM、SM药物残留基体标准物质样品。所获得的4种磺胺类药物残留基体标准物质样品,已完成6个月长期稳定性监测,样品性质稳定,特性量值准确可靠,为充分保证标准物质量值的准确可靠,将继续跟踪监测标准物质的稳定性以延长有效期。研制成果可用于质量控制、仪器校准等领域,对完善我国水产品药物残留检测工作具有很大的实用价值。本研究中制备的基体标准物质均匀性良好,稳定性符合标准物质技术要求,定值结果可靠,该方法对进一步开展水产品中磺胺类药物残留基体标准物质的制备提供了技术参考。

2.5 定值

2.6 不确定度评估


3 讨论
3.1 药浴时间对草鱼肌肉中SMZ、SFZ、SM2、SM1残留的影响
3.2 基体标准物质的均匀性与稳定性检验设计
3.3 基体标准物质的定值方法选择与不确定性影响分析
4 结论
