A型肉毒毒素对Meige综合征患者睡眠质量及血浆去甲肾上腺素、5-羟色胺的影响
2022-09-28赵日光张雪娟郝朝伟苏红军
赵日光 王 瑶 雷 东 张雪娟 郝朝伟 赵 琨 苏红军
天津市宝坻区人民医院神经内科 301800
Meige综合征为常见的节段性运动障碍性疾病之一,主要表现为眼睑痉挛和口—下颌肌张力障碍[1]。除头面部肌张力障碍外,Meige综合征常伴发非运动症状,其中以焦虑、抑郁、睡眠障碍最为常见[2]。BTX-A局部注射治疗Meige综合征安全有效[3],除运动症状改善外,是否可改善患者的睡眠质量方面的研究较少。因此,本文中对给予BTX-A治疗的Meige综合征患者进行BFMDRS评分、PSQI评分、血浆NE及5-HT评测,随访评定BTX-A治疗后1个月、3个月情况,分析BTX-A对Meige综合征患者睡眠质量的影响。
1 资料与方法
1.1 一般资料 选取2016年6月—2020年12月在我院神经内科接受BTX-A治疗的37例Meige综合征患者作为观察对象。其中女26例,男11例;年龄46~78岁,平均年龄(64.73±10.93)岁;病程5~23个月,平均病程(13.20±4.71)个月;临床表现为第Ⅰ型28例(75.68%),第Ⅱ型3例(8.10%),第Ⅲ型6例(16.22%)。纳入标准:(1)根据病史、症状体征、神经电生理及影像学检查明确诊断为Meige综合征。临床分型:第Ⅰ型为眼睑痉挛,第Ⅱ型为眼睑痉挛合并口—下颌肌张力障碍,第Ⅲ型口为口—下颌肌张力障碍。(2)除外脑卒中、颅内肿瘤、头外伤、脑炎、神经安定剂等所致的继发性头颈部不自主运动。(3)除外颞下颌关节综合征及下颌错位咬合。(4)无认知功能障碍。(5)无严重心脏、肝肾及肺部疾患。(6)未应用某些损害神经肌肉接头的药物,如奎宁、氨基糖苷类抗生素、吗啡等。(7)除外并发重症肌无力、肌无力综合征等某些神经肌肉接头传递障碍性疾病。(8)除外对肉毒毒素过敏者。研究经我院伦理委员会批准,所选对象均知情,并签署知情同意书。
1.2 方法 所选患者均给予注射用A型肉毒毒素(兰州生物制品研究所有限责任公司,批准文号:S10970037)局部注射。注射前先将BTX-A 冻干粉剂用0.9%氯化钠溶液稀释为25U/ml。根据患者痉挛肌肉分布进行个体化注射,主要注射肌肉包括额肌、眼轮匝肌、颧肌、颞肌、颊肌、咬肌、提上唇肌、颏肌等,每点注射1.25~2.5U,每例总量33~85U。
1.3 评价指标
1.3.1 临床量表检查:于治疗后1个月、3个月应用BFMDRS运动部分评定患者肌张力障碍严重度[4],应用PSQI评估患者睡眠质量[5]。PSQI包含睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物应用、日间功能障碍7项,总分0~21分,以PSQI总分>5分为有睡眠障碍,分数越高提示患者睡眠质量越差。
1.3.2 血浆NE及5-HT测定:于治疗后1个月、3个月采用ELISA法测定血浆NE及5-HT含量,血浆NE、5-HT ELISA检测试剂盒(FU-E10708、FU-E10687)购自北京方程生物科技有限公司,严格按照试剂盒说明书操作步骤进行检测。

2 结果
2.1 治疗不良反应 本组37例Meige综合征患者,注射BTX-A后7例出现轻度上睑下垂,5例出现鼻唇沟不对称,3例出现眼睛干涩,均在1~3周内自发缓解,无其他不良反应发生。
2.2 BTX-A治疗前后睡眠障碍患病率、BFMDRS和PSQI评分比较 37例患者BTX-A治疗后1个月、3个月睡眠障碍患病率以及BFMDRS、PSQI评分均低于治疗前(P<0.05);治疗后1个月与3个月相比,睡眠障碍患病率、BFMDRS和PSQI评分的差异无统计学意义(P>0.05)。见表1。
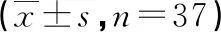
表1 BTX-A治疗前后睡眠障碍例数、BFMDRS评分、PSQI评分比较
2.3 BTX-A治疗前后血浆NE和5-HT水平比较 接受BTX-A治疗后1个月、3个月血浆NE水平均明显低于BTX-A治疗前,血浆5-HT水平均明显高于BTX-A治疗前(P<0.05);治疗后1个月与治疗后3个月相比较,血浆NE及5-HT水平的差异无统计学意义(P>0.05)。见表2。

表2 BTX-A治疗前后NE和5-HT比较
3 讨论
睡眠障碍是运动障碍性疾病最为常见的非运动症状,可由疾病本身引起,亦可为精神心理因素所致。Ferrazzano等[6]对60例眼睑痉挛患者的非运动症状进行分析,发现71%的患者并存有心境障碍、睡眠障碍、认知损害等非运动症状,其中睡眠障碍者达56%,与本文接近。本文结果显示,在接受BTX-A治疗后1个月和3个月睡眠障碍患病率及PSQI评分较治疗前明显下降,提示BTX-A的治疗可以改善Meige综合征患者睡眠障碍。王露丽等[7]对93例接受BTX-A治疗的三叉神经痛患者睡眠质量的研究发现,BTX-A可改善三叉神经痛患者睡眠质量,且在BTX-A治疗基础上给予心理行为治疗亚组的睡眠质量较单纯BTX-A治疗组明显提高。本文中BTX-A对Meige综合征患者睡眠质量的改善,可能通过对运动症状改善而减轻患者心理障碍实现,也可能为BTX-A对睡眠机制的调节实现,抑或两种机制均参与。本文为自身对照研究,未能对睡眠障碍改善的相关因素进行统计学分析,未能区分出其中确切的途径。BTX-A是否可改善Meige综合征患者非运动症状目前也存在不同观点。Ferrazzano等认为Meige综合征非运动症状可早于运动症状出现,且和运动症状的严重度无相关性,认为非运动症状是其原发症状之一,并非患者因过度关注运动症状而引起的心理障碍,BTX局部注射治疗不能改善非运动症状。但现有研究提示BTX-A对健康人群的睡眠质量亦有改善作用,为BTX-A改善Meige综合征患者睡眠质量提供间接证据。刘文先等[8]分析接受BTX-A美容除皱者(注射部位额肌、眉间肌、眼轮匝肌外侧)的睡眠质量发现,BTX-A面部局部注射可提高美容除皱队列人群的睡眠质量。
近年来的脑联络模式研究发现,Meige综合征除基底节结构功能变化外[9],其病理生化过程涉及基底节、脑干小脑、感觉运动皮层、视觉通路、边缘系统等结构功能异常。其中中脑—边缘系统多巴胺能通路参与睡眠调节,该通路中腹侧被盖区、伏隔核是两个重要核团[10]。与睡眠相关的神经递质有5-HT、多巴胺、乙酰胆碱、肾上腺素、γ-氨基丁酸等。上述解剖结构的破坏和神经递质传递功能障碍均能导致睡眠障碍。NE有维持觉醒作用,5-HT是引发非快速眼动睡眠的重要神经递质,NE升高、5-HT降低可引起警觉、失眠[11]。本文结果显示,TBX-A治疗后1个月血浆NE较治疗前明显下降,5-HT较治疗前明显上升,治疗后3个月仍保持稳定的血浆浓度,与睡眠质量变化一致。华健灿等[12]分析接受BTX-A治疗的原发性三叉神经痛患者队列中发现,BTX-A面部局部注射后1个月,血浆5-HT水平由(38.03±5.31)ng/ml上升至(76.44±9.35)ng/ml。BTX对神经递质的调节机制,可能通过神经反馈直接或间接地调节神经递质表达。Zhou等[13]的一项研究发现具有选择性裂解突触相关蛋白-25的BTX,可阻断含NE的囊泡与突触前膜融合,抑制NE释放、抑制交感神经活动。本文仅从血浆中影响睡眠的神经递质探讨了BTX-A对睡眠影响的机制,但NE、5-HT在脑神经网络联络中是否与外周血浆浓度有相同趋势的变化,尚需神经递质功能影像学研究及动物实验去提供更多的证据。
综上所述,BTX-A治疗Meige综合征在改善患者头面部肌张力障碍基础上,可能通过降低NE水平、增加5-HT水平,以长时间且有效地改善患者睡眠质量,提高患者生活质量。
