玻璃体切割手术联合全视网膜光凝术治疗糖尿病视网膜病变临床疗效观察
2022-09-28张雄
张 雄
(浏阳市集里医院,湖南 浏阳 410300)
糖尿病视网膜病变变(Diabetic retinopathy,DR)属于一类眼底病变,目前临床上关于其具体发病机制尚无明确的定论,主要包括代谢紊乱等情况,患病初期无明显的临床症状,若疾病确诊,则多数患者的视力已经受到一定程度的影响[1]。目前临床上对该类患者主要采取全视网膜光凝术(Panretinal photocoagulation, PRP)进行干预,虽然可有效抑制视网膜新生血管的生成或使已经形成的新生血管萎缩,保留有效的视功能,降低DR 致盲率,但不能有效提高视网膜功能,也不能控制高血糖对视网膜神经组织的损害作用,DR还是在不可逆性进展中。玻璃体切割手术(Pars plana vitrectomy,PPV)能够帮助患者及时清除玻璃体积血,将其临床症状进一步改善,从而使得患者的视力水平及时恢复正常[3]。玻璃体和视网膜紧密接触是否在DR 的发生与发展中发挥了相关作用,一直是DR 研究的热点问题之一。为了对其治疗过程、疗效、安全性等方面进行更加深入的探讨,本文共收治了92例DR患者,分为两组展开手术治疗,现报道如下。
1 资料与方法
1.1 一般资料 择取2019 年3 月~2021 年3 月至我院就诊的糖尿病视网膜病变患者92例,随机分为对照组和试验组各46 例。对照组男25 例,女21例,年龄48~78(62.12±2.58)岁,糖尿病病程1~12(5.69±1.12)年,DR 病程1~9(4.23±0.56)月,合计67眼,DR分期:Ⅰ期15眼、Ⅱ期16眼、Ⅲ期12眼、IV 期10 眼、Ⅴ期8 眼、Ⅵ期6 眼;非增殖性糖尿病性视网膜病变14例、增殖性糖尿病视网膜病变20例;高血压12 例;试验组男26 例,女20 例,年龄46~79(62.85±2.74)岁,糖 尿 病 病 程1~13(5.75±1.23)年,DR 病程1~8(4.15±0.52)月;合计66 眼,DR 分期:Ⅰ期18 眼、Ⅱ期17 眼、Ⅲ期8 眼、IV 期9眼、Ⅴ期7眼、Ⅵ期7眼;非增殖性糖尿病性视网膜病变15 例、增殖性糖尿病视网膜病变18 例,高血压13 例。两组性别、年龄、病程等一般资料差异无统计学意义(P>0.05),具有可比性。
1.2 纳入标准①眼底检查、彩色眼底照相及频域光相干断层扫描、眼底荧光素造影检查符合糖尿病视网膜病变诊断;②存在视物模糊、失明等情况;③未伴有其他类型的眼底严重病变;④患者知情并签署知情同意书。
1.3 排除标准①以往接受过全视网膜光凝术与玻璃体切割手术;②有其他眼部疾病,如白内障、眼部外伤史、视网膜脱离手术、葡萄膜炎、黄斑病变、青光眼等;③凝血功能障碍;④黄斑病变;⑤其他类型的全身性严重疾病。
1.4 方法
1.4.1 对照组 单纯采取全视网膜光凝术进行治疗。对患者的上下血管弓外、视乳头周围IPD外、黄斑区颞侧IPD 外给予光凝处理。相关参数设置:光斑为200μm,曝光时间为0.2s,能量光凝斑为200-300mV,光斑强度Ⅲ级,间隔时间0.2s。在全视网膜镜的辅助下对其后极部、赤道部与周边进行光凝处理,光凝斑为1000-1500 个。其中光凝视网膜上突出的新生血管丛附近无需直接光凝处理,后级部需将视盘与黄斑区域进行保留。
1.4.2 试验组 在对照组的基础上采取玻璃体切割手术治疗。23G 微创玻璃体切割手术,使用Millennium 玻璃体切割仪(美国Bausch&Lomb 公司),23G 微创玻璃体切割系统(荷兰D0RC 公司)包括压盘、穿刺刀、3根套管、1根灌注管、1个套管镊子、3个管塞,其中留置套管的长度为4.0mill但不包括其尖端,内径0.65mm,外径0.75mm。眼球后麻醉处理,经睫状体平坦部三通道进行手术,切除患者的中央部、后极部、巩膜切口周围基底部的玻璃体与皮质,之后切除新生血管膜,若血管膜无法完全分离,可采取分段切除的方式。将视网膜牵拉状态及时解除,若视网膜严重缺血、视网膜脱离等,可将硅油注入,若无此类情况,可完成气液交换后,将纯惰性气体于玻璃体腔内注入。手术完成后,及时进行眼底血管荧光造影,两组患者术后均将3mg 的地塞米松注射于半球后,可有效预防术后感染现象。
1.5 观察指标①最佳矫正视力(Best corrected vi‐sual acuity, BCVA);②眼内压(Intraocularpres‐sure, IOP):使用Goldmann 压平式眼压计测量眼内压。③光敏度:对比两组患者周边30°与60°的光敏度。采用HGD5电脑视野分析仪,给予0-60°视野视网膜光敏感度检测,585mm 为光源波长,0.5s 为刺激点持续时间,间隔1s,光敏感度26-0dB。④视力恢复率。提高:治疗前的视力水平大于0.1,治疗后,视力提升幅度大于等于2 行;改善:治疗后视力提升程度小于2 行;下降:治疗后视力水平无改善或者下降;恢复率=提高率与改善率之和[4-5]。⑤术后并发症发生率。
2 结果
2.1 视力 治疗前,两组患者的BCVA、IOP 差异无统计学意义(P>0.05)。治疗后,两组患者的BC‐VA、IOP 均较治疗前有所改善(P<0.05),且试验组治疗后的BCVA、IOP 显著优于对照组(P<0.05)。见表1。的光敏度差异无统计学意义(P>0.05)。治疗后,两组患者的周边30°与60°的光敏度均较治疗前提高(P<0.05),且试验组治疗后的周边30°与60°的光敏度均高于对照组(P<0.05)。见表2。
表1 两组患者治疗前后BCVA、IOP比较(± s)

表1 两组患者治疗前后BCVA、IOP比较(± s)
注:与治疗前比较,①P<0.05;与对照组治疗后比较,②P<0.052.2 光敏度 治疗前,两组患者的周边30°与60°
IOP(mmHg)15.23±1.95 13.70±2.10①②15.57±2.45 15.03±2.15①组别试验组例数46对照组46时间治疗前治疗后治疗前治疗后BCVA(deci)0.53±0.26 0.43±0.23①②0.55±0.28 0.67±0.26①
表2 两组患者治疗前后周边30°与60°的光敏度分析(± s,dB)

表2 两组患者治疗前后周边30°与60°的光敏度分析(± s,dB)
注:与治疗前比较,①P<0.05;与对照组治疗后比较,②P<0.05
周边60°18.63±2.58 24.71±3.26①②18.56±2.33 21.05±4.64①组别试验组对照组例数46 46时间治疗前治疗后治疗前治疗后周边30°22.36±2.63 29.26±3.58①②22.15±2.58 24.16±3.50①
2.3 视力恢复率 试验组视力恢复率为97.83%,对照组视力恢复率为82.61%;两组视力恢复率差异有统计学意义(P<0.05),试验组高于对照组。见表3。
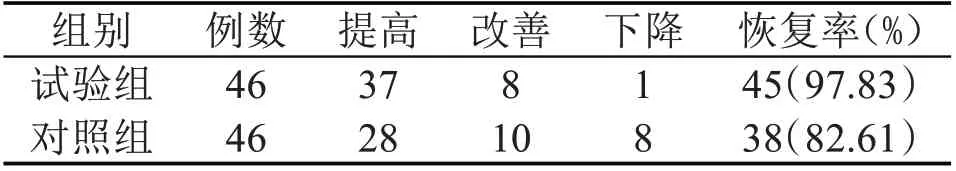
表3 两组视力恢复情况比较(ƒ,-R,P)
2.4 术后并发症 试验组术后各项并发症发生率均明显低于对照组(P<0.05)。见表4。

表4 两组术后并发症情况分析(ƒ,P)
3 讨论
糖尿病视网膜病变是以视网膜毛细血管病变为主要病理改变,随着社会经济的不断发展与人们生活方式的改变,糖尿病患病率已呈高发状态,作为糖尿病最重要慢性并发症的糖尿病视网膜病变发生率日益增高[6]。糖尿病视网膜病变的病理生理机制基本环节为糖代谢异常,患者长期处于高血糖状态,会引起蛋白质发生糖基化,而此类糖基化蛋白质可导致视网膜细动脉、微动脉损害,增厚血管基底膜,引发视网膜病变[7]。糖尿病视网膜病变患者进行眼底检查可发现不同程度视网膜微血管改变、出血渗出甚至动脉瘤,若未加以控制则可能导致视网膜脱离,对患者视力造成严重影响[8]。
目前,临床主要采取全视网膜光凝术PRP,目的在于预防和阻止视网膜或视盘新生血管的发展,以防止进一步发生玻璃体积血,以及视网膜纤维膜和牵拉性视网膜脱离。PRP 的基本原理是激光的光能转化为热能,破坏高耗氧视网膜色素上皮组织及光感受器复合体,使其瘢痕化,以改善视网膜缺血状态,减少血管内皮生长因子(VEGF)的产生,抑制视网膜新生血管的形成并促进已形成的视网膜新生血管的消退,降低因新生血管出血而导致视力下降的机率,减少PDR 的并发症如虹膜红变、牵拉性视网膜脱离等,有效阻止病变的发展。减弱视网膜的外屏障,增加脉络膜的氧供应至视网膜,改善供氧渠道[9]。视网膜周边的区域被光凝后,改变了血流分布,保障黄斑区的供氧,阻止病变进展,缓解严重的视力下降,从而保护视功能。研究表明PRP可使视力丧失的风险降低50%,但激光光凝在有效阻止视网膜血管病变进展的同时,也是一种损伤性治疗,有着一系列的并发症和副反应,治疗过程中应考虑其对视盘周围视网膜神经纤维层的损害,且其治疗后仍需长期的后续治疗以维持较长时间的视功能。
有研究表示玻璃体液中存在一些生物标志物促进了DR 的发生与发展。玻璃体液中炎性因子的表达、氧化应激反应、小分子表达的差异也成为当今研究的热点问题[10]。过往玻璃体视网膜手术应用于治疗PDR,主要是为了清除严重玻璃体混浊和积血,为行PRP 创造条件,或者解剖复位由牵拉所致的视网膜脱离,但大多数患者DR 已经进展到增殖期晚期,顺利完成手术也较难延缓视功能的进一步下降。然而,随着23G和25G微创玻璃体视网膜手术的开展,手术器械、技术和经验的进步改善了术后视力,玻璃体手术的安全性和成功率大幅提高,并相应减少了术中及术后的并发症,越来越受到眼科医生和患者的青睐[11]。
玻璃体切割术属于一类微创眼科手术,相比传统手术治疗方式,不会对患者造成较大的手术创伤,并发症发生率较低,促使血管新生的诱导因子进一步减少,解除新生血管对于视网膜的牵拉作用,早日消退黄斑水肿现象,将局部毒素、细菌等及时清除,使得患者的临床症状得到有效的改善,将视力水平提高,以免疾病继续发展。25G 经结膜不缝合微创玻璃体切割系统和与之配套的系列手术器械,不需要切开结膜、缝合切口和止血操作,显著缩短了手术时间。但眼内器械较细,硬度较小,容易弯曲,手术后低眼压等缺陷[12]。23G 微创玻璃体切割系统总结继承上述的优势,既保留了20G手术器械的刚性好,操作灵活,又兼有25G 不需切开球结膜,巩膜的穿刺口自闭,而且器械进出玻璃体腔都是通过套管,避免了器械反复进出对巩膜和睫状体的损伤。扩大了微创玻璃体切割系统手术适应证,使其不仅局限于黄斑疾病和简单玻璃体积血的手术,还能有选择地处理一些需要做大块膜组织切除和眼内操作较复杂的玻璃体视网膜手术患者[13]。
治疗后,试验组治疗后的BCVA、IOP 显著优于对照组(P<0.05),周边30°与60°的光敏度均高于对照组(P<0.05),视力恢复率高于对照组(P<0.05)。分析其中的原因可能是由于玻璃体切割手术能够及时切除含有脓液、积血、浑浊的玻璃体,将增生膜牵拉作用及时解除,使得屈光介质恢复至透明状态,利于视网膜的复位,便于手术的治疗,还能够将血管内皮生长因子及时抑制,稳定血-视网膜的屏障,将患者视力水平进一步提高。试验组视盘血管渗漏等并发症的发生率均明显低于对照组(P<0.05),说明联合手术治疗方案的安全性更高,可能是由于联合治疗方案能够弥补单纯手术治疗的不足之处,其中全视网膜光凝术便于毛细血管闭塞与小动脉的收缩,及时改善视网膜水肿等状态,使得新生血管形成概率降低,安全性较高。给予玻璃体切割手术治疗时,应将患者的所有玻璃体及时切除干净,以防残余玻璃体牵拉患者的视网膜,引发视网膜脱离、术后出血等情况,不利于手术的安全性。
综上,对糖尿病视网膜病变患者来说,玻璃体切割手术联合全视网膜光凝术治疗的效果较为显著,便于有效恢复患者视力水平,将其视野进一步改善,安全性较高,值得采纳并推广。但本研究样本量较小,缺乏随访,结果可能存在一定的偏倚,因此在今后的研究中还需扩大样本量并采用多中心协作方式进行长时间随访观察,以进一步证实本研究结论。此外,我们将进一步通过对玻璃体液分子生物学和蛋白组学的研究明确PPV 术后玻璃体的改变,为DR 提供新的治疗策略。
