影响颅内动脉瘤开颅夹闭术后预后的因素分析
2022-09-26郭东斌郑锦亮刘天庆
郭东斌 郑锦亮 刘天庆
颅内动脉瘤因患者脑内的动脉壁结构异常,或者是由于脑外伤、动脉硬化使脑动脉壁出现严重损伤、老化,促使局部血管壁向外逐渐膨胀、变大,从而形成囊状瘤体,作为临床上的一种脑血管疾病,一旦发生破裂出血后,具有较高的致残率和死亡率[1-2]。老年人群的发病率要高于中年人群。颅内动脉瘤会因情绪紧张、身体用力、疲劳等使血压升高而出现突发破裂,所引起的颅内蛛网膜下腔出血、出血后相关并发症等会使患者出现意识障碍、昏迷,甚至还会威胁患者的生命安全。开颅夹闭手术是目前治疗该疾病的常用方式,能够拯救患者生命,降低致死、致残率[3]。但是由于开颅瘤颈夹闭手术具有较高的风险性,而且毕竟只有少数的临床医生能够熟练完成和进行此类手术,还有相当数量的医务工作者对颅内动脉瘤的特点及它的表现认识还不够明确[4]。因此,本次研究对影响颅内动脉瘤开颅术后预后的因素进行分析,并提出针对性的临床治疗措施,以期对颅内动脉瘤的发生及发展有一个更全面、更深入的了解,更好地提高患者的健康质量水平,改善预后。
1 资料与方法
1.1 一般资料
采用回顾性分析方法,选择于2018年2月-2021年7月到龙岩市第一医院接受治疗的225例颅内动脉瘤患者为研究对象。纳入标准:(1)经临床上常规检查确诊为原发性颅内动脉瘤;(2)无手术禁忌证;(3)有一项或者多项症状:头痛、脑膜刺激征、脑神经功能障碍等;(4)认知功能正常,无精神异常。排除标准:(1)合并外伤性感染性或夹层颅内动脉瘤;(2)合并严重的肾器质性疾病;(3)合并恶性肿瘤;(4)基线资料不完整。其中207例患者预后效果良好,设为对照组,18例患者预后效果差甚至死亡,设为观察组。对照组:男女分别119、88例,年龄19~75岁,平均(45.98±4.65)岁;观察组中男10例,女8例,年龄19~74岁,平均(46.16±4.71)岁。两组一般资料比较差异无统计学意义(P>0.05),可对比。
1.2 手术方法
所有患者都接受开颅夹闭手术,选择Yasargil翼点为入路,自颧弓上,耳屏前1 cm的位置做一个切口,切口呈弧形,游离皮瓣,在冠状缝、颞上线交接位置的上方位置完成钻孔,将存在的骨瓣全部去除。切开硬脑膜后,需要将侧裂池慢慢切开,将颈内动脉池、视交叉池尽可能地开放,明确与血管之间的关系后,瘤体充分暴露在外。合理选择动脉瘤夹,调整好位置之后,将动脉瘤夹闭,随后进行止血,止血后缝合脑膜,监测患者的颅内压情况,如果发现患者存在严重的水肿现象,则需要接受骨瓣减压术,最后缝合头皮。
1.3 观察指标及评价标准
本次研究通过对本院电子病例档案查阅收集225例患者的病例资料,包括患者的性别、年龄、住院时间、高血压、手术时机、术中并发症、瘤颈情况、Hunt-Hess分级、CT Fisher分级。
颅内动脉瘤CT Fisher分级:所有患者均采用颅多普勒(TCD)脑血流、头颅CT检查;Fisher分级标准根据头颅蛛网膜下腔的出血情况判定,1级:无积血;2级:广泛性出血,积血厚度未超过1 mm;3级:积血厚度为1 mm及以上,4级:脑内血肿或者脑室内积血。所有患者同时采用CTA或者采用DSA检查动脉瘤的具体情况。
颅内动脉瘤Hunt-Hess分级:依据文献[5]《中国蛛网膜下腔出血诊治指南2015》中的相关标准对颅内动脉瘤Hunt-Hess分级情况进行评估,共分为Ⅰ~Ⅴ级;Ⅰ级:无任何症状,或者头痛程度较轻,有轻微颈强直症状;Ⅱ级:头痛程度为中度至重度,颈强直、颅神经麻痹症状明显,但无神经功能缺失现象;Ⅲ级:患者出现嗜睡、意识模糊的症状,轻度局灶性神经功能缺失现象;Ⅳ级:患者出现浅昏迷,中或者重度偏瘫,早期自主神经功能紊乱;Ⅴ级:患者深度昏迷,去脑强直,病情加速恶化。
预后情况:采用改良版Rankin评分量表对患者的预后情况进行评定,改良版Rankin评分0~3分为预后良好,改良版Rankin评分4~6分为预后差。其中0分:无任何不适感;1分:患者有轻微的不适感,无任何缺失表现,可以正常活动;2分:残疾程度为轻度,生活可以自理;3分:残疾程度为中度,可以行走;4分:残疾为中重度,患者无法自主下床活动;5分:重度残疾,患者需要长时期卧床,并由转人员照看;6分:死亡。
1.4 统计学处理
EpiData 3.1 进行数据录入,采用 SPSS 20.0 软件进行统计分析,计量资料用(±s)描述,用t检验或非参数检验,计数资料用率(%)表示,用χ2检验或Fisher确切概率检验,单因素分析P<0.05的因素进入多因素Logistic回归分析。
2 结果
2.1 影响颅内动脉瘤患者预后的单因素分析
两组年龄、性别、瘤颈情况方面对比差异无统计学意义(P>0.05);高血压、手术时机、术后并发症、Hunt-Hess分级、CT Fisher分级方面对比,差异有统计学意义(P<0.05),见表1。
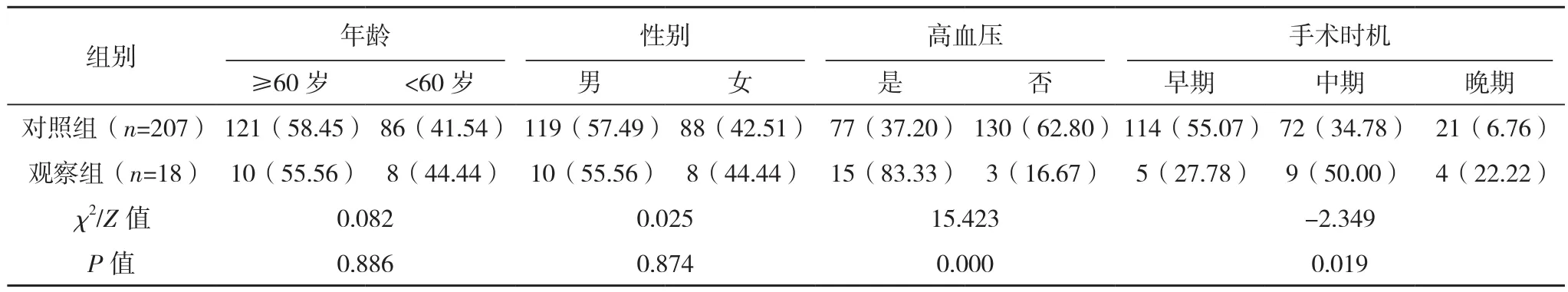
表1 影响颅内动脉瘤患者预后的单因素分析[例(%)]

表1(续)
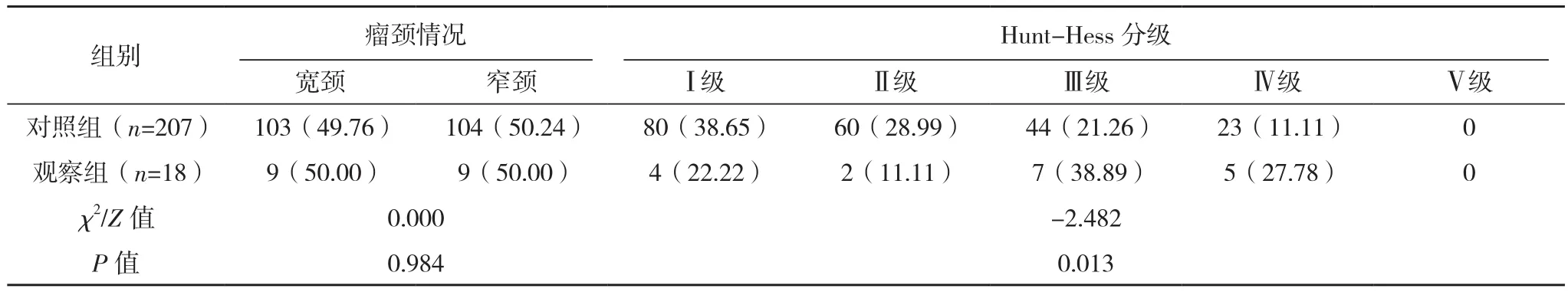
表1(续)
2.2 影响颅内动脉瘤患者预后的多因素分析
Logistic回归分析得知,高血压、手术时机、术后并发症、Hunt-Hess分级、CT Fisher分级均为影响颅内动脉瘤患者预后效果的主要危险因素(P<0.05),见表 2。
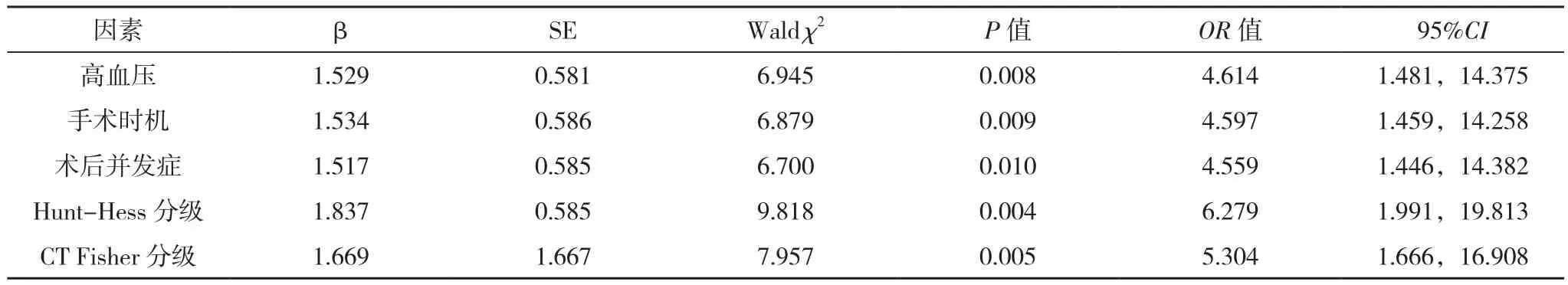
表2 影响颅内动脉瘤患者预后的多因素分析
3 讨论
颅内动脉瘤患者由于动脉血管壁出现明显增厚、血管极度狭窄,会严重发生颅内缺血的现象,甚至血液循环异常等,病情严重者则会出现继发脑血管痉挛、脑梗死等并发症,近些年,临床上采用开颅夹闭手术治疗,可以有效预防再出血,预后效果较好。及时了解影响颅内动脉瘤患者预后效果的危险因素,对积极采取有效方式治疗,改善预后具有至关重要的作用。如果患者长时期存在严重的慢性高血压,也会增加血管硬化、钙化的发生概率,对于手术的难度系数来讲也是关键性因素,另外,在围手术期如果没有及时控制患者的血压水平,则会导致患者的动脉瘤出现不同的破裂现象。临床研究数据表示,年龄大、合并高血压、术前Hunt-Hess分级Ⅲ~Ⅳ级都是影响患者近期效果的独立危险因素。本次研究结果显示,225例患者中207例患者预后良好,18例患者预后较差,分别占比92.00%、8.00%。经多因素分析发现,高血压、手术时机、术后并发症、Hunt-Hess分级、CT Fisher分级是影响颅内动脉瘤患者预后效果的主要危险因素。
3.1 高血压与预后
高血压患者动脉内膜会出现明显增厚的现象,而且中间有明显坏死或者弹性内板严重损坏,这样会导致动脉壁发生严重的局部膨胀,这种情况下会增加形成动脉瘤的概率,进而导致动脉瘤出现破裂[6]。颅内动脉瘤患者出血24 h后,颅内瘤体出现再破裂的风险可达10%,病死率达5.5%。高血压作为影响此疾病预后的独立危险因素,会促使患者心血管疾病发生,颅内血管壁严重受损,甚至发生血流动力异常,导致患者动脉血管管壁囊逐渐扩张,病情严重者还会出现动脉瘤破裂,对预后效果造成了严重的影响。在康慧斌等[7]研究中表明,高血压与动脉瘤破裂风险的存在相关性,与血流动力学的变化有着密切的联系。
3.2 手术时机与预后
临床上关于动脉瘤的手术时机都有各自的说法,争议较大,主要集中早期和晚期手术时机哪个对患者预后效果较好。动脉瘤首次破裂出现SAH后要面对的最大威胁就是二次出血和CVS,开颅手术时间距离动脉瘤破裂时间间隔大于2周,脑血管痉挛逐渐缓解,理论上2周后手术比在CVS高峰期手术效果要好,然而因为动脉瘤一次破裂后出现再破裂的可能非常大,而二次出血患者预后大都较差,残疾率和死亡率相当高。因此在临床实践当中,悲观的等待及将病患的手术时间延迟是一个不理智的选择,而应当在初次出血以后尽快地给予手术治疗,避免瘤体二次破裂出血导致更差的预后。国内一些学者也认为虽然早期(0~3 d)显微手术的手术脑组织水肿、粘连严重,镜下对瘤周组织结构的解剖不够清楚,瘤体很难完全暴露,勉强的牵拉使脑实质受压严重又容易产生暴力损伤,手术的困难程度相对较大,但早期手术可显著减少再出血风险,缩短患者的住院时间,降低住院费用。无论患者的病情级别高低,只要术者的手术经验丰富、所在医院条件允许,理应尽快地手术处理动脉瘤。
3.3 术后并发症与预后
手术并发症包括血管损伤、直接脑损伤、术后出血切口感染等。血管损伤主要是指在手术之后的24 h后,经观察可以发现患者的局部神经功能严重受损,且头颅CT检查可以发现部分脑梗死的现象。脑梗死会使患者脑部供血严重不足,甚至还会减少脑部供血区域的血流量,对脑部组织造成严重的损伤,阻碍预后发展。手术该过程中要尽可能地利用微创的方式将侧裂的脑部组织进行分离,采用脑压板轻微牵拉,促使颈内动脉充分暴露;同时,打开硬膜,实施常规操作,穿刺侧脑室额角,将脑脊液放出,这样的方式能够有效减少脑损伤的概率,降低开颅手术的风险系数;放出脑脊液后,颅内压明显下降,可轻松抬起额叶,暴露脑池和颈内动脉,避免过分分离外侧裂和对脑叶的过分牵拉而造成的直接脑损伤;同时,释放脑脊液不宜过快,应给予脑组织一定的适应期[8]。基于此,及早处理急性脑积水,术中Paine点穿刺侧脑室外引流术治疗能够有效抑制疾病发展,改善预后。
3.4 Hunt-Hess分级与预后
Hunt-Hess分级主要用来评价患者病情的严重程度及预后效果,可以作为有效反映患者临床症状和意识功能的重要指标。临床研究表明,术前Hunt-Hess分级与患者预后存在着密切的联系,等级越高,说明患者预后效果越差[9]。本次研究中发现,Hunt-Hess分级是影响颅内动脉瘤患者预后效果的独立危险因素,与以往研究结果一致。原因在于Hunt-Hess分级是根据患者自身意识水平来识别急剧局灶性神经系统的阳性体征情况,从而预估患者的病情严重程度和预后效果。Ⅰ级患者,临床上可以采用镇静、通便、长期卧床的方式进行干预,减少探访次数,缩短探访时间,尽可能地避免患者在干预期间打喷嚏、情绪激动,以此来降低再出血的发生概率[10]。Ⅱ级患者,需要在防止出血的基础上准确评估患者的头痛程度、性质,为患者讲解诱发头痛的原因,便于消除患者负面情绪,必要情况下需要注射镇静剂[11];针对Ⅲ、Ⅳ级患者,需要做好对各项生命指征、瞳孔大小、形态的监测,优先考虑颅内再出血的可能性;而Ⅴ级患者属于为重症患者,需要立即行气管插管,必要时呼吸机辅助呼吸治疗,确保患者呼吸通畅,重点监测患者血氧饱和度的变化情况,避免患者因缺氧而加重脑部损伤程度,同时还需要完成对血气值的监测,及时纠正患者可能出现的水电解质紊乱,维持生命体征稳定,确保患者生命安全的关键环节[12]。
3.5 CT Fisher分级与预后
CT Fisher分级主要根据动脉瘤破裂出血后在CT上对患者的出血量进行衡量,作为预测脑血管痉挛的基本要素。CT Fisher分级越高,说明患者的预后效果越差。研究表明,CT Fisher分级对预后效果影响非常大,可以准确评估患者术后病情的严重程度[13]。此次研究中,CT Fisher分级作为影响此疾病预后的独立危险因素。提示患者颅内出血量会随着CT Fisher分级的不断增高而上升,出血破入脑室后,则会导致患者脑血管发生痉挛,出现脑梗死及脑积水并发症,对患者的生命安全造成了严重的威胁。基于此,对于该分级较低者,在开颅夹闭手术后可以选择腰穿脑脊液的方式治疗;而对于分级较高者可以开颅夹闭术后采用综合疗法,重点考虑患者生命安全的风险系数;以此来改善预后。
综上所述,高血压、手术时机、术后并发症、Hunt-Hess分级、CT Fisher分级均属于影响颅内动脉瘤预后的独立危险因素,临床发现该类患者则需要立即对上述因素进行分析,并积极采取科学的治疗方式,能够显著提高临床效果,提高患者预后。
