盐酸埃克替尼治疗中晚期EGFR突变型非小细胞肺癌的效果
2022-09-26练晓珊陈富钦陈菊英王红哲
练晓珊 陈富钦 陈菊英 王红哲
中晚期表皮生长因子受体(EGFR)突变型非小细胞肺癌治疗方案常为化学治疗,常用药为多西他赛,能促进小管聚合成稳定的微管并抑制其聚解,从而达抗癌效果[1]。但临床实践发现,对于EGFR的突变,其不能竞争性与EGFR结合位点相结合,因此降低肿瘤标志物水平的效果不够显著[2]。盐酸埃克替尼具有特异型结合EGFR在ATP上的结合位点的特征,从而抑制磷酸化作用,以此控制肿瘤细胞的快速增殖[3]。但将其用于EGFR突变型非小细胞肺癌,其对降低患者体内肿瘤标志物水平的效果并未明确,基于此,本研究将探讨盐酸埃克替尼治疗EGFR突变型非小细胞肺癌的效果及安全性,报道如下。
1 资料与方法
1.1 一般资料
选取广州市泰和肿瘤医院2020年1月-2021年8月108例中晚期EGFR突变型非小细胞肺癌患者。纳入标准:(1)病理组织检查EGFR突变;(2)符合非小细胞肺癌诊断标准[4];(3)癌症分期为Ⅲ期及以上。排除标准:(1)对本研究药物出现不耐受情况;(2)出现严重脏器功能障碍。按照随机数字表法将其分为对照组(n=54)和观察组(n=54)。对照组男39例,女15例;年龄52~70岁,平均(61.55±7.40)岁;病理类型:腺鳞癌2例,腺癌23例,鳞状上皮细胞癌29例;癌症病程2~6年,平均(4.56±1.02)年;癌症分期:ⅢA期10例,ⅢB期33例,Ⅳ期11例。观察组男41例,女13例;年龄52~70岁,平均(61.60±7.43)岁;病理类型:腺鳞癌1例,腺癌22例,鳞状上皮细胞癌31例;癌症病程2~6年,平均(4.58±1.04)年;癌症分期:ⅢA期8例,ⅢB期34例,Ⅳ期12例。两组上述资料比较差异无统计学意义(P>0.05),有可比性。本研究经患者、家属签署知情同意书及医院伦理委员会批准。
1.2 方法
两组均于治疗期间禁止使用其他抗癌药物,自用药起,每个月行实验室肿瘤标志物及影像学等常规检查。
对照组:给予多西他赛注射液(德国Sanofi-Aventis Deutschland GmbH,国药准字J20140039,规格:0.5 ml∶20 mg)治疗,75 mg/m2多西他赛注射液静脉滴注,以3周为1个周期,每3周1次,共治疗4个周期(12周),采用该药物治疗前予以地塞米松(广东南国药业有限公司,国药准字H44024618,规格:0.75 mg×100 片)口服,8 mg/次,2次/d,连续用药3 d以预防过敏反应。
观察组:给予盐酸埃克替尼片(贝达药业股份有限公司,国药准字H20110061,规格:0.125 g×21片/盒)口服治疗,3次/d,1片/次,持续服药1个月。
1.3 观察指标及评价标准
(1)临床疗效:治疗后,根据WHO实体瘤疗效分析评价标准,完全缓解为影像学显示病灶完全消失;部分缓解为影像学显示病灶体积减小≥30%;稳定为影像学显示病灶体积减小<30%或者体积增大<20%;进展为影像学显示病灶体积增大≥20%或者出现新病灶。缓解率=(完全缓解+部分缓解)/总例数×100%[5]。(2)肿瘤标志物:治疗前、治疗后,采集两组患者静脉血,离心机(长沙湘锐离心机有限公司,型号:TG16-X)分离血清,经酶联免疫吸附法测验血清中细胞角蛋白19片段抗原(CYFRA21-1)及癌胚抗原(CEA)水平。(3)免疫功能:治疗前后,采集两组患者空腹静脉血液,经酶联免疫吸附法测验血液中CD8+、CD4+、CD3+、CD4+/CD8+水平。(4)不良反应:治疗期间,观察两组患者出现恶心、腹泻及皮疹不良反应的发生情况。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
治疗后,观察组缓解率(53.70%)高于对照组(31.48%)(P<0.05),见表 1。

表1 两组临床疗效比较[例(%)]
2.2 两组肿瘤标志物比较
治疗后,观察组CYFRA21-1、CEA水平均低于对照组(P<0.05),见表2。
表2 两组肿瘤标志物比较(±s)
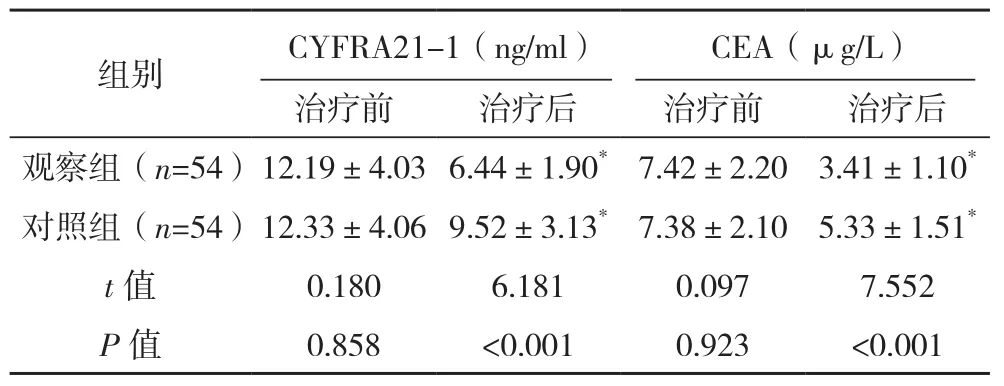
表2 两组肿瘤标志物比较(±s)
*与本组治疗前比较,P<0.05。
组别 CYFRA21-1(ng/ml)CEA(μg/L)治疗前 治疗后 治疗前 治疗后观察组(n=54)12.19±4.03 6.44±1.90*7.42±2.20 3.41±1.10*对照组(n=54)12.33±4.06 9.52±3.13*7.38±2.10 5.33±1.51*t值 0.180 6.181 0.097 7.552 P值 0.858 <0.001 0.923 <0.001
2.3 两组免疫功能比较
治疗后,观察组CD8+水平低于对照组,CD4+、CD3+、CD4+/CD8+水平均高于对照组(P<0.05),见表3。
表3 两组免疫功能比较(±s)
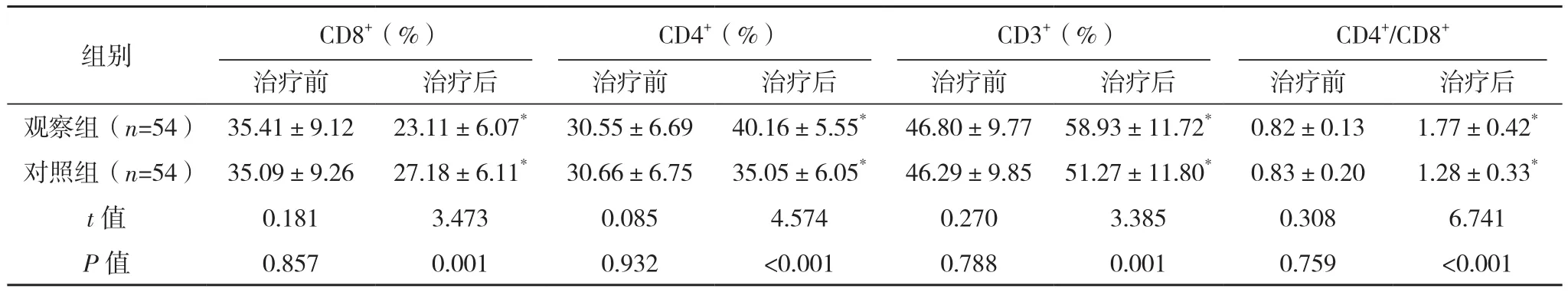
表3 两组免疫功能比较(±s)
*与本组治疗前比较,P<0.05。
组别 CD8+(%)CD4+(%)CD3+(%)CD4+/CD8+治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=54) 35.41±9.12 23.11±6.07* 30.55±6.69 40.16±5.55* 46.80±9.77 58.93±11.72* 0.82±0.13 1.77±0.42*对照组(n=54) 35.09±9.26 27.18±6.11* 30.66±6.75 35.05±6.05* 46.29±9.85 51.27±11.80* 0.83±0.20 1.28±0.33*t值 0.181 3.473 0.085 4.574 0.270 3.385 0.308 6.741 P值 0.857 0.001 0.932 <0.001 0.788 0.001 0.759 <0.001
2.4 两组不良反应比较
治疗期间,观察组腹泻、恶心各2例,皮疹1例,发生率为9.26%(5/54);对照组恶心3例,腹泻及皮疹各2例,发生率为12.96%(7/54)。两组不良反应发生率比较差异无统计学意义(χ2=0.375,P=0.540)。
3 讨论
中晚期EGFR突变型非小细胞肺癌在我国占比为40%~50%[6]。肺癌多数患者确诊后已达到中晚期,死亡率高,需及时有效的治疗以延长生命,放射性治疗对此类型疾病效果不佳,临床主要以化疗为主[7]。多西他赛水溶性低,能有效结合细胞内的微管蛋白,从而提高蛋白能力以形成微管,并抑制其聚解,进一步阻碍肿瘤细胞的有丝分裂[8]。而EGFR作为肺癌最常见的驱动因子,多西他赛难以靶向竞争EGFR结合位点,不能有效减少其与ATP的结合,难以抑制肿瘤细胞的生长,因此提高机体免疫力的效果不佳[9]。盐酸埃克替尼属于EGFRTKI类药物,可靶向结合ATP位点,以阻碍EGFR的驱动功能[10]。若将其应用于该疾病患者或许能够提高患者免疫力。
本研究显示,治疗后,观察组缓解率(53.70%)高于对照组(31.48%)(P<0.05)。治疗后,观察组CYFRA21-1、CEA水平均低于对照组(P<0.05)。说明盐酸埃克替尼治疗中晚期EGFR突变型非小细胞肺癌可显著降低患者肿瘤标志物水平,提高临床疗效。分析原因可能是EGFR是附着于上皮细胞膜上的糖蛋白,在癌症细胞内过表达,作为驱动癌症细胞生长的因子,主要通过RAS/MAPK、JAK/STAT等信号通路产生作用,从而促进细胞生长[11]。盐酸埃克替尼能与EGFR胞内结合,从而抑制其与ATP相作用,以促使酪氨酸激酶磷酸化[12]。且作为新兴靶向生物制剂,此药物具有高选择性,具有与细胞毒性药物完全不同的作用,它在进入肿瘤细胞后可有效结合小分子化合物,竞争ATP上的生长因子位点,从而有效阻碍激酶活性,进一步抑制EGFR受体表面的信号通路传导作用,阻碍了肿瘤细胞的生长及发展,从而降低肿瘤标志物水平,提高临床疗效,这在文兆明等[13]的研究中也有说明。
本研究显示,治疗后,观察组CD8+水平低于对照组,CD4+、CD3+、CD4+/CD8+水平均高于对照组(P<0.05)。两组不良反应发生率比较差异无统计学意义(χ2=0.375,P=0.540)。说明盐酸埃克替尼可显著提高患者免疫功能,且不增加药物不良反应。是由于病理状态下,机体为阻碍外来物质对机体产生的作用,免疫因子会出现异常分泌、过度表达的效果,以杀灭外界物质,主要以T淋巴细胞亚群主管的细胞免疫为主,CD3+作为成熟的T淋巴细胞表示机体的免疫功能状态,而CD4+、CD8+、CD4+/CD8+主要产生诱导、抑制、杀伤作用,当免疫因子水平过低常表示机体出现免疫抑制状态[14]。盐酸埃克替尼能有效竞争ATP上EGFR结合位点,抑制络氨酸酶激活,减少信号通路中细胞的繁殖,从而阻碍EGFR的进一步突变,抑制癌细胞的生长与转移及肿瘤细胞内血管的生成,进而提高免疫功能。李文格等[15]的研究中指出,此药物仅会出现轻微的皮疹、恶心等不良反应,其发生率为13.04%,安全性较高,笔者的研究与上述研究结果相似。
综上所述,盐酸埃克替尼可显著降低中晚期EGFR突变型非小细胞肺癌患者肿瘤标志物水平,提高患者免疫功能及临床疗效。
