保健食品原料中总砷及无机砷含量检测
2022-09-21何婷婷
何婷婷
(乌鲁木齐海关技术中心,新疆乌鲁木齐 830063)
近年来,药食同源产品在保健食品原料中的应用比例不断攀升,这些产品多为中草药类植物所制备而成。在中草药类植物的生长过程中,土壤中的砷元素会逐渐集聚在植株中造成一定程度的污染,对其含量进行检测至关重要。药食同源产品中砷元素的化合状态较多,因此需要从总砷含量和无机砷含量检测入手,实现更为准确的检测工作。
1 材料与方法
1.1 材料与试剂
选用人参作为实验样品,于东北某地采集,并经由当地科研机构鉴定后,阴干,低温保存待用。
硫脲、硼氢化钾、硝酸、过氧化氢、高氯酸、硫酸、氢氧化钠、维生素C、无水乙酸钠、磷酸二氢钠、EDTA、氨水和氢氧化钾,均为分析纯,并均采购自国药集团化学试剂有限公司。砷标准品溶液 (1000 mg/L),自国家标准物质研究中心取得。
1.2 仪器与设备
本次使用的实验仪器如表1所示。
1.3 实验方法
1.3.1 样品的前处理
在样品前处理环节中,实验人员按照 GB 5009.11—2014要求进行处理。①将样品放入电热恒温鼓风干燥箱中,设置温度为90 ℃,恒温鼓风干燥2 h。②干燥完成后,使用粉碎机将样品粉碎,过40目筛,并使用电子天平准确称取0.300 g样品,放置于微波消解罐中,加入7 mL硝酸,静置30 min。③将消解罐放入微波消解系统中,按照表2中的升温程序进行处理,同时微波消解系统保持1200 W功率运行,每个运行步骤的升温时间均维持5 min[1-2]。
在升温处理完成后,对处理后的样品采用湿法消解,此环节主要应用适量的硫酸、硝酸和高氯酸混合物,与样品充分混合后静置12 h,而后将混合体系放置于电热板上,迅速升温至200 ℃进行消解,消解过程中不断补加硝酸,确保消解环节的彻底。消解完成后对反应物进行冷却2次,冷却完成后,用水将上述溶液移至25 mL容量瓶中,再加入少量硫脲与维生素C的混合液,定容至25 min。以上环节全部结束后,在25 ℃条件下静置30 min,而后使用AFS分光光度计对液体中的总砷含量进行 测定。
在总砷含量测定完成后,进行无机砷的提取操作。①称取少量制备好的液体样品放置于塑料离心管中,加入适量浓度为0.15 mol/L的硝酸溶液后静置12 h。②将混合体系放置于恒温水浴锅中,设置温度为90 ℃,恒温2.5 h,并每30 min进行一次振摇。③恒温阶段完成后,将混合体系冷却至室温,并在离心机上进行15 min的高速离心。④离心后取上层清液,过液相色谱柱,以完成提取[3-5]。
1.3.2 检测条件设置
(1)设置电感耦合等离子质谱仪的检测条件,该设备以1550 W功率运行,并控制柱箱温度维持在30 ℃,其他参数的具体条件如表3所示。

表3 电感耦合等离子质谱仪检测条件设置
(2)对原子荧光光度计的相关参数进行设置,本次研究中,光度计采用As灯,灯光电流设置为 50 mA,同时光度计使用载气和屏蔽气,其流量分别控制为600 mL/min和1100 mL/min。
(3)对液相色谱柱的检测条件进行设置,色谱柱流速控制为1.000 mL/min,进样量控制为50.0 μL,使用适量的10 mmol/L无水乙酸钠、3 mmol/L硝酸钾、10 mmol/L磷酸二氢钠、0.2 mmol/L EDTA混合后,溶解于乙醇中,以此混合物作为流动相,对样品进行相关操作。
1.3.3 总砷及无机砷含量标准曲线测定
控制好各种检测条件后,首先吸取适量砷标准工作液,并将其等分为5组,每组分别加入不同体积的2%硝酸溶液,使得各组溶液的砷浓度分别为1.00 μg/L、 5.00 μg/L、10.00 μg/L、50.00 μg/L和100.00 μg/L,另准备一组等体积的2%硝酸溶液作为空白对照组,配制完成后,使用电感耦合等离子质谱仪进行检测。
在此基础上,进一步测定无机砷含量的标准曲线,此环节的基本步骤同前,但各组溶液的砷浓度变更 为2.50 μg/L、5.00 μg/L、10.00 μg/L、50.00 μg/L和100.00 μg/L。以标准工作液的浓度为横坐标,定量离子对峰面积为纵坐标,绘制标准曲线[6]。
2 结果与分析
2.1 标准曲线及及检出限
以标准工作液的浓度为横坐标,定量离子对峰面积为纵坐标,绘制标准曲线,拟合得到曲线方程。总砷标准曲线方程为y=4079.58x-315.23,相关系数为1.00。无机砷因化合价不同,存在两个标准曲线方程,三价砷的标准曲线方程为y1=26592.84x1+13113.02;五价砷的标准曲线方程为y2=62819.97x2+11512.83;两个标准曲线方程的相关系数均为1.000。
在此基础上,进一步确定总砷和无机砷的检出限。本次检出限的测定基于等离子质谱仪进行,首先取适量的1.00 μg/L的砷标准溶液进行测定,以3倍信噪比(S/N)计算检出限[7]。由此计算出总砷的检出限为 0.0008 mg/kg,无机砷的检出限为0.0006 mg/kg。
2.2 总砷含量的测定
取适量原料粉碎后的粉末样品,分别添加0.001 μg、 0.003 μg、0.010 μg的砷标准品,烘干后分别制备6组实验溶液,使用电感耦合等离子质谱仪对砷含量进行检测。结合标准曲线和元素响应值对砷含量进行计算,并以添加样品的回收率表示方法的准确度,以变异系数表示实验方法的精密度,具体计算结果如表4所示。
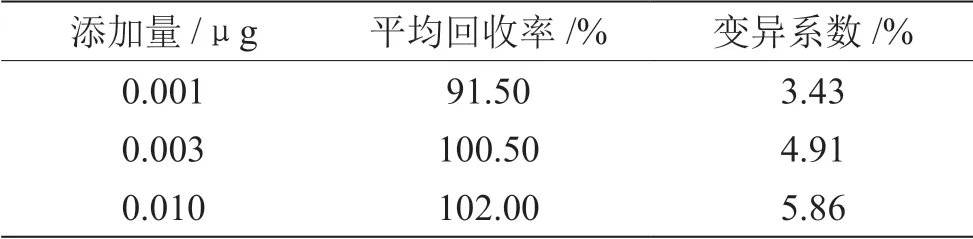
表4 添加回收率和变异系数检测结果(n=6)
从平均回收率和变异系数两方面来看,本次实验方法的准确度和精密度均符合检测要求。在此基础上,对本次实验方法的灵敏度进行检测,提取少量人参样品进行检测后,其砷含量为0.0265 mg/kg,RSD值为0.02%,而在相同条件下使用传统检测方法则未检出砷含量,证明本次应用的实验方法具有灵敏度较高和检出限较低的特点,对于痕量检测的作用更为显著。
在确定本次实验方法的有效性后,对本次所选择的人参样品中的总砷含量进行检测,检测结果为 (0.310±0.082)mg/kg,同时查阅国家标准GB 2762—2017所规定的食品污染物限量标准可知,保健食品原料中的总砷含量应当低于0.50 mg/kg。检测结果表明,本次选择的人参样品的砷含量并未超标,但其含量也难免存在相对偏高的情况。
2.3 无机砷含量的测定
取适量原料粉碎后的粉末样品,分别添加0.001 μg、 0.003 μg、0.010 μg的砷标准品,烘干后分别制备6组实验溶液,使用电感耦合等离子质谱仪对砷含量进行检测,根据检测曲线的峰面积对添加回收率和变异系数进行计算,结果见表5。
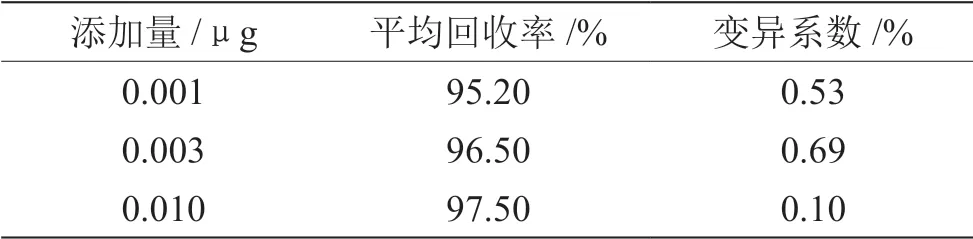
表5 无机砷平均回收率和变异系数计算结果
由表5可知,在本环节的检测中,无机砷的平均回收率为95.20%~97.50%,变异系数为0.10%~0.69%, 证明其准确度和精密度均符合检测要求。在此基础上,使用电感耦合等离子质谱仪对人参样品中的无机砷含量进行检测,检测结果如表6所示。

表6 人参样品无机砷含量检测结果(单位:mg/kg)
由表6可知,人参样品中无机砷对于总砷含量占比相对较高,超过70%,这表明在样品中存在不同比例的有机砷成分,以及一些风险未知的含砷化合物。相对而言,人参样品中的三价砷含量较低,五价砷含量较高,证明在这些人参的生长过程中,砷主要以五价砷的状态而存在。
3 结论
本研究采用微波消解-电感耦合等离子质谱法对人参样品中的总砷含量进行了测定,结果表明,该方法检测保健食品原料中砷含量有相对较高的准确度和精密度,能对保健食品原料中的总砷含量和无机砷含量实现较为准确的检测。预计该方法在食品检测领域会得到更多应用,以有效判断各种保健食品原料中的总砷和无机砷含量,为保健食品原料的产地鉴别、配制方法等方面研究提供更多的选择与借鉴参考。
