阿帕替尼合成路线综述
2022-09-19毛英宁刘梦欣张海洋李华良盛哲李占宇
毛英宁,刘梦欣,张海洋,李华良,盛哲,李占宇
(东北林业大学 化学化工与资源利用学院,黑龙江 哈尔滨 150040)
0 引言
癌症,也称为恶性肿瘤,是细胞生长失去正常调控机制所造成的,癌细胞的转移和扩散会导致人体正常机能受损,危害人类生命健康。目前,全球癌症发病人数和死亡率正在日益增长。在中国,胃癌发病率高居总体肿瘤发病的第三位[1]。胃癌早期病症并不明显,且较难被发现,许多患者错过了早发现、早治疗的机会,一经发现,已经进入癌症晚期阶段[2]。晚期胃癌通常以化疗、放疗手段进行治疗,对身体伤害性极大。与传统的放疗、化疗相比,靶向药物治疗具有更小的毒副作用、更好的治疗效果以及相对较长的耐受性[3]。阿帕替尼(Apatinib)是我国自主研制的一种小分子络氨酸酶抑制剂,是唯一一种口服治疗晚期胃癌的靶向药物。阿帕替尼能够特异性结合血管内皮生长因子受体(VEGFR-2)[4],阻断肿瘤血管生成,从而抑制癌症患者癌细胞的生长和转移,对晚期胃癌以及转移性胃癌具有很好的治疗效果。与奥沙利铂(Oxaliplatin)、替吉奥(Tegafur)等常见治疗胃癌的药物相比,阿帕替尼单药具有更好的治疗效果[5]。由此可见,绿色、高效的合成阿帕替尼具有十分重要的价值。
目前国内外已有很多制备阿帕替尼的工艺路线被报道,并且对合成方法不断改进。本文将详细对阿帕替尼的合成工艺路线进行归纳总结。阿帕替尼结构式如图1所示。

图1 阿帕替尼(Apatinib)结构式
1 阿帕替尼的合成路线
1.1 合成路线1
常见的路线多以2-氯-N-(4-1-氰基环戊基)苯基)甲酰胺6为关键中间体,关键中间体6与4-氨基甲基吡啶7发生取代反应,制得目标产物阿帕替尼8。由于最终产物后处理阶段需经过柱层析分离纯化,分离成本过高,且分离纯化过程较复杂,不适合工业化生产。关键中间体6的合成工艺路线如下所述。
A-1:如图2中路线所示,该路线以价廉易得的苯乙腈作为反应的起始原料[6],在相转移催化剂TEBAC和强碱氢氧化钠的共同作用下,与1,4-二氯丁烷反应生成中间产物2,混酸硝化得到1-(4-硝基苯基)-1-氰基环戊烷3,再用Fe还原得到中间体1-(4-氨基苯基)-1-氰基环戊烷4,最后与 2-氯烟酸酰胺化反应得到关键中间体6。
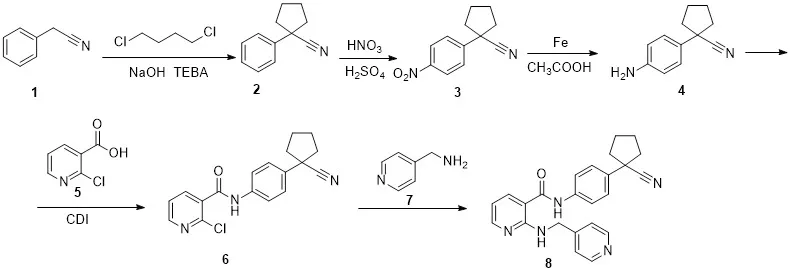
图2 以方法A-1合成阿帕替尼
A-2:随后,有路线[7]在此基础上对反应进行改进,如图3所示,以1,4-二溴丁烷代替1,4-二氯丁烷,以碱性更强的氢化钠为碱,并且加入碘化钠,使反应更容易进行。还原剂由Fe换成了三氯化铁,第四步酰胺化反应使用了反应活性更高的2-氯烟酰氯9。反应条件虽得到优化,但反应过程中仍存在很多问题。使用混酸硝化产物不具备选择性;铁还原硝基会产生大量的铁泥,污染性大。2-氯烟酰氯虽然有较好的反应活性,但成本大大增加;并且苯乙腈和1,4-二溴丁烷环合过程中氢化钠用量较大,实验操作过程中存在安全问题。由于最后一步有副反应发生,分离纯化过程较难,因此,此方法不适合工业化推广。
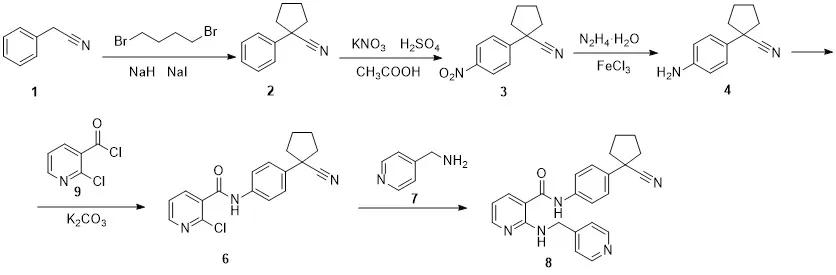
图3 以方法A-2合成阿帕替尼
A-3:如图4中路线所示,该路线以 l-(4-硝基苯基)-1-氰基环戊烷为起始原料[8],经过还原、酰胺化反应得到关键中间体6。此路线虽然步骤较短,但最终产物阿帕替尼8收率较低。并且反应过程中用到了价格昂贵的2-氯烟酰氯,导致反应成本大大提高,很难进行大规模工业化生产。

图4 以方法A-3合成阿帕替尼
A-4:如图5中路线所示,该路线以对硝基苯乙腈和2-氯烟酸为反应的起始原料[9],碱性条件下对硝基苯乙腈先经历环化反应,然后Pd/C甲酸胺还原得到中间体4;2-氯烟酸与二氯亚砜反应制得中间体2-氯烟酰氯9;最后,中间体4和9发生酰胺化反应得到中间体(2-氯-N-(4-1-氰基环戊基)苯基))6。第一步反应过程中碱的种类对反应过程有较大影响,最终使用5倍量的叔丁醇钾做碱,在碘化钠催化下制得中间体3,产率为92%。第二步Pd/C甲酸胺还原硝基,大大提高了反应的安全性和可操作性,同时收率可提升至98.4%。

图5 以方法A-4合成阿帕替尼
1.2 合成路线2
如图6中路线所示,赵建宏等[11]以 1-苯基-1-氰基环戊烷为起始原料,经硝化、还原得到中间体4;在HOBt和EDCI的作用下,中间体4与 2-氨基烟酸16经缩合制备2-氨基-N-(4-1-氰基环戊基)苯基)烟酰胺17,随后与 4-甲醛-吡啶被氰基硼氢化钠(NaBH3CN)还原制得最终产物阿帕替尼。该路线同样经历硝化、还原过程,并且原料2-氨基烟酸制备困难、价格昂贵,不利于工业化推广。

图6 以路线2合成阿帕替尼
1.3 合成路线3
如图7中路线所示,该路线以2-氯-3-吡啶甲酸甲酯为反应起始原料[10],在无机碱溶液中与化合物12反应得到中间体13;然后在叔丁醇钠的乙醇溶液中再与化合物14反应,经NaHSO3后处理得到最终产物阿帕替尼。该合成工艺路线短、过程简洁、反应条件简单、温和,但原料中4-重氮基甲基-吡啶和1-(4-溴苯基)-1-氰基环戊烷价格较高,制备难度大,不适合工业化生产。
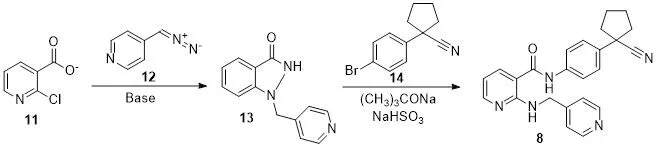
图7 以路线3合成阿帕替尼
1.4 合成路线4
如图8中路线所示,该路线以1-4-(叔丁氧羰基氨基)-苯基乙酸烷基酯为起始原料[12],经环合反应生成中间体20;在酸性条件下脱Boc得到1-(4-氨基苯基)-环戊烷甲酸烷基酯21;随后与2-氯烟酰氯进行酰胺化反应生成中间体22;再与4-氨基甲基吡啶反应得到中间体23;最后酯基经氨解、脱水反应制得目标产物阿帕替尼,反应收率为78.3%~80.0%。该路线在环合反应前对氨基进行上Boc保护,避免副反应发生。在整个过程中,原料价廉易得,反应设备安全,绿色环保、无污染,适合大规模工业化生产。
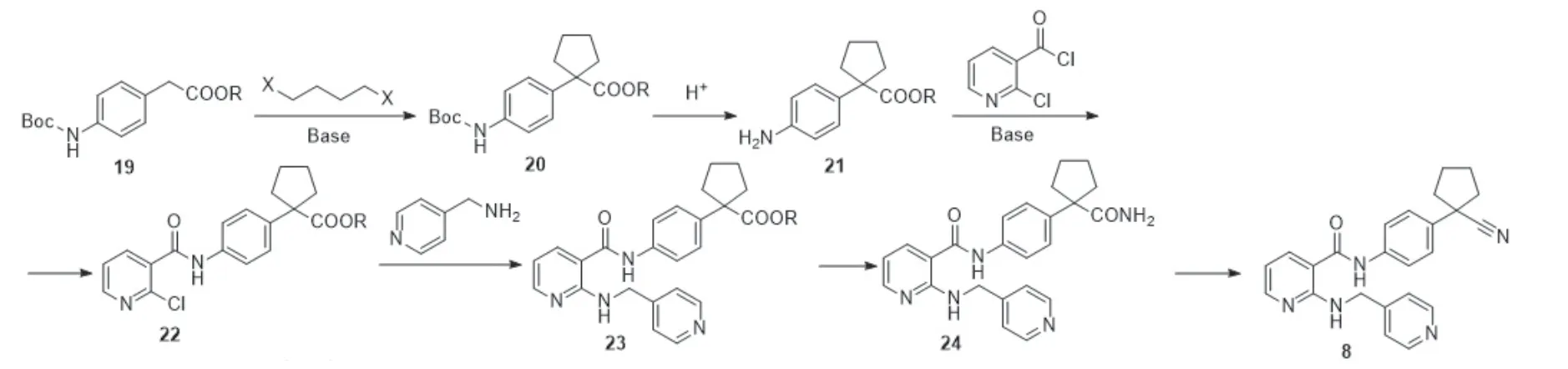
图8 以路线4合成阿帕替尼
1.5 合成路线5
如图9中路线所示,该路线以2-卤代-3-氰基吡啶25为起始原料[13],与4-氨基甲基吡啶经取代反应得到中间体26,随后经醇解反应得到中间产物27;其中,酯基再与化合物4经胺解化反应制备阿帕替尼。该路线起始原料中,由于氰基的邻对位活化效应,使得第一步取代反应更易进行,有效避免副反应发生;并且原料价廉易得、工艺流程简便;后处理简单,所得阿帕替尼的纯度高,液相纯度可高达99.96%;废水产生量少,绿色无污染;反应活性强、选择性高。

图9 以路线5合成阿帕替尼
1.6 合成路线6
如图10中路线所示,该路线以1-(4-氨基苯基)-1-氰基环戊烷4和丙二酸二酯28为起始原料[14],经过酰胺化反应制备中间体N-4-(1-氰基环戊基)苯基丙二酸单酯单酰胺29,再与4-氨基甲基吡啶经酰胺化反应得到中间产物30;随后与2-卤代丙烯醛31发生环化反应得到目标产物阿帕替尼。此路线为了使中间体4完全反应使用了过量丙二酸二酯,丙二酸二酯可通过减压蒸馏回收。该合成方法工艺流程简便、步骤少,三步就可制得最终产物;所用原料价廉易得;产生的废物少,安全绿色环保;副产物较容易除去,所制备的阿帕替尼液相纯度可高达99.96%,适合阿帕替尼工业化生产。

图10 以路线6合成阿帕替尼
1.7 合成路线7
如图11中路线所示,该路线相较于其他路线省去了一步酰胺化反应,直接以2-[(4-甲基)氨基吡啶]烟酸32为起始原料[15],经过酰氯化得到2-[(4-甲基)氨基吡啶]烟酰氯33,再与1-(4-氨基苯基)-1-氰基环戊烷进行胺解反应得到目标产物阿帕替尼。该路线得到的产物收率为94%,产物纯度为96%。此方法的酰氯化过程可利用多种酰氯试剂,例如碳酸三氯甲基酯、亚硫酰氯等。其中碳酸三氯甲基酯作为酰氯试剂时的反应温度高达130 ℃,反应能耗过高,且存在安全问题。
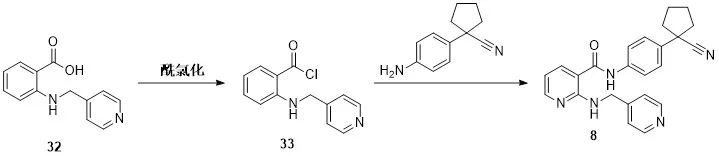
图11 以路线7合成阿帕替尼
2 结语
本文对当前报道的阿帕替尼合成路线进行了详细总结,各种合成方法的优缺点都有所差别。总体来说,阿帕替尼的合成路线整体改进方向为:使用廉价易得原料、缩短合成工艺路线、使用安全性高的反应装置、提高反应收率、开发温和、对环境友好的反应条件等。改进这些不足对阿帕替尼的高效合成提供很大帮助。
