从栝楼桂枝汤“异病同治”脑卒中和癫痫的网络靶标探讨其解痉作用机制
2022-09-13韩静蒋畅张继州邹俊胡娟
韩静,蒋畅,张继州,邹俊,2,胡娟,3
栝楼桂枝汤是张仲景的《金匮要略》中治疗外感热病引起的痉挛及内伤杂病中出现的抽搐、发痉、手足蠕动等症的经典方。方药由天花粉30 g、桂枝9 g、白芍9 g、甘草6 g、生姜9 g和大枣12枚组成,具有调和阴阳气血、柔润筋脉、养阴生津的功效。在临床实践中,该方用于治疗脑卒中后肢体痉挛,取得了显著的疗效[1-2]。该方在福建省第二人民医院使用已有十余年,临床疗效确切,已开发为院内制剂 (闽2013S0001)[3],主治脑卒中后痉挛性偏瘫、脊髓损伤后、下肢静脉曲张、帕金森病、小儿抽搐症、甲状腺功能亢进症、癫痫等出现肢体肌肉痉挛或震颤症状者。临床报道,栝楼桂枝汤不仅对脑卒中后肢体痉挛具有较好的疗效,也可用于治疗癫痫患者[4-5],改善症状并降低脑电图评分。
中医理论认为,不同疾病在其发展过程中,由于出现了相同的病机,可以辨证为同一证候,在治疗上可用同样的方法,即中药复方具有“异病同治”的功能,其基础是“证同治亦同”,“证”是治疗的关键。栝楼桂枝汤在中医临床实践中用于解除神经系统痉挛症状,所对的证是“痉证”。脑卒中后遗症患者中医证候表现为阴血亏虚、脉络受阻、筋脉失养,导致肢体痉挛拘急[6],采用栝楼桂枝汤主治。《金匮要略》中所述痉病“痉为病,胸满口噤,卧不着席,脚挛急,必齘齿”,与癫痫大发作全身骨骼肌持续收缩、项背强直、角弓反张基本相符[7],栝楼桂枝汤治疗癫痫的疗效亦在临床中得到证实。由此可见,栝楼桂枝汤具有“异病同治”的特性。
栝楼桂枝汤解痉作用的分子机制尚不明确,近年来,很多研究对栝楼桂枝汤干预脑缺血损伤的机制进行了探讨,发现该方对脑缺血损伤的细胞模型和动物模型的保护作用机制主要包括抗炎、抗凋亡、调节兴奋性和抑制性神经递质、促进神经发生及轴突重塑等[8-11]。然而,中药复方药味众多,成分复杂,作用靶标广泛,作为一个主要作用为缓解肢体肌肉痉挛或震颤症状的中药复方,上述研究尚不足以说明该方解痉作用的主要机制,若能从“异病同治”的角度对该方的解痉作用机制进行探讨,可在一定程度上缩小该方可能的作用靶标范围,对其解痉作用的核心机制有更清晰的认识。
近年来,网络药理学成为中药复方作用机制预测的新兴方法,其核心是以“网络靶标”为切入点,将方药与病证映射于生物分子网络,以网络为基础建立方药与病证的关联机制[12],通过网络拓扑结构分析预测中药作用的核心靶标及核心化合物。为了揭示栝楼桂枝汤解痉作用的核心药效机制,本研究采用网络药理学的研究方法探究该方“异病同治”脑卒中和癫痫的网络靶标,以期明确栝楼桂枝汤解痉作用的中心靶标通路,为后续药物的进一步开发提供理论依据。
1 材料与方法
1.1 栝楼桂枝汤的中药成分及靶标的收集 以栝楼桂枝汤各单味中药的拼音名为检索词,从中医药百科全书数据库(the encyclopedia of traditional Chinese medicine,ETCM)(http://www.tcmip.cn/ETCM/)中查询各单味药包含的化合物及其靶标信息[13]。查询2020版《中国药典》中各单味药的成分信息予以补充,并从中药系统药理学数据库(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)(http://tcmspw.com/tcmsp.php)获取相应补充成分的靶标[14]。最后在Uniprot数据库(https://www.uniprot.org/)中将所有靶标蛋白转换成标准基因名,建立数据集。
1.2 疾病靶标的预测 以“Stroke,Ischemic Stroke”“Cerebral Infarction”“Brain Ischemia”“Hemorrhagic Stroke”和“Epilepsy”为关键词,从DisGeNet(http://www.disgenet.org/)和MalaCards数据库(https://www.malacards.org/)中分别检索与脑卒中和癫痫相关的基因,建立脑卒中和癫痫疾病靶标数据集。
1.3 栝楼桂枝汤“异病同治”脑卒中和癫痫的靶标预测及靶标网络构建 采用Venny 2.1工具(https://bioinfogp.cnb.csic.es/tools/venny/index.html),将栝楼桂枝汤成分对应的靶标与脑卒中和癫痫相关基因绘制韦恩图,获得中药复方与疾病的交叉靶点,这些靶点可能是该复方治疗脑卒中和癫痫的相同潜在作用靶点。进一步采用STRING数据库(https://string-db.org/)对交集靶标进行蛋白相互作用分析,设置信度≥0.4为筛选标准,并将存在相互作用的靶标蛋白输入Cytoscape 3.6.0软件构建“靶标网络”。
1.4 基因功能及通路富集分析 采用DAVID 6.8在线工具(https://david.ncifcrf.gov/)对上述治疗靶标进行基因本体论注释(gene ontology,GO),并进行富集分析,同时进行京都基因和基因组百科全书(kyoto encyclopedia of genes and genomes,KEGG)通路富集分析,分类富集参数选择“Medium”。继而在Cytoscape 3.6.0软件构建“成分—靶标—通路”网络并进行网络分析,获得栝楼桂枝汤治疗脑卒中和癫痫异病同治的关键化合物和关键靶标及通路。
1.5 分子对接验证 选取1.4中分析获得的核心靶标及对其有调控作用的化合物进行分子对接验证。在PDB蛋白质结构数据库(https://www.rcsb.org)下载核心靶标蛋白质pdb格式的3D结构文件,通过PyMol(Ver.2.4)软件对受体蛋白进行去水分子及加氢处理。在PubChem数据库下载候选化合物的SDF格式结构文件,采用Chem 3D软件绘制三维结构,MM2力场优化构象后,保存为mol2格式文件,在AutoDockTools软件中转化为PDBQT 格式;采用AutoDock Vina(Ver.1.1.2)进行受体蛋白质与配体化合物的分子对接验证。
2 结 果
2.1 栝楼桂枝汤主要成分及对应靶标 栝楼桂枝汤由6味中药组成,各药材包含的主要成分经去重后共378个,相应的潜在靶标经去重后共886个(表1)。

表1 栝楼桂枝汤“成分—靶标”基本信息Tab.1 “Compound-target”basic information of Gualou Guizhi Decoction
2.2 栝楼桂枝汤治疗脑卒中和癫痫的共同靶标预测 在DisGeNet和MalaCards数据库中检索脑卒中和癫痫相关基因,分别获得脑卒中相关基因1 093个、癫痫相关基因1 239个,二者与栝楼桂枝汤的 886个靶标共存在45个交集靶标(图1)。

图1 栝楼桂枝汤与脑卒中和癫痫靶标的韦恩图Fig.1 Veen diagram of compound targets of Gualou Guizhi Decoction,stroke-related targets,and epilepsy-related targets
2.3 GO富集和KEGG通路富集分析 GO富集分析结果包括生物学过程(biological process,BP)、分子功能(molecular function,MF)和细胞组分(cellular component,CC)。栝楼桂枝汤治疗脑卒中和癫痫的45个共同靶标经DAVID在线工具分析,富集在16个聚类。聚类富集分数最高的簇如图2A所示,涉及的生物学过程主要有:离子型谷氨酸受体信号通路、化学突触传递、兴奋性突触后电位、N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptors,NMDAR)活性的调节等;涉及的分子功能主要有谷氨酸门控离子通道活性、离子型谷氨酸受体活性、NMDA谷氨酸受体活性等;细胞组分主要位于突触后膜、NMDA选择性谷氨酸受体复合物、突触后致密区和树突棘等。
KEGG通路富集分析显示,45个潜在作用靶标涉及的通路主要富集在2个聚类,聚类富集分数最高的簇包含14条通路,主要有肌萎缩性侧索硬化症、cAMP信号通路、Rap1信号通路、Ras信号通路、阿尔茨海默病、谷氨酸能突触、长时程增强、苯丙胺成瘾、多巴胺能突触、钙离子信号通路等(图2B)。
2.4 “成分—靶标—通路”网络构建及分析 采用Cytoscape 构建的栝楼桂枝汤治疗脑卒中和癫痫的“异病同治”的“成分—靶标—通路”网络见图3,共有191个节点、627条边。45个“异病同治”靶标由复方中132个成分靶向,平均连接度值为19.37,高于平均值的靶标有19个(表2)。对网络中的成分分析显示,靶向疾病靶标的栝楼桂枝汤化学成分的平均连接度值为2.23,高于平均值的成分有36个(表3),大部分来自天花粉、桂枝、白芍、甘草和大枣。
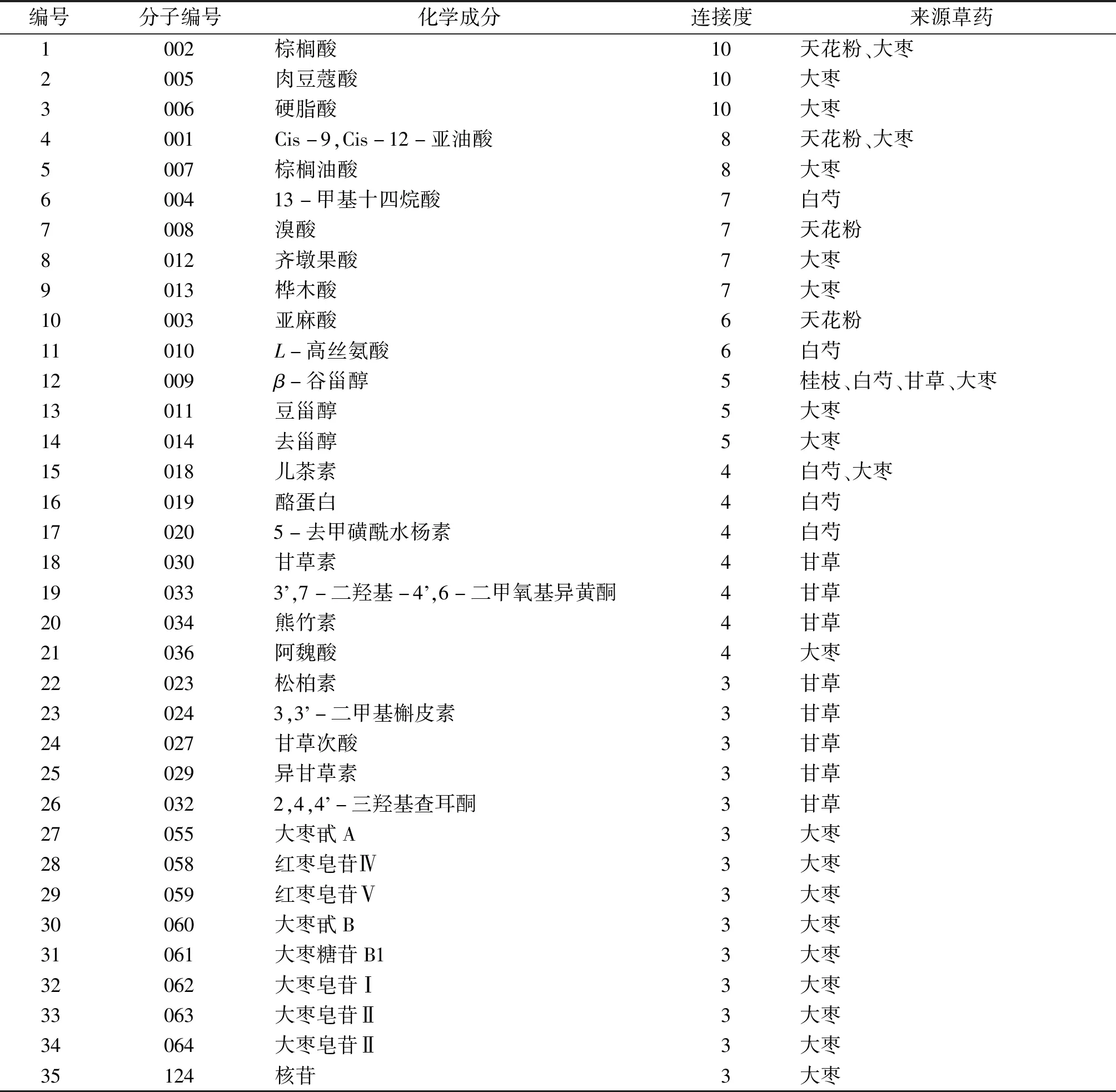
表3 栝楼桂枝汤“成分—靶标—通路”网络中的核心成分Tab.3 Main active compounds of Gualou Guizhi Decoction in the “compound-target-pathway”network
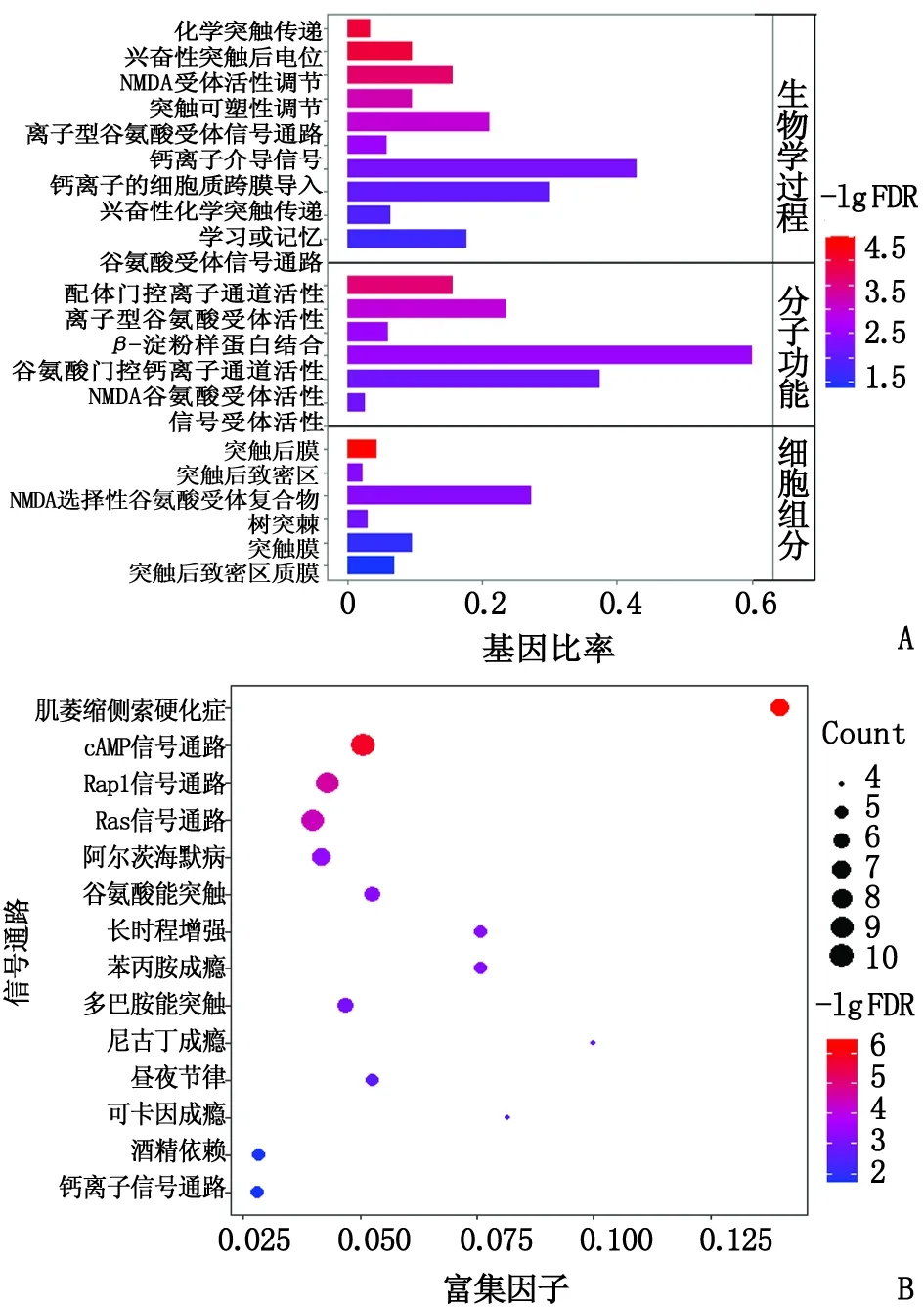
A:GO分析;B:KEGG通路分析。图2 栝楼桂枝汤治疗脑卒中和癫痫靶标的GO分析和KEGG通路分析Fig.2 Gene ontology and KEGG pathway analysis of the targets of Gualou Guizhi Decoction in the treatment of stroke and epilepsy
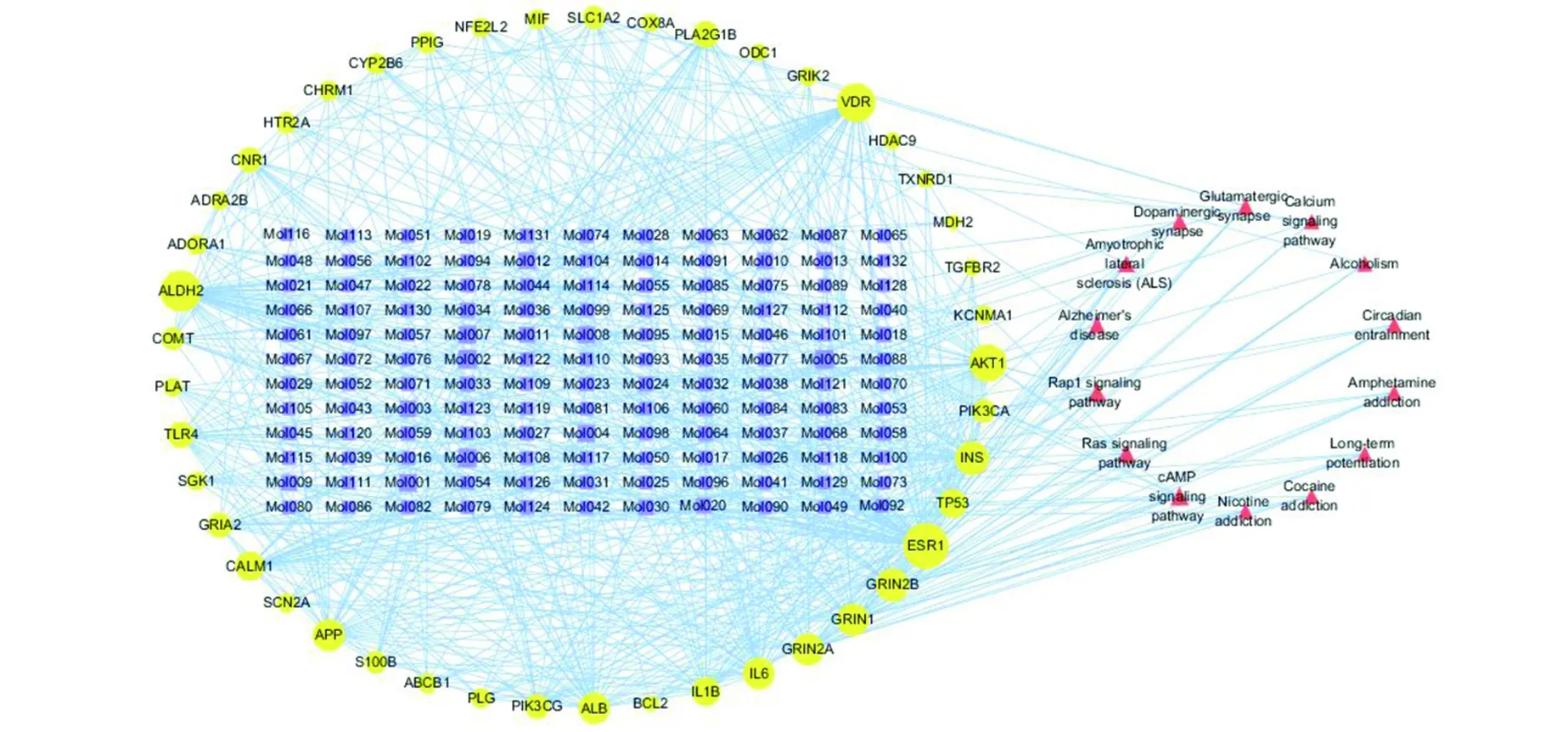
紫色:成分;黄色:靶点;红色:通路;节点:连接度的数量。图3 栝楼桂枝汤治疗脑卒中和癫痫的“成分—靶标—通路”图Fig.3 Compound-target-pathway interaction network of Gualou Guizhi Decoction in treating stroke and epilepsy

表2 栝楼桂枝汤“异病同治”的核心靶标Tab.2 Core targets of Gualou Guizhi Decoction in the effects of “treating different diseases with the same method”
进一步分析KEGG显著富集的14条通路及落在这些通路上的靶标构成的 “靶标—通路”网络,结果显示,每个靶标平均出现在3.78条通路中,而GRIN2A、GRIN2B、GRIN1、CALM1、GRIA2和AKT1等靶标所在通路数量均高于平均值,分别为14、13、13、10、9和4条。从“核心靶标—成分—草药”网络可见(图4),它们主要由来自天花粉、桂枝、白芍、甘草和大枣的β-谷甾醇、儿茶素、熊竹素、齐墩果酸、3’,7-二羟基-4’,6-二甲氧基异黄酮、皂苷元、亚油酸、棕榈酸、亚麻酸、13-甲基十四烷酸、肉豆蔻酸、硬脂酸、溴酸、L-α-氨基-δ-羟基戊酸、豆甾醇、桦木酸和去甾醇等23个成分所调控。
2.5 分子对接结果 核心靶标GRIN2A、GRIN2B和GRIN1均由β-谷甾醇、齐墩果酸、豆甾醇、L-高丝氨酸、桦木酸、去甾醇和溴酸所调节(图4),选取β-谷甾醇、齐墩果酸和豆甾醇3个活性报道较多的化合物分别与3个靶标进行分子对接。3个靶标分子与β-谷甾醇、齐墩果酸和豆甾醇的结合能大多小于-29.31 kJ/mol,其中β-谷甾醇和豆甾醇与GRIN1靶点的结合能较为相似,结合中心坐标略有差别;齐墩果酸和豆甾醇在与GRIN2A靶点的结合过程中虽具有较为相似的结合模式,但在结合能上存在差异(表4,图5)。
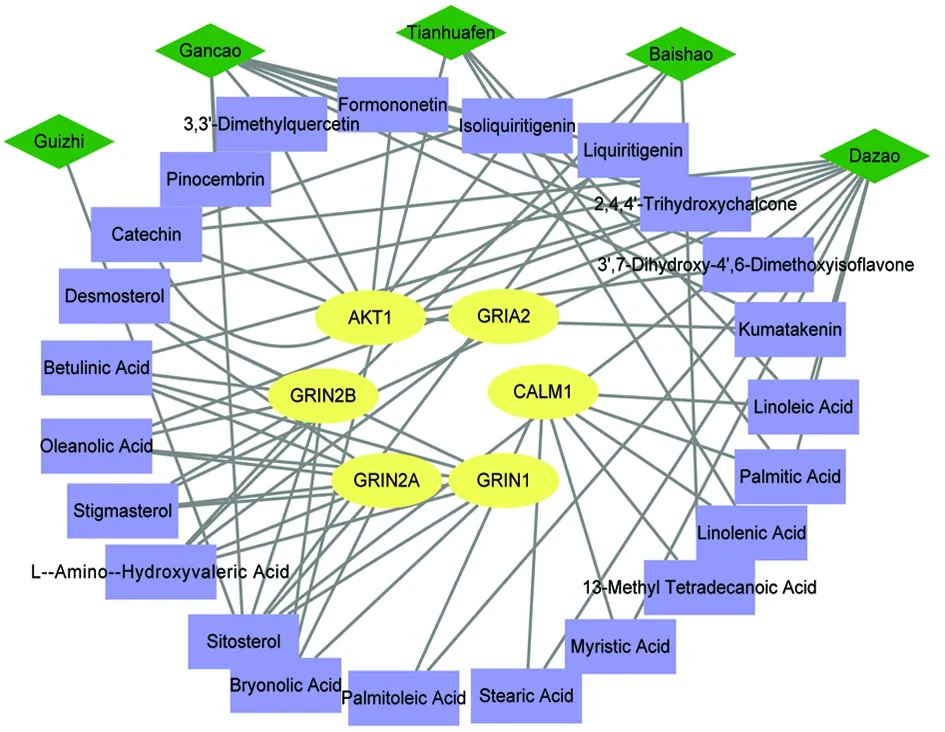
紫色:成分;黄色:靶点;绿色:草药。图4 栝楼桂枝汤“异病同治”的“核心靶标—成分—草药”网络图Fig.4 Core target-compound-herb interaction network of Gualou Guizhi Decoction in the effects of “treating different diseases with the same method”

表4 栝楼桂枝汤“异病同治”核心靶标—化合物结合能Tab.4 Binding degree of main active components to core targets of Gualou Guizhi Decoction in the effects of “treating different diseases with the same method”

蓝色虚线:氢键;灰色虚线:疏水相互作用;黄色虚线:离子相互作用。图5 化合物—靶点最优结合模式图Fig.5 Molecular docking diagram between compounds and core targets
3 讨 论
网络药理学研究方法由清华大学的李梢教授首次提出[15-16],由于其与中医药认识疾病的整体观、系统论的观点极为契合,近年来在中医药领域得到广泛应用。本研究应用网络药理学方法,通过构建栝楼桂枝汤“异病同治”脑卒中和癫痫的“中药—活性化合物—靶标”网络,进行网络拓扑结构分析,并结合分子对接验证,探讨该方解痉作用的关键靶标及通路,加深对其分子机制的认识。
脑卒中和癫痫的发病机制均十分复杂,发病均起于脑部损伤。虽发病机制不同,但二者发病后的肢体痉挛症状具有一定相似性,推测可能具有相似的分子生物学基础。本研究在DisGeNet和MalaCards数据库中获得脑卒中和癫痫的相关靶标分别为1 093和1 239个,共同靶标206个,这是2种疾病可“异病同治”的分子生物学基础。
在这些靶标中,有45个为栝楼桂枝汤化学成分所调节,说明栝楼桂枝汤可通过这些靶标发挥“异病同治”脑卒中和癫痫的作用。GO注释和KEGG通路分析结果显示,这些靶标的分子功能主要富集于对离子型谷氨酸受体通路的调节;细胞定位主要位于突触后膜、谷氨酸受体复合物等组分;涉及的信号通路主要聚集于神经系统疾病相关的通路,如谷氨酸能突触、长时程增强、多巴胺能突触、钙离子信号通路等。这些结果显示栝楼桂枝汤具有显著的神经系统药理活性。
对“靶标—通路”网络的分析显示,GRIN2A、GRIN2B、GRIN1、GRIA2、CALM1和AKT1等靶标出现在高于平均值的通路中,同时也是“成分—靶标—通路”网络的核心靶标,表明这些靶标可被栝楼桂枝汤中多味中药的多个成分共同调控,在靶标网络中具有重要作用。具体来看,GRIN2A、GRIN2B、GRIN1和GRIA2是离子型谷氨酸受体通路(GO:0035235)的主要组成部分,离子型谷氨酸受体包括NMDAR和α-氨基-3-羟基-5-甲基-4-异恶唑丙酸受体(α-amino-3-hydroxy-5-methyl-4-isoxazole propionate receptors,AMPAR)。GRIN2A、GRIN2B和GRIN1编码功能型NMDAR的组成亚基,GRIA2是AMPAR的组成亚基。谷氨酸受体通路在脑卒中和癫痫的发病中均为关键通路[17]。脑缺血后,细胞外谷氨酸蓄积,导致谷氨酸受体过度激活,从而引起细胞内钙超载和兴奋性神经元损伤。通过靶向谷氨酸受体功能调节抵消这种影响是脑缺血治疗研究领域的重要方向。离子型谷氨酸受体在癫痫的发作中起重要作用[18]。谷氨酸受体激动剂被证实在啮齿类动物模型中可引起癫痫发作,已有很多研究试图采用谷氨酸受体拮抗剂治疗癫痫发作,但结果并不一致。GRIN1是NMDAR的专有亚基,功能与NMDAR一致,其拮抗剂在体内显示出对缺血性神经元损伤的强大神经保护作用[19]。而GRIN2亚基赋予NMDAR独特的离子通道特性和细胞内运输途径,通过膜转运方式调节突触处NMDAR的数量,并与细胞内其他各种调节蛋白亚基发生特异性相互作用,从而控制生理病理进程[20]。CALM1钙调蛋白通过钙结合介导对大量酶、离子通道、水通道蛋白和其他蛋白质的控制。CAML1 mRNA的表达在缺血性脑卒中患者中显著增高[21]。
前期研究显示,栝楼桂枝汤可降低脑缺血大鼠脑脊液中谷氨酸水平,并下调脑组织AMPAR亚基和NMDA谷氨酸受体的蛋白质表达[8,22],作用于谷氨酸受体,干扰Ca2+与钙调蛋白的结合[23]。本研究分子对接验证显示,栝楼桂枝汤主要活性化合物齐墩果酸、β-谷甾醇、豆甾醇与NMDAR亚基GRIN1、GRIN2A和GRIN2B均有结合。分子对接的结合紧密程度由结合能体现,结合能数值越小,表明两者之间的结合越紧密。本研究靶标分子与主要活性化合物的结合能大多小于-29.31 kJ/mol,表明受体蛋白质与配体分子之间有较好的结合。这些结果与前期研究报道相互印证。回顾文献可发现,齐墩果酸是五环三萜类化合物,具有显著的神经系统药理活性,对脑缺血再灌注大鼠具有显著神经保护作用,可减少脑缺血所致的神经细胞凋亡[24];还有研究发现,齐墩果酸可延长癫痫发作潜伏时间,通过抗炎抗氧化起神经保护作用[25],通过维持海马突触可塑性改善Aβ诱导的AD大鼠记忆丧失[26],减弱NMDAR拮抗剂MK-801诱导的小鼠精神分裂症样行为[27]。此外,研究发现,含有β-谷甾醇和豆甾醇的药用植物Aloysiatriphylla可通过NMDAR发挥抗焦虑作用[28]。本研究AutoDock可视化分析显示,NMDAR亚基与齐墩果酸和β-谷甾醇等化合物之间有紧密的化学键连接,说明栝楼桂枝汤可通过这些成分作用于NMDAR,发挥抗痉挛作用。
此外,本研究结果还显示,在“化合物—靶标—通路”网络中高于平均度值的靶标有19个,均是能被栝楼桂枝汤中多味中药和多个成分共同调控的重要靶标。其中GRIN2A、GRIN2B、GRIN1、GRIA2、APP、CNR1和CALM1为神经系统疾病相关靶标,AKT1、IL-6、IL-1β、TLR4和PI3CG参与炎症反应,ESR1、ALDH2、INS、ALB和PLA2G1B为内分泌及代谢相关靶标。已有报道栝楼桂枝汤可调节癫痫患者血清IL-6和IL-1β的表达水平[29],但目前尚未见栝楼桂枝汤对APP、CNR1、TLR4及内分泌代谢相关靶标调节的直接报道。这些研究结果表明,栝楼桂枝汤作为一个中药复方,其作用是多靶点、多方向的,除了能调节离子型谷氨酸受体通路,还可能通过其他机制发挥解痉作用,值得进一步深入研究。
综上,本研究网络药理学分析结果表明,栝楼桂枝汤具有神经系统药理活性,作用于离子型谷氨酸受体活性调节通路中的GRIN2A、GRIN2B、GRIN1、CALM1和GRIA2等靶标是该方“异病同治”脑卒中后肢体痉挛和癫痫的关键分子机制。该方主要成分β-谷甾醇、齐墩果酸、豆甾醇等化合物是其发挥解痉作用的活性物质。除此之外,栝楼桂枝汤还可参与调节一氧化氮生物合成通路、炎症及内分泌代谢相关通路等,从多靶点对疾病网络进行调节。本研究基于网络药理学的分析方法,为栝楼桂枝汤解痉作用的机制研究提供了新的思路。然而,本研究作为一项网络药理学预测研究,尚存在一定局限性。本研究所获取的中药复方成分靶标来自数据库预测,后续还将开展基础实验佐证,据此对其确切机制进行进一步的深入探索。
