蝎毒素BmK M2的分离鉴定及其电生理活性研究
2022-09-07陈永根卢悟广
桑 明,陈永根,周 谦,曹 鹏,2*,卢悟广,2**
(1南京中医药大学附属中西医结合医院,南京 210028;2南京中医药大学药学院,南京 210023)
东亚钳蝎(Buthus martensiiKarsch,BmK)作为传统医药用于脑卒中、癫痫、抽搐等疾病的治疗已经有几千年的历史[1-2]。研究表明,蝎毒的活性物质主要是作用于Na+、K+、Cl-、Ca2+离子通道的毒素多肽。其中短链毒素由29 ~ 39 个氨基酸残基组成,含有3 对或4 对二硫键,主要作用于K+通道或者Cl-通道。作用于Na+离子通道的长链毒素主要由60~70 个氨基酸残基组成,并含有4 对二硫键。这些靶向离子通道的毒素不仅可以作为药物先导分子进入深入研究,还可以作为新型离子通道探针用于离子通道结构功能的研究。因此,分离纯化这些毒素多肽,并解析其结构与功能具有重要意义。
电压门控Na+通道在伤害(疼痛)刺激的传导和疼痛信息的传递中起着重要作用。伤害感受器是分布在周围神经中的感觉神经元,其主要表达Nav1.6、Nav1.7、Nav1.8 和Nav1.9 通道亚型[3-5]。其中每个通道亚型在疼痛信号传导中的作用由其生理特性和表达模式决定[3]。有研究表明,在特异性敲除小鼠伤害性感受器Nav1.7 后,小鼠对机械痛和热痛的敏感性均有不同程度的下降[6]。另有临床研究表明,患有慢性神经性疼痛患者的受损部位Nav1.8 表达过多[7],说明Nav1.7 和Nav1.8 与痛觉感受及病理性疼痛有着密切关联。因此开发针对Nav1.7 和Nav1.8 通道的探针或者抑制剂,对于研究其结构与功能并开发靶向药物具有重要的意义。但是,要鉴定出针对Nav1.7 或Nav1.8 具有强抑制作用而不影响其他Na+通道亚型的化合物一直是一项挑战。
截至目前,东亚钳蝎蝎毒中已报道有至少34条α毒素或者同源多肽[8],但是仅有13条α毒素的结构和功能得到了电生理和生化试验的确认[9]。尚有许多毒素没有被发现或没有被进行深入研究。例如α毒素作用的Na+通道亚型、选择性、作用机制等等。在已鉴定的东亚钳蝎毒素中,α 毒素BmK I 可通过激活Nav1.8 产生痛觉超敏[10]。BmK AGAP 可通过抑制Nav1.7 和Nav1.8 产生镇痛效果[11]。这些研究表明,由于东亚钳蝎毒素的镇痛作用,其毒素成分以及结构功能可能不同于其他种类蝎子来源的多肽毒素,因此值得进一步挖掘。
最近的研究表明,东亚钳蝎粗毒可以通过直接增强Nav1.7的活性产生致痛作用[12]。该研究表明东亚钳蝎毒液可以作为Nav1.7的探针库用于新型Nav1.7调节剂的筛选[12]。本研究从东亚钳蝎蝎毒中分离鉴定了一种Na+通道毒素,其序列与基于晶体学分析鉴定的BmK M2序列一致[13],并且与已报道的多条α 毒素具有较高的序列一致性。通过电生理测试和行为学实验发现,BmK M2 可通过调控Nav1.7 产生致痛活性。同时BmK M2 也可作为一种新型Na+通道探针,用于Na+通道结构与功能研究和靶向Na+通道的镇痛药物研究。
1 材 料
1.1 药品与试剂
SephadexG-50(美国GE Healthcare Life Sciences公司);三氟乙酸(TFA,色谱级,上海罗恩试剂);乙腈(CAN,德国Merck Drugs&Biotechnology 公司);KCl、MgCl2、CaCl2(分析纯,南京化学试剂股份有限公司);LipofectamineTM3000 转染试剂(L3000150,美国Thermo Fisher Scientific 公司);BCA 蛋白浓度测定试剂盒(碧云天生物技术研究所);生物技术蛋白质组学试剂盒(TO-760R00)、激光生物实验室MALDI校准套件(TO-724R00)、蛋白纯化回收试剂盒(KLANG,KL121208-50)(日本岛津公司);GpTx-1(一种Nav1.7 特异性抑制剂)由北京大学深圳研究院陈超博士赠送。其余试剂均为市售分析纯。
1.2 仪 器
AKTA 蛋白纯化系统、XK26-1000 色谱柱(美国GE Healthcare Life Sciences 公司);Milli-Q Biocel超纯水仪(美国Millipore 公司);Nanodrop 1000 紫外可见光分光光度计(美国Thermo 公司);C18反向色谱柱(4.6 mm × 250 mm,5 μm,大连依利特分析仪器有限公司);E2695 高效液相色谱仪(美国Waters 公司);落地式高速离心机(德国BeckmanCoulter 公司);pH 计(上海仪迈仪器科技有限公司);Olympus 倒置显微镜(日本奥林巴斯公司);MF-830 电极抛光仪(日本Narishige 公司);火抛光电极(美国World Precision Instruments 公司);水平电极拉制仪P97、右手自动微操MP-225(美国Sutter 公司);数模转换器Digidata 1550、单探头超低噪声膜片钳放大器Axon 200B(美国Molecular Devices 公司);ALA-VM8 全自动灌流系统(美国ALA 公司);Von frey 电子机械痛检测仪(美国IITC公司)。
1.3 质粒、细胞与动物
大鼠Nav1.8 表达质粒(rNav1.8)由上海生命科学研究所鲍岚研究员赠送;东亚钳蝎(产地陕西,经南京师范大学戴建华教授鉴定为东亚钳蝎);人Na+通道Nav1.7 稳转细胞株hNav1.7-HEK293 Cell Line 及Nav1.8 基 因敲 除小 鼠(Nav1.8 KO mice)由美国耶鲁大学医学院Stephen G.Waxman教授赠送;野生型C57BL/6J 小鼠,雄性,6 周龄,体重(20±2)g,购于常州卡文斯实验动物有限公司,合格证号:SCXK(苏)2021-0013;鼠神经母细胞杂交瘤细胞ND7/23细胞购于宁波明舟生物科技有限公司;rNav1.8-ND7/23 细胞利用LipofectamineTM3000 将rNav1.8 质粒转染至ND7/23 细胞获得。所有动物实验均符合动物伦理委员会标准。
2 方 法
2.1 BmK M2的分离纯化
利用电刺激法提取东亚钳蝎毒液,具体方法参考文献[12]进行。然后称取东亚钳蝎粗毒干粉1 g 于10 mL的玻璃样本瓶中,加入PBS 8 mL,4 ℃溶解过夜,使其充分溶解。低温(4 ℃)12 000 r/min离心30 min,然后用0.22 μm 滤膜过滤。使用PBS平衡SephadexG-50 凝胶过滤色谱柱,然后取滤液上样,同时打开HPLC 系统紫外检测器,在215 和280 nm 处测定吸收度,流速为0.3 mL/min,上样完成后用PBS 进行洗脱,利用自动收集装置收集各峰。将SephadexG-50 收集到的蝎毒组分P12 加入终浓度为0.2%海藻糖,进行冻干。冻干粉加入去离子水重新溶解至终浓度为5 g/L,低温(4 ℃)12 000 r/min 离心30 min,上清液用0.22 μm 滤膜过滤。然后使用HPLC 系统及C18反相HPLC 柱对过滤后的样品进行分离。在215 nm 波长处测定吸收度。蛋白分离使用的流动相是A(0.1%的三氟乙酸水溶液)和B(0.1%的三氟乙酸乙腈溶液),流速为1 mL/min。洗脱程序如下:0 ~ 5 min,95% ~90%,A;5~85 min,90% ~60%,A;85~85.1 min,60% ~ 95% A。分离得到的蛋白多肽峰冻干后存于-80 ℃备用。SephadexG-50 分子筛图谱参考本课题组前期的工作[14]。
2.2 多肽指纹图谱和氨基酸测序分析
将经HPLC 纯化后冻干的P12 用去离子水溶解后进行15%SDS-PAGE电泳,之后将目的蛋白条带切割,然后利用蛋白回收试剂盒回收多肽。多肽样品利用飞行时间质谱检测相对分子质量,然后采用岛津生物技术蛋白质组学试剂盒按照标准流程进行还原、烷基化、酶解,最后酶解肽段经MonoTip C18脱盐后浓缩上样,并利用岛津激光生物实验室MALDI校准套件进行校正。肽质量指纹图谱信号(PMF)用蛋白组学质谱分析软件Mascot上传至蛋白质序列数据库SWISS-PROT 进行肽段序列的分析,完成蛋白鉴定。N末端氨基酸测序参考本课题组前期工作进行[15]。
2.3 BmK M2的同源模建
同源模建参考使用Accelrys Discovery Studio 4.1 软件,并利用BmK M1 的。晶体结构(PDB ID:1SN1)作为模板对BmK M2 进行模型构建。然后对最佳同源模型进行MD 模拟,在AMBER 12 软件中优化得到模拟最佳的3D 结构,详细步骤见文献[16]。
2.4 电生理活性检测
BmK M2的电生理活性在hNav1.7-HEK293及rNav1.8-ND7/23 细胞上检测。所使用的细胞浴液及电极内液配方参考本课题组前期工作配制[12]。使用前加入河豚毒素(TTX,300 nmol/L)封闭ND7/23 细胞内源性Na 电流。使用Axopatch 200B 放大器在全细胞电压钳模式设置中记录电压门控Na+通道电流。拉制电极入水电阻控制在0.8 ~ 1.5 MΩ。负压形成高阻封接破膜后,串联电阻补偿85% ~90%消除电容瞬变后开始记录。补偿后的细胞稳定5 min 后,使用Clampex 10.5 软件,设置并运行刺激方案。对于Nav1.7 电流-电压实验,细胞保持在-120 mV 并逐步通过一系列步阶电压刺激(-80 至+60 mV,以5 mV 为增量,每个增量持续100 ms)。以内向电流峰值(I)和步阶电压(V)拟合I-V曲线。进一步确定每个细胞的反转电位(Vrev),并通过使用方程G=I/(V-Vrev)计算每个测试步阶电位(V)对应的电导(G)。激活曲线以每个脉冲电压的电导和脉冲电压为变量,通过玻尔兹曼方程拟合得到:
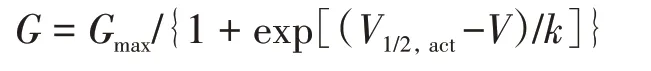
其中Gmax是最大Na 电导,V1/2,act是50% Na+通道被激活的电位,k是斜率因子。
对于稳态失活实验,细胞钳制在-120 mV,通过一系列持续500 ms的脉冲电压刺激(-100 至-10 mV,以10 mV 为增量)实现稳态快速失活,其余未失活的通道通过40 ms 步进去极化激活至-10 mV。快速失活曲线以玻尔兹曼方程拟合得到。I/Imax=Rin+(1-Rin)/{1+exp[(V-V1/2,inact)/k]},其中Imax是最大Na 电流V1/2,inact是50%Na+通道失活的电位,k是斜率因子,Rin为不发生失活的通道的比例,在统计软件GraphPad Prism 中用玻尔兹曼方程进行拟合,A1设为1,A2即为Rin。
对于关闭状态下的快速失活曲线,刺激方案参考Herzog 等[17]的工作进行:细胞钳制在-100 mV,前脉冲去极化至-70 mV,每次刺激逐渐增加前脉冲时间(时间从2 ms 增加至200 ms),然后给予去极化至0 mV,持续时间为20 ms的测试脉冲。以每个电流波的I/Imax和每次刺激的失活持续时间为变量作指数方程采用单指数拟合得到关闭状态下的快速失活曲线,并以获得的τ值进行作图。
2.5 动物行为学实验
选用野生型C57BL/6J 雄性小鼠(6 周,20 ± 2 g),共3组,每组5只,足底(左后肢注射体积10 μL)分别注射BmK M2(50 nmol/kg)7 μg 和BmK M2(50 nmol/kg)7 μg + GpTx-1(5 nmol/kg)。选 用Nav1.8 KO 雄性小鼠(6 周,20 ± 2 g)5 只,足底注射BmK M2(50 nmol/kg)7 μg。统计足底注射后30 min 内小鼠舔足和抖足的次数。小鼠舔足实验结束后,当疼痛行为(舔足、抖腿、悬腿)明显减少或消失,将待测小鼠置于金属网格上适应5 ~ 10 min,然后用Von frey 电子机械痛检测仪对给药足底机械阈值进行测试,当小鼠受到机械针刺激后会产生自然缩足(迈步不计算在内)时的力量阈值为其缩足阈值(以质量单位克计算),每只小鼠共重复测试5次,并以平均值作为最终参考值。
2.6 统计分析
所有统计数据均采用Origin 8.5 软件进行统计分析,GraphPad Prism 7.0 软件进行制图。数据表示为平均值±标准误差(SEM)。计量资料符合正态分布的使用进行统计描述;不符合正态分布则用M(P25,P75)描述。符合正态分布与方差齐性的两组计量资料采用两独立样本t检验;多组资料则采用One-Way ANOVA 和Tukey test 分别做两组间统计。P<0.05认为差异具有统计学意义。
3 结 果
3.1 BmK M2的分离与鉴定
为了分离东亚钳蝎蝎毒中的多肽,首先利用SephadexG-50 分子筛对提取的粗毒进行了分离。然后进一步对SephadexG-50分子筛的P7峰进行了HPLC 分离。HPLC 图谱中显示有23 个峰,其中峰形完整且可能为高纯度单体的有14个峰(图1-A)。在这14个单峰中,P12(红圈标注)的丰度较高。飞行时间质谱结果提示P12相对分子质量约为7 235(图1-B)。进一步通过N 末端氨基酸测序以及多肽指纹图谱鉴定发现P12 与已鉴定序列的α 毒素BmK M2 氨基酸序列一致(Uniprot no.P58488),由64 个氨基酸组成,包含4 对二硫键(图1-C)。这些结果提示,P12 是BmK M2,在蝎毒中的含量为0.5%~1%。
3.2 BmK M2的序列比对和同源建模
为进一步明确BmK M2 的结构并为其潜在生物学活性探索提供依据,将BmK M2 与多种已知Na+通道蝎毒素进行了序列比对。比对结果显示,BmK M2 的氨基酸序列与已发现的Na+通道毒素BmK M1、BmK M3、BmK M4、BmK M8、OD1、AaH2具有较高相似性,其中与BmK M1、BmK M3、BmK M4 的序列同源性分别高达96.88%、80.95%和81.25%,与BmK AGAP(Uniprot ID:Q95P69)的序列同源性为68.75%(图2-A)。进一步以已测定结构的BmK M1 作为模板对BmK M2 进行同源建模发现,BmK M2是一种典型的长链α毒素,具有α螺旋构成的核心区域以及β-转角构成的柔性C 端。与其他α 毒素类似,BmK M2 的结构被4 对二硫键(C12-C63、C16-C36、C22-C46、C26-C48)所稳定(图2-B)。尽管BmK M2与另两种已知的哺乳动物Na+通道毒素AaH2 及OD1 的序列同源性分别为59.09%和75%,但BmK M2 与AaH2 的3D 结构几乎一致。这些结果提示BmK M2可能与AaH2的活性类似,是一种潜在的Na+通道调节剂[9]。

Figure 1 Purification and identification of BmK M2
3.3 BmK M2 对Nav1.7 的I-V 曲线以及峰电流的影响
Nav1.7 表达于外周神经,是与疼痛信号传递最为密切的Na+通道亚型[18]。本研究利用全细胞膜片钳检测了BmK M2 对Nav1.7 电压-电流曲线的影响。结果显示BmK M2 显著增强电压门控Na+通道Nav1.7 的激活(图3-A)。如图3-B 所示:1 μmol/L BmK M2 可显著改变Nav1.7 初始激活电压阈值,激活电压和电流的反转电位,使得Nav1.7的I-V曲线左移(ΔV= -7 mV,n= 14,P<0.05)。但-10 mV 单电压刺激显示,BmK M2 对Nav1.7 的峰电流没有显著影响(图3-C)。该结果表明,BmK M2与其他已报道的α 毒素如AaH2、OD1等活性类似,但与BmK AGAP不同。
3.4 BmK M2对Nav1.7激活及稳态失活的影响
进一步研究了BmK M2 对Nav1.7 的激活和稳态失活曲线的影响。电生理结果显示,BmK M2在-140 mV 至-70 mV 期间加速失活,在-70 mV 至0 mV 期间延迟失活(图4-B)。加药前后的ΔV1/2fastinact(半数稳态快速失活电压)为-7.3 mV(n= 15,P<0.05)。同样的,如图4-C 所示,BmK M2 能够显著增强Nav1.7 的激活活性,使Nav1.7的激活曲线向超极化方向移动(左移,ΔV1/2,act=-8.6 mV,n=12,P<0.05)。

Figure 2 Homology modeling and molecular dynamics of BmK M2

Figure 3 Effect of BmK M2 on Nav1.7 expressed in HEK293 cells

Figure 4 Effect of BmK M2 on the activation and steady-state fast inactivation curves of Nav1.7 channels
3.5 BmK M2对Nav1.7关闭状态下失活的影响
电压门控离子通道的失活是内在的自动调节过程,是控制动作电位的发生和形状以及在可激发组织中建立发射模式所必需的[19]。在强去极化膜电势下的打开状态(开路状态灭活,OSI),以及在超极化和中度去极化膜电势下的开路前关闭状态(闭路状态灭活,CSI)都可能导致失活[19]。电压门控Na+通道的CSI可动态调节感觉神经元兴奋性并调节突触强度的变化[17]。但是关于蝎毒素对Na+通道亚型的CSI的影响的研究则甚少。电生理结果提示:给予1 μmol/L BmK M2 可显著减少Nav1.7 CSI的时间常数,使得通道开放的时间延长,持续电流增加。如图4-C 所示,给药前Nav1.7的CSI 时间 常数τ 在46 ms 左 右;给予1 μmol/L BmK M2 后τ 减少到9 ms 左右(n= 13,P<0.05)。这些结果提示,BmK M2 可能会增加DRG 神经元动作电位的发放频次和持续时间,产生致痛作用。

Figure 5 Effect of BmK M2 on the closed state fast inactivation of Nav1.7 channels
3.6 BmK M2对Nav1.8电生理活性的影响
Nav1.8 是表达在外周感觉神经元上的另一种主要的TTX-R Na+通道亚型,该通道的激活对于维持动作电位的重复发放至关重要[20]。之前有研究表明东亚钳蝎蝎毒素BmK I 可通过激活Nav1.8 引起痛觉过敏[10],而BmK I 与BmK M2 有较高的序列同源性,因此进一步检测了BmK M2 对Nav1.8 电生理活性的影响。结果图6-A、6-B 和6-C 所示,BmK M2 不影响Nav1.8 的电压依赖性激活和快速失活,也不能抑制其峰值电流(n= 13,P>0.05)。该结果表明BmK M2具有一定的选择性,为后续开展BmK M2 与Nav1.7 的相互作用研究提供了基础。

Figure 6 Effect of BmK M2 on Nav1.8 expressed in ND7/23 cells
3.7 BmK M2诱导Nav1.7依赖的疼痛行为
BmK M2 抑制Nav1.7 的失活将会降低动作电位发放阈值,从而诱发疼痛行为。因此,进一步测试了BmK M2 的致痛活性。结果提示,在野生型C57BL/6J(WT)小鼠后爪注射BmK M2 后可引起剧烈的疼痛行为和机械痛敏感(图7)。BmK M2引起的疼痛缩足行为在15 min时达到峰值,每5分钟的缩足次数达到70±12 次(n=5,P<0.001)。机械痛阈值低至1.22±0.34(n=5,P<0.001)。共同注射GpTx-1 显著降低了BmK M2 引起的疼痛缩足行为(图7A-7B,n= 5,P<0.001),每5 分钟的缩足次数仅为15±3次(n=5,P<0.001),并且逆转了BmK M2引起的机械痛敏感(图7-C)。机械痛阈升高至5.25±0.13(n=5,P<0.001)。在Nav1.8 KO 小鼠中,BmK M2 依然可以诱导显著的疼痛行为和机械痛敏感(图7,n=5,P<0.001)。这些结果表明BmK M2 的致痛行为可能是Nav1.7 依赖的,而与Nav1.8无关。

Figure 7 BmK M2 evoked pain response is abolished by Nav1.7 specific blocker(± s,n = 5)
4 讨 论
本研究采用Sephadex G-50分子筛和高效液相色谱技术从陕西东亚钳蝎蝎毒中纯化出蝎毒组分P12。利用多肽指纹图谱和氨基酸测序技术发现蝎毒组分P12 的氨基酸序列与基于晶体学分析预测的BmK M2 序列一致[12]。该毒素相对分子质量为7 235.59,含有4 对二硫键,然后利用同源建模技术构建了BmK M2 的分子模型。序列比对结果显示,BmK M2 的序列与已发现的Na+通道毒素BmK M1、BmK M3、BmK M4、BmK M8、OD1、AaH2具有较高的序列和结构相似性,均在N端和C端含有一段保守区域。因此该毒素是一种潜在的新型Na+通道调节剂。
Nav1.7 和Nav1.8 是外周神经中传递疼痛信号的两个主要Na+通道亚型,均在疼痛机制中起着重要作用,其中Nav1.7 在动作电位形成和传递中扮演关键角色。本研究结果显示,BmK M2 对Nav1.7 的峰值电流无显著影响,但可延迟Nav1.7的稳态以及关闭状态下失活,延长Nav1.7 的开放时间,增加其持续电流,增强DRG 神经元的动作电位(AP)的发放,从而导致痛觉超敏。而BmK M2不能抑制外周神经中另一个主要通道Nav1.8的峰值电流,也不会影响Nav1.8 电压依赖性激活和快速失活。进一步的行为学实验证实,BmK M2 可能通过Nav1.7而不是Nav1.8产生疼痛行为。
本研究结果表明,BmK M2 可作为一种新型的Na+通道探针用于Nav1.7结构和功能研究,这为后续开展BmK M2 与Nav1.7 的相互作用研究提供了理论基础。
