人工智能超声对乳腺癌早期诊断及预后评估的价值分析
2022-09-06淦凤萍肖雪花胡美娟
淦凤萍,肖雪花,胡美娟
九江学院附属医院超声科,江西 九江 332000
乳腺癌主要是乳腺上皮细胞在多种致癌因素影响下发生癌变,从而无限增殖引起的,早期常表现为乳房肿块、乳头溢液等症状,晚期则表现为肿瘤细胞向远处转移和浸润[1]。乳腺癌病因较复杂,且危险因素难以控制,难以做到乳腺癌的一级预防,临床目前主要以二级预防为主。提高乳腺癌早期诊断准确性对于疾病的二级预防意义重大,常规超声检查由于其无创、无辐射等优势是临床影像学诊断的重要部分,但对于操作的要求较高、依赖性较强,极容易出现漏诊及误诊[2]。近年来,人工智能技术在临床医学中高速发展,人工智能与超声结合具有较好的应用前景。本研究探讨人工智能超声对乳腺癌早期诊断以及预后评估的可行性及价值,为提高临床乳腺超声诊断率提供参考,现报道如下。
1 资料与方法
1.1 一般资料
收集2019年1月至2021年5月在九江学院附属医院检查的疑似早期乳腺癌患者的病历资料。纳入标准:女性;出现乳腺肿块或乳头溢液等疑似乳腺癌症状;影像学和组织病理学资料完整。排除标准:合并其他恶性肿瘤;合并严重脏器功能障碍;存在精神障碍。根据纳入、排除标准,共纳入310例疑似早期乳腺癌患者,年龄29~69岁,平均(46.58±9.47)岁;病理结果:恶性病变88例,良性病变222例。本研究经医院伦理委员会批准通过,所有患者均知情同意并签署知情同意书。
1.2 检查方法
超声检查分别由两名副高职称的超声医师进行,两名医师互不清楚对方诊断结果。彩色多普勒超声检查:采用迈瑞Resona I9高端彩色多普勒超声诊断仪,不运行Smart Breast智能系统,患者取仰卧位,充分暴露乳房和双侧腋窝,操作者手持探头,以乳头为中心,对周围乳腺、引流淋巴结等进行横、纵、斜等多方位检查,寻找肿块病灶区域,观察肿块附近的血流信号,明确腋窝淋巴结是否异常,结合图像特征中肿块的形态、大小、边界、包膜、回声和钙化情况进行诊断。同时根据具体情况调节仪器参数,使图片更加清晰、层次分明。
人工智能超声检查:采用装载了Smart Breast智能系统的迈瑞Resona I9高端彩色多普勒超声诊断仪进行检查,首先超声医师手动进行常规超声检查(操作同彩色多普勒超声检查),运行Smart Breast系统,系统对肿块病灶区域可以快速识别并进行定位。找到病灶区域后,手动重复性地对肿块区域进行多方位动静态超声图像采集(图像的采集标准:初步调整仪器参数,保证图像质量,如乳腺脂肪通常表现为中水平灰阶、远场深度刚好显示胸膜即可,超声医师可以根据具体情况进行局部聚焦观察等),采集完毕后系统进行肿块感兴趣区的自动绘制(超声医师若发现异常可对自动绘制的感兴趣区进行实际调整),并基于乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS)进行全自动分析,提取肿块的形态、大小、边界、回声、血流频谱等特征数据,随后系统输出肿块的影像特征和诊断结果并与对应病灶进行关联,医师可以根据患者情况添加多个病灶,最后医师确认无误后输出影像诊断报告。
1.3 观察指标
记录两种检查方法的结果并比较人工智能超声与彩色多普勒超声对早期乳腺癌的诊断价值。对比术后复发组和未复发组患者治疗前后的超声表现。
1.4 评价标准
恶性肿瘤[3]:①肿块表面凹凸不平,形状不规则,边界模糊不清且不见包膜,表现为浸润性生长;②回声不均匀,内部出现点状强回声;③淋巴结区域血流异常,纵横直径比不小于0.7。BI-RADS分级标准[4]:0级,具有明显体征但超声无明显异常,需要结合其他影像学进一步评估;1级,无明显乳腺癌体征,超声图像正常;2级,良性病变,经过多次复查图像基本可以排除恶性肿瘤;3级,可能属于良性病变,恶性肿瘤概率小于2%,需短期多次复查;4级,可能属于恶性病变,需要进行病理学诊断确认;5级,高度可能为恶性病变,需积极采取适当的诊断及对症处理。
1.5 统计学方法
采用SPSS 22.0软件进行统计分析,计量资料以均数±标准差()表示,组间比较采用t检验;计数资料以例数及率(%)表示,组间比较采用χ2检验;采用Kappa检验进行一致性分析,Kappa值≥0.40表明二者具有一致性,Kappa值越高一致性越高,Kappa值﹥0.75表明二者高度一致;以P﹤0.05为差异有统计学意义。
2 结果
2.1 诊断价值的比较
310例疑似乳腺癌患者经过病理学检查,阳性88例,阴性222例。彩色多普勒超声检查诊断乳腺癌的灵敏度、特异度、准确度分别为84.09%、70.72%、74.52%。人工智能超声检查诊断乳腺癌的灵敏度、特异度、准确度分别为86.36%、79.28%、81.29%。彩色多普勒超声和人工智能超声诊断乳腺癌与病理结果的一致性均一般(0.40﹤Kappa值﹤0.75),但人工智能超声诊断乳腺癌与病理结果的一致性更高。(表1、表2)
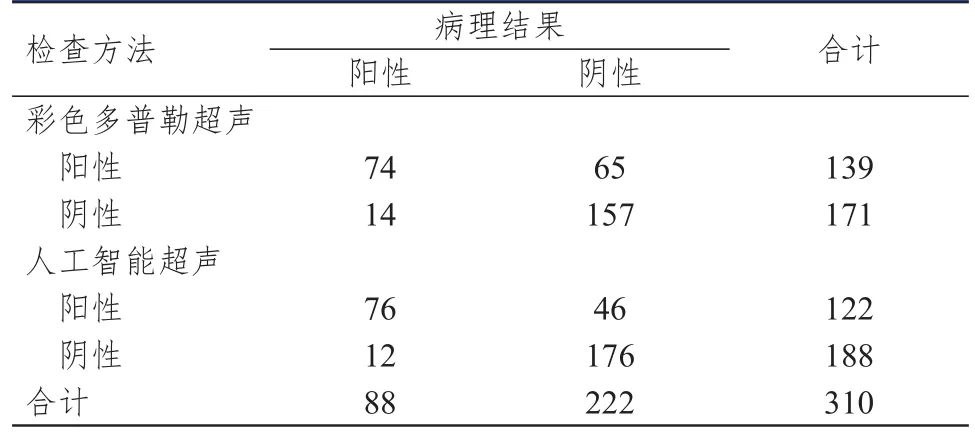
表1 彩色多普勒超声与人工智能超声诊断乳腺癌与病理结果的对照
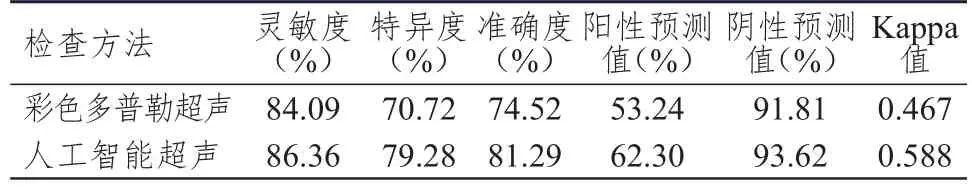
表2 彩色多普勒超声与人工智能超声对乳腺癌的诊断效能
2.2 超声影像学特征
两种超声影像结果显示,早期乳腺癌患者大多表现为以下特征:①肿块边界不清晰,呈锯齿状或蟹足状;②内部回声不均匀,表现为低回声;③纵横直径比大于1;④沙粒样等微钙化;⑤血流丰富,明显呈现高速高阻频谱;⑥皮肤凹陷、组织增厚水肿。从肿块形态来看,大部分恶性病变患者均可见边界不清晰的肿块,形态不规则,边缘不光整,主要表现为呈角、毛刺状。从声波模式来看,恶性病变主要表现为不均匀回声,部分患者还有沙粒样、弧形等微钙化。从血流形态来看,恶性病变区域血流信号明显增加,一般呈无规律性走向且血流阻力指数﹥0.7。良性病变患者大多表现出典型的良性超声特征,肿块包膜、声晕等界限清晰可见,形状规则,血流较少,也有部分良性病变患者出现了不规则、边界不清晰肿块以及血流阻力指数﹥0.7等表现,但多为0~Ⅰ级信号。
2.3 超声表现的比较
88例乳腺癌患者均进行手术治疗,根据预后复发情况分为复发组(n=10)和未复发组(n=78)。治疗后,复发组和未复发组患者超声表现中组织厚度、回声和血流形态比较,差异均有统计学意义(χ2=38.512、52.258、24.674,P﹤0.01)。(表3)
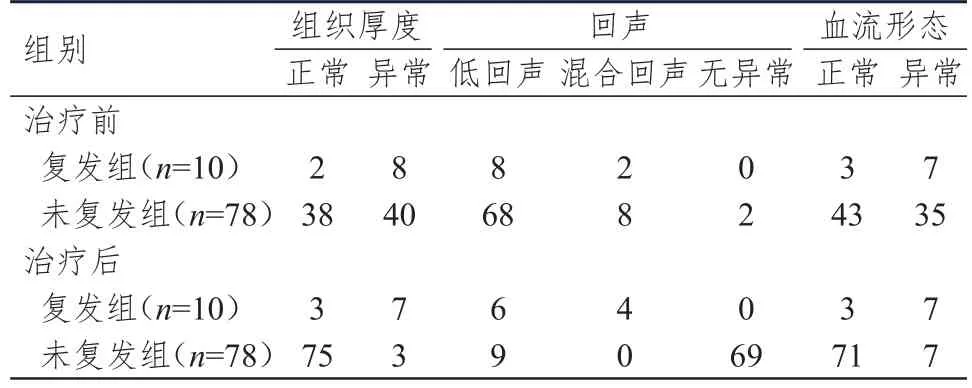
表3 治疗前后复发组与未复发组患者的超声表现
3 讨论
乳腺癌是威胁女性生命健康的头号杀手,近年来中国乳腺癌发病率呈逐年升高的趋势,提高其临床诊断率具有重要意义。随着科学技术的发展,计算机辅助诊断得到广泛应用,其是指将影像学等医学图像要素、特征进行提取、处理,通过结合感兴趣区,进行分类识别和疾病诊断,辅助临床医师更精准地对疾病进行诊断[5]。
医学影像学是临床医学领域的一个重要组成部分,人工智能相关技术系统在其领域内的应用已成为临床研究热点,人工智能技术已经在肿瘤影像学诊断中取得了良好的临床效果[6]。本研究结果显示,310例疑似乳腺癌患者经过病理学检查,阳性88例;彩色多普勒超声检查,阳性139例,真阳性74例;人工智能超声检查,阳性122例,真阳性76例。同时Kappa一致性分析显示,人工智能超声诊断结果与病理结果一致性更高。人工智能超声的特异度、准确度均明显高于彩色多普勒超声。这提示人工智能超声明显提高了准确度,有利于提高早期乳腺癌临床诊断的准确性,与相关研究结果类似[7-8]。分析其原因,人工智能超声可以有效缩短医师对超声图像特征的识别时间,在不影响诊断灵敏度的情况下提高特异度。Xu等[9]研究采用自动乳腺全容积扫描成像系统,在人工智能辅助软件的帮助下有效减少阅片时间,提高了诊断的准确度。由于手动超声检查对超声医师有较大的依赖性,诊断结果容易受其工作年限、临床经验、操作手法等客观因素的影响,从而出现漏诊及误诊。而人工智能系统自动提取并分析超声图像特征,不被客观因素影响。本研究结果显示,复发组和未复发组患者超声表现中组织厚度、回声和血流形态比较,差异均有统计学意义,绝大多数复发组患者出现组织厚度异常、回声异常、血流形态异常。这提示通过病灶周围组织厚度以及血流形态对乳腺癌患者进行预后评估是可行的,肿瘤细胞生长增殖后极易侵犯周围局部组织从而导致患者出现多种体征,当浸润在腺体和皮肤之间则引起酒窝状;浸润在淋巴管中,则引起淋巴管堵塞,出现橘皮征;这些异常皮肤体征引起正常解剖层次的改变,导致超声回声与周围正常组织不同,主要表现为低回声。同时肿瘤细胞的快速生长增殖需要大量的营养物质和氧气供应,因此其周围血流形态会受到影响。相关研究表明,乳腺癌患者超声影像特征越多越明显,其肿瘤异质性越强,复发风险越高[10]。超声检查可以及时发现这些微小症状,从而对预后进行评估。
综上所述,人工智能超声可以提高临床超声医师的诊断准确度,减少漏诊及误诊的发生,同时对于预后复发的评估具有较高的可行性,值得临床推广。但是本研究中部分良性病变患者也存在边界不规则和不清晰肿块,以及血流阻力指数﹥0.7等表现,超声诊断仍存在一定局限性,人工智能系统仍需进一步经过大数据训练,加强对不典型特征的辨识分析能力,进一步改进。
