改良式经皮肝动脉化疗药盒植入技术中国专家共识(2022 版)
2022-09-03中国抗癌协会肿瘤介入学专业委员会中国抗癌协会肿瘤介入学专业委员会化疗与免疫治疗分委会
中国抗癌协会肿瘤介入学专业委员会, 中国抗癌协会肿瘤介入学专业委员会化疗与免疫治疗分委会
肝动脉灌注化疗(hepatic arterial infusion chemotherapy,HAIC)是肝胆系统恶性肿瘤(原发性肝癌、胆管癌和转移性肝癌等)治疗的重要手段之一,通过在肝动脉直接灌注化疗药物,显著提高肝脏和肝脏肿瘤局部药物浓度并发挥抗肿瘤作用,得到多项临床研究验证[1-11],受到学术界越来越多关注[12]。 经皮肝动脉化疗留置导管药盒系统(简称肝动脉化疗药盒)是一套可供反复多次HAIC 治疗的体内导管药盒系统,主要由头端位于肝动脉内的留置导管和埋于皮下的药盒组成,其安全性和植入成功率已在既往研究中得以证实[13]。 与常规一次性经皮穿刺肝动脉留管化疗相比,植入式肝动脉化疗药盒可避免股动脉反复穿刺置管[13-17], 提高患者长时间持续HAIC 和反复多次HAIC 治疗的舒适性和依从性,同时降低治疗费用。
传统的肝动脉化疗药盒植入术需通过全身麻醉下外科剖腹手术完成,近年随着介入治疗相关器材及技术发展,已有研究显示经皮植入肝动脉化疗药盒的可行性及其微创化、并发症少等优势[15,18-19],并逐渐发展出改良式经皮肝动脉化疗药盒植入术。传统经皮肝动脉化疗药盒植入术尽管开展多年[20],但因留置导管头端游离, 导致导管移位率较高,肝动脉闭塞率高[21],临床使用率不高。 而改良式经皮肝动脉化疗药盒植入术采用管头固定技术和肝内外血流再分布术,具有创伤小、导管移位率低、实现全肝灌注、患者舒适性高、并发症少、药盒使用周期长等优点[22-24]。 由包括北京大学肿瘤医院介入治疗科在内的多个国内外中心完成的多项研究证实,改良式经皮肝动脉化疗药盒植入术可为肝胆系统恶性肿瘤患者提供安全可靠的HAIC 通路;多个前瞻性和回顾性临床研究显示,采用该技术完成的HAIC 治疗进展期原发性肝癌、肝内胆管癌、肝门胆管癌、胆囊癌等安全有效[4,6,25-26],其中两个前瞻性研究发表于Radiology杂志[4,6]。 目前国内对改良式经皮肝动脉化疗药盒植入术的标准化操作流程、 术后并发症防治及药盒维护缺乏统一认识, 为推动这一术式标准化和规范化建设,现组织多名专家在充分文献检索和临床实践基础上进行深入讨论并达成共识意见, 制定本专家共识,以供从事该技术的介入科和相关专业医师参考。
1 适应证和禁忌证
1.1 适应证
需行多次HAIC 治疗的进展期不可切除肝胆系统恶性肿瘤患者,包括原发性肝癌(伴门静脉等脉管癌栓、 肿瘤巨大或多发且预估TACE 治疗效果差、TACE 治疗后进展)、进展期肝内胆管癌、肝门胆管癌、胆囊癌伴肝内转移、转移性肝癌(如结直肠癌肝转移)等。
1.2 禁忌证
①对比剂过敏;②预穿刺部位局部感染或全身感染,如脓毒血症、菌血症等;③预穿刺部位曾接受放射治疗;④存在严重不可纠正的凝血功能障碍;⑤严重肝肾功能障碍;⑥合并其他基础疾患如心肺疾患等不能耐受手术;⑦不适合HAIC 治疗,如肝脏肿瘤负荷>70%,Child-Pugh 分级C 级,美国东部肿瘤研究协作组(ECOG)评分>2 分,大量腹水、肝外广泛转移、预计生存期<3 个月,白细胞计数<3.0×109/L,血小板计数<60×109/L 等。
2 术前评估和检查
肝动脉化疗药盒植入前需进行详细的术前评估,包括病史、体格检查、实验室检查和影像学检查等。
2.1 病史和体格检查
病史:①过敏史;②是否存在预穿刺部位放疗史;③是否存在血栓病史及凝血功能异常的个人史和家族史;④近期是否服用过抗凝药、抗血管生成靶向药。 体格检查:①预穿刺部位及药盒预植入部位皮肤情况;②是否存在影响药盒植入和植入后稳定性的局部软组织因素(如果存在,术前需进行相应影像学检查,排除禁忌后设计合适的药盒植入部位)。 心电图检查:必要时检查心、肺功能。
2.2 实验室检查
①血、尿、便常规检查;②凝血功能检查;③肝肾功能检查;④肿瘤标志物(AFP 及CEA、CA199、CA125 等)检查。
2.3 影像学检查
药盒植入前1 个月内完成腹部多期动态增强CT 或MRI 检查,必要时可行PET-CT 检查,考虑胆管癌或临床诊断肝细胞癌不成立时应行穿刺活检,以明确病理诊断。
3 知情同意与术前准备
3.1 知情同意
术前与患者/家属充分沟通, 详细告知患者病情、药盒植入必要性、治疗费用、植入过程、植入获益、植入过程中和植入后可能发生的风险以及并发症、替代治疗方案等,患者/家属签署治疗知情同意书。
告知患者药盒植入的获益: ①药盒可长期留置、重复使用;②可避免反复动脉穿刺插管,减少感染风险;③日常生活不受限制,提高生活质量。
告知相关风险和并发症:(见下文)
3.2 器械准备
手术包(包含剪刀、止血钳、手术刀、眼科剪、齿镊、缝线、持针器等)、穿刺针和导管鞘扩张器组件、1.8 m 超滑导丝、5 F Yashiro 导管/RH 导管、2.4~2.7 F微导管和相应微导丝、微弹簧圈、肝动脉化疗药盒系统(含5 F 导管、隧道针、药盒等)。
3.3 药品准备
1%利多卡因、对比剂、0.9%氯化钠溶液、普通肝素0.9%氯化钠溶液、地塞米松、阿托品、肾上腺素、 高浓肝素0.9%氯化钠溶液(500~1 000 U 肝素钠/mL)等。
3.4 患者准备
禁食4~6 h,训练床上解大小便;对有高血压病史者,术前可口服降压药控制血压;术前建立静脉通道;对无法控制排尿者,可留置导尿管;备皮。
4 手术步骤
改良式经皮肝动脉化疗药盒植入术主要步骤已有前期临床研究有所描述[22,27]。 具体步骤如下。
4.1 消毒铺巾
患者取仰卧位,聚维酮碘消毒,腹股沟区消毒区域上至脐水平线、下至大腿中段、两侧至双侧腋中线延长线; 锁骨下区消毒范围上至肩部上缘,下至脐水平线,两侧至腋中线,消毒完成后常规铺巾。
4.2 穿刺点选择及麻醉
股动脉入路一般选择右腹股沟皱褶上方1~2 cm处作为皮肤入点,触及股动脉搏动处作为股动脉穿刺点, 动脉穿刺点应在透视下股骨头投影上缘以内,锁骨下动脉入路一般选择左锁骨下锁骨中线外侧。 以1%利多卡因行局部浸润麻醉。
4.3 穿刺
用手术刀在预穿刺部位做一横向0.5 cm 左右皮肤切口,扩张真皮全层,采用改良Seldinger 技术行股动脉或锁骨下动脉穿刺,穿刺成功后进入导丝,沿导丝送入扩张管扩张穿刺通道, 交换置入Yashiro 等造影导管。 锁骨下动脉入路推荐超声导引下穿刺。
4.4 腹腔干和肠系膜上动脉造影
采用5 F 导管分别行选择性腹腔动脉、 肠系膜上动脉造影,2.6~2.7 F 微导管行肝固有动脉造影,以明确肝动脉解剖结构,包括肝动脉变异、肝动脉发出胃肠道供血动脉、肿瘤肝外寄生供血情况。
4.5 肝外血流再分布术
肝外血流再分布术(GRADE[28]循证等级B1)旨在保护性栓塞所有肝动脉发出的胃肠道供血动脉,再分布胃十二指肠区域原有血供模式, 避免HAIC时产生胃肠道异常药物灌注,减少急性胃十二指肠黏膜毒性反应(acute gastroduodenal mucosal toxicity,AGMT)。 若造影发现任何肝动脉发出的胃肠道供血分支(包括胃右动脉、副胃左动脉、十二指肠后上动脉等,图1①~④),微导管分别超选择插管后,以微弹簧圈栓塞至血流中断。 对于胃右动脉因开口角度问题无法顺行选择进入者,可经胃左动脉逆行进入胃右动脉起始部,以微弹簧圈栓塞(图1⑤⑥)[29-30]。
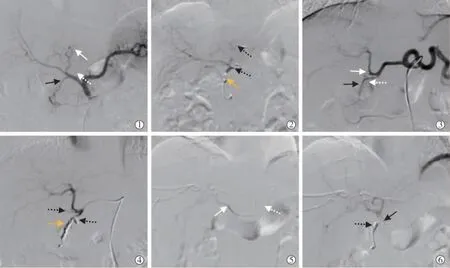
图1 肝外血流再分布术
4.6 肝内血流再分布术
肝内血流再分布术(循证等级B1)旨在有多支肝动脉变异如副肝左动脉从胃左动脉发出,副肝右动脉从肠系膜上动脉发出时,通过将多支肝动脉变成一支肝动脉(图2)实现全肝HAIC。上述造影发现多支肝动脉变异时,以微导管行超选择插管,并采用微弹簧圈充分栓塞变异的副肝左动脉和/或副肝右动脉,从而重新建立肝固有动脉供给全肝的动脉供血系统。

图2 肝内血流再分布术
4.7 管头固定的肝动脉化疗药盒植入术
管头固定的肝动脉化疗药盒植入术(循证等级B1)操作:
①留置导管准备:从肝动脉药盒系统中取出5 F留置导管, 以眼科剪或打孔器在距导管头端5 cm处开一长椭圆形侧孔, 侧孔大小为导管直径的1/3左右,能顺利通过微导管为宜。
②留置导管植入:沿Yashiro 导管送入1.8 m 超滑导丝,选择性送入GDA 的胃网膜右动脉分支;交换置入药盒留置导管,导管头端部分进入GDA 内,侧孔位于GDA 近端。
③导管头固定技术[13](图3、图4①~④):采用同轴微导管技术, 将2.4~2.7 F 微导管选择性通过留置导管的侧孔送入GDA 内, 选择合适大小微弹簧圈, 在留置导管头端导管外-GDA 内密集释放弹簧圈,将导管头固定在GDA 内。 对GDA 近端(离开口2 cm 以内) 发出的胰十二指肠后上动脉等分支者(图4⑤⑥),要超选择进入微导管后进行分别栓塞,避免药物对胃肠道黏膜的损伤。

图3 管头固定技术模式图
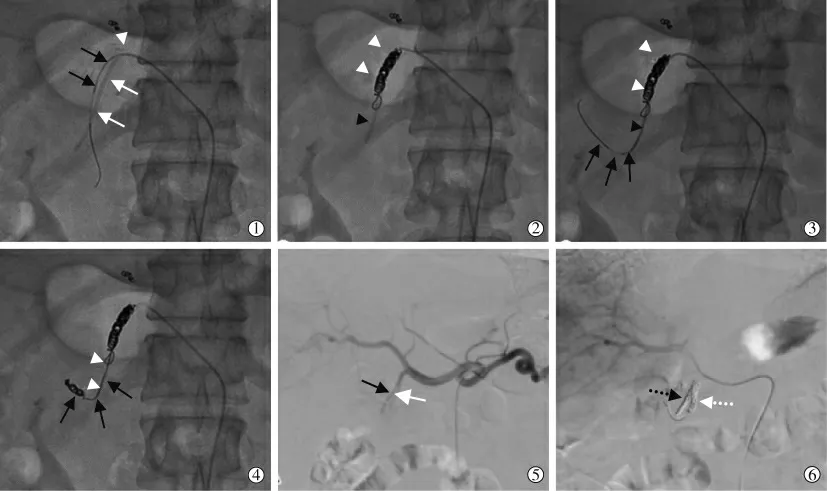
图4 管头固定技术
④留置导管端孔封堵术:封闭留置导管头端端孔,保证药物完全经过侧孔进入肝动脉。 采用同轴微导管技术,微导管通过留置导管端孔,释放2 mm×6 mm 微弹簧圈1 枚, 封闭留置导管端孔;若GDA 内血流为逆行血流,可不封闭导管端孔[31-32]。
⑤药盒植入:股动脉入路时,一般选择右髂前上嵴内侧2 cm 左右作为药盒植入部位,以1%利多卡因行局部麻醉;用手术刀做一3~4 cm 横向皮肤切口,以止血钳在皮下钝性分离出一足以容纳药盒的囊袋,穿刺处皮肤向右侧扩大切口1 cm;采用隧道针将留置导管从下切口引入上切口,剪掉多余导管,连接导管尾端和药盒,并将药盒埋置于右髂前上棘内侧皮肤下(图5①)。锁骨下动脉入路时,一般选择左锁骨下方4~5 cm, 锁骨中线外侧为药盒植入部位(图5②),植入方法基本同上。

图5 药盒埋置位置
⑥缝合:将药盒置入囊袋内,缝合皮肤切口,包扎。
4.8 造影确认药盒功能状态
用19 G 动脉药盒专用穿刺针穿刺入药盒内,注入对比剂确认药盒处无渗漏, 经药盒行肝动脉DSA 造影(1~1.2 mL/s ×6 s)和锥形束CT(CBCT)造影/CT 肝动脉造影(CTHA)(1~1.2 mL/s ×20 s,延迟15 s 扫描),验证肝脏及肝内肿瘤是否完全强化,有无胃肠道黏膜异常强化(图6)。
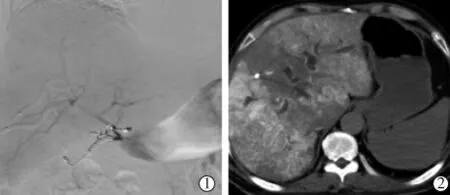
图6 DSA 和CTHA 造影明确药盒功能状态
4.9 肝素封闭肝动脉化疗药盒系统
采用高浓肝素0.9%氯化钠溶液(500~1 000 U/mL×2 mL)对药盒系统进行封闭。
5 肝动脉化疗药盒使用和维护
5.1 穿刺药盒造影
造影方法同4.8。每次HAIC 前明确肝动脉化疗药盒位置和功能状态,药盒有无渗漏,导管有无移位、打折、堵塞,肝动脉是否通畅,肝脏是否灌注完全,有无胃肠道动脉异常灌注等。
5.2 经药盒持续HAIC
经药盒行肝动脉造影评估药盒功能良好,才能行HAIC 治疗。 首次HAIC 治疗建议在药盒植入术后至少24 h 以上,对于有切口愈合不良因素者可适当延后HAIC 治疗。 推荐采用体外输液泵持续泵入化疗药物,浓度依赖性药物和时间依赖性药物的灌注时间不同,期间适当限制活动[33]。
常用HAIC 药物剂量和灌注时间: 奥沙利铂85~130 mg/m2(2~3 h),顺铂50~75 mg/m2(1~2 h),紫杉醇100~175 mg/m2(2 h)或100~200 mg/m2(24 h),白蛋白紫杉醇100~230 mg/m2(1~4 h),吉西他滨800~1 000 mg/m2(1~2 h),5-FU 1.0~2.4 g/m2(24~72 h)。
常用HAIC 方案:①FOLFOX 方案[7-9]:第1 天为奥沙利铂85~130 mg/m2(2~3 h),左亚叶酸钙400 mg/m2,5-FU 2 400 mg/m2灌注(24~46 h),每3周重复;②3 cir-OFF 方案(北 大 肿 瘤 医 院)[6,28]:第1、2、3 天连续灌注,每天奥沙利铂35~40 mg/m2灌注(2 h),5-FU 600~800 mg/m2灌注(22 h),左亚叶酸钙200 mg/m2静脉滴注(2 h),每4 周重复(对胆管癌和肠癌肝转移,推荐每周期奥沙利铂总量120 mg/m2,5-FU 总量2.4 g/m2;对原发性肝癌,推荐奥沙利铂总量105 mg/m2,5-FU 总量1.8 g/m2,每4 周重复)。
5.3 药盒维护
每次HAIC 结束后,采用高浓度肝素0.9%氯化钠溶液(500~100 0 U/mL ×2 mL)封闭药盒,药盒长期闲置期间推荐每月维护1 次。
6 常见并发症预防和处理
6.1 导管移位
①主要原因:患者动脉迂曲,腹腔干开口后往足侧走行;留置导管体内段张力过大;患者剧烈运动或过度拉伸运动。②预防:固定导管管头时尽可能采用微弹簧圈固定;调整留置导管松弛性;嘱患者术后1 个月内避免剧烈运动和特殊体位活动。③处理:如果留置导管侧孔移位至腹腔动脉,经药盒造影肝、脾动脉均显示,可采用弹簧圈栓塞脾动脉,再分布腹腔动脉血供完全供给肝。
6.2 导管堵塞
导管堵塞主要由血栓形成所致。 ①主要原因:肝素0.9%氯化钠溶液封闭药盒系统时动脉血液返流至导管内;药盒系统长时间未用肝素0.9%氯化钠溶液维护;患者高凝体质。②预防:肝素0.9%氯化钠溶液封闭药盒时以脉冲式注入,推注下拔针;定期进行药盒维护(每4 周1 次);高凝患者预防抗凝,2019 年9 月美国临床肿瘤学会(ASCO)发布肿瘤患者静脉血栓栓塞(VTE)防治指南,建议高风险肿瘤患者在开始化疗前Khorana 评分≥2 分, 无出血风险,进行血栓一级预防[34],建议服用利伐沙班10 mg,每日1 次。 ③处理:新鲜血栓通过注射肝素0.9%氯化钠溶液可再通;陈旧性血栓通过药盒系统推注高浓尿激酶,并保留4~24 h 后复查,部分患者可再通。
6.3 肝动脉闭塞
肝动脉闭塞主要由血栓和纤维鞘膜形成所致。①主要原因: 肝动脉纤细或受肿瘤侵犯引起狭窄;化疗药物和导管对动脉内壁刺激;动脉粥样硬化和自身高凝体质。 ②预防:对肝动脉特别纤细和明显狭窄者,放弃药盒植入;留置药盒导管时尽量避免侧孔接触动脉壁;肝素0.9%氯化钠溶液封闭药盒方法得当及时;对高凝体质者预防性抗血栓治疗(见6.2)。 ③处理:对新鲜肝动脉血栓和纤维鞘膜形成,通过药盒系统注射尿激酶(如50 万U),2~4 h 持续灌注后复查,部分患者可再通;不能再通者,可经膈下动脉、 胰背动脉等代偿动脉重新留置导管行HAIC 治疗[35-36]。
6.4 急性胃肠道黏膜损伤
①主要原因:未行肝外血流再分布术或完成不彻底,化疗药物部分灌注胃肠道,引起AGMT;既往慢性胃十二指肠炎症或溃疡;长期应用非甾体类抗炎药(NSAID)、阿司匹林、抗凝药、糖皮质激素等药物。 ②预防:肝外血流再分布术要完全;每次HAIC治疗前经药盒行肝动脉DSA 造影,如发现再通的胃肠道动脉,再次栓塞封闭;化疗期间行抑酸和保护胃黏膜治疗。 ③处理:对有明确症状患者,行胃镜检查, 明确是否存在胃十二指肠溃疡及其程度和范围;对明确的胃十二指肠溃疡,给予质子泵抑制剂(PPI)抑酸治疗,标准剂量,每日1~2 次,配合应用胃黏膜保护剂。
6.5 局部血肿
①主要原因:股动脉穿刺处渗血;切肤时出血;反复穿刺药盒;凝血功能较差;既往应用抗血管生成分子靶向药。 ②预防:扩张穿刺道时避免用导管鞘,并尽量避免多次交换导管;切开皮肤时发现较大的动脉分支出血予缝线结扎;避免多次反复穿刺药盒,拔针后药盒穿刺处皮肤压迫5~10 min;药盒植入术前, 大分子抗血管内皮细胞生长因子(VEGF)靶向药需停药4 周以上,小分子靶向药需停药3 d 以上。 ③处理:活动性出血时加压包扎8~12 h;对药盒周围大量皮下积血,穿刺抽吸,必要时切开皮肤清除淤血。
6.6 切口愈合不良
①主要原因:导管反折部分正对切口;切口不整齐、缝皮时皮缘对合不佳等;皮下淤血、合并感染等;埋置药盒后过早开始HAIC 治疗;患者本身存在影响切口愈合因素,如糖尿病、低蛋白血症、营养不良等。 ②预防:导管反折弓柔和,不要正对下切口切缘;皮肤切口整齐,缝合时皮缘对合整齐,推荐采用间断垂直褥式外翻缝合法;对存在影响切口愈合因素者,应推迟HAIC 治疗和拆线时间;纠正糖尿病和营养状态等。 ③处理:对切除不愈合的皮缘和坏死的皮肤组织重新缝合。
6.7 感染
①主要原因:药盒周围皮下积血;操作过程未严格无菌操作;糖尿病、机体免疫力低下等自身体质因素。②预防:严格无菌操作;术前及术后24 h 内预防性应用抗生素; 切口愈合前保持切口处清洁;严重皮下淤血及时清创; 纠正糖尿病等全身状态。③处理:全身应用抗生素;对形成脓腔者,切开清创并引流。
6.8 导管打折
①主要原因: 留置导管腹股沟反折角度过大。②预防: 术中制作角度柔和的留置导管反折弯;避免止血钳夹持导管的反折弯处。 ③处理:切开皮肤重新制作柔和的反折弯。
6.9 药盒翻转
①主要原因:皮下囊袋过大;导管和药盒连接后非受力状态下药盒非正面朝上;术后1 个月内剧烈运动。 ②预防:制作皮下囊袋大小适中;药盒和导管相连后保证药盒正面朝上;术后1 个月内避免剧烈运动。 ③处理:可先尝试手法复位,不成功者切开复位。
6.10 皮肤组织化学性坏死
①主要原因:穿刺针移位出药盒,导致化疗药物进入药盒周围皮肤和皮下组织内。 ②预防:蝶翼针穿刺入药盒过程中确保针完全进入药盒内,并透视下确认,妥善固定,嘱患者化疗期间避免过度运动和过度体位变化;对异常肥胖患者,推荐弹力绷带适当加压包扎。 ③处理:立即停止化疗药物注入,局部注入地塞米松2~4 mg 以减轻炎性反应;局部注射利多卡因止痛[37];如已出现皮肤溃疡、坏死等,及时清创缝合。
7 肝动脉化疗药盒护理
7.1 术前护理
术前按常规行双侧腹股沟区皮肤充分备皮、消毒。
7.2 术后常规护理
①嘱患者卧床休息6~12 h,观察生命体征,观察药盒植入部位是否存在渗血、红肿等情况,监测穿刺侧肢体足背动脉搏动。 予抗感染、补液,嘱患者多饮水。②一般于术后7~10 d 切口拆线,若患者自身存在影响切口愈合的因素如营养不良、 糖尿病等,应适当延长拆线时间或间断拆线;嘱患者避免剧烈运动,保持药盒植入部位皮肤清洁干燥。 ③经药盒HAIC 治疗过程中,定期观察药盒处有无红肿、疼痛等药物渗出表现,嘱患者在保证穿刺针固定良好的情况下进行适当体位活动,避免长期卧床引起下肢静脉血栓事件。
8 肝动脉化疗药盒拆除
8.1 适应证
①根据病情,预计无需再行HAIC 治疗;②药盒植入部位反复感染、 切口愈合不良以及上述严重并发症所致药盒不能正常使用; ③患者或家属要求取出。
8.2 操作过程
①完善血常规、 凝血功能和心电图等术前检查。 ②严格无菌操作。 患者取平卧位,局部消毒铺巾,1%利多卡因局部浸润麻醉, 切开药盒植入部位皮肤,暴露药盒及部分导管;游离药盒,并缓慢将导管自皮下隧道及股动脉内拔出,同时压迫导管进入股动脉部位;缝合伤口;加压包扎,并持续加压8 h。③嘱患者卧床9~12 h,观察生命体征,观察操作部位是否存在渗血、红肿等情况;予抗感染、补液。
9 结语
肝动脉化疗药盒植入术是介入治疗技术之一,本共识旨在推动HAIC 技术标准化、规范化建设,通过改良式经皮肝动脉化疗药盒植入规范化技术流程的共识形成和制定,使该技术能在国内各级医院规范化、合理化应用,提高HAIC 有效性和安全性,减少相关并发症发生, 为HAIC 介入技术在国内各级医院普及、推广和规范化应用提供条件。 国内改良式经皮肝动脉化疗药盒植入技术应用及维护工作任重道远,需要多学科医师、护理团队及患者共同努力。 本共识也将在临床实践中继续探索改进,使其更臻完善。
[参与本共识审核专家(按姓氏笔画排序):王茂强(解放军总医院第一医学中心)、朱 旭(北京大学肿瘤医院)、刘瑞宝(哈尔滨医科大学附属肿瘤医院)、李 肖(中国医学科学院肿瘤医院)、金 龙(首都医科大学附属北京友谊医院)、郭 志(天津医科大学肿瘤医院)、唐 军(山东第一医科大学附属省立医院)、程永德(上海介入放射学杂志社)、颜志平(复旦大学附属中山医院)。 编写专家(按姓氏笔画排序):于友涛(解放军总医院第四医学中心)、于海鹏(天津医科大学肿瘤医院)、王 松(青岛大学医学院附属医院)、王晓东(北京大学肿瘤医院)、王 健(北京大学第一医院)、朱海东(东南大学附属中大医院)、刘凤永(解放军总医院第五医学中心)、刘吉兵(山东省肿瘤医院)、刘 嵘(复旦大学附属中山医院)、刘 鹏(北京大学肿瘤医院)、刘玉金(上海中医药大学附属岳阳医院)、孙宏亮(中山大学孙逸仙纪念医院)、孙玮琦(哈尔滨医科大学附属肿瘤医院)、邹英华(北京大学第一医院)、宋金龙(山东省肿瘤医院)、李文涛(复旦大学附属肿瘤医院)、李晓光(北京医院)、李家平(中山大学附属第一医院)、李彩霞(山东大学齐鲁医院)、杨仁杰(北京大学肿瘤医院)、杨 光(河北医科大学第四医院)、杨武威(解放军总医院第五医学中心南院区)、陈在中(北京大学深圳医院)、吴 刚(郑州大学第一附属医院)、张跃伟(清华大学附属北京清华长庚医院)、张 靖(广东省人民医院)、段 峰(解放军总医院第一医学中心)、赵 明(中山大学附属肿瘤医院)、赵剑波(南方医科大学南方医院)、闻利红(北京大学肿瘤医院)、袁春旺(首都医科大学附属佑安医院)、徐 亮(北京大学肿瘤医院)、徐海峰(北京大学肿瘤医院)、高 堃(首都医科大学附属朝阳医院)、高 嵩(北京大学肿瘤医院)、曹 广(北京大学肿瘤医院)、靳 勇(苏州大学附属第二医院)、潘 杰(中国医学科学院北京协和医院)。执笔:王晓东、郑康炼(北京大学肿瘤医院)]
