剩余污泥中温和高温厌氧水解酸化产VFAs性能研究
2022-08-31熊惠磊张晓聪杨海洋段双妮刘海涛陈选平张志强施汉昌
熊惠磊,张晓聪,杨海洋,段双妮,刘海涛,陈选平,张志强,施汉昌,5
(1.北京协同创新研究院,北京 100094;2.湘南学院,湖南郴州 423099;3.湖南大自然环保科技有限公司,湖南郴州 423099;4.农业农村部规划设计研究院,北京 100125;5.清华大学,北京 100084)
剩余污泥是污水处理厂运行过程中产生的副产物,如未经有效处理处置会给环境和人体健康造成危害〔1〕。在众多剩余污泥处理处置技术中,厌氧消化技术是降解污泥中有机物的一种高效且有潜力的技术,同时可产生沼气作为可再生能源〔2〕。
根据厌氧微生物生长最适温度,将厌氧消化分为常温厌氧消化、中温厌氧消化和高温厌氧消化。目前研究者们重点关注中温厌氧消化(反应温度一般为35 ℃)和高温厌氧消化(反应温度一般为55 ℃)的产甲烷微生物和产沼气情况〔3−5〕,对于厌氧消化起始阶段产酸过程的研究较少。笔者从污泥颗粒粒径、颗粒有机物降解、可溶性化学需氧量(SCOD)、挥发性有机酸(VFAs)及氮磷营养元素溶出的角度开展研究,对中温和高温厌氧产酸阶段的优劣进行综合对比。
1 试验部分
1.1 试验用泥
试验使用污泥取自北京某污水处理厂转鼓浓缩机出口处,其主要特性见表1。
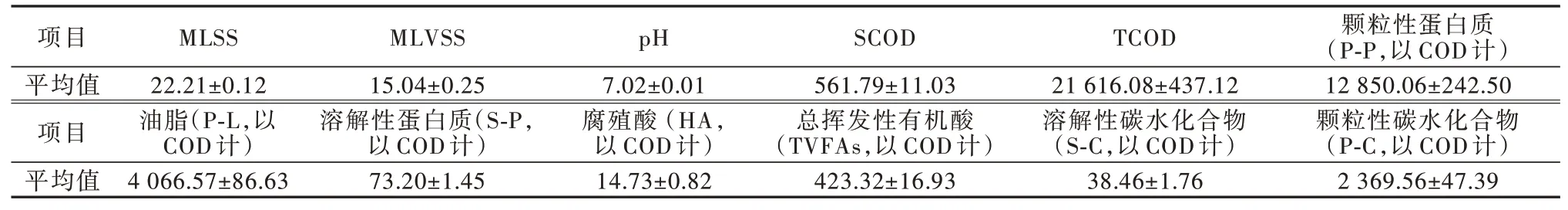
表1 剩余污泥特性Table 1 Characteristics of excess sludge
由表1可知,MLSS中有机成分比例(MLVSS/MLSS)为67.71%,P-P、P-C和P-L为浓缩污泥中的主要有机物,分别占TCOD 的59.45%、10.96%、18.81%;其中浓缩污泥中的P-L 占比显著高于国内南方地区污泥的比例〔6〕,可能是由于不同地域的气候差异和居民生活习惯不同。
1.2 试验装置与方法
将6 L 浓缩污泥平均加入到4 个有效容积为1.5 L的玻璃锥形瓶,每2 个锥形瓶为一组,分为中温组和高温组。用橡皮塞密封锥形瓶,不控制pH,采用自然驯化产酸菌群。将中温组和高温组锥形瓶分别放入2 个摇床,控制摇床转速为170 r/min,温度分别为35、50 ℃。4 个锥形瓶按一定时间间隔打开橡皮塞取样检测,整个试验过程中反应体系并非严格厌氧状态。
1.3 检测方法
1.3.1 蛋白质和腐殖酸的测定
总蛋白质采用分光光度法测定,换算为蛋白质系数(F),即总蛋白质含量〔7〕,根据文献调研F取6.25〔8−9〕。
采用三维荧光光谱定性分析溶解性蛋白质和腐殖酸〔10〕。溶解性蛋白质和腐殖酸的定量测定采用改进Lowry 方法〔11〕。
1.3.2 碳水化合物的测定
溶解性碳水化合物采用苯酚−浓硫酸法测定〔12〕。将泥水混合物(污泥和水解液)用高温盐酸预处理〔13〕,用苯酚−浓硫酸方法测定总糖。总糖减去溶解性碳水化合物即颗粒性碳水化合物含量。
1.3.3 脂肪的测定
采用索式提取重量法测定脂肪,溶剂可选择氯仿或正己烷〔14〕。
1.3.4 挥发性有机酸的测定
取粗滤、酸化〔15〕和精滤预处理后的水样,用气相色谱(GC)检测挥发性有机酸。6890N 气相色谱仪(安捷伦),氢火焰检测器(FID),色谱柱为极性柱HP-FFAP(30 m×0.25 mm×0.25 μm),载气为氮气(流速40 mL/min),进样体积1.0 μL,采用不分流模式。
进样口和检测器温度均为250 ℃;根据检测需要采用程序升温,起始温度70 ℃稳定3.5 min,再按升温步长20 ℃/min 升至180 ℃,在180 ℃稳定5 min,整个检测过程耗时14 min。
1.3.5 其他测定项目
除MLSS、MLVSS、ORP 和DO 外,其余项目均经0.45 μm 滤膜过滤后参照《水和废水监测分析方法》〔16〕测定。
2 结果与讨论
2.1 中温和高温对污泥粒径的影响
研究者常用污泥平均粒径(假定污泥颗粒近似球形)作为指示参数,表征污泥的物理特性〔17〕,一般认为污泥平均粒径越小越有利于反应的进行。厌氧产酸过程中,污泥粒径的比例分布如图1 所示。

图1 剩余污泥颗粒粒径分布Fig. 1 Particle size distribution of excess sludge
由图1 可见,中温和高温污泥的粒径均随厌氧产酸反应时间的延长而减小,反应48 h 后高温和中温污泥颗粒平均粒径分别为121、234 μm。高温条件可促进污泥絮体解离,使污泥颗粒粒径减小,从而增加微生物与有机物的接触几率。高温条件下MLVSS 的减量率为41.10%,明显高于中温条件MLVSS 的减量率(32.69%)。
2.2 中温与高温对颗粒性有机物降解的影响
多数研究者认为酶活性与细菌增长非直接耦合〔18−19〕,有机多聚物水解过程遵循一级反应动力学,如式(1)所示。

式中:CX——X类型颗粒性有机物的质量浓度,mg/L;
kX——X类型颗粒性有机物水解常数,h−1;
t——反应时间,h。
经过演算,式(1)可转化为式(2)。

MLVSS、P-C 和P-P 初 始 值 分 别 为21 356.8、2 369.56、12 850.06 mg/L 时,拟合结果如表2 所示。
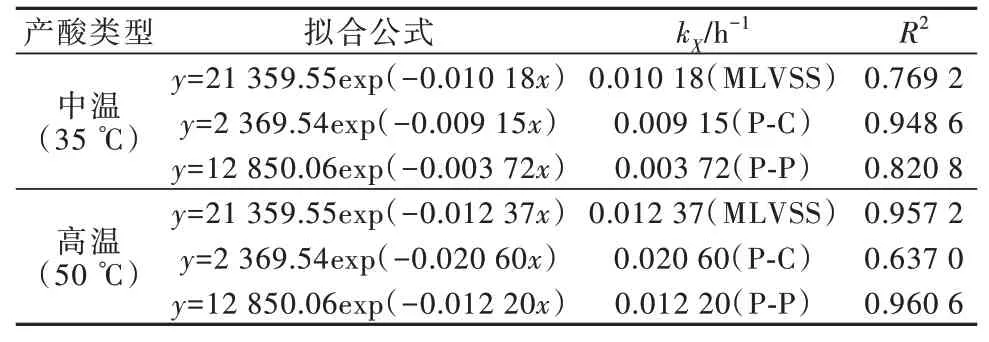
表2 MLVSS、P-C 和P-P 的拟合常数Table 2 Fitting constants of MLVSS,P-C and P-P
由表2 可见,高温条件可明显提高颗粒性有机物的水解常数,各类颗粒性有机物的水解常数由大到小依次为kP−C>kMLVSS>kP−P。颗粒性碳水化合物(P-C)更易被微生物降解利用,故P-C 的水解常数高于P-P。此外,由于污泥成分复杂(包括P-P、P-C 和死亡微生物等),MLVSS 的水解常数受这些有机物的影响,介于各颗粒性有机物水解常数之间。
P-P、P-C 和P-L 是污泥中重要的颗粒性有机物。在中温、高温厌氧水解产酸过程中,主要被分解的是P-P 和P-C,P-L 的分解率低于5%(见表3),表明P-L在厌氧水解产酸过程中很难被微生物利用和分解,与一些研究现象类似〔9,20〕。
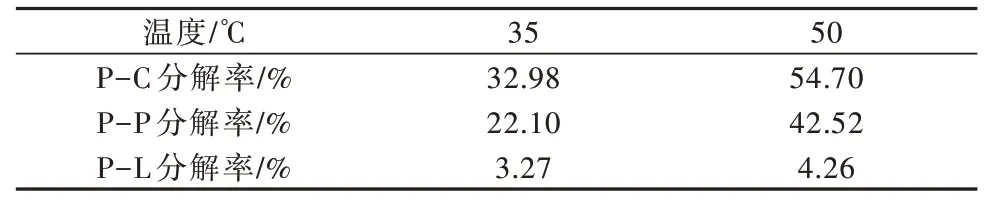
表3 P-C、P-P 和P-L 的分解率Table 3 Decomposition rates of P-C,P-P and P-L
颗粒性有机物含量可用MLVSS 表征,其中包括PP、P-C、P-L 和未知颗粒性有机物(Other)。通过分析颗粒性有机物的降解比例,可以揭示中温和高温产酸过程的降解类型。鉴于厌氧水解产酸过程中P-L 分解率<5%,因此分析过程未考虑P-L。中温和高温产酸过程中颗粒性有机物的变化情况如图2 所示。

图2 颗粒性有机物的降解情况Fig. 2 Degradation of particulate organic matter
由图2 可见,中温产酸过程中,未知颗粒性有机物是MLVSS 中的主要被分解物质,其分解比例远高于PP 和P-C;反应48 h 时未知颗粒性有机物、P-P 和P-C 占MLVSS 的分解比例分别为48.14%、40.67%、11.19%,分析原因认为中温时微生物的多样性显著优于高温条件〔21〕,厌氧微生物以未知颗粒性有机物作为底物进行分解代谢和合成代谢。在高温产酸过程中,反应初始阶段(0~12 h)降解物以未知颗粒性有机物和P-C 为主,反应后期(24~48 h)则为P-P;反应48 h 时未知颗粒性有机物、P-P和P-C占MLVSS的分解比例分别为22.99%、62.24%、14.76%。其中未知颗粒性有机物暂不能确定,猜测可能是厌氧产酸过程中活性污泥的微生物破壁后释放的胞内物质,有待进一步研究。
中温条件下P-P 的降解主要发生在36 h 后,而高温条件下P-P 的降解发生在12 h 后,表明高温条件下蛋白质降解菌的活性显著优于中温条件〔22〕,进一步说明高温有助于提高颗粒性有机物的降解效率。
2.3 中温与高温对溶出SCOD 的影响
水解和酸化是厌氧发酵的2 个步骤。其中,水解过程的作用为:(1)将复杂的不溶性物质转化成较复杂的可溶性有机物;(2)将微生物降解的有机多聚物分解为二聚物或单体,这些物质可通过细菌的细胞壁和细胞膜并进入水相。因此,水解过程中SCOD 会显著上升。而酸化过程主要通过多种微生物的共同作用将溶解性有机物转化为许多简单有机物,包括挥发性有机酸和乙醇等。由于有机物仅发生分子形式的变化,因此酸化过程中SCOD 相对保持稳定。中温和高温条件下厌氧发酵过程的SCOD 变化如表4 所示。

表4 中温和高温厌氧发酵的SCOD 变化Table 4 SCOD changes in anaerobic fermentation process under mesophilic and thermophilic conditions
由表4 可见,反应时间为0~24 h 时,中温和高温厌氧发酵过程的SCOD 一直处于快速增长状态;反应24 h 后SCOD 保持相对稳定。表明中温和高温厌氧水解酸化过程存在明显分界点,0~24 h 属于水解过程,24~48 h 属于酸化过程,加之高温条件下各类颗粒性有机物的水解常数均高于中温条件,因此高温条件下的SCOD 约为中温条件的2 倍。
SCOD 中除VFAs 外,还可能包含溶解性蛋白质、氨基酸和腐殖酸等有机物。采用三维荧光技术对反应48 h 水解液中的可溶性有机物进行定性分析,结果如图3 所示。

图3 污泥水解液的三维荧光谱图Fig. 3 Three-dimensional fluorescence spectra of sludge hydrolysate
由图3 可见中温和高温水解液中主要存在2 个荧 光 峰:λEx/λEm分别为220/350 的A 峰和275/350 的B 峰。查阅文献〔23−24〕认为A 峰可能为芳香性蛋白质,B 峰可能为色氨酸。
根据荧光分析并结合实际检测结果,认为SCOD 主要由VFA、HA、溶解性碳水化合物(S-C)、溶解性蛋白质(S-P)和未知溶解性有机物组成(见图4)。其中未知溶解性有机物无法定性,推测该物质可能是蛋白质或碳水化合物降解过程的中间产物。
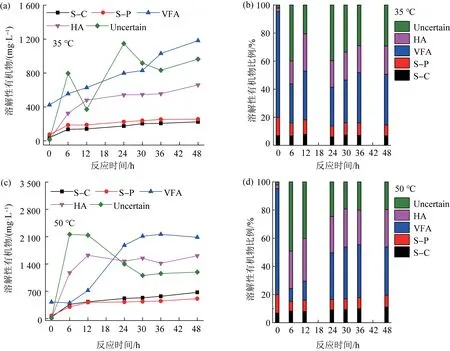
图4 水解液中SCOD 成分Fig. 4 SCOD component in hydrolysate
由图4 可见,中温和高温发酵过程中,VFA、HA、未知溶解性有机物是三类主要的溶解性有机物,其中VFA 呈增长趋势,HA 和未知溶解性有机物表现则各有不同。高温发酵中,运行12 h 后HA 和未知溶解性有机物浓度下降(此阶段VFA 迅速增加),表明中间产物的降解有助于厌氧体系的产酸过程。在中温条件下,HA 和未知溶解性有机物一直处于积累状态。中间产物的“高积累、慢转化”可能是中温发酵产酸效果明显低于高温条件的原因之一。
2.4 中温与高温对VFA 的影响
考察了中温、高温条件下VFA 的变化情况,如图5 所示。

图5 中温、高温厌氧发酵过程中VFA 的变化Fig. 5 VFA changes in anaerobic fermentation process under mesophilic and thermophilic conditions
由图5(a)~(d)可见,中温或高温厌氧发酵过程中,乙酸(HAc)始终为含量最高的有机酸。中温条件下HAc含量随反应时间的延长而增加,48 h 时达到最大值(596.21 mg/L);而高温条件下,当反应时间为0~24 h,HAc 迅速升高,在24 h 时达到最大值(1 072.04 mg/L),此后随着反应继续进行,HAc 略有降低,高温发酵终止时HAc 为913.75 mg/L。
中温发酵30 h前,丙酸(HPr)含量仅次于HAc,反应24 h时达到最大值(155.01 mg/L);30 h后异戊酸(i-HVa)含量升至第2位,48 h时最大质量浓度为216.55 mg/L。高温发酵过程中,反应12 h 后i−HVa 含量逐步升高,仅次于HAc,48 h 时达到最大值745.75 mg/L。
对比图5(a)、(b)、(e)、(f)可知,随着P-C 被大量分解,HAc 和HPr 含量随之上升,HAc、HPr 与P-C的分解存在一定相关性〔25〕;当大量P-P 被降解后,异丁酸(i-HBu)和i-HVa 明显增加,中温体系中的乙酸含量也上升,这是因为氨基酸在分解为戊酸、丁酸和丙酸的同时也会产生乙酸〔26〕。
2.5 中温与高温对氮、磷溶出的影响
氮元素是构成微生物体的重要元素之一,在污泥厌氧发酵过程中大量氮元素以氨氮形式释放到水相中。中温及高温条件下氮的溶出情况如图6(a)所示。
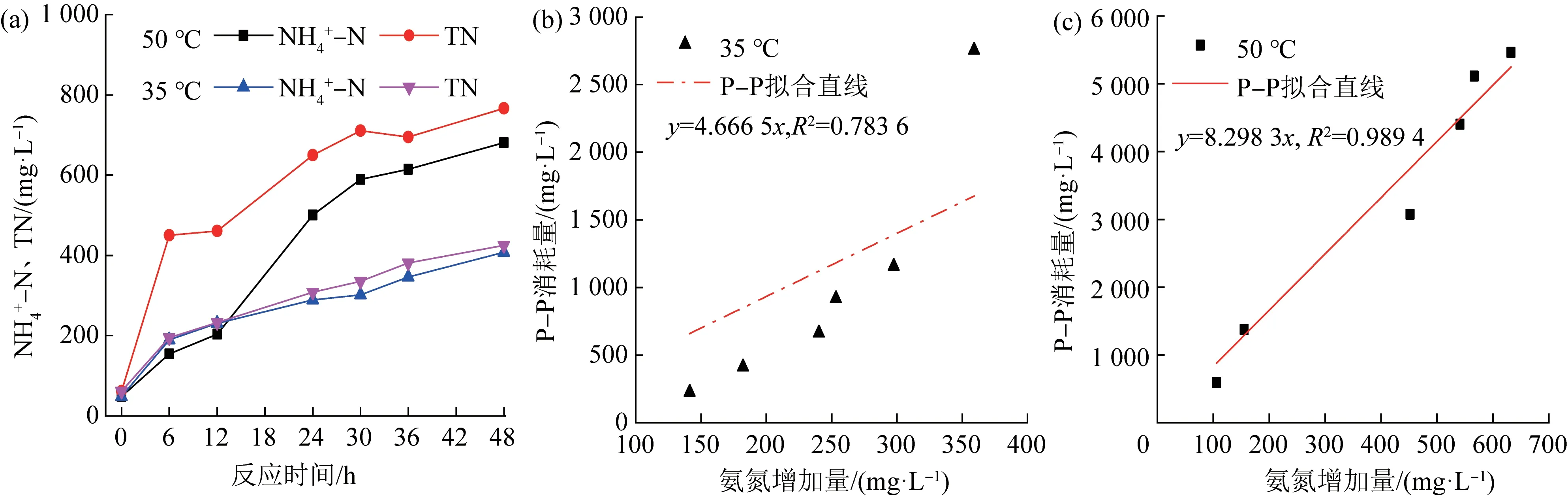
图6 氮元素的溶出量(a)及其与P-P 分解量之间的关系(b、c)Fig. 6 Dissolution of nitrogen(a)and relationship with P-P decomposition(b,c)
由图6(a)可见,0~12 h 期间高温和中温发酵体系的氨氮溶出量非常接近,但高温条件下的TN 比中温TN 高得多,表明高温体系中大量含氮有机物被释放出来;12~48 h 期间,高温体系的氨氮和TN 含量增多,与中温体系的氮溶出量的差距逐渐增大,应该与高温条件下更多颗粒性蛋白质(P-P)被降解有关,推测氮元素的释放与P-P 降解存在某种关联。此外,发现氨氮增量与P-P 分解量之间存在较好的线性相关性〔见图6(b)、(c)〕,建立氨氮增加量与P-P 分解量的关系式,如式(3)所示。

式中:y——t时刻P-P 分解量,mg/L;
x——t时刻氨氮的增加量,mg/L;
β——转化因子。
图6(b)、(c)中,中温和高温条件下的β分别为4.67、8.30,说明高温环境中蛋白质分解产生的多肽和氨基酸被微生物进一步转化为氨氮和VFAs,未出现明显的中间产物积累;而中温条件下水解液中含有相当比例的未知溶解性有机物(可能是蛋白质分解中间产物),中间产物的积累导致微生物分解蛋白质能力下降,仅有少量蛋白质被微生物分解和利用。
由于活性污泥中存在可作菌种的产酸微生物,以及作为基质的被分解微生物,因此试验采用自然驯化方式进行厌氧产酸。当被分解微生物死亡后,其体内磷元素进入水相作为产酸微生物的基质,供产酸微生物新陈代谢。考察了中温、高温发酵过程中磷元素溶出量及MLVSS 减量情况,如图7 所示。

图7 磷元素溶出量及MLVSS 减量情况Fig. 7 Changes in phosphorus leaching and reduction of MLVSS
由图7(a)可见,高温发酵0~12 h 时磷酸盐和TP迅速升高,表明磷的溶出速率大于磷利用速率,此阶段以污泥水解为主;12~48 h 时,磷酸盐和TP 明显降低,表明磷的溶出速率小于磷利用速率,此阶段以污泥产酸微生物自身增殖为主。在中温发酵体系中,磷酸盐和TP 始终呈上升趋势,可能是中温环境中产酸微生物活性较低且繁殖速率缓慢所致。
厌氧发酵体系中磷元素的来源主要为活性污泥本身,因此可通过计算污泥TP 的释放量估算MLVSS减少量。活性污泥通式为C118H170O51N17P,1 g 活性污泥含有0.01 g 磷原子〔27〕,当水解液中的TP 发生变化时,可判断(非)产酸微生物处于死亡或倍增状态。鉴于精确测定污泥体系的微生物含量变化非常困难,实际应用时常用MLVSS 代替,如式(4)所示。

式中:w——估算MLVSS 减量比,%;
ct——t时刻水解液中的TP,mg/L;
c0——0 时刻水解液中的TP,mg/L;
c'0——0 时刻污泥中TP 的估算值,174.58 mg/L。
MLVSS 减量比的实测值与估算值如图7(b)所示。高温发酵时,0~12 h 内MLVSS 减量比的实测值与估算值非常接近,此阶段污泥以水解为主,TP 随之溶出;12 h 后MLVSS 减量比的实测值与估算值差距逐渐增大,此阶段污泥以产酸为主,即产酸微生物利用溶出的磷元素进行自身增殖。中温环境中,MLVSS 减量比的实测值与估算值差距较大,表明TP变化不用于估算中温发酵时的MLVSS 变化。
3 结论
(1)高温厌氧发酵可显著促进污泥絮体的解离,使污泥颗粒粒径减小,增加微生物反应机率并提高反应效率。
(2)厌氧发酵过程中MLVSS、颗粒性碳水化合物和颗粒性蛋白质的水解过程均遵循一级反应动力学,且高温水解速率常数显著高于中温水解速率常数。
(3)厌氧发酵产酸液中的未知溶解性有机物可能是蛋白质或碳水化合物降解过程的中间产物,此类物质积累多、转化慢,可能是中温发酵产酸效果明显低于高温条件的原因之一。
(4)高温发酵获得的VFA 约为中温时的2 倍,且高温发酵产酸液VFAs 中大分子质量有机酸的浓度和比例更高。
