环磷酰胺联合甲强龙对急性百草枯中毒模型家兔肺组织氧化应激损伤的影响
2022-08-30蒋昌华重庆市涪陵中心医院重庆408000
蒋昌华 (重庆市涪陵中心医院,重庆 408000)
百草枯是目前世界上使用最为广泛的除草剂,人误食后主要作用于肺[1]。晚期肺纤维化导致的呼吸衰竭是百草枯主要致死原因[2]。我国作为农业大国,百草枯应用广泛,目前,虽然百草枯已属禁止药物,但因其在农业上应用效果显著,个别地区仍有使用,中毒病例数一直居高不下,由于救治技术进展缓慢,病死率位居第一[3-5]。为探索新的救治方法,提高百草枯中毒治疗成功率以及改善患者预后,本研究建立百草枯急性中毒家兔模型,探究环磷酰胺联合甲强龙的治疗效果,观察其对家兔肺组织氧化应激损伤的影响。
1 材料与方法
1.1 材料
1.1.1 实验动物 50 只8~10 月龄家兔,平均年龄(9.1±0.7)个月,体质量3 000~3 990 g,平均体质量(3 465.2±362.8)g,由维通利华动物技术公司提供。于30%~35%相对湿度、(23.8±1.5)℃环境中喂养1周,光照12 h/d。本研究经重庆市涪陵中心医院伦理委员会批准。
1.1.2 主要试剂 20%百草枯溶液购于南京杜邦生物化工公司;SOD、MDA 测试盒及HE 染色试剂盒购于南京建成生物工程研究所;家兔血清TGF-β1及PⅢP测试盒购于上海史瑞可生物科技有限公司;兔抗大鼠TNF-α、TIMP-1 ELISA 试剂盒购于美国R&D公司。
1.2 方法
1.2.1 建模 参考靳妍等[6]百草枯中毒小鼠建模标准进行建模,50 只家兔随机分为阴性对照组、百草枯组、甲强龙组、环磷酰胺组、联合治疗组,每组10 只。对各组家兔进行麻醉处理,去除背部体毛,固定,消毒,建模在无菌环境中进行。家兔实验前禁食不禁水12 h,百草枯组、甲强龙组、环磷酰胺组及联合治疗组腹腔注射20%百草枯溶液,12 h后,甲强龙组腹腔注射甲强龙(60 mg/kg),环磷酰胺组腹腔注射环磷酰胺(50 mg/kg),联合治疗组腹腔注射甲强龙(60 mg/kg)及环磷酰胺(50 mg/kg),以10%生理盐水溶解,阴性对照组注射等量生理盐水。观察各组家兔行为及肺外观变化。
1.2.2 血清采集 于1 d、2 d、3 d、4 d 对家兔耳缘进行静脉采血。将家兔固定于固定箱内,剪除耳缘静脉局部被毛,乙醇消毒,手指轻弹兔耳使其静脉充盈扩张,左手拇指按压家兔近心端,右手将针头刺入耳缘静脉使血液流出。血样放置于促凝真空管,2 h 内 3 000 r/min 离心,静置 5 min,取出血清样本,冷冻保存。
1.2.3 标本采集 取血完成后对家兔进行空气栓塞处死,立即开胸,分离肺组织送检。送检前将肺组织固定于4%甲醛溶液完全浸泡,24 h后行常规石蜡包埋及连续切片,组织学光镜检测,切片前进行HE染色。
1.2.4 HE 染色 烤干切片,脱蜡处理,顺序置于梯度浓度乙醇中复水3 min。苏木精染色15 min,清洗3次,盐酸-乙醇分化处理30 s,充分清洗,1%伊红染色,乙醇脱水,脱蜡,封片,显微镜下观察。
1.2.5 RT-PCR 检测 TNF-α mRNA、TIMP-1 mRNA表达 提取细胞总RNA,检测RNA纯度、含量,逆转录获得cDNA,设计引物序列,所得RNA 以逆转录试剂盒逆转录为cDNA,荧光定量PCR 仪扩增,反应条件:95 ℃预变性 90 s;5 ℃变性 10 s,60 ℃退火 30 s,共40 个循环。扩增反应结束后,65 ℃缓慢加热至95 ℃,建立 PCR 产物熔解曲线,2-ΔΔCt法计算,采用Primer Premier 6.0 软件设计 PCR 引物,由 Invitrogen公司合成引物。
1.2.6 ELISA 检测TGF-β1、HYP、PⅢP、NE 水平处死大鼠,收集外周血,30 min 内以1 500 r/min 离心20 min,取上清,-80 ℃保存待测。按试剂盒说明书检测TNF-α、TIMP-1蛋白及TGF-β1、PⅢP、NE水平,采用50 mm 碳酸盐包缓冲液稀释抗原,加入聚苯乙烯反应孔,加盖,4 ℃放置24 h,次日洗涤3次,干燥,0.1 ml/孔加入稀释的待测标本,并加入阳性和阴性对照,42 ℃放置60 min,移除液体,洗涤3 次,干燥,0.1 ml/孔加入TNF-α、TIMP-1蛋白及TGF-β1、PⅢP、NE抗体,放置60 min,移除液体,洗涤3次,抛干,加入底物液混匀,加入0.1 ml邻苯二胺遮光反应20 min,0.05 ml/孔加入2 mol/L H2SO4终止反应。
1.2.7 黄嘌呤氧化酶法检测SOD 水平 取聚苯乙烯试管,分为测量管、对照管。提取样品,于上清中加入10倍体积的蒸馏水,配制为1%溶液。测量管、对照管内均加入1.0 ml 试剂盒试剂,测量管加入样品50 μl,对照管内加50 μl蒸馏水,放入旋涡混匀器充分混匀,37 ℃恒温水浴40 min。显色:对照管、测量管中各加2 ml 显色剂,室温放置10 min。采用蒸馏水调零分光光度法计算(波长550 nm,1 cm光径)。
1.2.8 MDA 检测 取聚苯乙烯试管,分为标准管、标准空白管及测量管、测量空白管,标准管中加入10 nmol/L 四乙氧基丙烷0.1 ml 与试剂盒试剂,标准空白管加0.1 ml无水乙醇与试剂,测量管加入0.1 ml肌肉组织匀浆上清与试剂盒试剂,测量空白管加0.1 ml 肌肉组织匀浆上清与试剂盒试剂,摇动试管架混匀,标准管、标准空白管、测量管置于3 ml 硫代巴比妥酸与1 ml 双蒸水,测量空白管置于硫代巴比妥酸3 ml 与50%冰乙酸1 ml。所有试管置于旋涡混匀器混匀,试管口采用保鲜薄膜扎紧,针头刺出1 个小孔,95 ℃水浴40 min,流水冷却,4 ℃、3 500~4 000 r/min 离心10 min,移液器吸取上清,加入比色皿内待检,蒸馏水调零分光光度法计算MDA值。
1.2.9 肺湿/干重比检测 取家兔右肺上叶,切除多余结缔组织,擦拭表面血液,天平称量,80 ℃烘烤48 h,称量,计算肺湿/干重比。
1.3 统计学分析 采用SPSS21.0软件进行统计学分析,计量资料以表示,多组间比较采用单因素方差分析,P<0.05为差异具有统计学意义。
2 结果
2.1 HE 染色结果 阴性对照组家兔肺组织肺泡结构较为清晰,且肺泡壁薄,仅有少数红细胞。百草枯组家兔肺泡萎缩塌陷较为明显,且已出现大量纤维化改变。环磷酰胺组与甲强龙组家兔肺组织内纤维化缓解,联合治疗组纤维化明显缓解(图1)。

图1 各组家兔肺组织病理学变化Fig.1 Pathological changes of lung tissue of rabbits in each group
2.2 TNF-α、TIMP-1 mRNA 表达 如表 1 所示,与阴性对照组、甲强龙组、环磷酰胺组及联合组相比,百草枯组 TNF-α、TIMP-1 mRNA 表达升高,与阴性对照组相比,甲强龙组、环磷酰胺组及联合治疗组TNF-α、TIMP-1 mRNA 表达升高,与甲强龙组相比,环磷酰胺组及联合治疗组TNF-α、TIMP-1 mRNA 表达降低,且联合治疗组 TNF-α、TIMP-1 mRNA 表达低于环磷酰胺组(P<0.05)。
表1 各组家兔肺组织 TNF-α、TIMP-1 mRNA 表达(,n=10)Tab.1 TNF-α and TIMP-1 mRNA expressions in lung tissue of rabbits in each group(,n=10)

表1 各组家兔肺组织 TNF-α、TIMP-1 mRNA 表达(,n=10)Tab.1 TNF-α and TIMP-1 mRNA expressions in lung tissue of rabbits in each group(,n=10)
Note:Compared with negative control group,1)P<0.05;compared with paraquat group,2)P<0.05;compared with methylprednisolone group,3)P<0.05;compared with cyclophosphamide group,4)P<0.05.
TIMP-1 mRNA 1.04±0.15 2.23±0.231)1.88±0.171)2)1.57±0.171)2)3)1.41±0.151)2)3)4)Groups Negative control Paraquat Methylprednisolone Cyclophosphamide Combined treatment TNF-α mRNA 1.12±0.19 2.45±0.261)1.83±0.181)2)1.65±0.161)2)3)1.31±0.131)2)3)4)
2.3 SOD 及 MDA 含量比较 建模 2 d、4 d 后,与阴性对照组、甲强龙组、环磷酰胺组及联合治疗组相比,百草枯组SOD含量降低、MDA 含量升高,与阴性对照组相比,甲强龙组、环磷酰胺组及联合治疗组SOD 含量降低、MDA 含量升高,与甲强龙组相比,环磷酰胺组及联合治疗组SOD含量升高、MDA 含量降低,且联合治疗组SOD 含量高于、MDA 含量低于环磷酰胺组(P<0.05,表2)。
表2 各组血清SOD及MDA含量比较(,n=10)Tab.2 Comparison of serum SOD and MDA contents in each group(,n=10)

表2 各组血清SOD及MDA含量比较(,n=10)Tab.2 Comparison of serum SOD and MDA contents in each group(,n=10)
Note:Compared with negative control group,1)P<0.05;compared with paraquat group,2)P<0.05;compared with methylprednisolone group,3)P<0.05;compared with cyclophosphamide group,4)P<0.05.
Groups 4 d 4.21±0.31 10.68±0.751)8.83±0.581)2)7.12±0.421)2)3)6.15±0.371)2)3)4)SOD/(U·ml-1)2 d 269.53±16.24 203.36±10.211)221.57±11.561)2)231.57±12.361)2)3)252.63±14.471)2)3)4)4 d 272.36±18.34 146.25±11.271)164.25±10.791)2)195.31±11.791)2)3)212.15±12.641)2)3)4)Negative control Paraquat Methylprednisolone Cyclophosphamide Combined treatment MDA/(nmol·ml-1)2 d 5.16±0.29 9.95±0.421)8.69±0.351)2)6.75±0.421)2)3)5.41±0.421)2)3)4)
2.4 血清 TGF-β1、PⅢP 及 HYP 水平比较 建模2 d、4 d 后,与阴性对照组、甲强龙组、环磷酰胺组及联合治疗组相比,百草枯组TGF-β1、PⅢP及HYP 水平升高,与阴性对照组相比,甲强龙组、环磷酰胺组及联合治疗组TGF-β1、PⅢP及HYP 水平升高,与甲强龙组相比,环磷酰胺组及联合治疗组TGF-β1、PⅢP及 HYP 水平降低,且联合治疗组 TGF-β1、PⅢP 及HYP水平低于环磷酰胺组(P<0.05,表3)。
表3 各组血清TGF-β1、PⅢP、HYP水平比较(,n=10)Tab.3 Comparison of serum levels of TGF-β1,PⅢP and HYP in each group(,n=10)
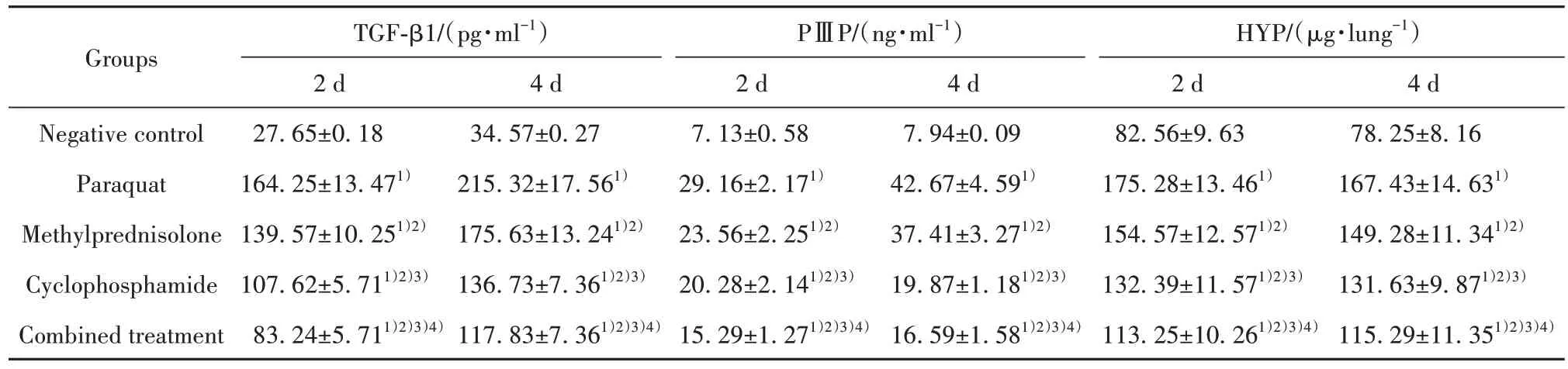
表3 各组血清TGF-β1、PⅢP、HYP水平比较(,n=10)Tab.3 Comparison of serum levels of TGF-β1,PⅢP and HYP in each group(,n=10)
Note:Compared with negative control group,1)P<0.05;compared with paraquat group,2)P<0.05;compared with methylprednisolone group,3)P<0.05;compared with cyclophosphamide group,4)P<0.05.
Groups 4 d 78.25±8.16 167.43±14.631)149.28±11.341)2)131.63±9.871)2)3)115.29±11.351)2)3)4)TGF-β1/(pg·ml-1)2 d 27.65±0.18 164.25±13.471)139.57±10.251)2)107.62±5.711)2)3)83.24±5.711)2)3)4)4 d 34.57±0.27 215.32±17.561)175.63±13.241)2)136.73±7.361)2)3)117.83±7.361)2)3)4)PⅢP/(ng·ml-1)2 d 7.13±0.58 29.16±2.171)23.56±2.251)2)20.28±2.141)2)3)15.29±1.271)2)3)4)4 d 7.94±0.09 42.67±4.591)37.41±3.271)2)19.87±1.181)2)3)16.59±1.581)2)3)4)Negative control Paraquat Methylprednisolone Cyclophosphamide Combined treatment HYP/(μg·lung-1)2 d 82.56±9.63 175.28±13.461)154.57±12.571)2)132.39±11.571)2)3)113.25±10.261)2)3)4)
2.5 NE 水平及肺上叶湿/干重比 与阴性对照组、甲强龙组、环磷酰胺组及联合治疗组相比,百草枯组NE 水平及肺上叶湿/干重比升高,与阴性对照组相比,甲强龙组、环磷酰胺组及联合治疗组NE 水平及肺上叶湿/干重比升高,与甲强龙组相比,环磷酰胺组及联合治疗组NE 水平及肺上叶湿/干重比降低,且联合治疗组NE 水平及肺上叶湿/干重比低于环磷酰胺组(P<0.05,表4)。
表4 各组NE水平及肺上叶湿/干重比比较(,n=10)Tab.4 Comparison of wet/dry weight ratio of upper lobe and NE level in each group(,n=10)

表4 各组NE水平及肺上叶湿/干重比比较(,n=10)Tab.4 Comparison of wet/dry weight ratio of upper lobe and NE level in each group(,n=10)
Note:Compared with negative control group,1)P<0.05;compared with paraquat group,2)P<0.05;compared with methylprednisolone group,3)P<0.05;compared with cyclophosphamide group,4)P<0.05.
Wet/dry weight ratio/%3.59±0.12 9.86±0.791)8.71±0.371)2)6.16±0.211)2)3)4.32±0.411)2)3)4)Groups Negative control Paraquat Methylprednisolone Cyclophosphamide Combined treatment NE/(10-3 U·L-1)2.57±0.08 15.42±3.241)10.79±0.811)2)6.35±0.461)2)3)5.36±0.431)2)3)4)
3 讨论
百草枯对植物、人类、动物均有较强毒性,主要作用于肺,误食早期多出现急性肺损伤,晚期则发生肺纤维化,病死率高达60%~80%[7]。研究发现,腹腔注入百草枯构建大鼠模型,第1 天就会对肺组织造成严重损伤[8]。百草枯主要使体内生成氧自由基诱导脂质过氧化,从而导致组织细胞,尤其是肺组织出现氧化性损伤[9]。百草枯中毒后,肺部由于出现大量超氧阴离子自由基,引起较强烈的外源性氧化应激反应,导致肺组织细胞DNA 大量凋亡。甲强龙作为临床常用激素类药物,属于糖皮质激素,可缓解机体中毒,但副作用较多[10]。环磷酰胺属于烷化剂类免疫抑制剂,作为细胞毒性药物,能够杀死有丝分裂及进入循环周期的细胞,破坏内部DNA结构,阻断细胞复制,因此具有较强的免疫抑制作用[11]。研究表明,环磷酰胺可抑制动物体液免疫和细胞免疫,导致免疫抑制[12]。
早期急性肺炎与后期肺纤维化是百草枯中毒过程显著的病理改变,其中炎症细胞浸润及炎症因子释放具有重要作用。研究显示,百草枯导致肺纤维化过程的主要机制为炎症反应,炎症细胞因子水平在中毒过程中均升高[13]。其中 TNF-α 作为主要细胞因子参与肺损伤形成,在肺组织炎症反应中发挥重要作用,通过观察TNF-α 水平能够反映肺损伤过程中炎症反应严重程度。研究显示,急性百草枯中毒发展过程中,TIMP-1 水平升高,发展为肺间质纤维化中,与TIMP-1表达密切相关[14]。随着TNF-α、TIMP-1 细胞因子在肺纤维化发病及病理过程中的作用备受关注,本研究同时检测TNF-α、TIMP-1 mRNA 及 TNF-α、TIMP-1 蛋白水平,结果显示,环磷酰胺联合甲强龙治疗,TNF-α、TIMP-1 mRNA 及TNF-α、TIMP-1蛋白水平显著下降,说明二者联合治疗能够降低百草枯中毒过程中的炎症反应。
百草枯作用于机体后,会被肺泡细胞摄取,导致氧化还原反应中大量OFR 出现,机体处于氧化应激状态,从而释放炎症因子,细胞及线粒体钙稳态失衡,引发过氧化反应造成肺损伤[15]。SOD 作为机体内重要的自由基清除剂,MDA 作为脂质过氧化终产物之一,临床上常用于评价机体氧化损伤程度[16]。本研究显示,环磷酰胺联合甲强龙对急性百草枯中毒模型家兔进行治疗,SOD 下降程度与MDA上升程度较低,说明二者联合治疗可抑制氧化应激,缓解肺损伤。
研究认为TGF-β 是启动纤维化形成的枢纽,可诱导成纤维细胞向肌成纤维细胞转化,从而促进胶原合成、分泌,使成纤维细胞增殖数增加,从而导致纤维化[17]。其中 TGF-β1 作为重要的致纤维化因子,临床认为其是抗纤维化治疗理想靶点[18]。PⅢP是Ⅲ型前胶原转化成Ⅲ型胶原时释放的多肽,其水平出现增高说明组织纤维化开始,是早期肺纤维化诊断的有力评价指标[19]。本研究显示,环磷酰胺联合甲强龙治疗急性百草枯中毒模型家兔,TGF-β1、PⅢP及HYP水平降低,说明二者联合治疗可抑制肺纤维化形成。
NE是中性丝氨酸蛋白酶的一种,可分解钙黏连素,导致肺纤维网状支架塌陷及增加肺毛细血管膜通透性,血浆蛋白及活性物质较多地渗进肺间质、肺泡,导致机体非心源性肺水肿[20]。研究显示,NE是导致肺组织损伤、加重肺不张过程中重要的酶,因此,NE变化监测可预测肺组织损伤情况[21]。研究表明,肺组织中湿/干重比能够间接说明肺内漏出液体多少,漏出液体越多,肺湿/干重比越高,同时灌洗液回收率也随着增高[22]。本研究显示,环磷酰胺联合甲强龙治疗急性百草枯中毒模型家兔,NE水平及肺上叶湿/干重比降低,说明二者联合治疗可减轻肺组织损伤、肺不张及肺内漏液情况。
综上所述,环磷酰胺联合甲强龙治疗急性百草枯中毒模型家兔,可缓解急性百草枯中毒家兔炎症反应,抑制氧化应激及肺部纤维化形成,减轻肺组织损伤,同时缓解肺不张以及肺内漏液情况。
