氯苯低压热解的原位同步辐射光电离质谱研究
2022-08-24许鸣皋文武赵龙杨玖重朱宝忠孙运兰潘洋
许鸣皋,文武,赵龙,杨玖重,朱宝忠,3,孙运兰,3∗,潘洋∗
(1 安徽工业大学冶金工程学院, 安徽 马鞍山 243032;2 中国科学技术大学国家同步辐射实验室, 安徽 合肥 230026;3 常州大学石油工程学院, 江苏 常州 213164)
0 引 言
工业冶金、垃圾焚烧和石油化工等生产生活所排放的烟气和飞灰中会产生对环境和健康有害且难以自然降解的氯苯类(CBs)、氯酚类(CPs)、多氯萘(PCNs)、多氯联苯(PCBs)和二噁英(PCDD/Fs)等副产物[1]。这类物质是破坏臭氧层、导致温室效应和光化学烟雾形成的主要原因之一[2]。其中,CBs 作为重要的原料和中间体,亦被应用于医用有机合成、工业生产和实验室溶剂使用等多种领域。然而, 无论是工业废气、垃圾焚烧还是废弃原料所排放的CBs,除其本身具有高度污染和生物积累的特性外,也是形成PCDD/Fs 和PCNs 等多种高毒性环境污染副产物的重要前驱物[3,4]。《大气污染物综合排放标准》(GB16297-1996)中明确规定了氯苯类污染物排放浓度不超过60 mg·m−3。
CBs 污染物的传统处理方法是通过高温焚烧,使其转化为CO2、H2O 和HCl 等产物,而高温下又无法遏制CBs 进一步转化为毒性和危害性更强的PCDD/Fs 和PCNs 等副产物[2]。因此关于CBs 在高温下的热分解路径以及如何有效地抑制氯苯聚合和加氯反应成为关注的研究重点。由于CBs 热解过程的复杂性和受实验技术手段的限制,前人对CBs 热解研究十分有限[5],特别是关于反应中间体的研究并无报道。氯苯作为CBs 代表性物质广泛应用于工业和科学研究[6−12]。Vin 等[3]利用射流搅拌反应器和流动管反应器对氯苯热解、氯苯/氢反应、氯苯/甲烷反应进行研究,利用气相色谱/质谱(GC/MS)对产物进行分析,建立了动力学模型,并发现氢加成对氯化和双环产物的形成有很强的抑制作用。Liu 等[5]利用GC/MS 研究了氯苯在HCl 气氛下热解过程中PCBs 的形成,发现氯原子取代量较少的氯化苯生成的PCBs 较多。GC/MS 虽然是一种成熟的定性定量分析方法,但分离时间较长,无法进行原位检测,导致一些活性反应中间体信息缺失。原位同步辐射光电离质谱技术(SR-PIMS)将超声分子束取样与同步辐射真空紫外光电离质谱技术相结合,不仅能通过射流冷却降低不稳定中间体的平动温度,减少碰撞,从而实现对不稳定中间体的探测,还能通过调谐同步辐射光子能量对待测物进行扫描,通过电离能不同来甄别复杂气相反应产物中的活泼气相中间物种和同分异构体。此外,同步辐射光真空紫外光电离是一种软电离方式,实验中所产生的碎片极少。该技术已经在热解、燃烧、分析和催化等领域得到了广泛应用[13−17]。
本文利用流动管反应器结合SR-PIMS 技术在4 kPa 压力对氯苯热解进行研究,获得了低压条件对反应产物性质和浓度的影响机制,分析了关键中间体苯炔的形成过程,总结了低压对于含氯有机物形成的影响规律,为研发更好的新技术方法进而减少甚至防止含氯有机危险废物的排放提供基础理论指导。
1 实验部分
1.1 主要仪器与装置
本工作中氯苯热解实验是在中国科学技术大学国家同步辐射实验室燃烧光束线站(BL03U)完成。实验装置在以往的报道中已有完整描述[18]。飞行时间质谱仪的质量精度为44.6×10−6(质荷比m/z=112),分辨率为2098(质荷比m/z=112)。
图1 是原位同步辐射光电离质谱及流动管热解装置示意图。该实验装置由流动管热解反应器(i)、差分腔(ii)、电离室(iii)和反射式飞行时间质谱仪(iv)四部分组成。流动反应器置于热解腔中,有效加热长度为150 mm。石英喷嘴置于流动反应器出口处附近,产物通过喷嘴取样进入差分室,再经过镍制漏勺(美国Beam Dynamics 公司)准直形成超声分子束进入到电离室中。差分室连接热解腔和电离室,分子束在电离室内与同步辐射光交叉,被真空紫外光电离成离子。电离室与飞行时间质谱仪相连,离子在电离室中被推斥进入质谱中检测。流动管反应器温度测量的误差为±30 K,具体的测温过程详见文献[18]。

图1 原位同步辐射光电离质谱及热解装置示意图Fig.1 Schematic diagram of in-situ synchrotron radiation photoionization mass spectrometry and flow reactor pyrolysis system
1.2 主要材料与试剂
氯苯(C6H5Cl,99.5%)购于阿拉丁(上海)试剂有限公司。氩气(99.999%)购置于南京特种气体有限公司。
1.3 实验条件及方法
将氯苯液体通过注射泵以0.009 mL·min−1流速(498 K)送入汽化罐中,然后用氩气完全稀释。混合气体以1 L·min−1(273 K,101.325 kPa)的总流量流入石英流动管反应器内。流动管内的压力精确控制在4 kPa。氯苯的初始摩尔分数为0.002。
实验压力条件为4 kPa。根据热解炉温度和光子能量两种参数的不同设定,实验主要通过固定光子能量(10 eV 和11 eV),再通过已知测温曲线对热解炉进行温度设定,即“温度”作为单一变量,扫描热解炉的温度最终获得热解母体、氩气和热解产物随温度变化的信号图谱。即在温度873∼1373 K 范围内以间隔50 K 为固定温度点采集时长为60 s 的质谱图。

通过比对NIST 数据库以及光子电离截面数据库[19]中物种已知电离能信息,可推测本次实验中所探测到的产物信息。以上获得的产物质谱信号经过数据处理软件处理,可获得随温度变化的摩尔分数曲线,详细流程可参见文献[18]。物种i的离子信号可以写为式中Si(T,E,t)为被测物种i的离子信号(即i物种信号的积分强度),其中T是反应温度,E是光子能量,t是反应时刻;C为比例常数;Xi(T,t)为在温度T下某个反应时刻t时物种i的摩尔分数;σi(E)为物种i在光子能量E时的光电离截面;Di为物种i的质量歧视因子,只与其分子量相关,且可以从实验上确定;Φp(T,E,t)为在光子能量E时的光子通量;F(k,T,P)为经验仪器取样函数(由产生分子束的取样喷嘴的几何构型和气体动力学特性决定,与反应室的温度T、压力P和样品的比热容比k相关)。光电离定量可参照Cool 等[20]提出的物种摩尔分数即物种浓度再根据式(1)来计算,实验中利用物种的光电离截面大小不同,对物种进行定性与定量分析并对同分异构体进行区分,详细介绍可参见李的工作[21,22]。由式(1)可以通过已知的物种摩尔分数和光电离截面结合待求物种的光电离截面进而计算出待求物种的摩尔分数。
氯苯转化率“α”的计算公式为

式中I1、M1分别是氯苯进口和在线监测的摩尔分数,M2为热解产物在线监测的摩尔分数,N代表产物分子式中含碳元素的数量。
2 结果与讨论
2.1 氯苯低压热解
2.1.1 热解物种鉴定
图2 展示了在压力为4 kPa、光子能量为11 eV 条件下,不同热解温度下的氯苯热解光电离质谱图。由于在光子能量小于12.02 eV 时,氯苯不能发生光解而产生碎片[12],表明质谱图中新出现的信号峰为氯苯热解产物。表1 汇总了本工作中热解产物通过质谱定标的鉴定结果以及文献中各相关产物的光解电离能。

表1 氯苯及主要热解产物鉴定结果Table 1 Species identification of chlorobenzene pyrolysis

图2 光子能量为11 eV、压力为4 kPa 时不同温度下氯苯热分解光电离质谱图。(a)873 K;(b)1173 K;(c)1223 K;(d)1323 K;(e)1373 KFig.2 Photoionization mass spectra of chlorobenzene pyrolysis at different thermal decomposition temperatures with photon energy of 11 eV and pressure of 4 kPa. (a)873 K;(b)1173 K;(c)1223 K;(d)1323 K;(e)1373 K
2.1.2 氯苯及产物随温度的变化规律
为了对产物的形成机制进行分析,根据产物的种类不同,将产物分成以下三类: 1)小分子产物(≤C6);2)芳烃产物(AH);3)含氯芳烃产物(Cl-AH)。图3 展示了4 kPa 热解产物随温度变化的摩尔分数柱状趋势图。可见,小分子产物摩尔分数明显高于另外两类产物。结合文献[3,12,34,35]和氯苯以及产物随温度变化规律绘制了氯苯热解的反应路径图,如图4 所示。
图3(a)为氯苯摩尔分数随温度变化的趋势图。从图中分析可知氯苯在1173 K 后开始出现明显且持续性转化,在最高温1373 K 时被转化近40%。

图3 4 kPa 条件下氯苯热解产物的摩尔分数柱状图。(a)氯苯;(b)小分子产物(≤C6);(c)芳烃产物(AH);(d)含氯芳烃产物(Cl-AH)Fig.3 Mole fraction histograms of chlorobenzene pyrolysis products at 4 kPa. (a)Chlorobenzene;(b)small molecule product(≤C6);(c)aromatic hydrocarbon product(AH);(d)chlorinated aromatic hydrocarbon product(Cl-AH)
氯苯热解主要生成小分子产物(≤C6),其中包含丁二炔、乙烯基乙炔、己三炔、苯炔和苯。图4 展示了小分子产物的生成路径。氯苯分子解离的第一步是通过H 和Cl 原子脱除反应(R1-3),进而形成了苯基自由基(•C6H5)、氯苯基自由基(•C6H4Cl)和苯炔。Vin 等[3]报道了在氯苯热解过程中C-Cl 键断裂的能量为95 kcal·mol−1,而C-H 键断裂所需能量更高。Vin 等[3]和Xu 等[12]研究表明,氯苯热解中H 和Cl 与自由基之间的反应(R4-5)是消耗氯苯导致苯基自由基大量生成的主要途径。苯基自由基结构极不稳定,势必通过加氢反应(R6)和消氢反应(R7)生成结构更为稳定的苯和苯炔[34,35]。虽然氯苯可以通过分子内消除HCl 进而生成苯炔,但是该反应对苯炔的贡献相对较小[3,12]。从图3(b)可以看出苯和苯炔在氯苯低压热解产物中占据主导地位,进一步说明了苯和苯炔是氯苯初始热解的主要产物。
氯苯热解过程主要有以下反应:

Wang 等[34]报道了苯基自由基通过加氢反应和消氢反应生成苯和苯炔所需克服的能垒分别为20 kcal·mol−1和106.6 kcal·mol−1,从图3(b)可以看出,苯的生成温度为1173 K,低于苯炔的生成温度1223 K,在1223∼1273 K 温区内,苯是摩尔分数最高的产物。然而,当温度超过1273 K,苯炔的摩尔分数则大幅增加,这是由于高温使得苯基自由基的消氢反应逐渐占据热分解路径的主导地位[36,37]。
苯环结构在高温下将发生断键开环, 苯炔通过断开C-C 键分解成结构更为稳定的短链产物[35], 例如丁二炔。Zhang 等[36]研究表明,在较高的温度下,苯炔容易裂解为乙炔和丁二炔。从图3(b)可以看出,在1273∼1373 K 温区内丁二炔和苯炔摩尔分数的增幅最大且具有一致性。此外,苯炔通过开环也可以形成己三炔[36],而乙烯基乙炔则来源于丁二炔的氢加成反应。在1273 K 以后,乙烯基乙炔和己三炔摩尔分数也有所增加,二者的生成路径可参见图4。氯苯热解的另一个主要产物苯在低压热解也容易通过消氢反应生成苯基自由基[35],进而通过形成苯炔通道形成小分子产物。通过以上分析可以发现苯和苯炔是氯苯低压热解的主要产物,苯炔是形成小分子路径的关键中间体。
从图3(c)-(d)中可以看出,芳烃和氯化芳烃类产物的摩尔分数较低,是氯苯低压热解过程中的次级产物。次级产物生成温度主要集中在1273∼1373 K 温区内。Comandini 等[38]报道了联苯烯是由苯炔通过自加成反应而形成,高温下苯炔大量生成联苯烯。从图3(c)可以发现,芳烃产物中联苯烯摩尔分数最高,是主要芳烃产物,其生成温度为1273 K,并在1273∼1373 K 温区内急剧增加,具有与苯炔相似的增长规律。此外,联苯可以在高温条件下通过苯和苯基自由基加成反应生成[35],如图4 所示。从图3(c)发现,联苯在1323 K有明显增加,但增加趋势较缓,与苯的增幅趋势相似。从上文可知,氯苯主要初始热解产物为苯和苯炔,由于联苯烯和联苯是由初始热解产物的后续反应生成,因此其生成量较其他后续产物更高,此外,高温下联苯烯生成量明显高于联苯。图4 中苯乙炔、萘主要由初始产物和间接产物的后续反应形成,生成量较低。
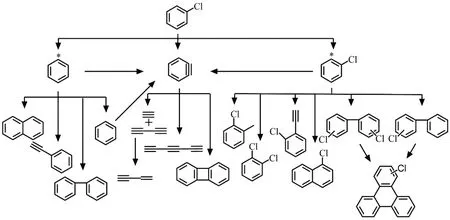
图4 氯苯热解反应路径图Fig.4 The pyrolysis pathways of chlorobenzene
在氯苯热解过程中,虽然含氯芳烃产物的生成量主要为痕量级别,但是危害极大。含氯芳烃产物在结构上分别含有1-3 个苯环结构。2-氯甲苯、2-氯苯乙炔和邻二氯苯都含有1 个苯环结构。其中,2-氯甲苯形成于氯苯基自由基与间接产物甲烷之间的加成反应[12],主要形成于1223∼1373 K 温区内。2-氯苯乙炔的形成途径类似于苯基加成/脱氢加乙炔(HACA)[35]形成苯乙炔的机制,是通过氯苯基自由基与乙炔加成反应[12]。邻二氯苯的生成路径是通过氯苯邻位H 发生Cl 取代反应。1-氯萘、氯联苯和二氯联苯均拥有2 个苯环结构。其中,1-氯萘形成类似于H 提取/乙烯基乙炔加成(HAVA)机制[39],主要通过C6+C4 反应形成;氯联苯和二氯联苯则直接来源于自由基(苯基和氯苯基自由)与分子(氯苯和苯)之间的聚合反应。氯化三亚苯为3环结构,其形成机制类似于苯基加成/脱氢环化(PAC)机制[39],通过苯基自由基与氯联苯或二氯联苯所形成。芳烃和含氯芳烃产物的摩尔分数明显低于小分子产物,这是由于低压的反应条件减少了分子间的碰撞频率,减弱了聚合反应,导致氯苯热解倾向于形成小分子。
2.2 与常压热解的对比
为了进一步直观分析氯苯的热解过程,图5 比较了氯苯在4 kPa 与101 kPa 流动管热解实验[12]中的转化率曲线变化规律。由图可见,氯苯在不同压力下的转化率随温度变化曲线明显不同。在氯苯转化率为32%时,对比低压与常压条件下的温度点之间的差值,可获知热解温区相差约200 K,与文献[40]所描述燃料在不同压力下热解趋势的演变规律相符。低压促使氯苯热解温度升高,且温度越高,与常压下氯苯相同消耗量时的温度值相差越大。

图5 4 kPa 和101 kPa[12]压力条件下氯苯转化率随温度变化趋势图Fig.5 The trend diagram of chlorobenzene conversion rates with temperature at 4 kPa and 101 kPa[12]
图6 比较了不同压力下部分产物选择性变化规律。值得注意的是,苯炔在4 kPa 条件下选择性最高可达到7%,而101 kPa 时最高时仅为1.7%。基于低压可以降低反应速率、增加中间体寿命的特性,进一步验证了苯炔是该体系中重要反应中间体。
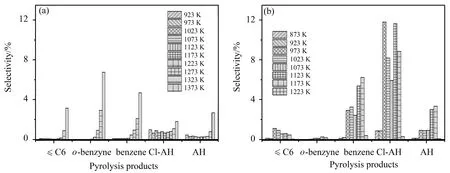
图6 不同压力下部分热解产物选择性柱状图。(a)4 kPa;(b)101 kPaFig.6 Selectivity histograms of some pyrolysis products under different pressure. (a)4 kPa;(b)101 kPa
此外,由图6(a)可以看出,低压增加了C6 以下小分子产物的生成。作为氯苯的初始热解产物,苯在低压和常压下的选择性峰值并未出现明显差异。对于Cl-AH 产物,最大选择性由常压下的12%下降至4 kPa下的不到2%,表明低压降低了加成聚合路径形成的产物例如氯化芳烃的生成。Vin 等[3]曾报道,常压下流动管热解生成含氯类产物路径占消耗氯苯的贡献值达到了38.8%。其他芳烃产物的最大选择性和苯的规律类似,低压和常压下变化不是非常明显。
3 结 论
本研究开展了873∼1373 K 氯苯低压流动管热解实验研究,通过分析产物随温度变化规律以及低压对热解体系的影响,探究了氯苯分解路径上的关键产物和压力对各产物的影响机制,光电离质谱研究结果表明:
1)4 kPa 压力下,氯苯初始分解温度区间为1173∼1223 K,而芳烃类产物开始形成温度为1273 K。此外,热解主要产物为小分子产物(≤C6 产物)。
2)苯炔和苯是氯苯低压热解的主要产物。
3)苯炔是氯苯热解形成小分子路径的关键中间体。
4)低压减弱了氯化芳烃的形成路径,其产物选择性由101 kPa 下的12%下降至4 kPa 下的2%,下降了近6 倍。
