甲磺酸阿帕替尼联合依托泊苷治疗铂耐药复发性卵巢癌二例
2022-08-24郭依琳王武亮
郭依琳,王武亮
卵巢恶性肿瘤是女性生殖系统最常见的三大恶性肿瘤之一。卵巢癌早期症状不明显,大部分发现时已经是晚期,严重威胁女性的生命和健康。手术联合铂类化疗是目前卵巢癌标准的治疗方案,虽然绝大多数患者临床上有改善,但仍有许多患者出现疾病复发。复发性卵巢癌患者预后较差,5 年生存率低。因此,探究卵巢癌发生发展的分子机制,寻找有效的治疗靶点具有重要的意义。血管内皮生长因子(vascular endothelial growth factor,VEGF)及其受体VEGFR 在肿瘤血管和淋巴管生成中发挥重要作用。甲磺酸阿帕替尼(Apatinib Mesylate)是一种小分子VEGFR-2 酪氨酸激酶抑制剂,已被证实在多种恶性肿瘤中均有显著疗效,但其在卵巢癌治疗领域中的研究较少。本研究报告2 例铂耐药的复发性卵巢癌患者接受甲磺酸阿帕替尼联合依托泊苷(Etoposide)治疗,初步探索其疗效和安全性。
1 病例报告
1.1 病例1患者 女,62 岁,因卵巢癌术后第二次复发2个月余,于2019 年11 月6 日就诊于郑州大学第二附属医院(我院)门诊。患者足月产3 次,早产0 次,流产0 次,现在子女3 个,50 岁自然绝经,无高血压、冠心病、糖尿病史,否认家族性肿瘤史及遗传性疾病病史。既往因右下腹疼痛1 个月余,于2014 年3 月16 日入濮阳市油田总医院(外院)治疗。入院查血清糖类抗原125(CA125)为326.2 U/mL,盆腹腔增强CT 示:双侧卵巢囊实性包块。患者接受紫杉醇+卡铂新辅助全身静脉化疗3 个疗程。2014 年5 月26 日,患者于外院行卵巢肿瘤细胞减灭术,手术切除子宫、双侧附件、大网膜和盆腔淋巴结。术后病理示:双侧卵巢中-低分化浆液性乳头状囊腺癌,累及双侧输卵管,大网膜及盆腔淋巴结可见癌转移。基因检测未发现乳腺癌易感基因(BRCA1 和BRCA2)存在突变。患者术后接受紫杉醇+卡铂全身静脉化疗6 个疗程,根据实体瘤反应评估标准(RECIST1.1)和妇科肿瘤协会基于CA125 疗效评估标准(GCIG-CA125),患者疗效评估为完全缓解(complete response,CR)。2019 年2 月8 日,患者出现下腹痛,查CA125 为204.8 U/mL,彩色超声检查示:腹膜后可见数个大小不等的实性低回声团块,较大的2 个分别位于肠系膜上动脉起始段腹主动脉前方,大小约为22 mm×16 mm和26 mm×18 mm。各项检查及检验结果提示肿瘤复发,患者遂接受紫杉醇+卡铂全身静脉化疗5 个疗程,化疗结束后CA125为27.6 U/mL,疗效评估为部分缓解(partial response,PR)。2019年9 月21 日,患者复查CA125 为163.7 U/mL,彩色超声检查示:腹膜后数个大小不等实性低回声团块,较大者约23 mm×16 mm,右侧肾上腺区可见24 mm×16 mm 低回声结节,考虑肿瘤第二次复发。2019 年11 月6 日遂到我院门诊就诊,复查CA125 为399.0 U/mL,胸腹盆腔增强CT 示:右侧肾上腺见肿块影,约为34 mm×19 mm,腹膜后多发肿大淋巴结,见图1A。2019 年11 月7 日患者开始接受甲磺酸阿帕替尼(375 mg/次,1 次/d,3 周为1 个治疗周期)联合依托泊苷(50 mg/次,1 次/d,连续口服2 周,停药1 周,3 周为1 个治疗周期)治疗。2019年12 月19 日,患者在接受2 个周期治疗后,CA125 降至37.4 U/mL,盆腹腔增强CT 示:右侧肾上腺肿块影缩小至26 mm×13 mm,见图1B,疗效评估为PR。患者用药期间出现白细胞计数降低和中性粒细胞计数降低,调整用药剂量,甲磺酸阿帕替尼剂量减至250 mg/次,1 次/d,依托泊苷剂量不变。2020 年8 月27 日,患者治疗14 个周期后,CA125 水平上升至108.0U/mL,CT 检查未提示影像学进展,继续用药观察。2020年10 月29 日,盆腹腔增强CT 示:结肠旁淋巴结出现新发病灶,右侧肾上腺肿块影增大,疗效评估为疾病进展(progressive disease,PD),患者无进展生存期达11.7 个月。在药物不良反应方面,患者治疗期间出现白细胞计数降低,中性粒细胞计数降低,恶心,贫血,未出现高血压和蛋白尿,经过对症治疗后均明显好转。患者于2020 年10 月30 日结束甲磺酸阿帕替尼联合依托泊苷方案治疗,于2021 年9 月16 日病逝。

图1 病例1 接受甲磺酸阿帕替尼联合依托泊苷治疗前后盆腹腔增强CT 图像
1.2 病例2患者 女,48 岁,因卵巢癌术后第一次发现复发14 d,于2021 年6 月21 日就诊于我院门诊。患者足月产1,早产0 次,流产0 次,现在子女1 个,无高血压、冠心病、糖尿病史,否认家族性肿瘤史及遗传性疾病病史。既往因体检发现腹部包块7 d,于2020 年9 月15 日入信阳市中心医院(外院)治疗。入院查血清CA125 为30.24 U/mL,盆腹腔增强CT 示:左侧卵巢囊实性包块,大小约73 mm×85 mm×100 mm。2020 年9 月21 日,患者于外院行卵巢肿瘤细胞减灭术,手术切除子宫,双侧附件,大网膜、阑尾和盆腔淋巴结。术后病理提示,左侧附件高级别浆液性癌,腹膜和骶韧带病灶可见癌组织,右侧附件、大网膜、阑尾及盆腔淋巴结未见癌转移。基因检测未发现BRCA1 和BRCA2 基因存在突变。患者术后接受多西他赛+卡铂全身静脉化疗5 个疗程,疗效评估为CR。患者术后绝经。2021 年6 月7 日,患者复查CA125 为55.9 U/mL,彩超检查示:左侧附件区可见36 mm×33 mm 混合包块。遂就诊于我院门诊,查胸腹盆腔增强CT 示:盆腔内多发结节样软组织影,较大的2 个分别为41 mm×33 mm 和27 mm×27 mm,直肠前方病灶范围10 mm×19 mm,右肺下叶结节影,见图2A。各项检查及检验结果提示肿瘤复发。2021 年6 月24 日,患者开始接受甲磺酸阿帕替尼(375 mg/次,1 次/d,3 周为1 个治疗周期)联合依托泊苷(50 mg/次,1 次/d,连续口服2 周,停药1 周,3 周为1 个治疗周期)治疗。2021 年9 月18 日,患者在接受3 个周期治疗后,CA125 降至12.6 U/mL,盆腹腔增强CT 示:盆腔内多发结节样软组织影较前缩小,2 个大小分别约23 mm×12 mm 和14 mm×13 mm,直肠前方病灶较前缩小,大小约8 mm×11 mm,见图2B,疗效评估为PR。在药物不良反应方面,患者治疗期间出现天冬氨酸转氨酶升高,恶心,体质量下降,血小板计数降低,未出现高血压和蛋白尿等。上述不良反应经对症治疗后均明显好转。目前患者已治疗4.3 个月,且仍在治疗中。
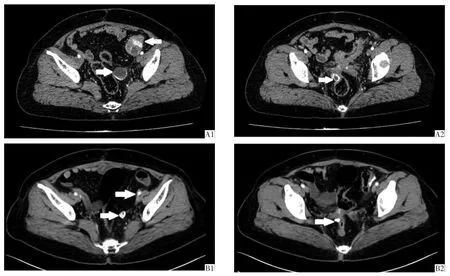
图2 病例2 接受甲磺酸阿帕替尼联合依托泊苷治疗前后盆腹腔增强CT 图像
2 讨论
卵巢癌是最常见的妇科恶性肿瘤之一。2020 年公布全球女性卵巢癌新发病例313 959 例,死亡病例207 252 例[1]。由于卵巢癌患者的临床症状不典型,70%的患者就诊时即为晚期[2]。手术联合化疗是卵巢癌标准的治疗方式,但仍有超过75%的患者在完成了标准的初始治疗后出现疾病复发[3]。根据末次化疗时间和复发时间,可分为铂敏感复发性卵巢癌和铂耐药复发性卵巢癌。铂耐药复发性卵巢癌患者对一线铂类药物不敏感,通常选用非铂类药物治疗,但预后仍较差[4]。
抗肿瘤新生血管靶向药物用于卵巢癌治疗越来越受到国内外专家重视。VEGF 是血管系统发育过程中最重要的细胞因子。VEGF 与VEGFR 结合,促进肿瘤增殖和转移[5]。VEGFR-2 是卵巢恶性肿瘤血管生成的主要受体,抑制VEGFR-2 可以作为抑制肿瘤血管生成的有效策略[6]。目前,已开发的VEGFR-2抑制剂包括索拉非尼(Sorafenib)、西地尼布(Cediranib)和甲磺酸阿帕替尼等。
甲磺酸阿帕替尼是一种新型口服小分子酪氨酸激酶抑制剂,靶向作用于细胞内VEGFR-2 的ATP 结合位点,阻止磷酸化和随后的下游信号传导,抑制肿瘤组织新生血管生成和发挥抗肿瘤的作用[7]。目前,甲磺酸阿帕替尼被我国食品药品监督管理总局批准上市用于晚期胃腺癌或胃-食管结合部腺癌三线或三线以上的治疗[8],但其用于卵巢癌的治疗仍处于临床研究阶段。对于铂耐药复发或难治性卵巢癌,甲磺酸阿帕替尼单药治疗的客观缓解率(objective response rate,ORR)和疾病控制率(disease control rate,DCR)分别为18.2%~41.4%和47.1%~81.8%[9-11],高于依托泊苷、长春瑞滨、伊立替康、奥沙利铂和吉西他滨等其他单药的ORR(10%~37%)[12]。但是,甲磺酸阿帕替尼单药治疗仍未有报道达到CR 的病例。因此,甲磺酸阿帕替尼联合各种化疗方案是否能够获得CR或更好的疗效需要进一步研究。
依托泊苷是一种细胞周期特异性抗肿瘤药物,通过干扰DNA 拓扑异构酶Ⅱ,抑制肿瘤细胞DNA损伤修复,发挥抗肿瘤作用[13]。依托泊苷是治疗复发性卵巢癌经典的口服药物,其ORR、CR 和PR 分别为26.8%、7.3%和19.5%[14]。有研究探索了甲磺酸阿帕替尼联合依托泊苷用于铂耐药复发性卵巢癌的有效性和安全性。Lan 等[15]发表了一项前瞻性Ⅱ期临床试验,报道了甲磺酸阿帕替尼(500 mg/次,1 次/d)联合依托泊苷(50 mg/次,1 次/d,连续口服2 周,停药1周,3 周为1 个治疗周期)治疗35 例铂耐药复发性卵巢癌患者,ORR 和DCR 分别高达54%和86%。Huang 等[12]研究也获得了相似的临床效果。然而,Lan等[15]研究中82%的卵巢癌患者因为药物不耐受而下调了甲磺酸阿帕替尼的剂量,该研究患者平均甲磺酸阿帕替尼暴露剂量只有369.9 mg,且剂量下调后患者仍能从中获益。因此,本研究中对2 例铂耐药卵巢癌患者进行甲磺酸阿帕替尼(375 mg/次,1 次/d,3周为1 个治疗周期)联合依托泊苷治疗。2 例患者在初次疗效评估时均达到PR,且治疗期间CA125 均降至正常。值得注意的是,病例1 患者无进展生存期达到11.7 个月。
甲磺酸阿帕替尼常见的不良反应包括高血压、蛋白尿、消化道症状、手足综合征、骨髓抑制和转氨酶升高等[16]。大多数不良反应可以通过下调剂量、支持及对症处理以及暂停给药予以控制。本研究2 例患者出现白细胞计数降低、贫血、血小板计数降低、肝功能异常、恶心和体质量下降,未出现高血压、蛋白尿等其他不良反应。病例1 曾因2 次白细胞计数降低和中性粒细胞计数降低调整用药剂量,阿帕替尼剂量减至250 mg/次,1 次/d,依托泊苷剂量不变。剂量调整后未出现更严重的不良反应,且疗效评估提示仍有效。
综上所述,甲磺酸阿帕替尼联合依托泊苷用于铂耐药的复发性卵巢癌治疗可能是有效且安全的,但还有待于大规模的随机对照的多中心临床研究去证实,并进一步探索最佳联合药物及剂量,为临床提供一种有效的治疗方案。
