基于中红外光谱技术桂枝茯苓胶囊浓缩过程快速检测方法研究
2022-08-16王玉琴徐芳芳张永超章晨峰王振中
王玉琴,徐芳芳,张 欣,吴 云,张永超,章晨峰,王振中
基于中红外光谱技术桂枝茯苓胶囊浓缩过程快速检测方法研究
王玉琴1,徐芳芳2, 3*,张 欣2, 3,吴 云2, 3,张永超2, 3,章晨峰2, 3,王振中2, 3*
1. 南京中医药大学,江苏 南京 210023 2. 江苏康缘药业股份有限公司,江苏 连云港 222001 3. 中药制药过程新技术国家重点实验室,江苏 连云港 222001
应用衰减全反射中红外光谱(mid-infrared spectroscopy,MIRS)技术建立桂枝茯苓胶囊(Guizhi Fuling Capsules,GFC)浓缩过程中没食子酸、芍药苷、苯甲酸、苯甲酰芍药苷及挥发油桂皮醛和肉桂酸的定量分析模型,实现GFC浓缩过程的质量控制。以HPLC检测值为参照,采集GFC浓缩过程的MIRS,结合偏最小二乘(partial least square,PLS)法分别建立6种指标性成分的定量模型。没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷及桂皮醛的校正集相关系数(cal)分别为0.992、0.977、0.986、0.985、0.974、0.980,验证集相关系数(pre)分别为0.985、0.961、0.988、0.993、0.978、0.975,校正均方根误差(corrected root mean square errors,RMSEC)分别为0.132、0.771、0.042、0.044、0.075、0.185,预测相对偏差(relative standard error of prediction,RSEP)和相对误差均小于10%。MIRS技术具有快速方便、结果可靠的优点,可以应用于GFC浓缩过程中挥发油桂皮醛和肉桂酸及其他指标性成分的测定,为GFC浓缩过程的在线监控提供了一种新方法。
桂枝茯苓胶囊;中红外光谱;挥发油;没食子酸;芍药苷;桂皮醛;肉桂酸;质量控制;移动窗口偏最小二乘;组合间隔偏最小二乘;定量分析
桂枝茯苓胶囊(Guizhi Fuling Capsules,GFC)由桂枝、桃仁、牡丹皮、白芍、茯苓5种中药组成,其处方来源于东汉张仲景所著《金匮要略》中的桂枝茯苓方[1]。现用于女性瘀血阻络所致癥块、经闭、痛经、产后恶露不尽;子宫肌瘤,慢性盆腔炎包块,子宫内膜异位症,卵巢囊肿见上述证候者。GFC处方中诸多中药材中都存在中药挥发油,且大多数挥发油均具有良好的临床疗效[2],在中药复方制剂生产中,中药挥发油种类、含量变化大[3],对于含有挥发油的中药复方制剂来说,如何控制中药挥发油的质量尤为重要[4]。GFC的桂枝药材中主要的挥发性物质有桂皮醛和肉桂酸,药理研究表明,肉桂酸和桂皮醛分别是桂枝药材抗菌消炎、解热镇痛的活性成分。
近红外光谱(near-infrared spectroscopy,NIRS)技术和中红外光谱(mid-infrared spectroscopy,MIRS)技术是快速、准确、无损的绿色过程分析技术[5]。以NIRS为主的过程分析技术逐渐应用于中药制备过程的实时监测[6-9],罗晓芳等[10]将NIRS技术应用于丹参浓缩过程的在线监测,采用NIRS对丹参水提液的浓缩过程进行分析,建立了浓缩过程中有效成分含量的定量模型,及时反映浓缩过程的状态。李华雨等[11]为研究再造烟叶生产浓缩过程中挥发性香味成分的变化,采用同时蒸馏萃取-气相色谱-飞行时间质谱法测定了样品中234种挥发性香味成分。
在GFC浓缩过程中,挥发油桂皮醛和肉桂酸会随蒸汽挥发,目前的报道中缺少在线监测浓缩过程中挥发油桂皮醛和肉桂酸的研究,由于在GFC浓缩过程中,会出现絮状样品,会直接影响样品对近红外光的吸收和散射[12-13],从而导致NIRS的变异,本研究采用MIRS技术,以HPLC测定没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷及桂皮醛的含量,结合偏最小二乘(partial least square,PLS)法建立6种指标性成分的定量分析模型[14-18],实现GFC浓缩过程中挥发油及其他指标性成分的快速测定,为挥发油桂皮醛和肉桂酸的在线监测提供新方法,为含挥发油的中药复方制剂提供一种新的质量控制方法。
1 仪器与材料
1.1 仪器
原位FT-IR React IR 702L型红外光谱仪,梅特勒-托利多(中国)公司;Ulitmate3000型高效液相色谱仪,赛默飞世尔科技(中国)有限公司;Mettler Toledo ME104E型电子天平,Mettler公司;H1650-W型湘仪高速离心机,湖南湘仪离心机仪器有限公司;Milli-Q IQ7000型超纯水系统,默克化工技术(上海)有限公司。
1.2 材料
没食子酸、芍药苷、苯甲酸、肉桂酸及桂皮醛对照品,中国食品药品检定研究院,供含量测定用,批号分别为110831-201906、110736-202145、100419- 201703、110786-201604、110710-202022,质量分数分别为91.5%、95.1%、99.9%、98.8%、99.5%;苯甲酰芍药苷对照品,成都德斯特生物技术有限公司,批号为DST211210-053,质量分数为98.19%;乙腈,色谱纯,西格玛里奥里奇(上海)贸易有限公司;水,超纯水,自制;其余试剂均为分析纯。
GFC浓缩过程样本均由江苏康缘药业股份有限公司提供,样本信息见表1。
1.3 数据处理软件
采用Unscramble(version 11,挪威Camo Analytics公司)软件进行光谱预处理,采用Origin (version 8.0,美国Origin Lab公司)软件及Minitab(version 19.1,美国LLC公司)绘图,采用Minitab(version 19.1,美国LLC公司)进行配对检验,采用Matlab(version 2019a,美国MathWorks公司)软件进行样本划分、变量筛选及模型构建。
2 方法与结果
2.1 样本收集
醇提液浓缩过程取样:在浓缩过程中在线取样,浓缩过程4~5 h,前0.5 h取1个样,后续10 min取1个样,本实验取7个批次样品共145个样品,批号及数量见表1。
2.2 含量测定
含量测定方法参照企业内控标准。李家春等[19]依据GFC生产工艺,建立了生产过程中浸膏的定量指纹图谱控制方法。
表1 浓缩过程样本信息
Table 1 Condense process sample information
批号数量批号数量 z22030121z22041021 z22030221z22041121 z22030321z22041220 z22030420
2.2.1 对照品溶液的制备 取没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷、桂皮醛对照品适量,精密称定,加50%甲醇制成分别含100、250、15、10、30、20 µg/mL的混合对照品溶液。
2.2.2 供试品溶液的制备 前1.5 h取样品3 g,1.5~2.5 h取样品2 g,后续取样品1 g,精密称定,置25 mL量瓶中,用50%甲醇溶解,超声处理(250 W、40 kHz)30 min,放冷,摇匀,12 000 r/min离心(半径为9.5 cm)10 min,上清液用微孔滤膜滤过,即得供试品溶液。
2.2.3 色谱条件 色谱柱为Waters Symmetry C18柱(250 mm×4.6 mm,5 μm);流动相为0.02%三氟乙酸水溶液-乙腈,梯度洗脱:0~5 min,5%乙腈;5~20 min,5%~17%乙腈;20~30 min,17%~19%乙腈;30~40 min,19%~26%乙腈;40~60 min,26%~88%乙腈;60~70 min,88%乙腈;体积流量1 mL/min;柱温30 ℃;检测波长230、275 nm;进样量10 μL。对照品及GFC样品色谱图见图1。
以z220301、z220302、z220303、z220304批GFC浓缩为例,各指标成分含量变化规律如图2所示。在GFC的浓缩过程中,设备会自动适时补料,至全部药液吸入设备中;浓缩过程中,芍药苷、苯甲酸、没食子酸、苯甲酰芍药苷的含量随浓缩的进行,呈现逐渐上升的趋势;前1.5 h,肉桂酸和桂皮醛含量呈现逐渐上升的趋势,随着浓缩过程中药液的自动补充和挥发油类成分随蒸汽的挥发,浓缩后期肉桂酸含量出现不规律变化,桂皮醛含量出现下降趋势。
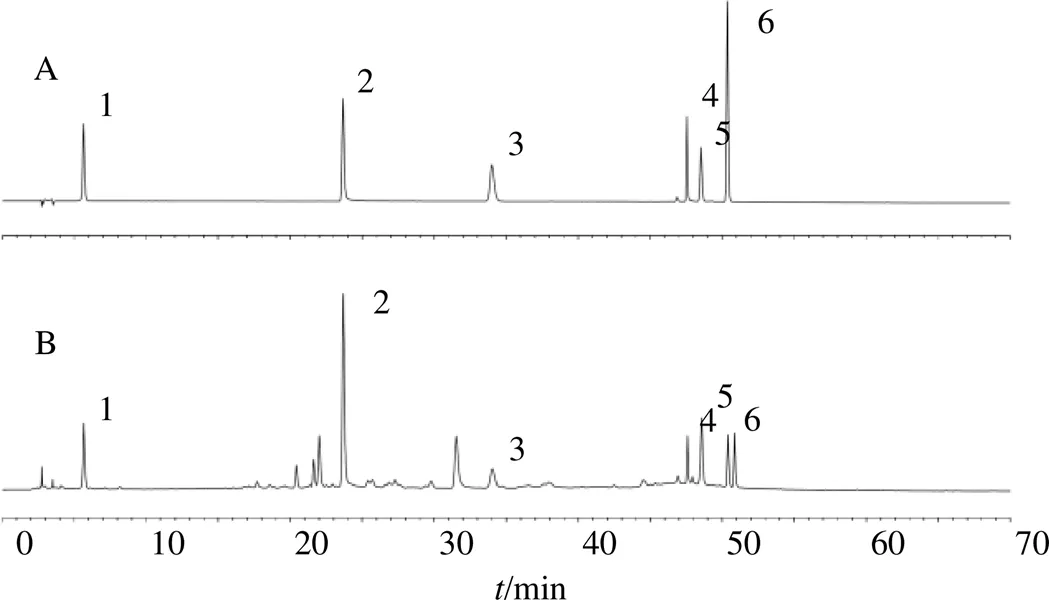
1-没食子酸 2-芍药苷 3-苯甲酸 4-肉桂酸 5-苯甲酰芍药苷 6-桂皮醛
2.3 MIRS的采集
在室温条件下,打开中红外光谱仪,预热仪器40 min,以空气为扫描背景,取适量样品滴于探头上,进行MIRS扫描,扫描结束后,清洗探头,探头洁净后进行下一次扫描。光谱扫描条件:扫描次数为32次,扫描速率为7次/秒,分辨率4 cm−1,光谱扫描范围是648~3000 cm−1,每个样品扫描2次,取平均光谱作为样品的光谱数据。采集的样品MIRS见图3。
2.4 模型建立研究
2.4.1 样本划分 通过K-S划分法,将样品以4∶1比例进行校正集和验证集的划分,最终得到校正集116个样品,验证集29个样品。本研究的K-S划分法在Matlab中进行。
2.4.2 光谱预处理方法的选择 为了消除光谱采集的误差,建立准确的MIRS模型。本研究采取不同的光谱预处理方法对MIRS进行预处理,分别建立没食子酸、芍药苷、苯甲酸、肉桂酸、桂皮醛、苯甲酰芍药苷的PLS定量模型。
常用的光谱预处理方法有Savitzky-Golay(S-G)平滑、移动窗口平滑(9点)、矢量归一化法、标准正则变换(standard normal variate,SNV)、多元散射校正(multiplicative scatter correction,MSC)、基线校正。通过决定系数()、校正均方根误差(root mean square errors of calibration,RMSEC)、交叉验证均方根误差(root mean square errors of cross validation,RMSECV)、预测均方根误差(root mean square error of prediction,RMSEP)、性能偏差比(ratio of performance to deviation,RPD)与预测相对偏差(relative standard error of prediction,RSEP)来评估模型的性能。决定系数越大,模型拟合效果越好;RMSEC和RMSEP分别指校正模型与验证模型中参考值与预测值之间的偏差,越小模型预测性能越好[15];RSEP指参考值与预测值之间的相对偏差,越小模型性能越好;性能偏差比(RPD)表示模型预测性能,一般RPD大于2.5时,模型预测性能较好。综合评价各性能指标来评估模型性能。
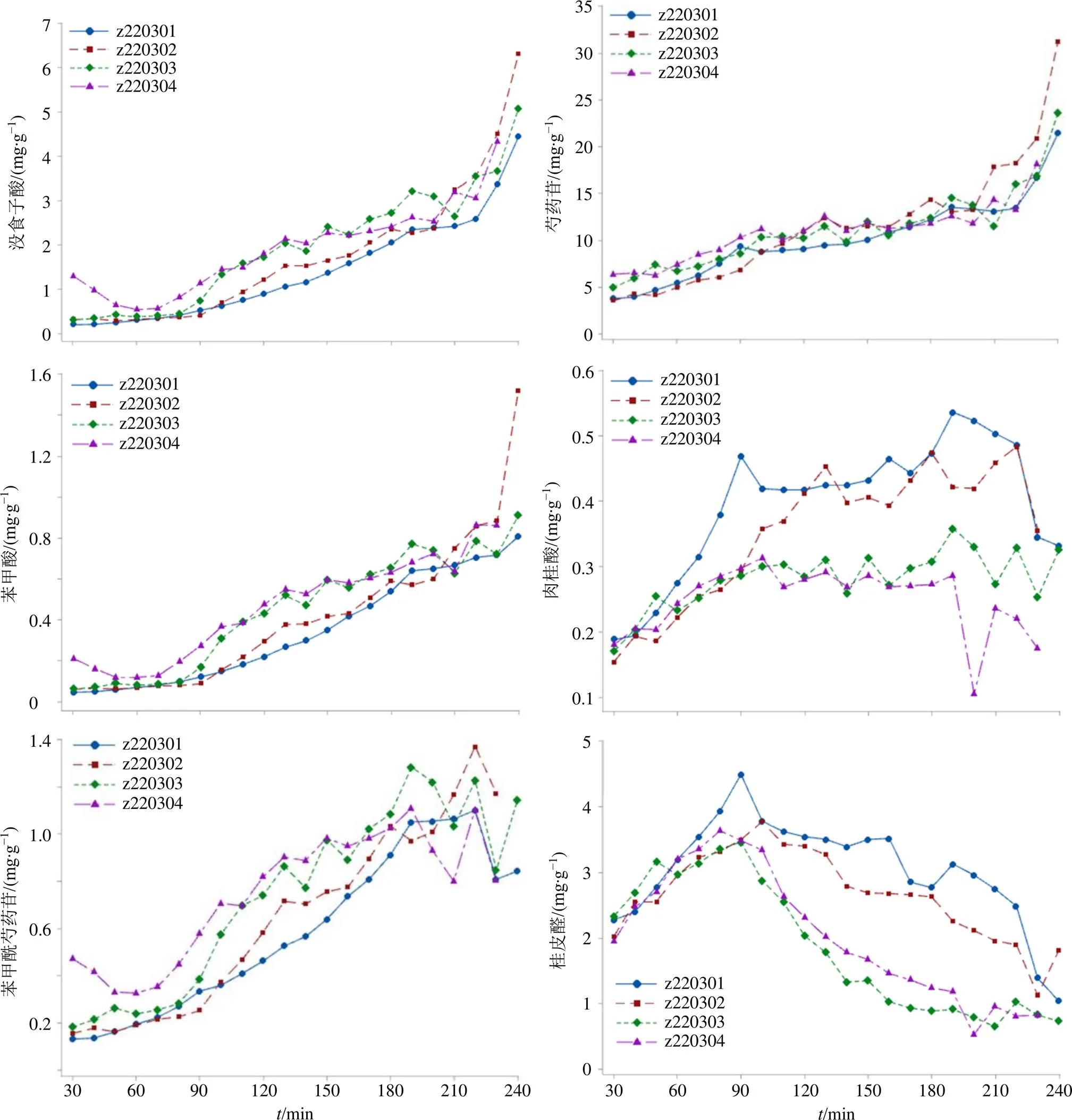
图2 含量变化趋势图
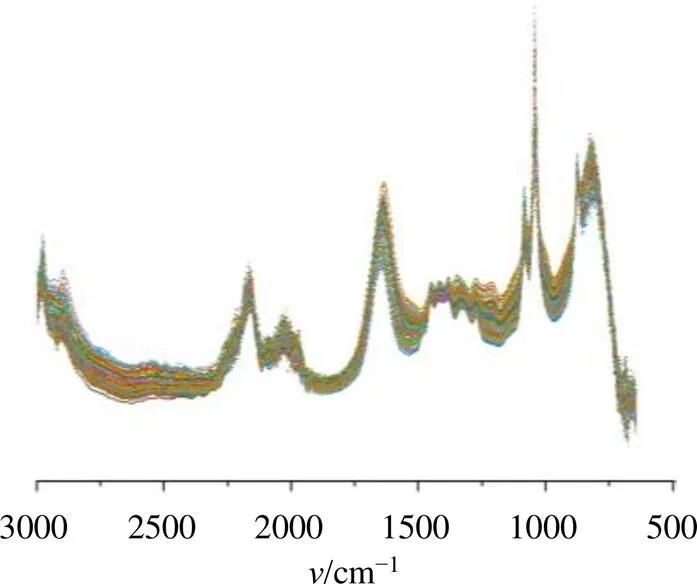
图3 145个样品MIRS图
表2是采用不同光谱预处理方法建立6种指标性成分的PLS定量模型,以RPD与RSEP的大小来确定最佳的光谱预处理方法。从模型结果看,苯甲酸、苯甲酰芍药苷采用S-G平滑对光谱进行预处理时建模效果好,RPD分别为4.03、3.63,RSEP分别为14.32%、11.68%,没食子酸采用原始光谱建模效果好,RPD为4.16,RSEP为10.77%,芍药苷、肉桂酸、桂皮醛分别是采用基线校正、移动窗口平滑、归一化法对光谱进行预处理时,建模效果最优,RPD分别为3.61、3.76、1.84,RSEP分别为9.30%、10.94%、18.13%。
表2 不同预处理方法建模结果分析
Table 2 Analysis of modeling results of different pretreatment methods
成分预处理方法校正集验证集 rcalRMSECRMSECVrpreRMSEPRPDRSEP 没食子酸无预处理0.9830.1880.2150.9700.2264.1610.77 S-G0.9850.1800.2100.9680.2354.0011.21 移动窗口平滑0.9850.1780.2080.9680.2344.0111.17 归一化法0.9830.1910.2170.9630.2493.7611.91 基线校正0.9830.1870.2170.9700.2363.9811.26 MSC0.9810.1980.2290.9630.2533.7112.07 SNV0.9820.1950.2250.9630.2553.6812.18 芍药苷无预处理0.9770.7770.9920.9630.8983.619.30 S-G0.9660.9441.0880.9580.9453.439.78 移动窗口平滑0.9740.8181.0090.9620.9023.609.34 归一化法0.9700.8881.1230.9511.0123.2110.48 基线校正0.9770.7711.0190.9610.8983.619.30 MSC0.9680.9071.0810.9600.9413.459.74 SNV0.9690.9021.0730.9600.9413.459.74 苯甲酸无预处理0.9780.0520.0770.9680.0603.8614.94 S-G0.9720.0590.0750.9720.0574.0314.32 移动窗口平滑0.9760.0550.0760.9700.0583.1014.46 归一化法0.9740.0570.0730.9700.0623.7515.39 基线校正0.9770.0530.0790.9660.0633.6715.73 MSC0.9730.0520.0780.9660.0653.5316.32 SNV0.9790.0510.0780.9640.0643.6114.78 肉桂酸无预处理0.9730.0590.0760.9650.0593.4912.61 S-G0.9720.0600.0760.9540.0583.5812.29 移动窗口平滑0.9850.0610.0760.9660.0583.7610.94 归一化法0.9640.0580.0760.9660.058 3.5412.44 基线校正0.9720.0600.0760.9610.059 3.4812.65 MSC0.9630.0680.0790.9640.057 3.6012.25 SNV0.9650.0670.7770.9660.056 3.6612.04 苯甲酰芍药苷无预处理0.9590.1290.1480.9520.096 3.1613.91 S-G0.9470.1060.1350.9660.0843.6311.86 移动窗口平滑0.9560.0970.1370.9560.0923.3113.18 归一化法0.9580.0940.1350.9480.1003.0414.54 基线校正0.9440.0970.1440.9600.0943.2613.45 MSC0.9580.0940.1440.9500.0973.1414.03 SNV0.9590.0930.1410.9510.0973.1513.96 桂皮醛无预处理0.9070.3340.5270.8270.4591.8018.55 S-G0.8880.4280.5030.8310.4561.8118.42 移动窗口平滑0.9000.4070.5160.8280.4591.8018.54 归一化法0.9130.4510.5060.8360.4491.8418.13 基线校正0.9150.3760.5280.8050.4851.7019.62 MSC0.9220.3600.5240.8180.4721.7519.06 SNV0.9240.3560.5170.8240.4641.7818.76
2.4.3 光谱波段的筛选 选择合适的光谱波段,可以剔除光谱数据中的无用信息,降低光谱维度,提高模型预测精确度和稳健性。本研究在上述筛选出的最佳预处理方法基础上采用组合间隔偏最小二乘(synergy interval partial least squares,siPLS)、间隔偏最小二乘(interval partial least squares,iPLS)、移动窗口偏最小二乘(moving window partial least squares,mwPLS)的方法进行光谱筛选。
iPLS是将光谱数据等分成多个等宽光谱区间,每个区间进行建模研究,选择最佳光谱区间。本研究将全波段光谱划分为20个子区间,以RMSECV为评价指标,筛选最佳光谱区间。
siPLS是将全光谱划分为多个等间距子区间,把子区间随意组合建模。本研究是把全光谱划分为20个子区间,再以子区间组合数为3建立模型,以RMSECV选取最佳建模区间。
mwPLS是将1个窗口沿着光谱波数方向移动,每移动1个点,建立1个PLS模型。本研究以初始窗口宽度为11,以10为步长依次增加窗口宽度,建立了窗口宽度为11~81的PLS模型,并根据RMSECV选取最佳建模区间。优选区间建模于全光谱建模的比较如表3所示。
各波段筛选方法的模型性能如表3所示,以RSEP、RPD为主要评价指标,筛选出建模的最佳光谱区间。由表3可知,没食子酸模型采用siPLS与mwPLS进行变量筛选后,RPD变大,RMSEP变小,说明筛选变量提升了模型预测性能,综合分析模型所有评价指标,没食子酸建模最佳波段为1120~1340、1460~1572 cm−1;芍药苷模型在筛选变量后,变量数虽然有所减少,但RPD变小,RMSEP变大,模型性能降低,而原始光谱校正集相关系数(cal)、验证集相关系数(pre)均较大,RMSECV、RMSEC、RMSEP均较小,因此,采用原始光谱建模效果更好,波段为648~3000 cm−1;苯甲酸采用mwPLS筛选变量模型性能有所提升,建模效果最佳,故选用波段976~1448 cm−1进行建模;肉桂酸采用siPLS筛选变量后,模型性能有所提升,RPD、cal、pre也较大,故选用波段1228~1340、1460~1572、1692~1804 cm−1进行建模;苯甲酰芍药苷采用mwPLS法进行波段筛选后,RPD最大,PSEP最小,且cal、pre均变大,故选用波段1064~1296 cm−1建模;桂皮醛在采用siPLS筛选波段后,RPD、cal、pre均变大,与原始光谱相比,RMSECV、RMSEC、RMSEP均变小,因此选用波段1112~1340、1460~1572 cm−1建模效果最佳。
通过波段筛选,得到没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷、桂皮醛的最佳建模波段分别为1120~1340、1460~1572 cm−1,648~3000 cm−1,976~1448 cm−1,1228~1340、1460~1572、1692~1804 cm−1,1064~1296 cm−1和1112~1340、1460~1572 cm−1。
2.4.4 主成分数的选择 主成分数的选择影响MIRS定量分析模型的稳定性和预测性,本研究采用留一交叉验证法,以RMSECV为指标,考察主成分数对模型的影响,当RMSECV最小时,所选主成分数最佳,确定没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷、桂皮醛的最佳主成分数分别为7、6、16、10、15和13。
2.4.5 模型的建立 将经过预处理后的光谱数据与样品含量数据关联[20-22],采用PLS法建立MIRS的定量模型,最优的建模性能参数如下表4所示。
由表4可看出所有模型的RMSECV、RMSEC、RSEP值较小,cal、pre的值接近于1,RPD均大于3,具有良好的预测性能,可用于指标性成分的定量预测。为验证MIRS模型预测结果的可靠性,对没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷、桂皮醛定量模型的验证集中参考值与预测值进行配对检验,结果值依次为0.311、0.811、0.369、0.745、0.121、0.677,值均大于0.05,说明参考值与预测值之间无明显差异。
2.5 生产验证及应用
模型预测的准确性需用外部验证集来验证,通过对比MIRS模型预测值和真实值的误差来评价模型性能。没食子酸、芍药苷、苯甲酸、肉桂酸、苯甲酰芍药苷、桂皮醛模型预测值与样本实测值的绝对误差及相对误差见表5,结果显示这6种指标成分的平均相对误差均小于10%,说明经过生产实际验证,该模型较为稳健。
3 讨论
本研究引入MIRS技术监测GFC的浓缩过程中挥发油的含量变化,将MIRS与化学计量学相结合,采用不同光谱预处理方法和筛选波段方法,结合PLS建立了GFC浓缩过程中没食子酸、芍药苷、苯甲酸、苯甲酰芍药苷以及挥发油桂皮醛和肉桂酸的PLS定量分析模型,这6种指标性成分的平均相对误差均小于10%,RPD均大于3,模型预测性能较好,结果表明该方法准确,满足分析要求,为GFC浓缩过程挥发油桂皮醛和肉桂酸的监测提供了新思路,为实现GFC浓缩过程在线含量测定打下研究基础,拓展了GFC浓缩过程的质量控制手段。
表3 优选区间与全光谱建模的比较
Table 3 Comparison between preferred interval and full-spectrum modeling
成分筛选方法变量区间/cm−1校正集验证集 rcalRMSECRMSECVrpreRMSEPRPDRSEP 没食子酸全光谱648~30000.983 0.188 0.215 0.970 0.226 4.16 10.77 siPLS1112~13400.992 0.132 0.153 0.985 0.162 5.79 7.75 1460~1572 Ipls1112~12240.988 0.160 0.174 0.967 0.251 3.74 11.98 mwPLS1300~15320.992 0.129 0.159 0.986 0.179 5.25 8.72 芍药苷全光谱648~30000.977 0.771 1.019 0.961 0.898 3.61 9.30 siPLS1112~13400.979 0.792 0.016 0.963 0.906 3.58 9.38 1692~1804 Ipls1692~18040.949 1.149 1.354 0.907 1.450 2.24 15.02 mwPLS1296~15280.968 0.907 1.041 0.962 0.920 3.53 9.53 苯甲酸全光谱648~30000.972 0.059 0.075 0.972 0.057 4.03 14.32 siPLS1228~13400.987 0.040 0.048 0.982 0.041 5.62 9.34 1460~1572 1692~1804 Ipls1112~12240.976 0.054 0.058 0.982 0.045 5.17 10.21 mwPLS976~14480.986 0.042 0.055 0.988 0.036 6.45 7.28 肉桂酸全光谱648~30000.985 0.061 0.076 0.966 0.058 3.76 10.94 siPLS1228~13400.985 0.044 0.052 0.993 0.027 7.57 5.82 1460~1572 1692~1804 Ipls1112~12240.981 0.049 0.057 0.983 0.038 5.49 8.02 mwPLS1092~13240.979 0.051 0.061 0.982 0.044 4.68 9.41 苯甲酰芍药苷全光谱648~30000.947 0.106 0.135 0.966 0.084 3.63 11.86 siPLS996~11080.956 0.097 0.112 0.969 0.078 3.92 11.22 1112~1340 1692~1804 Ipls1112~12240.965 0.086 0.103 0.966 0.078 3.92 11.23 mwPLS1064~12960.974 0.075 0.098 0.978 0.065 4.66 8.93 桂皮醛全光谱648~30000.913 0.451 0.506 0.836 0.449 1.84 18.13 siPLS1112~13400.980 0.185 0.236 0.975 0.184 4.49 7.45 1460~1572 Ipls1112~12240.954 0.279 0.327 0.924 0.313 2.64 12.65 mwPLS1052~12840.962 0.255 0.309 0.950 0.254 3.26 10.25
在中红外模型建立过程中,选择最优的光谱波段可以提高模型的准确度和稳定性,降低无关价值光谱信息的干扰,筛选波段后,RPD变大,说明筛选特征波段可以提升模型性能。研究建立了GFC的浓缩过程中红外定量模型,后续还需添加样本增加样本数量以及扩大有效成分含量范围,提高模型精度和稳定性。
表4 最佳模型的评价参数
Table 4 Evaluation parameters of best model
项目校正集验证集 rcalRMSECRMSECVrpreRMSEPRPDRSEP 没食子酸0.9920.1320.1530.9850.1625.797.75 芍药苷0.9770.7711.0190.9610.8983.619.30 苯甲酸0.9860.0420.0550.9880.0366.457.28 肉桂酸0.9850.0440.0520.9930.0277.575.82 苯甲酰芍药苷0.9740.0750.0980.9780.0654.668.93 桂皮醛0.9800.1850.2360.9750.1844.497.45
表5 验证集样本预测值与实测值的对比
Table 5 Comparison of predicted and measured values in validation set sample
指标成分平均绝对误差/(mg∙g−1)相对偏差/% 没食子酸0.0287.30 芍药苷0.5967.36 苯甲酸0.0246.49 肉桂酸0.0235.18 苯甲酰芍药苷0.0417.21 桂皮醛0.1225.41
利益冲突 所有作者均声明不存在利益冲突
[1] 丁玥, 曹泽彧, 柯志鹏, 等. 桂枝茯苓胶囊质量标准提升对制剂主要药效影响的研究 [J]. 中国中药杂志, 2015, 40(19): 3786-3793.
[2] 刘媛, 臧振中, 伍振峰, 等. 中药挥发油质量控制的现状、问题与对策 [J]. 中草药, 2018, 49(24): 5946-5951.
[3] 王晓禹, 吴国泰, 杜丽东, 等. 中药挥发油新型制剂及其质量控制的研究现状 [J]. 中国药房, 2021, 32(20): 2551-2555.
[4] 李钰, 姚俊宏, 殳叶婷, 等. 肉桂油与桂皮醛体外透皮吸收促进作用比较研究 [J]. 中国中药杂志, 2018, 43(17): 3493-3497.
[5] 王馨, 徐冰, 徐翔, 等. 中药质量源于设计方法和应用: 过程分析技术 [J]. 世界中医药, 2018, 13(3): 527-534.
[6] 彭璐, 钟淑梅, 廖鹏程, 等. 基于近红外光谱技术快速定量分析天麻有效成分 [J]. 医药导报, 2022, 41(6): 858-862.
[7] 刘永好, 严妲妲, 鲁萍, 等. 近红外光谱法测定桂枝药材中肉桂酸与桂皮醛的含量研究 [J]. 皖西学院学报, 2017, 33(5): 85-88.
[8] 张叶霞, 潘金火, 蔡宝昌, 等. 银黄口服液近红外光谱测定和相关性模型建立 [J]. 中成药, 2016, 38(3): 565-569.
[9] 李因坤, 魏瑞霞, 李艳芳, 等. 小儿消积止咳提取过程中近红外定量模型研究 [J]. 中国现代中药, 2022, 24(2): 320-326.
[10] 罗晓芳. 统计过程控制在丹参注射液生产质量控制中的应用研究 [D]. 杭州: 浙江大学, 2008.
[11] 李华雨, 薛建中, 王毅博, 等. 再造烟叶生产浓缩过程中挥发性香味成分的变化 [J]. 烟草科技, 2018, 51(12): 52-64.
[12] 程淑艳. 影响近红外光谱分析结果的因素探析 [J]. 化工管理, 2018(26): 29-30.
[13] 李勇, 魏益民, 王锋. 影响近红外光谱分析结果准确性的因素 [J]. 核农学报, 2005, 19(3): 236-240.
[14] 李亚惠, 李艳肖, 谭伟龙, 等. 基于近、中红外光谱法融合判定黑果枸杞产地及品质信息 [J]. 光谱学与光谱分析, 2020, 40(12): 3878-3883.
[15] 王燕波. 近红外及中红外光谱分析技术用于表征人血清白蛋白和免疫球蛋白G结构变化的研究 [D]. 济南: 山东大学, 2018.
[16] 孙迪, 李梦婷, 牟美睿, 等. 近-中红外光谱融合技术速测奶牛场粪水氮磷含量 [J]. 光谱学与光谱分析, 2021, 41(10): 3092-3098.
[17] 罗德芳, 彭杰, 冯春晖, 等. 可见光-近红外、中红外光谱的土壤有机质组分反演 [J]. 光谱学与光谱分析, 2021, 41(10): 3069-3076.
[18] 徐芳芳, 杜慧, 张欣, 等. 在线中红外光谱监测热毒宁注射液金银花与青蒿醇沉过程7种指标成分研究 [J]. 中草药, 2021, 52(10): 2909-2917.
[19] 李家春, 梁娜, 肖伟, 等. 定量指纹图谱技术在桂枝茯苓胶囊过程质量控制中的应用 [J]. 中国中药杂志, 2010, 35(24): 3270-3273.
[20] 王广, 刘宇, 夏兰欣, 等. 直链淀粉的傅里叶衰减全反射中红外特征光谱筛选与定量分析 [J]. 食品科学, 2021, 42(24): 335-340.
[21] 于喆源, 杨玺文, 王晓霞, 等. 中红外光谱技术对临泽小枣中多糖的定量分析 [J]. 食品工业, 2021, 42(5): 249-252.
[22] 邹胜琼, 段学, 田敏, 等. 中红外模型快速检测白酒基础酒中总酯的含量 [J]. 酿酒, 2021, 48(3): 74-77.
Research on rapid detection method of concentration process of Guizhi Fuling Capsules based on mid-infrared spectroscopy
WANG Yu-qin1, XU Fang-fang2, 3, ZHANG Xin2, 3, WU Yun2, 3, ZHANG Yong-chao2, 3, ZHANG Chen-feng2, 3, WANG Zhen-zhong2, 3
1. Nanjing University of Chinese Medicine, Nanjing 210023, China 2. Jangsu Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China 3. State Key Laboratory of New-tech for Chinese Medicine Pharmaceutical Process, Lianyungang 222001, China
The quantitative analysis models of gallic acid, paeoniflorin, benzoic acid, benzoyl paeoniflorin, cinnamic aldehyde and cinnamic acid in the concentration process of Guizhi Fuling Capsules (GFC) were established by attenuated total reflection mid-infrared spectroscopy (MIRS) to realize the quality control of GFC concentration process.Based on the HPLC detection values, the mid-infrared spectra were collected during the concentration process of GFC, and the quantitative models of six indicator components were established by partial least squares (PLS) method.Calibration set correlation coefficients of gallic acid, paeoniflorin, benzoic acid, cinnamic acid, benzoyl paeoniflorin and cinnamaldehyde were 0.992, 0.977, 0.986, 0.985, 0.974, 0.980, respectively. Validation set correlation coefficients were 0.985, 0.961, 0.988, 0.993, 0.978, 0.975, and corrected root mean square errors (RMSEC) were 0.132, 0.771, 0.042 0.044, 0.075, 0.185, respectively. The relative standard error of prediction (RSEP) and relative error were less than 10%.MIRS has the advantages of fast, convenient and reliable results, can be applied to the determination of cinnamic acid, cinnamic acid and other indicative components in the concentration process of GFC, providing a new method for online monitoring of the concentration process of GFC.
Guizhi Fuling Capsules; mid-infrared spectroscopy; volatile oil; gallic acid; paeoniflorin. cinnamaldehyde; cinnamic acid; quality control; moving window partial least squares; combinatorial interval partial least squares; quantitative analysis
R283.6
A
0253 - 2670(2022)16 - 5026 - 08
10.7501/j.issn.0253-2670.2022.16.012
2022-04-19
连云港市重大技术攻关“揭榜挂帅”项目:中药口服固体制剂智能化连续制造关键技术研究(CGJBGS2101);2022年中央财政转移支付地方项目:基于重点研究室研究领域的中医药多学科研究能力提升项目中药提取精制新技术
王玉琴,女,硕士研究生,研究方向为中药新药的研究与开发。E-mail: 2990282445@qq.com
王振中,研究员,研究方向为中药新药的研究与开发。E-mail: kyyywzz@163.com
徐芳芳,女,博士,研究方向为过程分析技术。E-mail: 879164331@qq.com
[责任编辑 郑礼胜]
