气相⁃离子迁移谱法检测沙林气体的方法研究
2022-08-15王学峰钱廷碧贺金娜
杨 姝 王学峰 高 适 钱廷碧 贺金娜
(陆军防化学院履约技术中心,北京 102205)
甲氟膦酸异丙酯又被称作沙林(GB),是典型的神经性毒剂之一,作为有机膦酸类物质,其毒理作用是通过抑制生物体内的乙酰胆碱酯脢,导致生物的神经出现紊乱。它的挥发度高,毒性强,潜伏时间短,是战场上最为常见的化学毒剂之一。沙林经呼吸道致毒时,蒸汽/气溶胶暴露半致死浓度(LCT50inh)为35 mg·min/m3(暴露2分钟为3 ppm),在0.01 ppm 浓度的毒剂蒸汽下暴露2分钟就会出现缩瞳现象,立即威胁生命和健康浓度(IDLH)为0.02 ppm[1]。由于化学毒剂有着易于合成、价格低廉、难防难控等特点,有效的检测方法可以对沙林毒气进行定性定量,提高防护能力。
1 气相色谱‐离子迁移谱方法概述
离子迁移谱技术(Ion Mobility Spectroscopy,IMS)是上世纪60 年代发展起来的微痕量检测技术。IMS 的工作原理是电离进入离子化区域中的气体分子,根据不同离子在电场中的迁移速率不同进行区分。其对化合物的检测下限可低至ppb 级,有着应用范围广,技术成本低,分辨率高,容易被小型化等优点,被广泛应用于对化学毒剂、危险品、爆炸物和毒品的检测和鉴定[2],适用于有机膦毒剂分析检测[3,4]。尽管IMS 有着诸多优点,但是由于其主要是通过区分离子迁移时间来进行分析的,所以难以对迁移率相同或相近的物质进行区分;由于直接对气体分子离子化,所以在检测类似物混合物时可能会出现离子在电离区互相湮灭的情况;检测成分较为复杂的物质时,容易受到其中浓度较大的物质的影响,不利于分析[2,5]。
气相色谱技术(Gas chromatography,GC)是实验室中较为常见的气相检测手段,广泛的应用于易挥发型化学物质以及有毒有害物质的检测中[6]。GC 技术发展较为成熟,一般为了提高检测速度和准度,经常将气相色谱技术与火焰光度计、质谱仪、氮⁃磷探测仪等技术进行联用。气相色谱⁃离子迁移谱法(GC⁃IMS)是将上述两种技术联用的极具前景的新检测手段[7],二者联用有效利用GC 的高效分离能力,弥补IMS 对迁移率相近混合物检测不灵敏的缺点,并且降低空气湿度对IMS的影响;而IMS的准确定性,可以改善GC重复性差、对复杂化合物难以定性的情况。另外,GC⁃IMS 相较于常用的GC⁃MS 技术,接口更简单,不需要真空环境,日常更容易维护和使用[2]。
通过配套软件LAV 的自带插件可以对复杂化合物的特征进行整合分析,获得保留时间、漂移时间和信号强度的综合谱图,提供全面的图像。如图1 所示的3 类谱图,分别为3D 投影平面顶视图、3D⁃IMS 色谱图以及离子流图。顶视图中的一个点即是色谱图中的一个峰,表示着一种化合物。根据不同化合物的性质,同一种化合物可能产生单体、二聚体乃至三聚体。化合物的浓度不同,顶视图中给点的颜色饱和度不同。
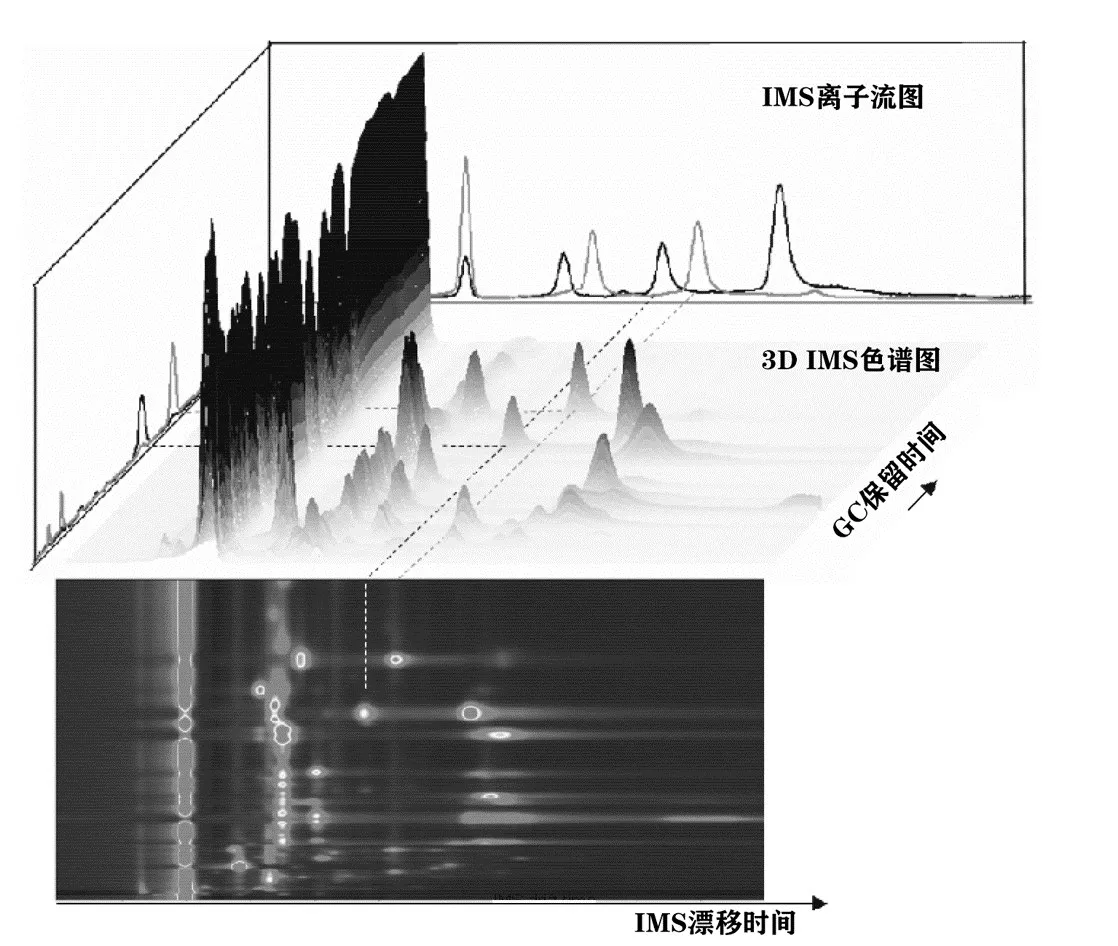
图1 GC‐IMS 软件测试谱图[8]
GC⁃IMS 可以直接对气体样品进行快速分析,现在多用于对食品气味的分类、检测、评价[7,9⁃17],尚未应用在毒剂气体测试分析中。针对毒剂气体发生的测试,过去多采取的方法是,利用有机溶剂(乙醇、乙腈等)进行1~3 小时的采集,再使用分光光度计法进行定量分析,一般全流程操作需要2~4 小时。利用GC⁃IMS 则可以直接对气体分子进行检测分析,大大缩短了采集气体所需要花费的时间,因此本研究旨在运用GC⁃IMS 法实现对沙林气体进行快速检测。
2 实验部分
2.1 主要仪器及试剂
毒剂气体发生器,自制;GC⁃IMS 气相离子迁移谱联用仪;气体流量控制模块;冷肼;0 号柴油;16种多环芳烃(PAHs)混标;盐酸联苯胺(A.R)、过硼酸钠(A. R),乙醇(A. R);沙林(GB)含量大于98%,自制。
2.2 实验平台
实验采用空气压缩机供气,经过五级干燥塔干燥后由气体流量控制模块(MFC)对气路的流量进行控制。干燥塔为自制800mL 不锈钢塔串联而成,内装分子筛、活性炭、无水CaCl2。如图2 所示经过干燥后的空气进入毒剂气体发生器,经由冷阱控制气室的环境温度,通过温度调控挥发度配制不同浓度的染毒气体。挥发的气体,通过细孔被空气气流带出,再在气体流量控制模块中与空气混合。为避免气流产生的扰动,控制气路中的流速始终保持在700mL/min。
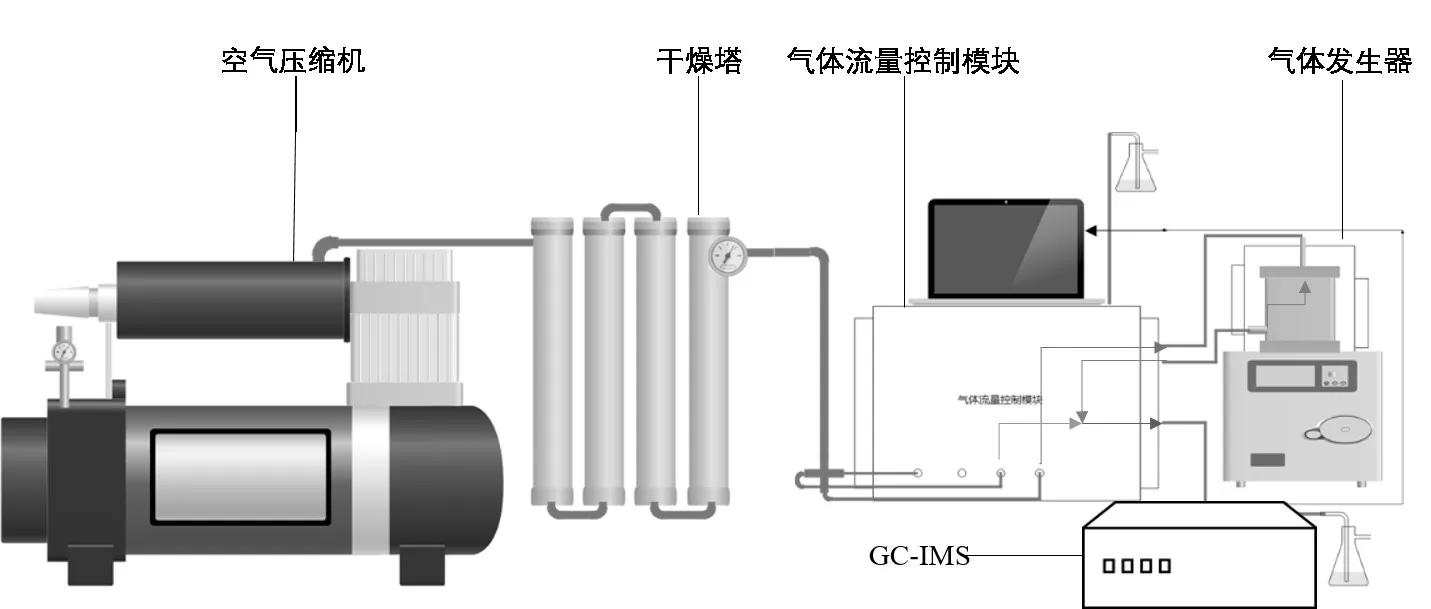
图2 实验平台
将气路直(旁)接接入GC⁃IMS 中进行检测(图3),气路中毒剂气体的浓度由溶剂吸收采集,采用分光光度计进行标定。

图3 气路连接
2.3 实验方法参数
GC⁃IMS 内部气路如图4 所示,由电子压力控制器1(EPC1)控制IMS 检测器的漂移气体,EPC2控制色谱柱载气。气体样品经过六通阀进入色谱柱,色谱柱洗脱后通过IMS 进行检测。
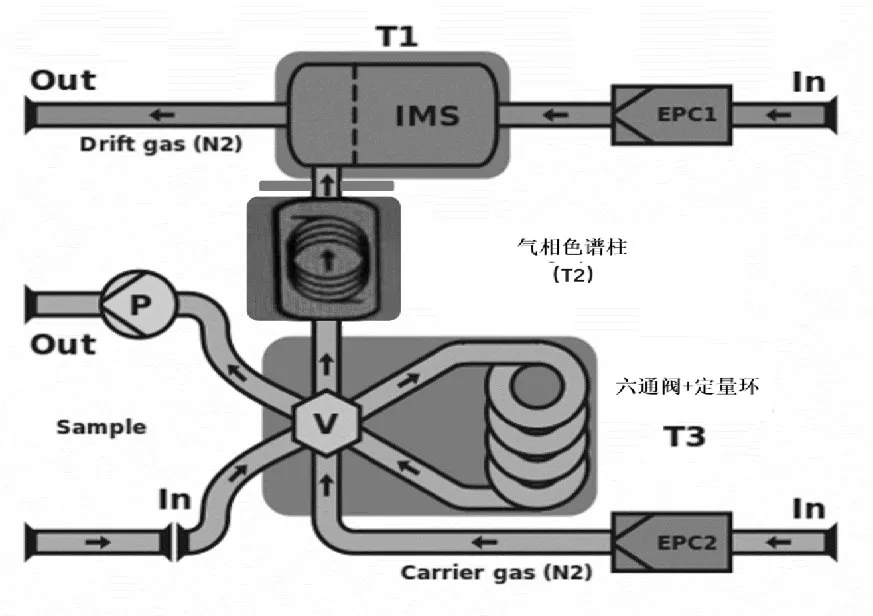
图4 GC‐IMS 内部设置[8]
预设GC 条件为:色谱柱:DB⁃5,长15m,直径0.53 mm,膜厚0.25 μm;进样体积:1000μL;色谱柱温度:60 ℃;定量环温度:60 ℃;载气:高纯N2,纯度≥99.999%。
预设IMS 条件:漂移管长度:5 cm;管内电压:400 V/cm;漂移管温度:45 ℃;漂移气为高纯N2;电离源:氚源;检测模式:正离子模式;IMS 温度:45 ℃。
探索检测沙林气体时GC 的载气终止流量、检测时长、进样量条件;IMS 的检测模式条件,以建立检测的工作曲线以及最低检出限,建立GC⁃IMS 法测定化学毒剂沙林气体的方法体系。
3 结果与讨论
3.1 GC‐IMS 条件的确定
3.1.1 对沙林的定性
根据挥发性化合物在GC⁃IMS 中的漂移时间和气相色谱保留时间,通过外标法使用C4~C9 的正酮作为校准液进行检测,与实测物质的保留指数进行对照,最后利用Library Search 软件及其数据库进行查找配对,从而对检测的物质进行定性。本实验定性结果为图5 所示,谱图表明气路中的挥发性物质有单体及二聚体,检测到的物质为沙林。

图5 软件定性结果
3.1.2 检测模式的选择
分别在正离子模式与负离子模式下对0.313 μg/L(50ppb)的沙林气体进行检测,测试谱图如图6 所示,在正离子模式下可以检测到沙林气体的反应离子峰,负离子模式下未见离子峰,因此选择正离子模式进行检测。

图6 不同离子模式下的谱图对比
3.1.3 气相色谱分离条件的选择
3.1.3.1 载气最终流量的设定
GC⁃IMS 采取的是程序升流技术,通过载气流量的线性增加达到分离效果。本实验对0.313 μg/L 在不同升流程序下的沙林气体的色谱条件进行了摸索。
设置初始流量为2mL/min,载气终止流量设定为5mL/min、15mL/min、20mL/min、30mL/min、50mL/min、80mL/min 、100mL/min、120mL/min 分别进行检测,谱图如图7。结果表明载气流量的增幅越少,色谱峰的拖尾情况越严重,响应越小,该浓度下终止流量高于80mL/min 时离子峰分离较好,载气流量在100mL/min~150mL/min之间时峰型差异不大。
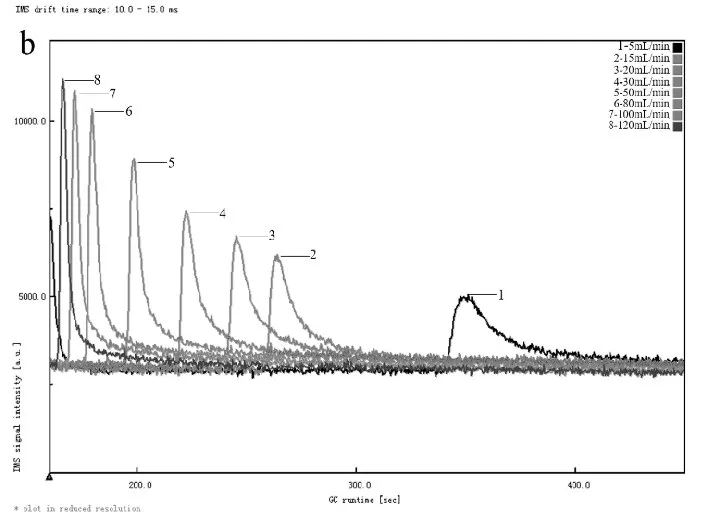
图7 载气终止流量不同时的谱图(5~120mL/min)
进一步检测1.876 μg/L(300ppb)浓度的沙林气体发现,初始流量为2mL/min,载气最终流量分别设为50mL/min、100mL/min、150mL/min 进行检测时,测试结果如图8。综合测试结果表明,载气流设定从2 mL/min 线性增至150mL/min 时分离效果最好。这主要是因为载气流速上升时,离子快速通过迁移区,导致到达检测极的离子随之增加,信号强度也就随之增加。
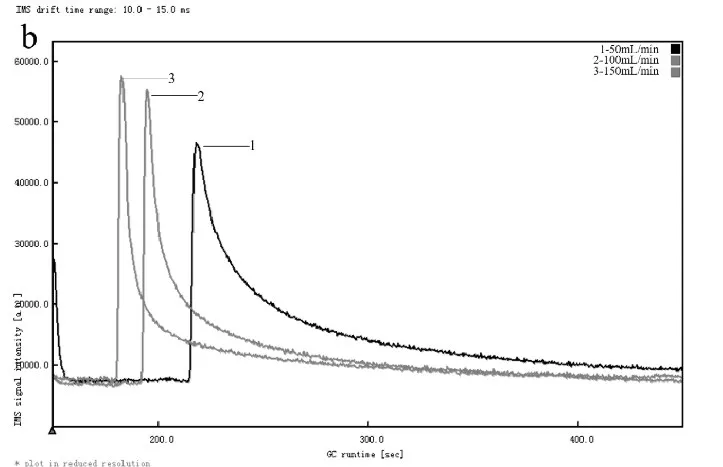
图8 载气终止流量不同时的谱图(50, 100, 150mL/min)
3.1.3.2 检测时长的选择
固定载气最终流量,考察检测时间对谱图的影响,检测时间分别设为:3 min、6 min、8 min、10 min、13 min、16 min,如图9 所示,检测时间越长出峰越晚,响应值也有所下降,峰型不佳;时间过短则会导致离子迁移时间不够,出峰过早容易受噪音影响。测试结果表明,检测沙林气体的时间在8~10 min 较合适。
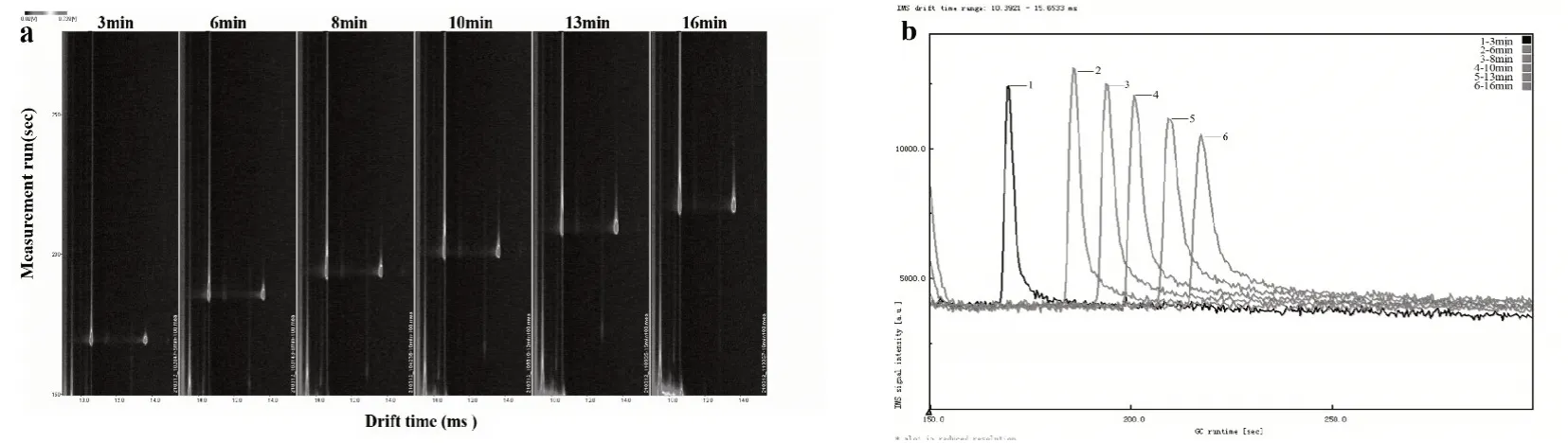
图9 检测时间不同时的谱图
3.1.3.3 进样量的设定
GC⁃IMS 可以通过改变定量环体积以及进样时间控制气体的进样量,气体进样量过大会导致定量环中死体积增大,影响峰形导致峰拖尾,进样量过小会导致检测到的气体量少,响应不明显。本仪器定量环为固定环1000μL,故而只讨论进样时间对检测的影响。如图10 可以看出进样时间过短时响应较小,时间过长时拖尾较明显,因此对沙林气体的检测,进样时间在10s~20s 时分离较好。

图10 进样时间不同时的谱图
3.2 确定检测沙林气体方法
通过上述实验,可以得知检测沙林气体的最佳条件为:正离子模式下检测,初始载气的流量为2mL/min,进样15s,稳定2 min,而后在2~10 min 内将载气流量线性增至150 mL/min。因此,将GC⁃IMS 法测试沙林气体的检测条件确定为:
GC 条件:色谱柱:DB⁃5;进样体积:1000μL;色谱柱温度:60 ℃;定量环温度:60 ℃;运行时间:15 min;载气:高纯N2,纯度≥99.999%;载气流量:初始2 mL/min,在10~25s 时进样15s,保持2 min后在10 min 内线性增至150 mL/min,之后在150 mL/min 流速下稳定5 min。
IMS 条件:漂移管长度:5 cm;管内线性电压:400 V/cm;漂移管温度:45 ℃;漂移气为高纯N2(纯度≥99.999%);流速:150 mL/min;检测模式:正离子模式;IMS 温度:45 ℃。
3.3 检测沙林气体的工作曲线与回归方程
由毒剂气体发生器发生沙林气体浓度分别为0.0375、0.0563、0.156、0.294、0.819,1.307、2.07、2.627 μg/L。由GC⁃IMS 检测,而后以浓度为横坐标,以各浓度对应的分析物离子峰(analyte ion peak,AIP)强度(三维图对应所得峰体积)为纵坐标,分别拟合绘制出GB 单体和二聚体的Boltzman函数标准曲线如图11。
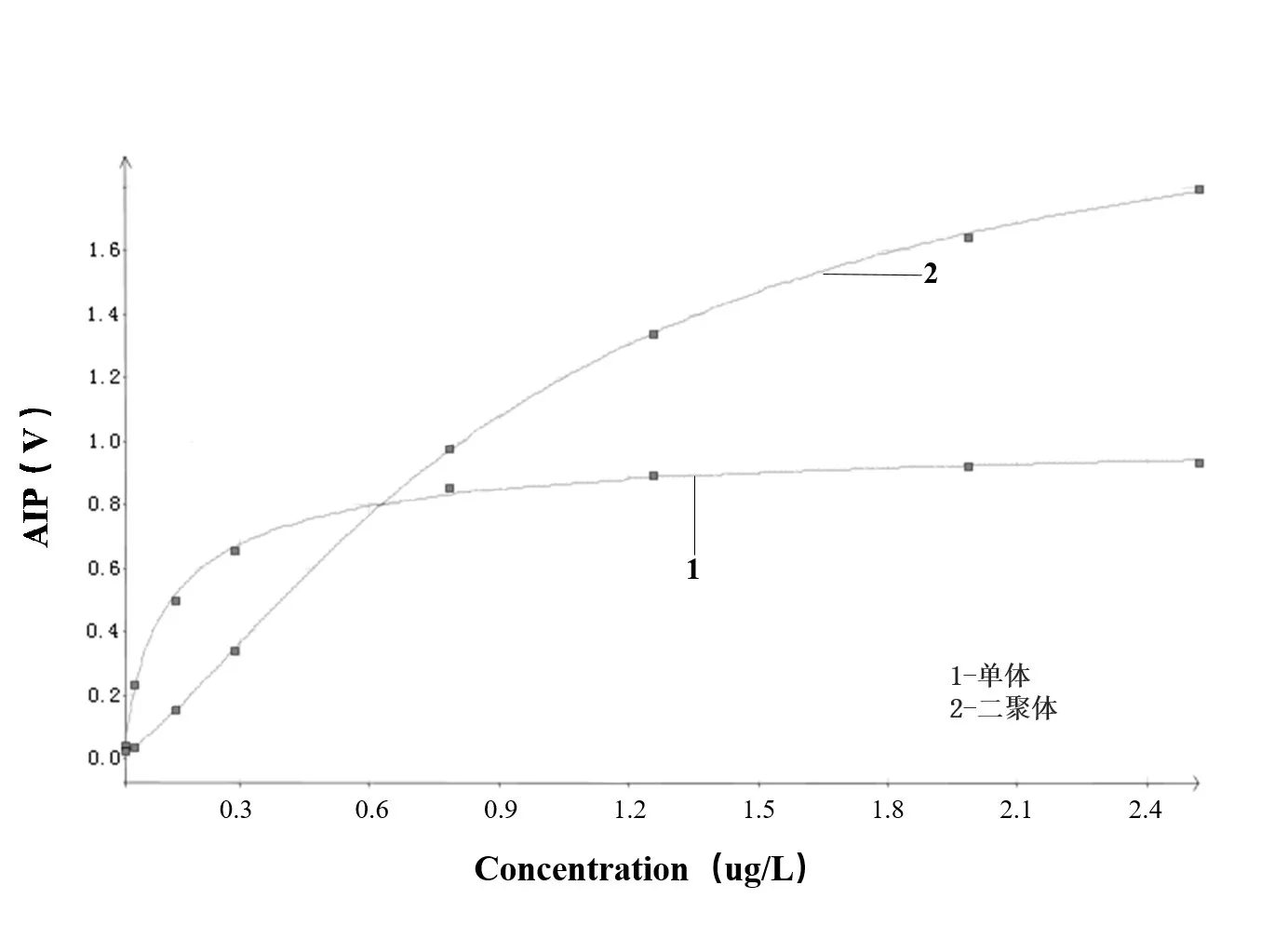
图11 GC‐IMS 检测GB 的bolzman 函数标准曲线
并得出Boltzman 函数回归方程如下:

根据此方程计算可得,低浓度(低于1 μg/L)时GB 单体区域信号标线的标称浓度与校准浓度之间相对标准偏差均小于5%,高浓度(高于1 μg/L)时GB 二聚体区域信号标线的标称浓度与校准浓度之间相对标准偏差均小于5%,因此在低浓度测试时以单体区域信号曲线为理想曲线,高浓度测试时以二聚体区域信号曲线为理想曲线。
3.4 环境中废气类干扰物对沙林检测的影响
实际中检测沙林气体时,要考虑到环境空气中可能存在的一些废气的干扰,其中包括含有苯环类物质和碳氢化合物。因此本实验将含有16种多环芳烃(PAHs)的混合标准样品代表苯环类干扰物,将0 号柴油代表碳氢化合物干扰物,考察了GC⁃IMS 方法检测废气中沙林的干扰情况。
将沙林与含有16种混标的PAHs 同时注入2L配气瓶中,分别考察PAHs(总)与沙林的质量比为1∶1、10∶1、100∶1、500∶1 这4种情况下,对GC⁃IMS方法检测沙林的影响。实验表明,当PAHs 与沙林的质量比为500∶1时,GC⁃IMS 已经无法分辨沙林的色谱峰,PAHs 与沙林质量比为100∶1时,GC⁃IMS可以明显检测出沙林,其信噪比S/N 为19,PHAs 与GB 的出峰完全分离,由此可以看出,PAHs 对沙林的检测无明显影响。考察了柴油与L 的质量比为10∶1、100∶1、500∶1 这3种 情 况 下 柴 油 浓 度 对GC⁃IMS 检测沙林气体的影响。实验表明,即使柴油与沙林的质比值达到500∶1时,含柴油的空白样品中没有检测出沙林,柴油与GB 的出峰完全分离,空气中碳氢化合物对该方法检测沙林无明显影响。
3.5 检出限
GC⁃IMS 对0.0375 μg/L(6ppb)沙林气体的检测噪音平均值约为0.009V,信号强度为0.0476,根据最低检出限公式D=3N×Q/I,其中N 噪音值,Q 为进样气体浓度,I 为响应信号强度。计算可以得出本研究所用方法对GB 气体的检测下限约为0.0214 μg/L(3.4ppb)。这对痕量毒剂气体的定量分析提供了一定的数据支撑,实际检测过程中能对目标物进行定量或半定量,有助于化学毒剂侦检精准度的提高。
4 结论与展望
利用GC⁃IMS 可以直接对气体分子进行检测分析,大大缩短了采集气体所需要花费的时间,因此运用GC⁃IMS 建立了更加高效检测沙林气体的方法。对沙林气体的测试可以看出,GC⁃IMS 可以较好地定性,考察了干扰物对该方法没有明显影响。利用此方法检测下限可以达到0.0214 μg/L,且响应信号与浓度可以通过Boltzman 函数建立回归方程,实现了定量或半定量检测,提高了对有毒有害气体检测的效率。
