Castleman 病1例 并 文 献 复 习
2022-08-13刘修平韦超洁
刘修平 韦超洁 杨 炯
武汉大学中南医院呼吸与危重症医学科 湖北 武汉 430071
Castleman 病(Castleman disease,CD)是 一 种罕见的反应性慢性淋巴组织增殖性疾病,又被称为血管滤泡性淋巴组织增生症、巨大淋巴节病或血管瘤性淋巴样错构瘤。该病由Benjiamin Castleman博士于1956年首次报道类似于胸腺瘤的纵隔肿物[1],故而命名为Castleman 病。截至目前,该病的病因及发病机制尚不明确。由于我们对Castleman病的认识不足,临床上容易出现漏诊、误诊,本文将武汉大学中南医院确诊的一例Castleman 病患者的资料进行整理,对其进行回顾性分析,并复习相关文献。
1 资料与方法
患者,女性,50岁,因发现左侧颈部淋巴结肿大及肺占位2月余,胸闷1 个月,于2018年9月26 日入院。患者2月余前发现颈部淋巴结肿大,无其它不适,遂立即于当地医院行胸部CT 平扫,提示右肺中叶肿块,遂于我院胸部肿瘤科就诊,行胸部增强CT(2018⁃07⁃16)示:右肺中叶内侧段及左肺下叶后基底段软组织结节影并纵隔及双侧腋下多发肿大淋巴结,炎性可能性大,不除外恶性。遂于当日行CT引导下肺穿刺检查及淋巴结活检检查,术后肺部病理检查提示:送检肺组织内纤维明显增生,肺泡萎缩,局部慢性炎性细胞聚集;免疫组化检测,肺泡上皮ALK⁃1(-)、Ki⁃67(+)、TIF⁃1(+)。左侧颈部淋巴结活检病理检查示:送检淋巴结呈反应性增生,其内未见癌(未做免疫组化)。余检查如:肿瘤标志物(呼吸道)、肝肾功能血脂电解质、腹部CT 平扫、脑平扫MRI、全身骨ECT 均未见异常,后患者出院,嘱患者出院1月后复查胸部CT。2018⁃08⁃14患者于我院复查胸部平扫CT 提示:右肺中叶内侧段及左肺下叶后基底段软组织结节影并纵隔及双侧腋下多发肿大淋巴结,较前变化不明显,未予以相应处理,嘱患者定期观察随诊。患者近1 个月来出现胸闷不适,呈加重趋势,于当地医院完善胸部CT 平扫检查提示:右肺不张,右肺肿块,右侧胸腔积液。为求进一步诊治,于我院呼吸内科门诊就诊,以“胸腔积液、肺部占位性质待查,淋巴结肿大原因待查”收入。
既往体健,无特殊病史,入院查体:左侧颈部淋巴结肿大,右肺呼吸音低,双肺未闻及干湿性啰音。外院胸部CT 示:右肺肺不张并肿块,右侧胸腔积液。入院后,血常规检查WBC:5.7×109/L,RBC:4.19×1012/L,Hb:124 g/L,PLT:142×109/L,淋巴细胞绝对值0.69×109/L↓,ESR 36 mm/h↑,ALB 34.4 g/L↓,PCT 0.25 ng/mL↑,IgG 20.2 g/L↑,肝酶、肾功能心肌酶、传染病四项、凝血象、CEA、ACE、IgG4、真菌D 葡聚糖等未见异常。隧行胸腔穿刺抽液术进一步明确诊断,胸水常规:黄色清晰无凝块,比重1.022,黏蛋白试验阴性,有核细胞数1 890 个/μL,中性粒细胞占8%、淋巴细胞86%、间皮细胞6%。胸水生化:胸水蛋白52.7 g/L↑、胸水ADA 27 U/L↑,余项正常范围内;胸水脱落细胞学、胸水抗酸未见异常,根据上述检查诊断仍不明确。联系病理科,对既往CT 引导下肺穿刺活检组织及左侧颈部淋巴结活检组织加做免疫组化检查,结果提示:送检肺组织内见纤维明显增生,肺泡萎缩,局部慢性炎性细胞聚集,免疫组化检测,增生之纤维SMA(+),CD34(-),浆细胞:CD38(+),CD138(+),IgG4(-),IgG(+)。淋巴结活检示(左侧颈部淋巴结活检):Castleman 淋巴结病(混合型,玻璃样血管型及浆细胞型)。免疫组化检测,CD3(T 细胞+),CD20(B 细胞+),CD21(FDC网+),CD38(浆细胞+),CD138(浆细胞+),Lambda(浆细胞+),Kappa(浆细胞+),Ki⁃67(Li 生发中心高表达),HIV⁃8(-)。遂诊断Castlemen 病(混合型,玻璃样血管型及浆细胞型),完善血液内科会诊,隧转入我院血液内科进行专科治疗,予以口服沙利度安片治疗,建议联合化疗(CHOP)治疗,患者因经济原因拒绝,要求出院于外院进一步就诊,随访得知患者出院后加用地塞米松片联合沙利度安片口服治疗,目前患者随访1年,胸闷症状消退,颈部淋巴结较前减小,正进一步随访中,拟近期返院复查。患者双肺及淋巴结CT 照片见图1 和图2。

图1 患者双肺CT 图片
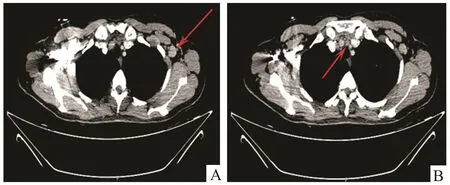
图2 患者淋巴结CT 图片
2 文献复习及结果讨论
目前,Castleman 病在临床上较为罕见,临床及影像学表现具有多样性,对于其诊治尚缺乏统一标准。根据临床病情累及部位的不同,可将该病分单中心型Castleman 病(unicentric Castleman disease,UCD)和多中心型Castleman 病(multicentric Castle⁃man disease,MCD)。根据组织病理学的不同,可以将该病分为透明血管型 Castleman 病(hyaline⁃vascular variant Castleman disease HV⁃CD),浆细胞型Castleman 病(plasma cell vari⁃ant Castleman disease,PC⁃CD)和混合型Castleman病[2]。该病人病程中可触及颈部淋巴结肿大,CT 可见纵隔及腋下多发淋巴结肿大,肺部可见两处占位并可明显强化,为多中心型Castleman 病。虽肺穿刺病理检查未提示Castleman 病诊断,可能于活检未准确获取病变组织相关,但患者多发淋巴结肿大、病理检查及相应临床表现支持MCD 诊断。左侧颈部淋巴结病理检查可见典型的洋葱皮样改变,并可见透明样变性小血管,其中可见散在的淋巴细胞及浆细胞浸润,在CD38 染色中尤为明显。
在临床上,UCD 又称为局灶型Castleman 病,其发病率为47%~81%,病理类型有60%~75% 为HV⁃CD,发病年龄主要集中在30~40岁,发病部位常集中于纵隔淋巴结(60%~75%),主要临床表现为局部淋巴结肿大,近90%的患者并无全身症状。MCD 患者发病占比为19%~53%,最常见病理类型为PC⁃CD,其占比为77%,发病年龄较UCD 大,多集中于50~60岁,在临床上表现为多个脏器受到累及和多部位的淋巴结肿大,伴随临床症状既表现为发热、消瘦、盗汗、全身乏力,化验结果为血清IL⁃6 升高,血细胞减少,脾脏肿大和高免疫球蛋白血症等全身症状,部分患者可出现胸腔、腹腔及心包积液等[3],预后与UCD 相比较差。此例患者起病初期未出现明显症状,仅以影像学提示肺部占位入院,合并纵隔、腋窝及颈部淋巴结肿大,病理检查未提示恶性肿瘤即出院。故如文献报道,当肺部占位且有淋巴结肿大时,注意Castleman 病、肺癌、淋巴瘤等恶性肿瘤之间相鉴别。
在Castleman 病的诊断方面,由于该病患者的临床表现具有多样性,影像学检查无特异性,因此该病确诊较困难。Frizzera[4]于1988年提出了MCD疾病的诊断标准:具有明显表现的组织病理学改变,显著肿大的淋巴结已经累及周围淋巴结,有多个系统的器官受累及表现,并且排除其它可能的病因。Arlet 等[5]于2010年也提出了此病诊断过程的金标准:淋巴结活组织检查、术中、术后病理学检查以及免疫组织化学染色等。虽然淋巴结活检病理检查为Castleman 病诊断的金标准,但淋巴结病理特征性不强,需要由富有经验的病理医生认真检查,明确诊断。此患者病程中出现漏诊一次,后出现明显症状后引起医生警觉,加做淋巴结病理免疫组化得以确诊为Castleman 病(混合型、玻璃样血管型及浆细胞型)。

图3 患者病理切片图
目前对CD 的治疗方案和预后结果根据类型不同差异较大。对于UCD 普遍采用对切除病变部位淋巴结的治疗方案,多数患者手术后可长期存活,极少复发,PC⁃CD 型的全身症状在手术切除发生病变的淋巴结后迅速消失。对于累及少部位的MCD可采取手术切除结合化疗进行治疗;对于累及到多个病变部位的MCD 目前并没有有效治疗方案,在一项大规模的回顾性分析研究中,50%MCD 患者都采用了糖皮质激素作为一线治疗方案,其中有56.6%患者获得临床改善。该种治疗方法可使病情缓解,但停药后易复发[6],故目前一般不考虑糖皮质激素作为单药治疗MCD。因MCD 是一种潜在的淋巴增生性恶性疾病,病变广泛,且多具有侵袭性,因此在临床方面还经常需要采取的联合化疗治疗[7],常见化疗方案为CHOP(R±CHOP)。既往有研究表明,采用CHOP 化疗方案治疗的患者,约50%可获得较为持久的缓解,但不良反应较多,且停药后易复发[8]。随着人们对MCD 的发病机制了解逐渐深入,已有一部分学者针对MCD 进行了免疫调节治疗,其中沙利度胺可以通过降低TNF⁃α、IL⁃6 和IL⁃10 的水平用以发挥抗炎作用[9]。此外,抗IL⁃6 受体抗体(Tocilizumab)[10]以及抗IL⁃6 单克隆抗体(西妥昔单抗)[11]也可用于治疗MCD,但停药后易复发。因此,对于MCD 患者制定出安全有效且经济的治疗方案是我们面临的巨大挑战。在本文涉及的病例中,患者先于胸外科就诊病理检查未检查出肺癌、淋巴瘤等恶性肿瘤后出院。因出现胸闷即检查出胸腔积液,遂于呼吸科就诊,在前次住院的病理切片上加做免疫组化,确诊为Castleman病,遂转入我院血液内科进一步治疗,予以口服沙利度胺片,建议联合化疗(CHOP)治疗,患者拒绝(经济原因),要求出院于外院进一步就诊,随访得知患者出院后加用地塞米松片联合沙利度安片口服治疗,目前患者随访1年,胸闷症状消退,颈部淋巴结较前减小,正进一步随访中,拟近期返院复查。
文献报道,绝大部分CD 是多克隆起源的,利用PCR 技术对相关基因(CD 免疫球蛋白基因、TCR受体基因)进行重排后结果多为阴性,但也有少数CD 是单克隆增生,并有转化为淋巴瘤可能,其中B细胞淋巴瘤多见,且多见于HIV(+)患者[12]。Cas⁃tleman 病发生恶化的机制可能是在其增生的过程中发生了基因突变,FDC 介导的淋巴细胞或血管内皮增生,可发生向淋巴瘤的转化,并导致肉瘤的发生,如Kaposi 肉瘤或FDC 肉瘤 等[13]。故对于确诊CD的患者,加强后期随访是该病监测最重要的策略。
该患者就诊及诊断过程较复杂,先后于胸外科、呼吸内科和血液内科住院治疗后确诊为MCD。期间出现漏诊一次,故加强该病的病理学检查、提高临床医生对于Castleman 病的临床认识及病理医生对于该病的病理所见尤为重要。
