铝合金牺牲阳极在淡海水环境下腐蚀产物及其形成过程分析
2022-08-12牟俊生朱帅帅
牟俊生 朱帅帅
(青岛双瑞海洋环境工程股份有限公司,山东 青岛 266101)
0 引言
铝合金牺牲阳极原材料来源广,制造工艺简单,价格低廉,通过合金化的方式,可限制和阻止表面形成连续性氧化膜,促进表面活化,使合金具有较负的电位和较高的电流效率[1],成为海洋环境中性价比较高的牺牲阳极材料。但铝合金牺牲阳极在工作时,表面会生成一层胶状的腐蚀产物,目前,海淡水环境下铝合金牺牲阳极腐蚀产物的形成机理和过程,鲜有研究,本文通过铝合金牺牲阳极在海淡水环境下的加速腐蚀试验,定性分析铝合金牺牲阳极在海淡水环境下腐蚀产物的形成机理和过程,以便进一步分析腐蚀产物对牺牲阳极本身及工作环境的影响。
1 试验
1.1 铝合金牺牲阳极阴极保护模拟试验
试验所用阳极材料为5kg子弹头形状铝合金牺牲阳极;阴极为φ400×180mm的Q235碳钢环形桶,尺寸为φ400×180mm;介质为75Ω·cm的弱碱性淡海水,pH值为8.0;试验过程中,铝合金牺牲阳极、碳钢环形桶、108L淡海水置于尺寸为φ500×650mm的PE桶中,为保证牺牲阳极腐蚀速率的稳定性,铝合金牺牲阳极、碳钢环形桶阴极分别连接至直流电源的正负极两端,并通0.018A的恒定电流,开路电压为1.05V,外部电路的通电时间60×24h,牺牲阳极恒电流加速腐蚀装置示意图如图1所示。

图1 牺牲阳极恒电流加速腐蚀装置示意图
1.2 测试与表征
(1)腐蚀介质的变化
铝合金牺牲阳极经过60×24h恒定电流加速腐蚀后,在阴极桶内壁下部及阴极桶底部区域出现明显的白色沉淀物,而阴极桶与PE桶之间的白色沉淀物质相对较少;对阴极桶内外的水介质,照射红外激光,在介质内出现红色光柱,表现出明显的丁达尔效应,在试验过程中,阴极桶壁上陆续有气泡产生,如图2所示。

图2 阴极桶底部腐蚀产物及反应后介质的丁达尔效应
试验结束后,对阴极桶内外的海水分别进行pH测试,pH值如表1所示;

表1 试验前及试验后阴极桶内外pH值
(2)腐蚀产物成分分析
取阴极桶底部的白色沉淀腐蚀产物,经晾干、洗涤再晾干后进行XRD分析,其谱图如图3所示,谱图显示,白色沉淀物主要为氢氧化铝。

图3 白色沉淀物XRD谱图
为进一步分析原样中的成分,对原样分别进行稀释10000倍后IC阴离子分析、原样ICP-OES测试分析,其测试结果分别如图4、表2所示。
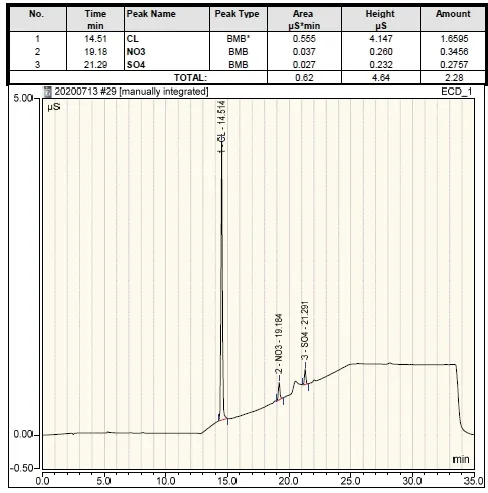
图4 原样稀释约10000倍的IC阴离子谱图
图4图谱中经扣除空白后计算,原样中的阴离子主要是Cl-和SO42-,其中Cl-含量约为1.94%,SO42-含量约为0.09%。
表2原样消解的ICP-OES测试数据表明,原样中铝元素含量约为1.99%,钠元素含量约为1.59%,钙元素含量约为0.05%,镁元素含量约为0.06%,钾元素含量约为0.03%。
四是着力加强风险管控。统一组织对大队进行内控制度执行情况审计,平时不定期进行抽样审计和专项审计,加强农业生产风险管控和防范。严格执行《苏垦农发内控制度手册》,建立健全农业生产经营管理责任追溯追究制度。
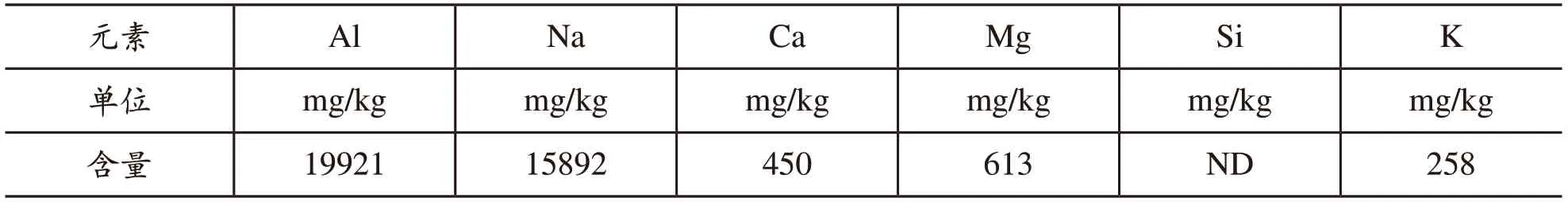
表2 原样消解的ICP-OES测试数据
2 讨论与分析
2.1 阴极区OH-离子的产生
牺牲阳极加速腐蚀装置中阴极所用材质为碳钢,为氢析出中超电势金属[2],氢在碳钢上析出的超电势,服从Tafel经验公式:
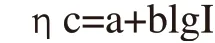
其中:
a≈0.5~0.7V,碳钢材质下的经验数值;
b≈100~140mV,经验常数;
S=3.14×40×18cm=2260.8cm2,本实验中阴极的面积;
I=0.018A/2260.8cm2≈8×10-6A/cm2,阴极桶的电流密度;
计算得:

即碳钢的氢超电势为0~0.19V,本实验中,阴极与阳极的开路电压已为1.05V,已达到碳钢材阴极上氢气析出的电压,在该电压下,阴极区的氢经过电化学步骤和电化学脱附步骤[2]:

(2)电化学脱附步骤
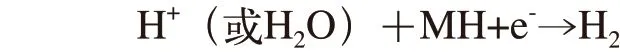
氢气的析出,造成阴极区H+被连续消耗,由于在一定温度下水的电离平衡常数K为定值,
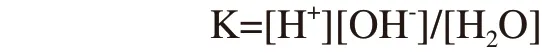
K为一定温度下水的电离平衡常数;
[H+]为一定温度下水中H+的物质的量浓度;
[OH-]为一定温度下水中OH-的物质的量的浓度;
[H2O]为一定温度下H2O的物质的量浓度。
根据平衡移动原理,随着阴极区H+消耗,氢离子的浓度减小,水的电离平衡正向移动,水的电离过程不断进行,正向移动产生了更多的H+和OH-,但是H+被不断消耗,这样就有大量的OH-剩余,溶液里OH-的数目相对增多,并导致阴极区pH值增大。
2.2 阳极区Al3+的产生及与OH-的反应
Al作为一种活泼金属,在本实验中在外部电流的作用下被氧化生成Al3+,Al→Al3++3e-;阳极区的Al3+和溶液中及阴极区新产生的OH-在阴阳极电势差的影响下,分别向阴极和阳极移动[3],形成Al3+和OH-的相向移动,随着反应的进行和Al3+、H+的定向移动,在弱碱性的淡海水环境中,Al3+与过量的OH-接触并发生反应,由于阳极区域与阴极区域的pH值是变化的,朱志平[4]等研究人员发现Al3+与OH-在水中的反应是非常复杂的,首先生成水合铝离子Al(H2O)63+,在进一步的水解作用下,继续生成单核水解产物Al(OH)2+、Al(OH)2+、Al(OH)4-和多核水解产物Al2(OH)24+、Al6(OH)153+、Al7(O H)174+、Al8(OH)204+、Al13(OH)345+,而这些水解产物是具有胶体性质的混凝剂,这些胶体物质在布朗运动的作用下,相对均匀的分布于整个海水介质环境中,使得反应后的海水介质,在用激光照射时,出现明显的光柱,也就是出现丁达尔效应。
随着本实验中铝阳极在通电过程中的不断氧化,海水介质中的Al3+浓度不断增加,逐渐生成Al(OH)3(S)沉淀,其具体反映过程[4-6]是:
(1)反应初期:阳极氧化生成的Al3+与阴极水解产生的OH-反应生成离子化合物Na[Al(OH)4],其离子反应式为:Al3++4OH-=[Al(OH)4]-;此时电解质溶液为清澈状态;
(2)反应中期:随着反应的进行,受电势差影响定向移动至阳极附近的OH-不断被消耗,Na[Al(OH)4]逐渐积累,电解液中Na[Al(OH)4]浓度逐渐趋于饱和,当达到饱和后,Na[Al(OH)4]分解产生为NaOH和Al(OH)3(S),Na[Al(OH)4]→Al(OH)3(S)+NaOH;
(3)反应后期:Al(OH)3(S)沉淀量逐渐增大,在阴极桶底部出现大量白色沉淀。
2.3 电解质中阴离子对溶胶的聚沉
于跃芹[7,8]等研究发现,Cl-、SO42-等对氢氧化铝胶体具有聚沉作用,且阴离子的价数越高,聚沉能力越大。因此,海水介质中的主要阴离子Cl-的存在,对氢氧化铝胶体转为Al(OH)3(S)沉淀,起到了一定的促进作用。
3 结语
(1)牺牲阳极加速腐蚀试验中,阴阳极电势差已超过碳钢上的析氢电位,海水水解产生的H+在阴极不断消耗,并形成氢气析出,随着氢气的析出,阴极区OH-离子剩余,导致阴极区pH值升高;
(2)铝阳极在外部电场的作用下,不断被氧化为Al3+,阳极区生产的Al3+和阴极区生成的OH-相向移动,并发生反应,生成铝的单核、多核水解产物,水解产物为胶体性质的混凝剂,在布朗运动的作用下,均匀分布于海水介质中,在激光照射下,出现丁达尔效应;
(3)铝的单核、多核水解产物与浓度不断增大的Al3+进一步发生反应,形成Al(OH)3(S) 沉淀。
