盐酸头孢噻呋注射液在鸡体内的药物代谢动力学研究
2022-08-11王淑婷田丽华王玉东宋翠平
刘 坤,王淑婷,田丽华,王玉东*,宋翠平*
(1.中国动物卫生与流行病学中心,农业农村部动物及动物产品卫生质量监督检验测试中心,山东 青岛 266032;2.青岛市黄岛区农业农村局,山东 青岛266400)
头孢噻呋(ceftiofur)又名“赛得福”,是第一个专门用于动物的第三代头孢类抗菌素[1],由Benard Labeouw在1984年率先合成,后由美国法玛西亚-普强公司[2]制作成盐酸盐悬浊液和钠盐冻干粉。1988年,该药在美国首次上市,因其抗菌活性优良,药物动力学良好的特点,先后被日本、美国等国家正式批准用于动物的呼吸道感染疾病的治疗,显示了在兽医临床应用的广阔前景[3]。近年来,该药物在我国被广泛使用,被制成各种剂型,广泛用于兽医临床。2021年我国批准了美国2家公司的盐酸头孢噻呋注射液2种新兽药的进口注册[4]。头孢噻呋在体内分布广泛,在体内生成有活性的代谢产物,进一步转化成无活性的产物,从粪和尿中排泄[5-6]。对革兰氏阳性菌和革兰氏阴性菌的抗菌活性较强[7],具有广谱杀菌作用,对头孢噻呋敏感的病原菌主要有溶血性巴氏杆菌、多杀性巴氏杆菌、胸膜肺炎放线杆菌[8-9],及葡萄球菌、链球菌等。其作用机制为作用于细菌内的转肽酶,阻断粘肽的合成,可使细菌缺失细胞壁而死亡,达到快速杀菌的效果[10]。临床主要用于治疗溶血性巴氏杆菌和胸膜肺炎放射杆菌引起的动物呼吸道感染疾病。
头孢噻呋对动物的的毒性作用较小,不良反应一般在用药几天后才出现,主要表现为皮疹等过敏症状。头孢噻呋与妥布霉素或氨基糖苷类药物联合使用对肾有毒性作用,如何减少毒副作用,对药物进行药代动力学研究非常必要。本试验旨在通过比较三种盐酸头孢噻呋注射液在白羽鸡体内的药代动力学参数变化规律,以判断新研制的盐酸头孢噻呋的药物动力学参数是否符合有关标准,同时,为国内创新药物研究和现有药物的临床合理用药,以及确定用药间隔及频次、制定休药期和防止兽药残留提供参考。
1 材 料
1.1 试验动物 40只健康白羽鸡,25日龄,体重1.4 kg左右,由山东亚太中慧鸡场提供,鸡群已按规定日龄接种新城疫、传染性支气管炎、传染性法氏囊病等疫苗,未使用过任何药物。饲养在试验鸡舍普通饲养笼具内,温度控制在(20±2)℃。饲喂不含任何抗菌药物的饲料,每天定时定量给料两次。临床观察一周,表现健康。试验前12小时及给药后4小时禁食,供给充足饮水,禁食后水中加1%的葡萄糖以补充试验动物体力。
1.2 试验器材 Agilent 2100高效液相色谱仪;电子天平JY2012型,北京科技仪器厂;台式离心机LGT-18G型,上海沪西仪器厂;微型涡旋混合仪WH-6型,天津精密科学仪器有限公司;分析天平AUY180型,岛津试验计测事业部;液体快速混合机YKZ型,哈尔滨医疗器械厂;超声波清洗机XKQ-200B,南京超声仪器有限公司;高速分散均质机 FJ-400型,成都标本模型厂;轨道式摇床KS510 digital型,德国IKA公司;MCX小柱MCX BondElut Varian 1CC 100MG,德国CNM公司。
1.3 试验药品及试剂 盐酸头孢噻呋注射液:美国盐酸头孢噻呋:规格:100 mL∶5 g美国硕腾,含量5%,批号0A4SM。大中农盐酸头孢噻呋:规格:100 mL∶5 g河南大中农动物药业有限公司,含量5%,批号兽药6288288。新研制盐酸头孢噻呋:规格:100 mL∶5 g山东某生物科技公司,含量5%。
乙腈(南京化学试剂股份有限公司)、氯化钾(上海市化学试剂厂)、四硼酸钠(上海化学试剂有限公司)、三氟乙酸(美国TEDIA天地试剂有限公司)、二硫赤鲜醇(Amrosce 02450)、碘乙酰胺(美国ACROS生物有限公司)、乙酸铵(天津化工有限公司)
1.4 主要溶液的配制 头孢噻呋储备液:称取头孢噻呋对照品,用0.05 mol/L的乙酸铵溶液稀释成每1 mL中约含头孢噻呋1000 μg的溶液,作为头孢噻呋备用液,临用前用0.05 mol/L的乙酸铵溶液配成梯度浓度为0.5-200 μg·mL-1的标准液。
2 方 法
2.1 动物试验
2.1.1 分组及给药 40只健康白羽鸡,随机分成四组。空白组10只,注射生理盐水,2.5 ml/kg体重。另外三组肌肉注射(美国盐酸头孢噻呋、大中农盐酸头孢噻呋、新研制盐酸头孢噻呋)给药进行药动学试验,试剂均为2.5 mg/kg体重。
空白组(10只):编号K1~K10
试验1组(10只):美国盐酸头孢噻呋编号A1~A10
试验2组(10只):大中农盐酸头孢噻呋编号B1~B10
试验3组(10只):新研制盐酸头孢噻呋编号C1~C10
2.1.2 采样及保存 通过鸡翅下静脉采集血液样品。给药前采一次空白血。按照2.5 mg.kg-1b.w剂量给试验鸡肌肉注射(美国盐酸头孢噻呋、大中农盐酸头孢噻呋、新研制盐酸头孢噻呋)给药后分别于15、30、45 min及1.5、2、2.5、4、6、8、24、30、48、72、96、144 h采集血样。每次采血1.5-2 mL,放入含EDTA-2K的离心管中,离心、分离血浆、-20 ℃保存,待测。
2.2 血浆中药物含量分析方法
2.2.1 色谱条件 色谱柱:Agilent TC-C18(4.6 mm×250 mm,ID);流动相A为0.1%三氟乙酸水溶液,流动相B为乙腈,按下表进行梯度洗脱;流速为每分钟1 mL;检测波长为266 nm;柱温为30 ℃。进样量为50 μL。

表1 色谱柱梯度洗脱表
2.2.2 样品分析前预处理 将冷冻存放的血浆,放在常温下自然解冻,然后摇匀取血浆0.5 mL放入10 mL具塞离心管中,加入1.2 mL提取液,涡旋1 min混匀,放入50 ℃恒温摇床,20 min。取出静置,待冷却到室温,加入0.5 mL 10%碘乙酰胺溶液,涡旋10 s,用锡纸包好放入30 ℃恒温震荡培养箱中,200 r/min衍生30 min。衍生后的混合液体加20%的磷酸100 μL酸化,加水1.25 mL混匀。4 ℃,12000 r/min离心20 min,取上清液备用。
MCX小柱依次加入3 mL甲醇、3 mL水活化,然后加入上一步衍生化所得的上清液,再依次加入3 mL水、3 mL色谱甲醇来淋洗;加入2 mL乙酸铵:乙腈(85+15,v/v)混合液洗脱;用0.22 μm微孔滤膜滤过所得的洗脱液,精确量取40 μL溶液注入液相色谱仪。
2.2.3 标准曲线的建立 取9支离心管,依次加入空白血浆0.45 mL,再依次加入50 μL系列浓度的头孢噻呋标准液(0.5-200 μg·mL-1),涡旋混匀,制备的样品中含头孢噻呋的系列浓度为0.05-20 μg·mL-1,第一支管作空白对照。按2.2.2 样品分析前预处理方法进行处理后,测定。将药物峰面积与相应药物浓度作线性回归,求标准曲线的相关系数和回归方程。
2.2.4 灵敏度(最低检测限、最低定量限)、回收率、精密度的考察 分别将0.1、2和40 μg·mL-1三种药物浓度的样品当作考察对象,每个浓度制作三份样品,按照血浆样品分析前预处理方法处理,进行高效液相测定,测出日间变异系数、日内变异系数,连续测3 d。
回收率:加样提取液的药物峰面积/标准溶液的峰面积×100%
日内、日间变异系数(精密度):标准差/平均数×100%
最低检测限:三倍信噪比时,仪器测定的进样药物量与样品溶液浓度的比值。
最低定量限:十倍信噪比时,进样药物量被定量测定的最低量。
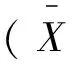
3 结果与分析
3.1 方法专属性 在试验建立的色谱条件下,血浆中的DCA与其他干扰杂质可以有效分离,色谱见图3-图6。DCA的出峰时间在9.2 min。
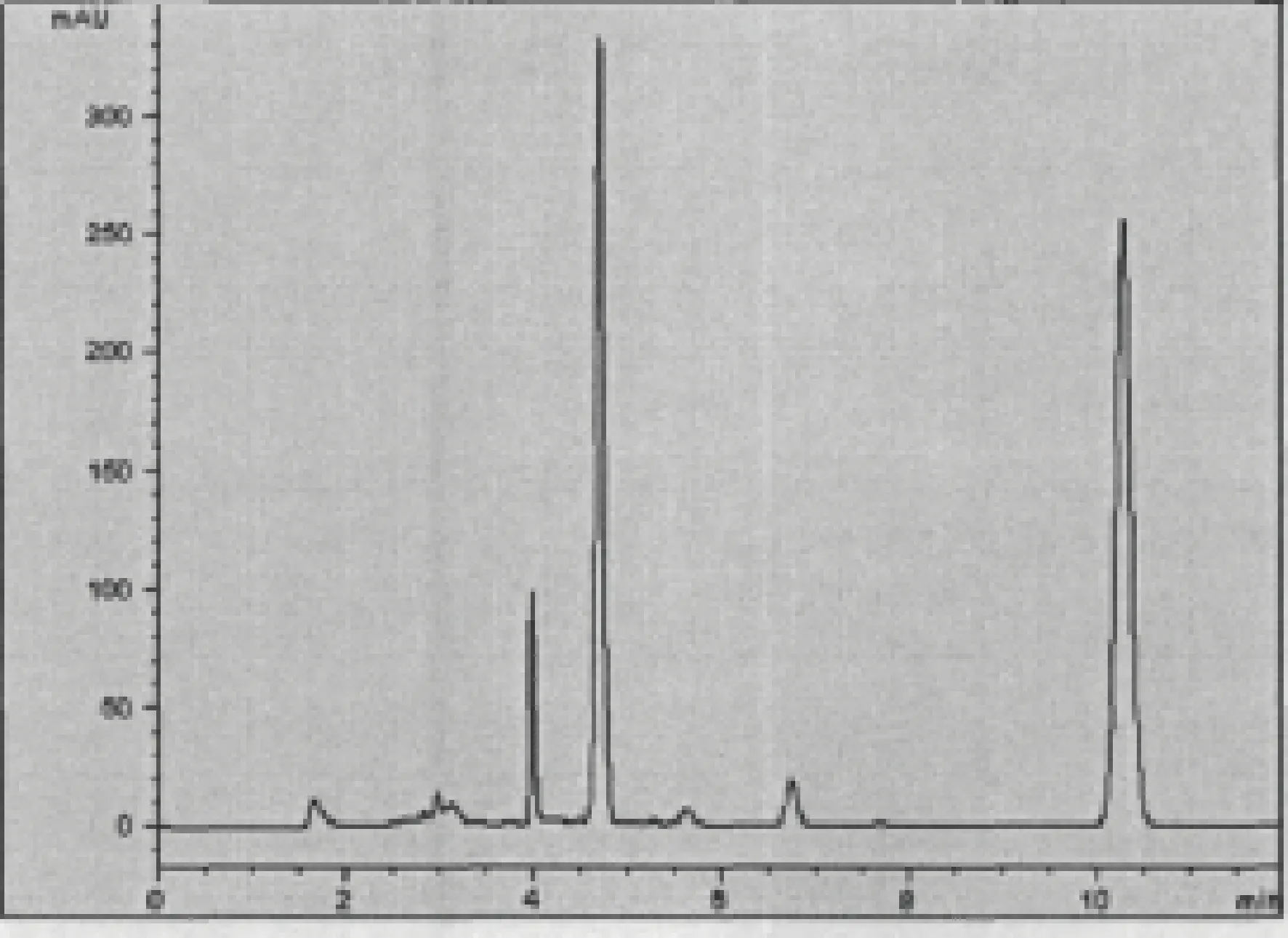
图1 空白血浆色谱图
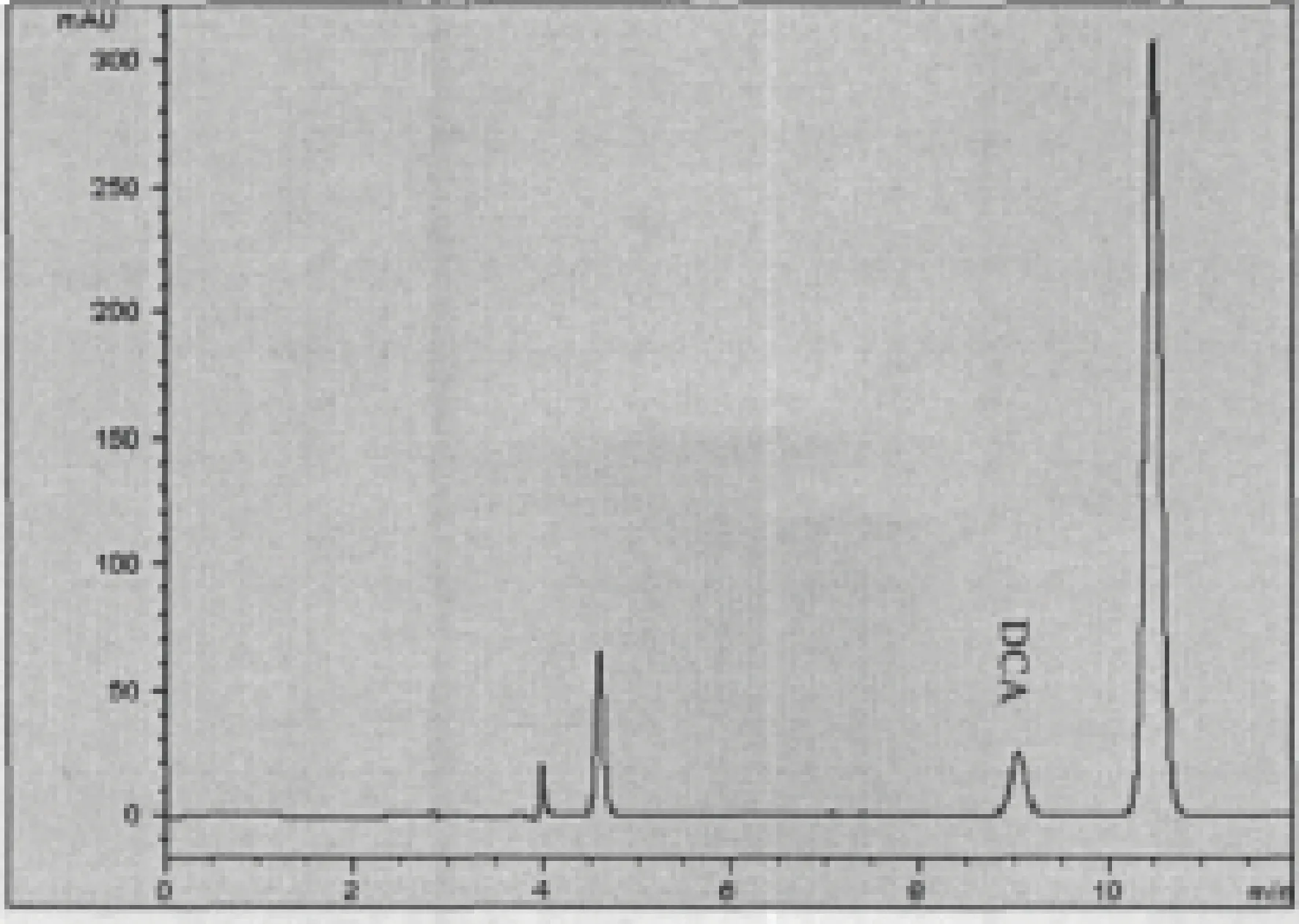
图2 标准溶液色谱图
图3 空白血浆添加盐酸头孢噻呋色谱图
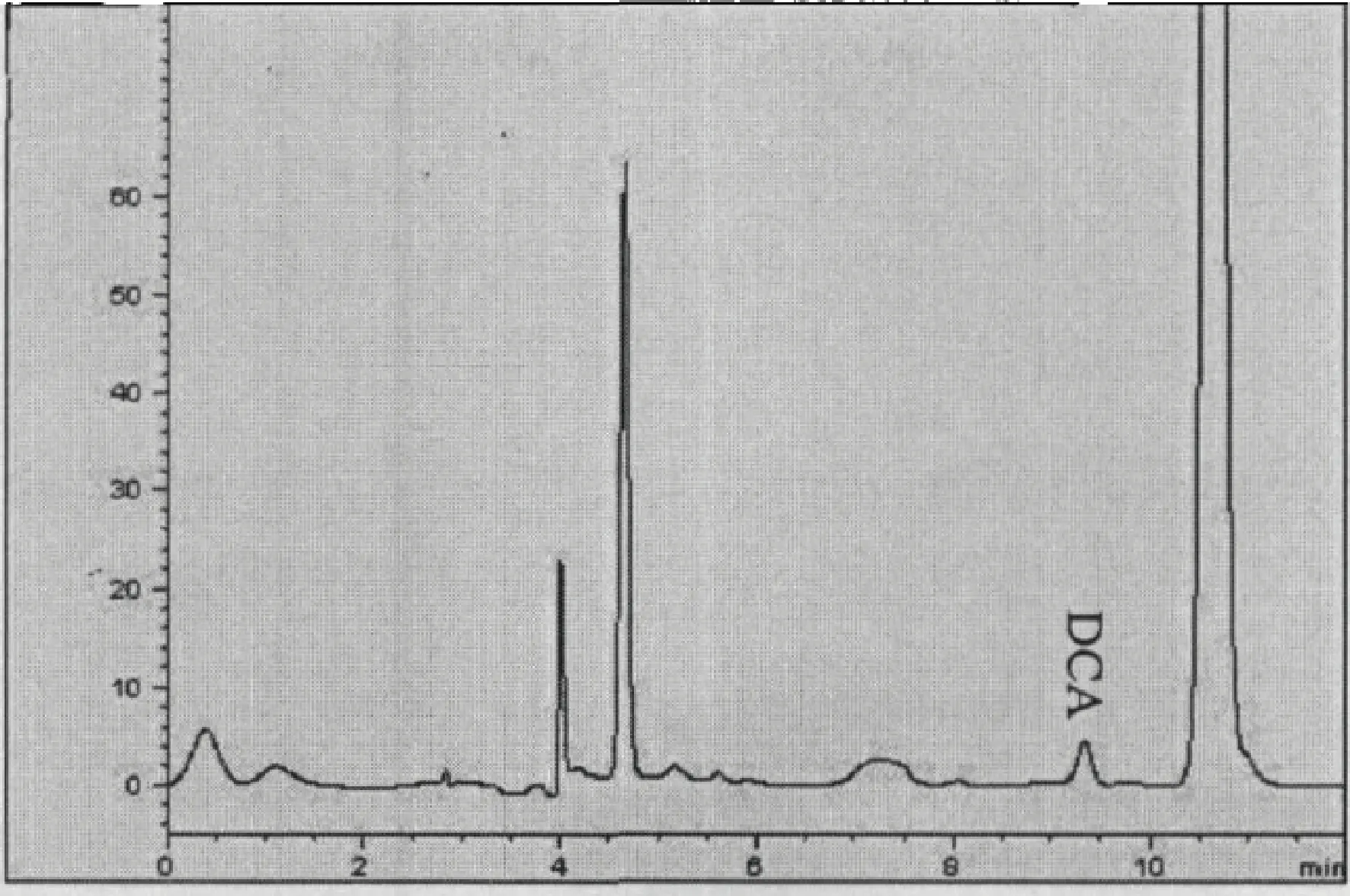
图4 实测色谱图
3.2 标准曲线和线性范围 经过不断摸索试验条件,血浆标准工作曲线的药物浓度线形范围、回归方程均符合试验的要求。线性范围在0.05至40之间,相关系数是0.999。回归方程(x:标准品在空白血浆的浓度,y:药物峰面积)和相关系数见表2。标准曲线图见图6。
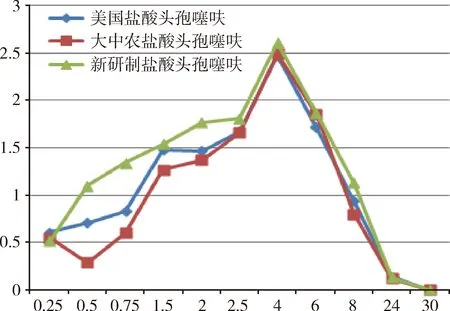
图6 鸡肌注射美国盐酸头孢噻呋、大中农盐酸头孢噻呋和新研制盐酸头孢噻呋后血药浓度-时间曲线

表2 盐酸头孢噻呋在血浆中的标准曲线和相关系数
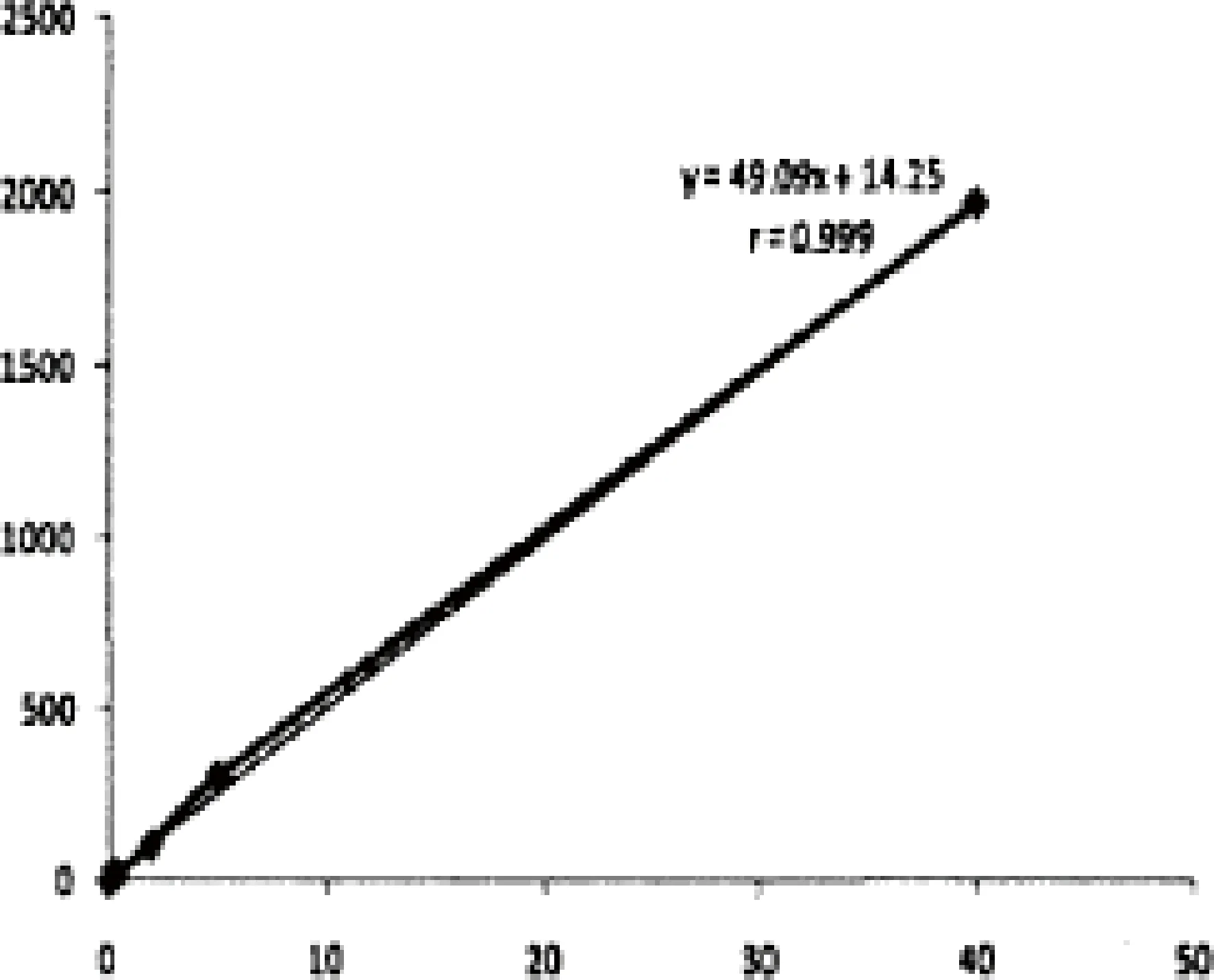
图5 DCA在血浆中的标准曲线
3.3 方法学验证数据
3.3.1 灵敏度考察 最低检测限:0.05 μg/mL;最低定量限:0.1 μg/mL。
3.3.2 回收率和精密度考察 血药浓度在0.1、5、40 μg/mL时,回收都在90%左右,精密度在2.97至4.63之间,均符合试验要求。按照样品预处理方法,在血浆中添加药物,测得精密度和回收率数据见表3。
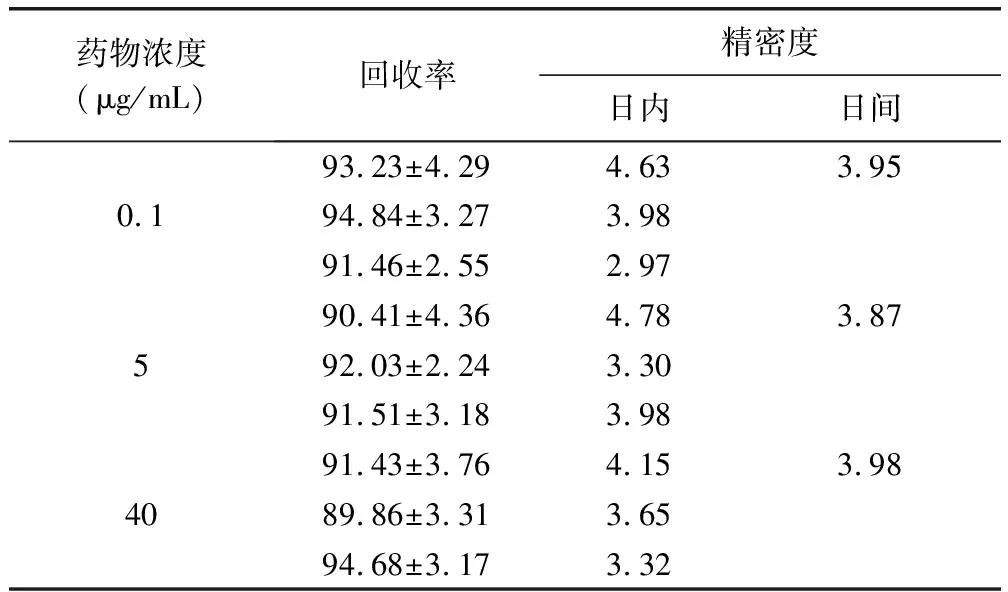
表3 鸡空白血浆添加盐酸头孢噻呋的方法学考察结果
3.4 血浆中的药物浓度 白羽鸡肌肉注射盐酸头孢噻呋后,体内血药浓度在4时达到最大值,30时已检测不到药物,表明药物在30时药物已基本代谢完。各时间点血浆药物浓度测定结果见表4和图7。
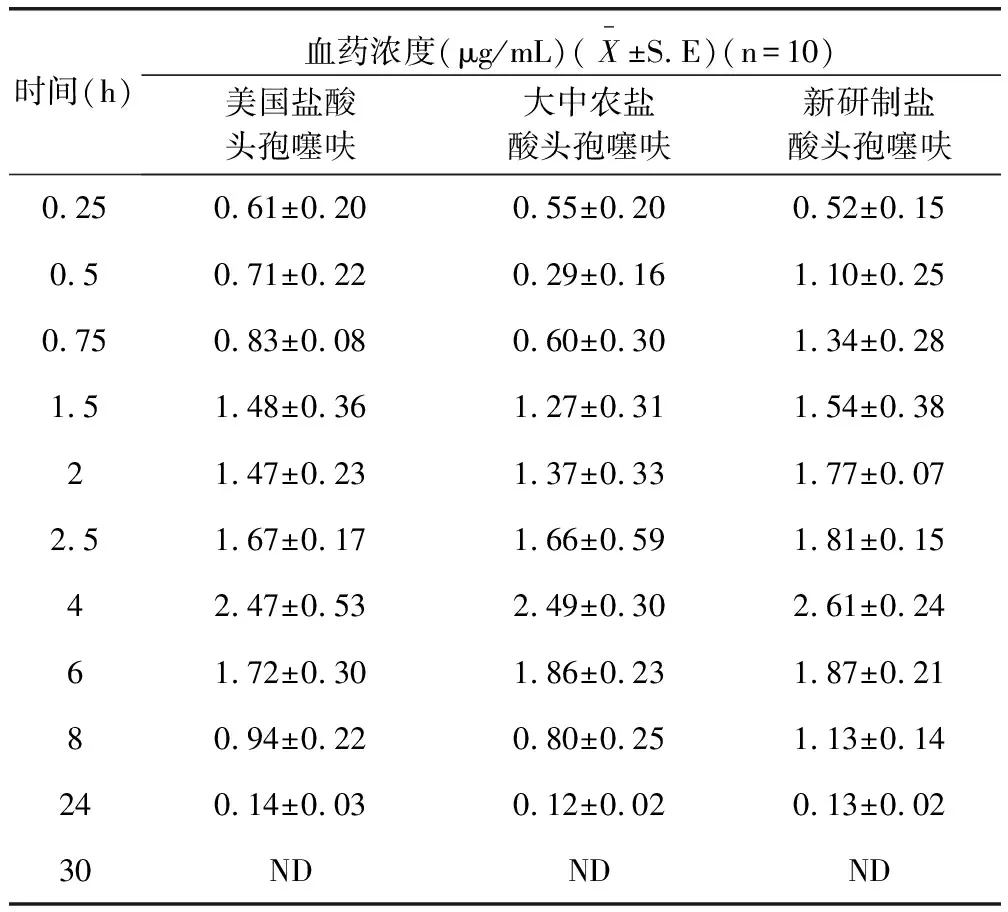
表4 鸡单次肌注盐酸头孢噻呋(2.5 mg.kg-1)血药浓度
3.5 头孢噻呋药物动力学参数 三种盐酸头孢噻呋(2.5 mg.kg-1 b.w.)的平均药动学参数采用SPSS比较差异性,见表5。
通过表5中的各项平均药物动力学参数可以看出,白羽鸡肌肉注射美国盐酸头孢噻呋4个小时后,血药浓度达到峰值,最高血药浓度为2.47 μg.mL-1,血浆中平均消除半衰期为4.22 h,AUC为19.1 μg.h.mL-1,平均滞留时间MRT为7小时;注射大中农盐酸头孢噻呋4 h后,血药浓度达到峰值,最高血药浓度为2.49 μg.h.mL-1,血浆中平均消除半衰期为4.02小时,AUC为21.1 μg.h.mL-1,平均滞留时间MRT为7 h;注射新研制盐酸头孢噻呋4 h后,血药浓度达到峰值,最高血药浓度为2.61 μg.h.mL-1,血浆中平均消除半衰期为4.22 h,AUC为24.1 μg.h.mL-1,平均滞留时间MRT为7 h。结果表明三种剂型的药物动力学参数差异不显著。

表5 三种盐酸头孢噻呋(2.5 mg.kg-1 b.w.)的平均药动学参数差异性分析结果
4 讨论与结论
白羽鸡肌肉注射头孢噻呋注射液后,三种药物达峰时间一样,都是注射药物后4 h血药浓度达峰值。通过注射液峰浓度来看,本新研制盐酸头孢噻呋的最高血药浓度稍微偏高,这是优势。
4.1 血浆样品的分离和提取 药物进入体内后快速的失去β-呋喃甲酰基,生成有活性的代谢产物,在血浆中很少以游离状态存在,主要与半胱氨酸形成二硫化合物,与血浆蛋白或组织蛋白结合形成去呋喃甲酰蛋白复合物,还可形成二聚物。本试验选用碘乙酰胺作为衍生试剂,采用二硫赤鲜醇作为提取剂,该方法每天处理四十多个样品,简单方便,比1990年Jalan[11]的每天处理十几个样品先进许多。新研制盐酸头孢噻呋的预处理方法可用于生物等效性的研究和药动学的研究。
4.2 提取液浓度的选择 在血浆样品中加入不同浓度的提取液,观察对回收率的影响。取含有0.02%、0.2%、2%三个浓度的二硫赤鲜醇提取液,每个浓度取5个重复,回收率分别为65.61%、90.5%和67.46%,所以试验中提取液浓度选为0.2%。加入不同浓度衍生试剂到样品中,观察对回收率的影响,取含有0.14%、1.4%、14%三个浓度的碘乙酞胺溶液提取液,每个浓度取5个重复,回收率分别是67.61%、90.53%和65.76%,所以试验中衍生试剂的浓度选用1.4%。
4.3 组织样品色谱条件的选择 Barker等[12]曾报道了美国盐酸头孢噻呋在动物组织中的高效液相检测方法,所用的色谱柱是AglentTC-C18柱。本试验所采用的流动相也是AglentTC-C18柱。将衍生后的DCA进行高效液相检测,经紫外分光光度计测定,结果显示,DCA在266 nm处有最大吸收峰,并且干扰较小,因此检测DCA的检测波长选用266 nm。
4.4 白羽鸡肌肉注射盐酸头孢噻呋的药动学特征 头孢噻呋抗菌活性优良,在临床中前景广阔。头孢噻呋能治疗犬的泌尿系统感染;马、羊、猪的肺炎、呼吸道感染等疾病,还可用于仔猪的断尾和断齿等引起的伤口感染;牛的子宫炎、呼吸道感染、腐蹄炎;本药对沙门氏菌和大肠杆菌等病原菌引起的鸡苗死亡有显著地防治效果[13-14]。
陈启友等[15]随机将12头健康猪分为两组,分别注射美国辉瑞美国盐酸头孢噻呋注射液、上海公谊兽药厂的长效盐酸头孢噻呋注射液,每头5 mg/kg。比较了进口头孢噻呋注射液和国产头孢噻呋注射液猪肌肉注后的药物动力学特征。结果表明:参数tmax、Cmax、MRT差异极显著(P<0.01),长效盐酸头孢噻呋注射液肌注给药比美国盐酸头孢噻呋注射液吸收慢,达峰时间推后,达峰浓度较低,驻留时间延长;参数AUC、Kel、t1/2无显著性差异(P>0.05)。
张志成等[16]以制剂的稳定性当作评价指标, 以玉米油为溶媒,加入适量的辅料,采用正交设计的方法,据盐酸头孢噻呋药物的特性设立了盐酸头孢噻呋混悬剂的制备方法。采用6个月加温加湿,10天光加速试验的方法对制备的混悬剂进行质量评价,研究了对盐酸头孢噻呋混悬剂的稳定性,结果外观性状、粒度等指标均无明显变化,表明该制剂对光、热稳定,基本符合药剂学中规定的混悬剂的要求,可顺利进行注射给药。试验证明该制剂稳定性好,工艺简单,刺激性小,具有较好的缓释效果;制剂的主要制剂学参数与辉瑞公司生产的盐酸头孢噻呋注射用混悬剂的主要制剂学参数比较差异不显著。药物动力学是药物通过各种途径进入动物体内后,吸收、分布、代谢和排泄的过程的“血药浓度-时间”变化规律的一门科学。试验结果表明,白羽鸡肌肉注射进口药、国产药和新研制的药后,三种药物吸收和消除速度差异不显著。总的来说,新研制盐酸头孢噻呋、大中农盐酸头孢噻呋和美国盐酸头孢噻呋注射液的药物动力学相当。
4.5 结论 试验进行了三种剂型药物动力学参数比较,经过研究发现,通过比较显示美国盐酸头孢噻呋、大中农盐酸头孢噻呋和新研制的药物各种参数差异不显著(P>0.05)。新研制盐酸头孢噻呋的各项参数符合药物标准。
