降低TiCl4中SiCl4含量的工艺研究
2022-08-11姜志刚
姜志刚
(中信钛业股份有限公司,辽宁 锦州 121005)
四氯化钛(TiCl4)是生产海绵钛和氯化法钛白必不可少的中间产物[1-2]。随着海绵钛和氯化法钛白生产的不断发展,需要大量四氯化钛。不论用哪种方法制得的粗TiCl4均需经进一步提纯才能应用[3]。其中TiCl4中的SiCl4是重要杂质之一。SiCl4含量偏高不仅会影响到商品精TiCl4的售价,还会影响到氧化系统的生产。由于中信钛业氯化法钛白粉生产工艺没有除Si装置,且精制系统不具备除硅功能,较高硅含量的精TiCl4直接进入氧化系统,可能对氧化工序的工艺控制和钛白粉的产品质量造成一定的影响。
20世纪90年代锦州建成了我国第一座万吨级氯化法钛白粉厂,并首次在国内采用大型化的熔盐氯化系统。其中生产的TiCl4中的SiCl4含量波动较大,是熔盐氯化非常突出的问题。据历年来生产统计结果,TiCl4中SiCl4质量分数最高时可达到0.5%,质量分数大于0.2%的TiCl4更是屡见不鲜;也频繁出现过SiCl4质量分数较低的现象,几乎全部小于0.1%。本文从工艺技术方面着手,利用低硅时生产数据,结合理论分析的结果,找到了控制TiCl4中SiCl4含量的技术方案。经过20多年年的艰苦努力,熔盐氯化系统得到逐步完善,氯化技术逐步成熟。
1 TiCl4中SiCl4含量波动原因的分析
1.1 原料中硅的形态对氯化率的影响
通过对硅的氯化率进行过详细计算对比得出,利用物料平衡的原理计算硅的氯化率3.56%高于以相对氯化率计算出的SiO2氯化率1.5%~2.0%,由此判断氯化偏高除了与氯化炉内壁的冲刷腐蚀有关,还可能与钛渣中SiO2的存在形态有关,分析原因如下。
1.1.1 SiO2的形貌增加了它的氯化程度
电子显微镜观察显示,钛渣中的SiO2主要分布在钛物相颗粒的表面(晶界之间)。SiO2的这样存在形式,大大增加了其与氯气等接触的几率,也就增加了SiO2的氯化程度。
1.1.2 SiO2以玻璃相存在,更容易氯化
自然界中SiO2的存在形态主要有:石英、方石英、磷石英和玻璃4种。1 100 K时各种形态的二氧化硅加碳氯化的平衡常数和自由能对比见表1。由表1可见,玻璃态的SiO2更容易被氯化,而且氯化的程度要高一些。

表1 1 100 K时各种形态的二氧化硅加碳氯化的平衡常数和自有能[4]
X-射线衍射和电子探针分析表明,高钛渣中的SiO2(Al2O3)主要是以玻璃相存在于钛物相的晶界之间,钛渣中物相成分如表2所示。

表2 钛渣中物相成分
1.1.3 CaO的氯化加速了SiO2的氯化
由于CaO、SiO2、Al2O33种组分均富集在钛物相的晶界间,相互结合以CaO·nSiO2或Al2O3·nSiO2形式存在,由于CaO最容易氯化,使与CaO结合的SiO2转变成新生态的SiO2,加速、加剧了硅的氯化。
1.2 氯气浓度对硅氯化率的影响分析
统计分析熔盐氯化系统连续5个月分别使用纯氯生产和循环尾气生产时的TiCl4中SiCl4含量情况,见图1。

图1 对接生产与纯氯生产时TiCl4中SiCl4质量分数对比
从图1可以看出,使用纯氯生产时TiCl4中SiCl4质量分数明显偏高。根据热力学计算,富态料中各组分在800 ℃下优先氯化的顺序为:CaO、MnO、MgO、Fe2O3、FeO、TiO2、Al2O3、SiO2。理论上,TiO2优先于SiO2和Al2O3发生反应,当控制反应使TiO2达到全部氯化时,氯化剩余物(残渣)主要成分为SiO2和Al2O3。但对于熔盐系统,熔盐的黏度较大,局部过剩的Cl2并不能马上与其他颗粒接触发生反应,造成了钛渣颗粒中SiO2的部分氯化。当生产时使用纯氯气,提高了局部过剩氯气的浓度,增加了熔盐中氯气与SiO2接触的几率,提高了SiO2的氯化率。反之,当对接生产时,降低了熔盐中局部过剩氯气的浓度,降低了氯气与SiO2接触的几率,SiO2的氯化率相对较低。
另外,因为SiCl4(g)+O2→SiO2+2Cl2(1 000K)反应的吉布斯自由能为-236 104 J,大于TiCl4(g)+O2→SiO2+2Cl2(1 000 K)反应的吉布斯自由能(-105 980 J),当使用循环氯气生产时,氧气成分的存在,存在着O2与SiCl4接触的可能性,从一定程度上降低了系统SiCl4的质量分数。
1.3 系统投料量对硅氯化率的影响
统计分析11个月熔盐氯化废盐中的SiO2质量分数与对应的粗TiCl4中SiCl4质量分数的关系,见图2。
由图2中可以看出这样的一个规律,废盐中SiO2质量分数越大,TiCl4中SiCl4质量分数就越低,当废盐中SiO2质量分数大于1.0%时,TiCl4中SiCl4质量分数一般都会低于0.1%。经分析,造成这一现象的主要原因是,熔盐氯化系统中大部分Si会被主气流吹到收尘系统,少量的Si悬浮在熔盐的表面,当Si的氯化率高时,悬浮在熔盐表面的少量SiO2颗粒很快被氯化而使废盐中SiO2的质量分数变小;当条件发生变化,Si的氯化率变低时,则会出现SiO2颗粒在熔盐表面的富集,废盐中SiO2的质量分数偏高的现象。由此可以推断,废盐中SiO2的质量分数是体现Si的氯化率大小的一个重要指标。

图2 废盐中Si质量分数与对应的SiCl4质量分数关系
对11个月废盐的成分进行了对比,可以看出废盐中∑Ti质量分数大部分在1.0%以下,说明TiO2氯化得较为彻底,有少部分∑Ti质量分数大于1.0%的废盐说明该阶段的TiO2氯化不够彻底。同时对废盐成分中∑Ti质量分数大于1.0%时对应的SiO2质量分数进行了分析,结果见图3。
从图3中可以看出,当废盐中∑Ti质量分数大于1.0%时,废盐中的SiO2质量分数基本大于1.0%,且随着∑Ti质量分数的增加,废盐中的SiO2质量分数也会明显增加,当废盐中∑Ti质量分数达到10.0%以上时,废盐中的SiO2质量分数会超过5.0%。

图3 废盐成分中∑Ti质量分数大于1.0%时对应的SiO2质量分数
也就是说,废盐中∑Ti质量分数增加时,会促使系统中Si的氯化率降低。当废盐中∑Ti质量分数增加时,说明系统的投料量相对增多,造成了TiO2在熔盐的中残留,同时也使熔盐层剩余的氯气量减少,降低SiO2与氯气接触的几率;又因为TiO2优先于SiO2发生氯化反应,TiO2的存在也会降低SiO2与氯气接触的几率,两方面原因将同时导致SiO2的氯化率大大降低。
根据以上的分析,统计了熔盐氯化系统与氧化对接运行氧化较为稳定的4个时间段,高硅时段与低硅时段系统的投料量(钛渣投料量,后同)与TiCl4中SiCl4质量分数的关系。氧化较为稳定的时间段,根据物料衡算进入熔盐氯化系统的氯气量也应该比较稳定,以此值与投料量之间的比值(Cl2/钛渣)反映系统投料量的大小。Cl2/钛渣的值越小,投料量越大。对接状态下,Cl2/钛渣比值与SiCl4质量分数的对应关系如表3所示。
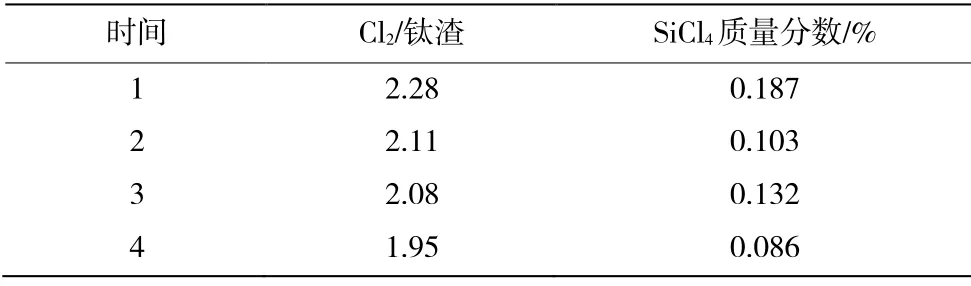
表3 对接生产时Cl2/钛渣与SiCl4质量分数列表
从表3中可以看出,随着系统投料量的增加,Cl2/钛渣比值的变小,SiCl4的质量分数则会相应地降低。系统的投料量直接影响着SiO2的氯化率,影响着粗TiCl4中SiCl4的质量分数。
2 结 论
1)钛渣中SiO2形态对TiCl4中SiCl4含量有一定影响,即玻璃态的SiO2含量越低,越易被氯化SiO2越少,TiCl4中SiCl4含量越低。
2)氯化过程使用的氯气浓度会影响TiCl4中SiCl4含量,即氯气体积分数在70%~100%范围内越低,TiCl4中SiCl4含量越低。
3)氯化过程Cl2/钛渣的比值对TiCl4中SiCl4含量有一定影响,即在满足正常理论反应配比的前提下Cl2/钛渣的比值越低,TiCl4中SiCl4含量越低。
