《中国药典》2020年版蛋黄卵磷脂细菌内毒素检测
2022-08-08裴宇盛赵小燕
裴宇盛,赵小燕,陈 晨,高 华,蔡 彤
(中国食品药品检定研究院化学药品检定所药理室,北京 102629)
蛋黄卵磷脂是从蛋黄中提取精制而得的天然磷脂混合物,是一端亲水另一端疏水的两亲分子,为天然的表面活性剂[1]。因此,在脂肪乳、脂质体等特殊注射剂得到广泛的使用[2]。细菌内毒素是细菌死后或者自溶后留下的位置,仍然具有致热性,其主要成分是类脂A核心多糖和特异性多糖[3]。蛋黄卵磷脂作为注射用辅料,设立了细菌内毒素检查项目,并且蛋黄卵磷脂(供注射用)是《中国药典》2020年版四部收载品种。目前药典中的方法为“取本品,以无水乙醇充分溶解,进一步使用细菌内毒素检查用水稀释至实验所需浓度(该溶液中乙醇浓度应大于20%),依法检查(通则1143),每1 g中含内毒素的量应小于2.0 EU”[4]。
药用辅料性质较特殊,该品种的内毒素检查在实际应用过程中产生了一些问题。根据国家药典委员会征求意见的反馈,经归纳主要存在以下问题:①部分企业按药典规定的原方法回收率不能在50%~200%之间,不能排除蛋黄卵磷脂对内毒素检测的干扰;②由于蛋黄卵磷脂天然表面活性剂的性质加上内毒素本身容易被吸附的问题,对于该辅料是选择凝胶法还是定量法作为常用的检测方法存在不同意见(目前许多药物或辅料的细菌内毒素检查项目中选择凝胶法作为常用的方法[5]);③该辅料是用检查用水溶解还是无水乙醇溶解存在不同意见。
为了准确检测蛋黄卵磷脂的质量,保障相关制剂的临床使用安全,本研究旨在建立新的蛋黄卵磷脂的内毒素检测方法,为药典修行提供依据。
1 材料与方法
1.1 主要材料与试剂Elx808型酶标仪(美国BioTek公司);S-0520型细菌内毒素检查法检测反应板(湛江安度斯生物有限公司);AE240型电子分析天平(瑞士梅特勒公司);MultiReax全能型振荡器(德国Heidolph公司);15 mL无热原离心管(美国CORNING公司)。
无水乙醇(分析纯,国药集团化学试剂有限公司);吐温80(化学纯,国药集团化学试剂有限公司);细菌内毒素国家标准品(批号:150800-201601,中国食品药品检定研究院);检查用水(批号:2103110,湛江安度斯生物有限公司);动态浊度法鲎试剂(批号:2009042,湛江安度斯生物有限公司),动态浊度法鲎试剂(批号:J1382L,美国CHARLES RIVER公司);蛋黄卵磷脂(批号:19110807、19110407、19110607,南京绿叶制药有限公司),蛋黄卵磷脂(批号:11NF9332、11NH1661,费森尤斯卡比华瑞制药有限公司),蛋黄卵磷脂(批号:A40210203、A40210204,A40210205,广州白云山汉方现代药业有限公司)。
1.2 方法
1.2.1标准曲线的可靠性验证 取细菌内毒素国家标准品1支,按要求用1 mL细菌内毒素检查用水复溶,在振荡器上振荡15 min混匀,用检查用水稀释到标准曲线所需要的浓度,即:104、103、100、10 EU·L-1的标准细菌内毒素稀释液,每步稀释都应在振荡器上混匀30 s。每一浓度平行2孔,同时BET水作为阴性对照平行2孔。研究使用两个厂家的鲎试剂(湛江安度斯生物有限公司及美国CHARLES RIVER 公司)。按要求复溶所需的鲎试剂,取标准曲线所需标准细菌内毒素稀释液,阴性对照每孔0.1 mL加入检测板,随后每孔加入0.1 mL鲎试剂,上机检测。当阴性对照的反应时间大于标准曲线最低点时,所有试验结果进行双对数转换,转换后进行线性拟合。拟合方程为LgT=a·lgC+b,线性拟合的相关系数|r|≥0.980时,标准曲线的可靠性符合规定。
1.2.2干扰试验 最大稀释倍数(MVD)计算 根据MVD=c L·λ-1,按标准曲线可靠性验证项下制备标准曲线,λ为10 EU·L-1;L为供试品的内毒素限值,根据药典规定,蛋黄卵磷脂的内毒素限值为2.0 EU·g-1;c为供试品溶液的浓度,本研究蛋黄卵磷脂浓度为0.1 kg·L-1。即:MVD=(2.0 EU·g-1×0.1 kg·L-1)÷10 EU·L-1=20倍。
供试品原液的制备 蛋黄卵磷脂不溶于水,因此使用助溶剂作为溶剂制备其溶液。制备助溶剂的方法为2.5 g吐温80:2.7 mL无水乙醇。制备的蛋黄卵磷脂溶液,需用细菌内毒素检查用水稀释后再进行内毒素检测。但在用水稀释的过程中,如果蛋黄卵磷脂浓度较高,蛋黄卵磷脂会从溶液中析出,出现浑浊或沉淀,干扰试验结果。经实验摸索,需配制适量蛋黄卵磷脂供试品溶液浓度为0.1 kg·L-1,进行后续实验。
供试品溶液与供试品阳性对照(positive product control, PPC)的制备 取0.1 kg·L-1的供试品原液1 mL加入试管中,加入检查用水10 μL(供试品阳性对照加入5×105EU·L-1的内毒素标准溶液10 μL),在振荡器充分混合(4 min),混合后取0.1 mL加入到已含0.9 mL检查用水的试管中,在振荡器充分混合(4 min),混合后取0.5 mL加入到已含0.5 mLBET水的试管中,在振荡器充分混合(2 min),此时即为稀释20倍的供试品溶液,PPC中添加标准内毒素的浓度为250 EU·L-1。
按照药典规定方法进行检测,见Tab 2、3。
2 结果
2.1 标准曲线的可靠性验证结果使用两个厂家的鲎试剂(TAL),|r|> 0.980,见Tab 1。

Tab 1 Results of assurance of criteria for standard curve
2.2 干扰试验及检查法结果3个蛋黄卵磷脂厂家的8批样品的回收率均符合药典中规定的50%~200%,见Tab 2、3。
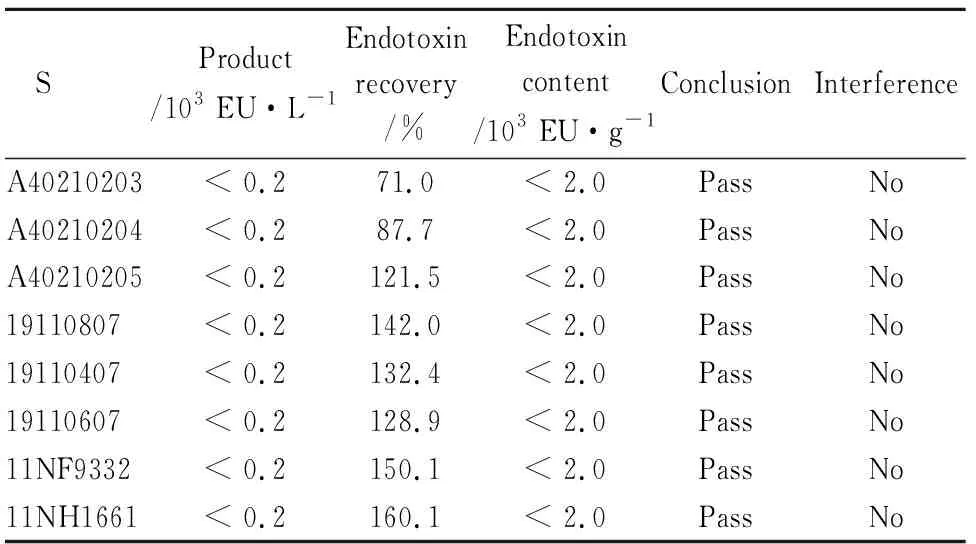
Tab 2 Results of interference test and KCA assay(Zhanjiang A&C)
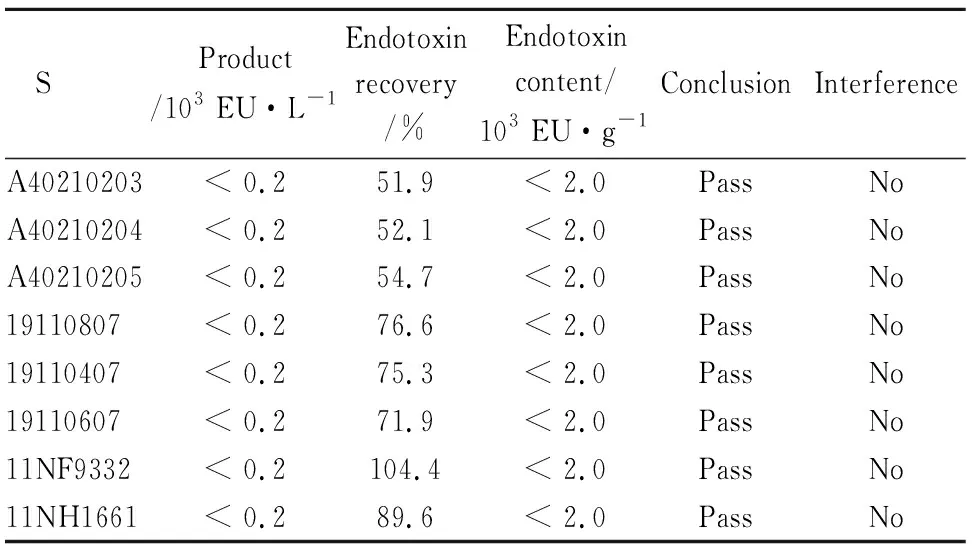
Tab 3 Results of interference test and KCA assay (CHARLES RIVER)
3 讨论
3.1 研究结论使用上述方法,采用两个来源的鲎试剂,3个蛋黄卵磷脂厂家的8批样品,回收率均符合药典中规定的50%~200%,符合干扰试验要求,解决了目前的内毒素检查法在实际应用中的问题。建立了具有较好耐用度的蛋黄卵磷脂细菌内毒素检查方法,为药典修订提供了依据。
3.2 方法的耐用度对该研究方法进行了方法的耐用度检验。除了“2”项下所呈现的结果,对蛋黄卵磷脂浓度调整为0.02 kg·L-1、PPC中添加标准内毒素的浓度调整为100 EU·L-1、对应标准曲线采用103~1 EU·L-1检测范围的试验条件下,采用上文所描述的两个鲎试剂厂家的鲎试剂检测,均能够得到回收率通过的结果,且样品符合规定。
3.3 蛋黄卵磷脂的干扰原因经过大量前期研究,蛋黄卵磷脂干扰内毒素检测的主要原因有3个,一是蛋黄卵磷脂本身因表面活性作用,作为极易形成包裹内毒素的结构对内毒素检测造成干扰;二是卵磷脂本身溶解度较低,无论是直接用水溶解产生浑浊,还是在乙醇溶解之后使用检查用水稀释过程中出现析出,都会而影响检测;三是乙醇本身对检测具有干扰作用,当浓度低于5%时干扰作用可被消除[6]。
3.4 采用乙醇溶解的依据研究表明由于蛋黄卵磷脂在水中溶解度极低,使用检查用水分散蛋黄卵磷脂,出现明显的浑浊现象,不能得到均一的溶液。细菌内毒素体积极小,一般认为在1~5 nm3[7]。肉眼可见的颗粒会将内毒素包裹起来,在检测过程中不能检测到颗粒内部包裹的内毒素。所以为了准确检测蛋黄卵磷脂中的所有内毒素,选择使用无水乙醇溶解蛋黄卵磷脂。
3.5 采用动态浊度法进行检测的依据浑浊对动态浊度法和动态显色法均具有干扰作用[8-9],凝胶法属于终点检测,过程中的浑浊对其无影响,从这方面来说,凝胶法相比其他方法具有明显的优势。然而凝胶法的检测限只能达到30 EU·L-1,相比动态浊度法10 EU·L-1来说,无法将蛋黄卵磷脂进一步稀释,无法排除卵磷脂本身的干扰。经过研究,将蛋黄卵磷脂检测浓度降低更有利于干扰的排除,因此选择了动态浊度法进行检测。同时也进行试验将蛋黄卵磷脂的限值提高至6.0 EU·g-1时,参考药典规定及上述方法制备供试品溶液及供试品阳性对照溶液,得到的结果符合药典规定凝胶法中样品不干扰内毒素检测。但是,对于提高限值还需要进一步研究讨论。
3.6 原方法的存在的其他问题《中国药典(四部)》2020年版要求蛋黄卵磷脂以无水乙醇充分溶解,进一步使用细菌内毒素检查用水稀释至实验所需浓度(该溶液中乙醇浓度应<20%)。对于乙醇浓度的要求,是由于乙醇本身也会对检测造成干扰,研究进行过程中也考察了30%的乙醇溶解蛋黄卵磷脂,观察到不同厂家蛋黄卵磷脂的溶解度出现极大差异,这表明同为蛋黄卵磷脂物理性质方面仍具有较大差异,在药典执行过程中,不同厂家干扰情况存在差距应由产品本身差异造成。提示应进行更多耐用度试验。这与药品的内毒素检测有较大差异。药品的内毒素检测一般情况下不会出现不同厂家样品干扰情况不同的情况。针对药用辅料的内毒素检测方法的建立,应尽可能采用更多的样品研究。
3.7 采用超滤离心法尝试排除干扰利用蛋黄卵磷脂与细菌内毒素的分子量差异大,滤过蛋黄卵磷脂,对截留内毒素进行检测。研究过程中摸索了超滤膜对于无水乙醇的化学相容性,发现乙醇浓度<70%时不会影响在实验过程中超滤膜的稳定性。摸索乙醇浓度<70%时蛋黄卵磷脂的溶解性,蛋黄卵磷脂在70%乙醇中溶解度8 g·L-1。在3、10、20 ku截留不同分子量的超滤离心管中,筛选出截留分子量为10 ku的超滤离心管。PPC中添加标准内毒素的浓度也进行了摸索,最终选择1.0 EU·L-1。离心时转速为5 000g,离心3次,每次离心15 min。经过上述条件摸索,经回收率验证,可对蛋黄卵磷脂进行检测,但该方法的重复性较差。
3.8 尝试采用鲎试剂稀释排除干扰使用上述及原方法等各种实验方法得出的结果都显示回收率低于50%的结果,推断蛋黄卵磷脂由于其表面活性剂作用,形成了包裹内毒素的结构,使内毒素无法准确被检测出来,为了排除该干扰,采用供试品稀释过程中使用鲎试剂作为溶剂稀释供试品,增加内毒素与鲎试剂的接触,在稀释过程中和卵磷脂形成的包裹内毒素的结构相互竞争。该方法经过试验验证可得到回收率在50%~200%的检测结果。并且具有较好的重复性。该方法主要存在的问题是,样品和标准曲线采用了不同的反应体系,尝试采用了稀释过的鲎试剂以及降低回收率试验中内毒素添加浓度等方法,证明所采用的鲎试剂稀释液对反应体系没有影响。由于该方法不同于常规排除干扰的方法,验证方法复杂,需要进一步研究确定。
3.9 尝试采用ELISA法排除干扰尝试利用ELISA法排除干扰的原理基于结合步骤不仅使用了结合缓冲液,同时也增加了在37 ℃恒温下长时间(18 h)结合的优势,使内毒素充分被检测孔里的特异性蛋白结合,考虑应用此方法可使内毒素被充分的检测。根据ELISA使用说明,必须测试有机溶剂的化学相容性,经过试验验证,在乙醇浓度低于30%时不会对检测结果造成干扰。但由于蛋黄卵磷脂溶解度问题,无法获得适宜浓度的蛋黄卵磷脂的30%乙醇溶液。需将限度值放宽约10倍才能进行试验。因此该方法对蛋黄卵磷脂检测还需摸索其他化学相容性好且对蛋黄卵磷脂肉溶解度高的有机溶剂。
3.10 尝试采用萃取法排除干扰为了排除蛋黄卵磷脂对检测的干扰,利用蛋黄卵磷脂易溶解于氯仿的特性,参照文献[10]设计,采用将蛋黄卵磷脂溶解于氯仿后再用内毒素检查用水萃取其中内毒素。空白试验采用内毒素标准品通过二甲基溶解后,加入氯仿中,可以被内毒素检查用水成功萃取。然而,当蛋黄卵磷脂加入后,形成了乳化现象,经回收率验证,该方法无法将内毒素准确提取。如进一步研究需更换萃取的有机溶剂,或采取混合有机溶剂进行萃取研究。