艾司西酞普兰血药浓度/剂量比的影响因素研究Δ
2022-08-03钟璐莲郭媛媛盛小茜贾晓健
钟璐莲,陈 政,郭媛媛,刘 云,盛小茜,贾晓健
(1.深圳市精神卫生中心/深圳市康宁医院药学部,广东 深圳 518118; 2.深圳市精神卫生中心/深圳市康宁医院研究所,广东 深圳 518118)
抑郁症是一种以显著且持久的心境低落为主要临床特征的精神疾病,调查结果显示,我国有超过9 500万例的抑郁症患者,是全球抑郁症患者数最多的国家[1]。抑郁症给个人、家庭带来了极大的痛苦,并造成了沉重的经济负担。目前,抑郁症的治疗药物主要有选择性5-羟色胺再摄取抑制剂(SSRI)、5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRI)以及其他三环、四环类抗抑郁药。其中,艾司西酞普兰(SSRI类药物)因其临床疗效好、安全性更高,已成为临床治疗抑郁障碍的一线药物[2-4]。但其引起的以神经系统损伤为主的药品不良反应[5]影响了治疗效果及患者依从性,因此,有必要对艾司西酞普兰进行血药浓度监测。此外,艾司西酞普兰在《AGNP精神科治疗药物监测共识指南:2011》的四个监测等级中为推荐(二级)级别,治疗的参考浓度范围为15~80 ng/mL。艾司西酞普兰是我院2021年使用数量和销售金额最多的药物,为进一步了解其临床使用情况,探讨其血药浓度/剂量比(C/D)的影响因素,本研究对相关信息进行回顾性分析,为临床治疗提供参考。
1 资料与方法
1.1 资料来源
通过我院电子病历系统收集2019年10月至2021年11月使用艾司西酞普兰的住院患者的病历资料,整理患者的血药浓度、日剂量、性别、年龄、联合用药、药品厂家和基因分型等基本信息。纳入标准:服用艾司西酞普兰达到稳态血药浓度的住院患者(艾司西酞普兰半衰期为30 h,血药浓度经5个半衰期约7 d可达稳态)。数据剔除标准:超过监测下限、未达到稳态血药谷浓度和联合应用2种以上抗精神病药的监测数据。共纳入符合标准的艾司西酞普兰住院患者275例,男性98例,女性177例;年龄12~76岁,平均年龄为(32.73±15.13)岁;艾司西酞普兰平均日剂量为(15.67±4.91) mg/d,平均稳态血药浓度为(31.95±23.19) ng/mL,平均C/D值为(2.03±1.23) d/L。其中,艾司西酞普兰血药浓度低于参考浓度范围(15 ng/mL)的患者66例,占24.00%;在参考范围内(15~80 ng/mL)的患者195例,占70.91%;>80 ng/mL的患者14例,占5.09%,见表1。
1.2 血样采集及血药浓度测定方法
服用艾司西酞普兰的住院患者,清晨给药前采集其血浆3~5 mL作为血药浓度监测样本。采用LC-MS/MS 8030型超高效液相质谱联用仪(日本岛津公司)对艾司西酞普兰血药浓度进行检测。
1.3 基因检测
基因型测定在我院研究所分子生物学实验室完成。CYP2D6检测包括*1(正常)、*2、*4、*10和*41等5个位点;CYP2C19检测包括*2、*3和*17等3个位点。采用柱提取法提取DNA(DNA提取试剂盒生产厂家为上海莱枫生物科技有限公司)。采用基因检测试剂盒(武汉友芝友医疗科技有限公司)进行DNA的聚合酶链反应(PCR)。采用ABI 7300型实时荧光PCR扩增仪(美国ABI公司)进行扩增。
1.4 CYP2D6、CYP2C19基因分型
综合CYP2D6等位基因携带情况,将患者进行分组。(1)正常代谢型:未携带CYP2D6*4、CYP2D6*10和CYP2D6*41,即*1/*1、*1/*2和*2/*2;(2)中间代谢型:携带CYP2D6*4(1个)或CYP2D6*10或CYP2D6*41,即*1/*10、*2/*10、*4/*10、*10/*10、*1/*41、*2/*41、*10/*41、*4/*41和*1/*4。
综合CYP2C19等位基因携带情况,将患者进行分组。(1)快代谢型:未携带CYP2C19*2和CYP2C19*3,即*1/*17、*17/*17和*1/*1;(2)中间代谢型:携带CYP2C19*2和CYP2C19*3,即*1/*2、*1/*3、*2/*17和*3/*17;(3)慢代谢型:同时携带*2或(和)*3,即*2/*2、*3/*3和*2/*3。
1.5 统计学方法
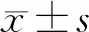
2 结果
2.1 血药浓度与其影响因素的多元线性回归分析
运用SPSS 25.0统计软件分析得到多元线性回归方程:艾司西酞普兰=-37.69+5.88×年龄-0.92×厂家-0.2×性别+1.36×联合用药+13.62×CYP2D6基因代谢型-8.39×CYP2C19基因代谢型+4.27×剂量(R2=0.650),见表2。

表2 多元线性回归分析:不同自变量对艾司西酞普兰浓度的影响
2.2 性别、年龄、联合用药、厂家、代谢酶CYP2D6和CYP2C19代谢型对艾司西酞普兰C/D值的影响
2.2.1 性别:275例患者中,男性患者98例,女性患者177例。分析结果显示,女性患者的艾司西酞普兰C/D值明显高于男性,差异有统计学意义(P=0.021<0.05),见表3。
2.2.2 年龄:按照年龄,将患者分为未成年组(<18岁)62例、成年组(18~65岁)205例及老年组(>65岁)8例。分析结果显示,各年龄组患者艾司西酞普兰C/D值的差异无统计学意义(P>0.05),见表3。
2.2.3 联合用药:临床药物治疗方面,我院艾司西酞普兰较常与喹硫平、奥氮平和利培酮联合应用。分析结果显示,无联合用药组患者艾司西酞普兰的平均C/D值为(2.03±1.31)d/L;联合利培酮组患者艾司西酞普兰平均C/D值为(1.61±0.80) d/L,联合氯氮平组为(2.99±1.90) d/L,两组间的差异有统计学意义(P=0.035<0.05);联合普萘洛尔组患者艾司西酞普兰平均C/D值为(1.28±0.52) d/L,联合奥美拉唑组为(3.00±1.04) d/L,两组间的差异有统计学意义(P=0.030<0.05);联合普萘洛尔组患者艾司西酞普兰平均C/D值为(1.28±0.52) d/L,联合氯氮平组为(2.99±1.90) d/L,两组间的差异有统计学意义(P=0.021<0.05),见表3。
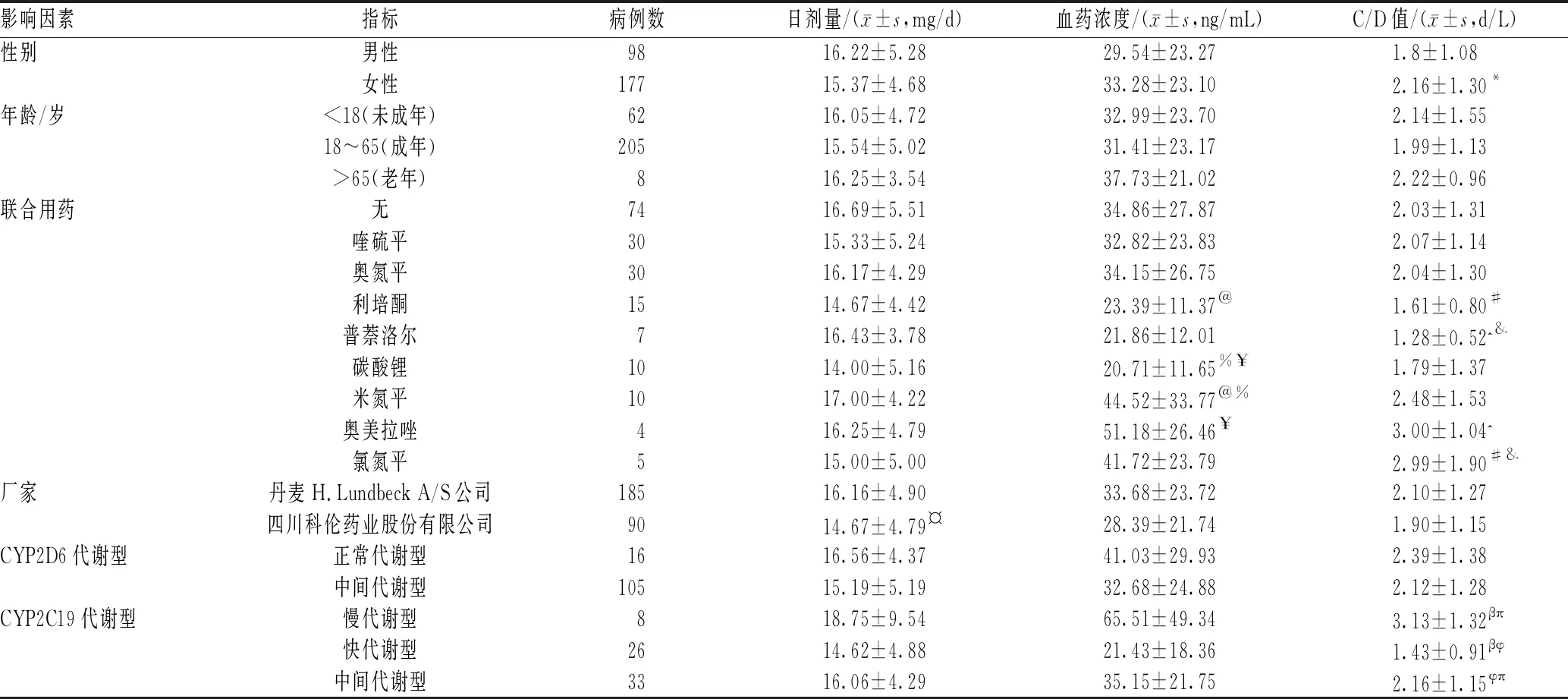
表3 性别、年龄、联合用药、厂家、CYP2D6和CYP2C19代谢类型对艾司西酞普兰C/D值的影响
2.2.4 厂家:本研究中,使用原研药(草酸艾司西酞普兰片,丹麦H.Lundbeck A/S公司)的患者185例,使用国产仿制药(草酸艾司西酞普兰片,四川科伦药业股份有限公司)的患者90例。分析结果显示,使用不同厂家药品的患者艾司西酞普兰C/D值比较,差异无统计学意义(P>0.05),见表3。
2.2.5 代谢酶CYP2D6、CYP2C19代谢类型:本研究中,代谢酶CYP2D6为正常代谢型的患者16例,中间代谢型105例,代谢酶CYP2D6正常代谢型与中间代谢型组间艾司西酞普兰平均C/D值的差异无统计学意义(P>0.05);代谢酶CYP2C19慢代谢型的患者8例,快代谢型26例,中间代谢型33例,CYP2C19慢代谢型与快代谢型、快代谢型与中间代谢型、慢代谢型与中间代谢型组间艾司西酞普兰平均C/D值的差异均有统计学意义(P<0.05),见表3。表3中,有90例患者联合其他用药,未逐一列出;另有87例患者未测基因型。
3 讨论
艾司西酞普兰为丹麦H. Lundbeck A/S公司研发的SSRI类药物,用于治疗抑郁和惊恐障碍,常用日给药剂量为10~20 mg,因起效快、症状改善效果更明显且有效率更高等优势成为临床一线用药[6]。
因药物剂量直接影响血药浓度,故以C/D值作为评价指标来探讨性别、年龄、联合用药、厂家、代谢酶CYP2D6和CYP2C19代谢类型等因素对艾司西酞普兰C/D值的影响。本研究中,女性患者艾司西酞普兰C/D值明显高于男性,差异有统计学意义(P=0.021<0.05)。在药动学方面,大多数抗抑郁药的吸收、分布、代谢和排泄存在一定程度的性别差异,如相较于男性患者,女性患者代谢酶CYP2C19活性较低[7]。在药效学方面,多数学者认为女性使用SSIR类药物的效果优于男性;但另有研究结果显示,男性服用艾司西酞普兰的效果优于安慰剂组,而女性服用的效果接近安慰剂组[8]。一般认为,艾司西酞普兰无需因性别差异调整剂量[9]。
联合用药方面,艾司西酞普兰联合其他药物与单独使用艾司西酞普兰时艾司西酞普兰C/D值的差异无统计学意义(P>0.05),但个别艾司西酞普兰联合用药组间C/D值的差异有统计学意义(P<0.05)。临床上,抑郁障碍常伴精神及其他躯体疾病症状,为提高疗效及降低药品不良反应发生率,常联合用药,但易引起药动学方面的相互作用。艾司西酞普兰为CYP2D6酶抑制剂,同时少部分经CYP2D6代谢,利培酮、氯氮平和普萘洛尔为CYP2D6酶底物,联合应用可能会影响经CYP2D6代谢药物的血药浓度;奥美拉唑为CYP2C19酶抑制剂,联合应用时会增加艾司西酞普兰的血药浓度。药物代谢酶作用机制复杂,联合应用时需考虑药物之间是否存在药动学相互作用,了解各药的主要代谢酶及该药是否为其他药物的酶抑制剂/诱导剂。如需联合应用有相互作用的药物,应做好血药浓度监测。
本研究中,代谢酶CYP2C19慢代谢型、快代谢型和中间代谢型三组患者艾司西酞普兰C/D值的差异有统计学意义(P<0.05)。艾司西酞普兰血药浓度影响因素的多元线性回归分析结果佐证了艾司西酞普兰主要代谢酶为CYP2C19[10]。代谢酶CYP2D6非艾司西酞普兰血药浓度差异的主要影响因素。本研究所统计的使用艾司西酞普兰的患者中代谢酶CYP2C19慢代谢型较少,以快代谢和中间代谢型居多,与汉族人群的CYP2C19基因多态性主要分布于快代谢和中间代谢的研究结果一致[11]。有研究建议制定个体化给药方案,同时对使用艾司西酞普兰患者的CYP2C19基因型进行检测[12]。CYP2C19为快代谢型时,血药浓度达峰时间延长或不能达到有效治疗浓度,导致治疗失败的风险更高[13];CYP2C19为慢代谢型时,对药物的代谢速度减慢,药物疗效增强的同时增加了不良反应发生风险[14]。一项Meta分析结果显示,经过6周标准剂量的艾司西酞普兰治疗后,慢代谢型患者较其他代谢型具有良好的疗效,且没有相关后期不良反应[15]。因此,临床使用艾司西酞普兰疗效不佳且患者代谢酶CYP2C19为快代谢型或慢代谢型时,建议临床医师采取先调整药物剂量替代更换药物的做法[16]。
本研究中,各年龄组、不同厂家组患者艾司西酞普兰C/D值的差异无统计学意义(P>0.05)。尽管艾司西酞普兰治疗儿童及青少年抑郁症时出现自我伤害或想法的发生率与安慰剂组相近[17],在用药过程中仍需留意“增加儿童及青少年的自杀念头和行为风险”黑框警示。依基因表型、血药浓度调整给药剂量,可以提高青少年抗抑郁药治疗的有效性、安全性及耐受性[18-19]。对于老年抑郁症患者,研究结果显示,艾司西酞普兰等SSRI类药物治疗老年抑郁症患者疗效相当,但需要降低高龄患者剂量[20]。艾司西酞普兰国产仿制药(草酸艾司西酞普兰片,四川科伦药业股份有限公司)作为国家集中采购的第一批中选药品,单片价格约为原研药(草酸艾司西酞普兰片,丹麦H.Lundbeck A/S公司)的1/4,从药物经济学角度考虑,推荐选用通过一致性评价的艾司西酞普兰国产仿制药,不仅有同样的治疗效果,还能缓解患者的就医负担。
综上所述,艾司西酞普兰的C/D值与性别、代谢酶CYP2C19代谢类型有关,部分联合用药对其有一定影响,不同厂家对其无明显影响。年龄、CYP2D6代谢类型对艾司西酞普兰C/D值的影响需进一步扩大样本量验证。临床可结合血药浓度、基因分型、临床诊疗效果及药物经济学优化给药方案,提高药物疗效及患者依从性。
