乳粉中微生物检测的实验室间比对结果分析
2022-08-02林双庆王仍瑞许秋贝郑小文杨玉贞
林双庆 王仍瑞 许秋贝 郑小文 杨玉贞
(厦门海关技术中心 福建 厦门 361000)
1 前言
实验室间比对是指按照预先规定的条件,由多个实验室对相同或类似的样本进行检测的组织、实施和评价[1],可作为能力验证的补充,强化实验室质量控制,是多种外部质量控制的方法之一。漳州市是福建省出口食品农产品的重要城市,2015年其食品农产品出口量居全国地级市首位[2]。本次实验室间比对评价了漳州地区以出口为主的63家食品企业的微生物检测能力,以帮助企业内部实验室查找日常检测工作中存在的问题,制定相应措施以保持或提升其微生物检测能力。本次实验室间比对共涉及6个微生物检测项目,2个定量项目包括菌落总数和大肠菌群,4个定性项目包括金黄色葡萄球菌、沙门氏菌、副溶血性弧菌和单核细胞增生李斯特菌。
2 材料与方法
2.1 主要仪器与试剂
恒温培养箱(F-0.5P,日本医化仪器公司);全自动微生物鉴定仪(VITEK2 Compact 30,法国生物梅里埃公司);生物安全柜(HF1200,上海力康生物医疗科技控股有限公司);冷冻干燥机(LFD5508,韩国DAIHAN LABTECH公司);高压灭菌锅(VB-95,德国SYSTEC公司);TSA固体培养基、BHI液体培养基、BPW液体培养基,APW液体培养基(北京陆桥技术股份有限公司);NaN3、海藻糖、谷氨酸钠(国药集团化学试剂有限公司);0.85%无菌生理盐水(实验室自制)。
2.2 标准菌株
鼠伤寒沙门氏菌(ATCC14028);金黄色葡萄球菌(ATCC6538);表皮葡萄球菌(CMCC26069);副溶血性弧菌(ATCC17802);单核细胞增生李斯特氏菌(ATCC19115);英诺克李斯特氏菌(ATCC33090);大肠埃希氏菌(ATCC25922);阴沟肠杆菌(CICC 21539)。菌株均来自专业机构保存的可溯源标准菌株。
2.3 方案设计
按参试实验室所报项目发放样品,定量项目随机发放1份考核样品,定性项目随机发送2份考核样品(阴性样本或阳性样本),每份样品对应1个唯一编号。参试实验室按《乳粉中微生物项目比对实验参试指导书》进行样品接收、检测和结果报送。方案同时赋予每个实验室1个代码,结果分析和能力评价均以实验室代码表示。
2.4 样品制备
将标准菌株在BHI液体培养基中复苏,增菌备用(副溶血性弧菌在APW液体培养基中复苏);在含有保护剂的乳粉基质中添加预定浓度的目标菌悬液(部分项目添加背景干扰菌),充分混匀,装入西林瓶,冷冻干燥后完成制备。
菌株添加前需进行菌株纯度和关键生化特性验证;基质、保护剂和西林瓶等样品制备所需试剂耗材需经无菌处理,并在无菌环境中完成样品制备;致病菌样品在相应的生物安全等级区域完成制备。
2.5 检测方法
建议检测方法为GB4789系列国家食品安全标准[3-8]。
2.6 均匀性和稳定性检验
样品均匀性检验方法:样品分装后,随机抽取10份样品,每份样品重复测试2次,定性样品的测试结果均与样品指定值(阳性或阴性)一致时,说明该样品符合要求。定量样品依据CNAS-GL003:2018《能力验证样品均匀性和稳定性评价指南》中的单因子方差分析法(F检验法)进行均匀性检验[9]。
样品稳定性检验方法:(1)在贮存温度(4℃)下,于均匀性检验完成后的第10、20天,随机抽取3个样品进行检测;(2)在模拟样品的运输条件下(2天时间内样品可送达各实验室),将样品分别置于20℃、36℃和42℃环境条件下,于均匀性检验完成后的第3、6天,随机抽取3个样品检测。每个样品重复测试2次。定性样品的测试结果与样品指定值(阳性或阴性)均一致时,说明该样品符合要求。将定量样品的测试结果与均匀性检测数据进行比较,采用T检验法(依据CNAS-GL003:2018“5.2”中的内容)进行稳定性评价。均匀性和稳定性检验结果表明,样品之间不存在显著性差异,满足实验室间比对样品要求。
2.7 统计分析的设计和结果评价原则
定性项目:将参试实验室的检测结果与实验设计的指定值(阳性或阴性)进行比较,若两者结果一致,能力评价为“满意”;若结果不一致,能力评价为“不满意”。定量项目:参照CNAS-GL002《能力验证结果的统计处理和能力评价指南》和CNAS-CL01-A001《检测和校准实验室能力认可准则在微生物检测领域的应用说明》的稳健统计方法,确定指定值X和能力评定标准差σ[10-11],计算Z比分数(Z值),利用Z值进行结果评价。当|Z|≤2.0时,结果为“满意”;当2.0<|Z|<3.0时,结果为“可疑”;当|Z|≥3.0时,结果为“不满意”。
3 结果与分析
3.1 检测结果总体情况分析
本次实验共有65家实验室参与,收回368个实验结果。菌落总数项目共有63家实验室参加并报送结果,各反馈结果的实验室Z比分数见图1。统计数据表明,共有52家结果为“满意”,占比82.5%;5家结果为“可疑”,占比7.9%;6家结果为“不满意”,占比9.5%。
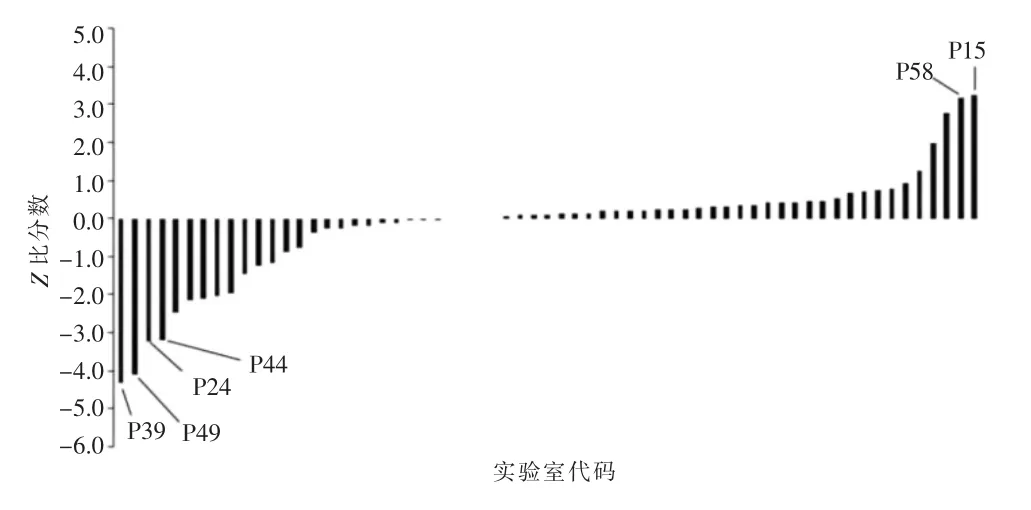
图1 菌落总数测定结果Z比分数分布柱状图
大肠菌群项目共有63家实验室参与,有5家结果无具体数值(大于或小于某个数值),未参与统计分析和结果评价,各反馈结果的实验室Z比分数见图2。统计数据表明,共43家结果为“满意”满意,占比74.1%;8家结果为“可疑”,占比13.8%;7家结果为“不满意”,占比12.1%。
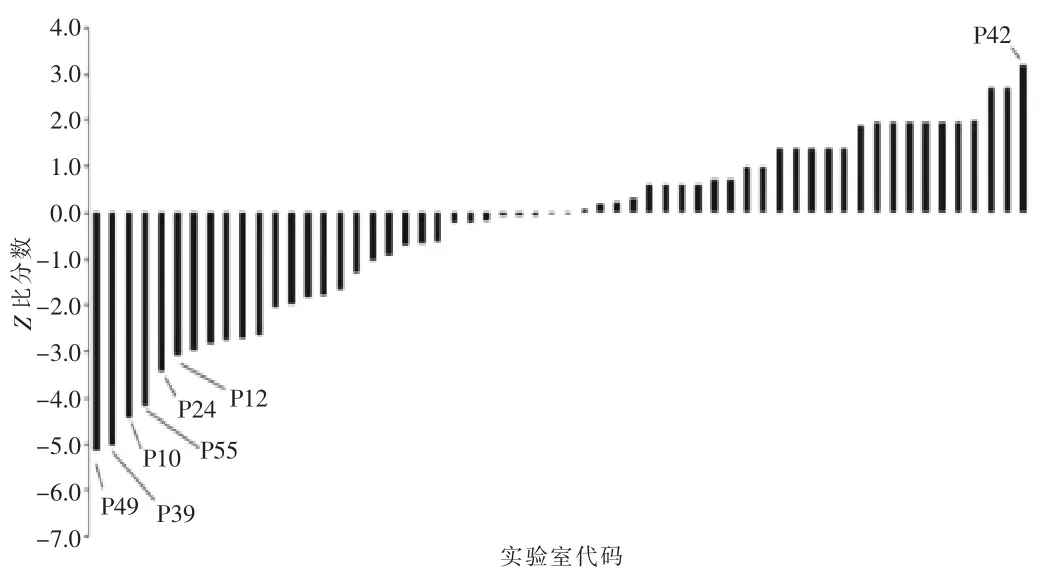
图2 大肠菌群测定结果Z比分数分布柱状图
2个定量项目的检测结果见表1。

表1 2个定量项目结果满意的实验室家数及百分比
金黄色葡萄球菌项目共有43家实验室参与,收回86个结果,41家实验室结果为“满意”,占比95.3%;2家结果为“不满意”,占比4.7%。
沙门氏菌项目共有38家实验室参与,收回76个结果,37家实验室结果为“满意”,占比97.4%;1家结果为“不满意”,占比2.6%。
副溶血性弧菌项目共有22家实验室参与,收回44个结果;单核细胞增生李斯特氏菌项目共有18家实验室参与,收回36个结果,均未出现不满意结果。
4个定性项目检测结果见表2。
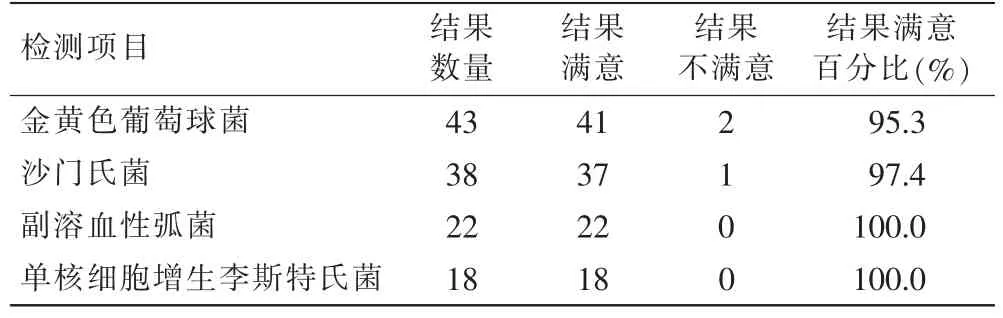
表2 4个定性项目结果满意的实验室家数及百分比
3.2 检测方法情况
除1家实验室的副溶血性弧菌项目采用SN/T 0173行业标准外,其他实验室和其他项目均使用GB 4789系列国家食品安全标准进行检测。
3.3 不满意结果分析
对本次实验反馈的结果进行分析,部分实验室出现可疑或不满意结果的原因可能为:
(1)样品处理不合理。未严格按照参试指导书制备样品,例如,未充分洗脱西林瓶内的样品或使其出现溢洒;分割一部分样品进行检测;样品溶解不充分,导致样品菌数发生变化。
(2)检验人员经验不足。有5家实验室未能给出大肠菌群MPN计数法检测结果的具体数值,说明其未能充分评估样品中的大肠菌群含量,未选择合适的稀释梯度进行实验。若实验过程中出现未对样品充分混匀、移液器使用不规范、培养基温度过高等情况,也会影响检测结果。
(3)检测方法使用不当。部分实验室未能使用现行有效标准,如代码P7实验室采用已废止的标准GB 4789.2-2010和GB 4789.3-2010,代码P11实验室采用的SN/T 0173-2010由SN/T 0173-2018替代[12]。
(4)出现假阴性结果可能原因:培养基质量不能满足实验要求,未分离出典型菌落;进行生化实验时,未使用标准菌株作阴阳性对照;仅挑取1~2个可疑菌落进行生化实验,结果为假阴性时直接判定结果。
(5)出现假阳性结果可能原因:在同时检测2份样品的过程中,发生了交叉污染,阴性样品受阳性样品污染,出现假阳性结果;培养基出现典型或可疑菌落后,未按要求进行生化和血清验证就判定为阳性结果。
4 讨论
本次实验室间比对实验定量项目结果的满意率较低,菌落总数为82.5%,大肠菌群为74.1%;定性项目结果的满意率较高,4个项目均达到90%以上。影响检测结果准确性的因素有检测人员、仪器设备、样品处理、标准物质、检测方法、设施与环境条件、试剂材料等[13],在检测过程中应对这些因素进行合理有效的控制。结果为“不满意”的实验室应当增加相关项目的外部质控活动频次,及时发现不足和积累经验,不断提升自身检测业务能力,有效控制食品安全风险,确保检测质量符合国家标准要求。
