绿色催化氧化合成邻硝基苯甲醛
——一个氧化合成教学实验
2022-08-01李胜杨爽刘永浩赵子卓张琦黄治炎
李胜,杨爽,刘永浩,赵子卓,张琦,黄治炎
陕西师范大学化学化工学院,西安 710119
2021年5月28日,习近平总书记在中国科学院第二十次院士大会、中国工程院第十五次院士大会、中国科协第十次全国代表大会上强调:“必须深入实施科教兴国战略,实现高水平科技自立自强。”创新人才培养已形成社会共识,是实现高水平科技自立自强的主要抓手之一[1–3]。有机化学学科最大特点就是创造新物质、实现新功能、满足新需求,学生着迷于有机合成是因为在实验过程中能合成新物质,能体会到“创造”的快乐。有机化学实验是落实化学创新人才培养的重要基础课程之一[4]。张树永等[5]在解读《化学类专业本科教学质量国家标准》[6,7]中建议:“在实验内容的设计上要体现新颖性。要将一些化学实验的新方法、新原理、新物质、新功能引入到实验教学中来,使实验教学内容更多地贴近实际、贴近前沿,使实验内容与教师的科研、高校的地方和行业的特色对接,与学生未来就业与发展需要对接,提高实验的新颖性、实用性和趣味性。”
近年来,有机合成化学领域取得了长足的发展,形成很多绿色合成技术用于制备重要的精细化学品。实验教材唯有与时俱进,将最新的绿色合成方法应用于实验教学,才能激发学生对有机化学、合成化学等的兴趣。在新形势下,设计环境友好型新创实验已然成为有机化学实验教学改革的重要抓手之一。在实验教学中,采用以“科学问题为目标导向”的实验教学指导原则,将相关科学问题的解决过程融入有机化学实验教学,有助于培养化学类专业本科生发现问题、分析问题和解决问题的内生动力和综合能力,激发创新意识和潜能,提高人才培养质量[8–10]。
本文选择重要医药中间体邻硝基苯甲醛的合成工艺为研究案例,以相应关键科学问题的解决过程为主线,将最新发展的绿色催化氧化合成工艺开发为有机化学基础实验,引导学生理解绿色化学和催化氧化反应的重要意义。具体教学和实验实施过程如图1所示,通过引出科学问题、引导分析问题、解决问题,设计实验方案、反思与评价等环节将有机化学理论知识、有机化学实验基础操作和科学探究方法等串联起来,夯实化学类人才培养实验教学基础。实验过程包含实验预习、实验设计、实验探究、结果解析、讨论与展望等五个环节,植入从事有机化学方法学和合成工艺研究的基本思路,培养学生解决较为复杂有机合成问题的综合能力。

图1 以“科学问题为目标导向”的探究型实验教学模式
1 实验部分
1.1 背景介绍
邻硝基苯甲醛是一种非常重要的精细化学品,在医药、染料和农药等领域有着广泛的应用,如常用于合成治疗心血管疾病药物硝苯地平、尼索地平、恩卡尼、盐酸氨溴索等(图2),全球年需求量超过1000吨,工业上主要以邻硝基苄醇为原料,通过控制氧化反应(微课介绍氧化反应的发展历程)条件制备得到。

图2 邻硝基苯甲醛及相关药物分子结构
截至目前,以邻硝基苄醇为原料,文献或专利报道制备邻硝基苯甲醛的化学合成方法主要分为三类:1) 基于有机小分子2,2,6,6-四甲基哌啶氧化物(英文名称:2,2,6,6-tetramethyl-1-piperidine-N-oxyl,简称TEMPO)与金属铜或铁的协同催化体系[11];2) 次氯酸钠氧化体系[12];3) 稀硝酸或氢溴酸/双氧水氧化体系。前两种方法采用空气、氧气或廉价易得的试剂为氧化剂,副产物为水,具有绿色化学特征。然而,TEMPO易残留在产品中带来基因毒性,沸石负载的金属催化剂易流失和污染产品[11]。次氯酸钠氧化选择性差,副产物邻硝基苯甲酸比例高[12]。硝酸对设备腐蚀性强,所得副产物对空气和水均形成污染[13],这都是产业界亟待解决的问题。
产物过度氧化为羧酸是次氯酸钠氧化体系产率低的主要原因。如图3所示,受邻位硝基吸电子诱导和共轭效应的影响,邻硝基苯甲醛可通过形成水合物,继而被进一步氧化为副产物邻硝基苯甲酸。
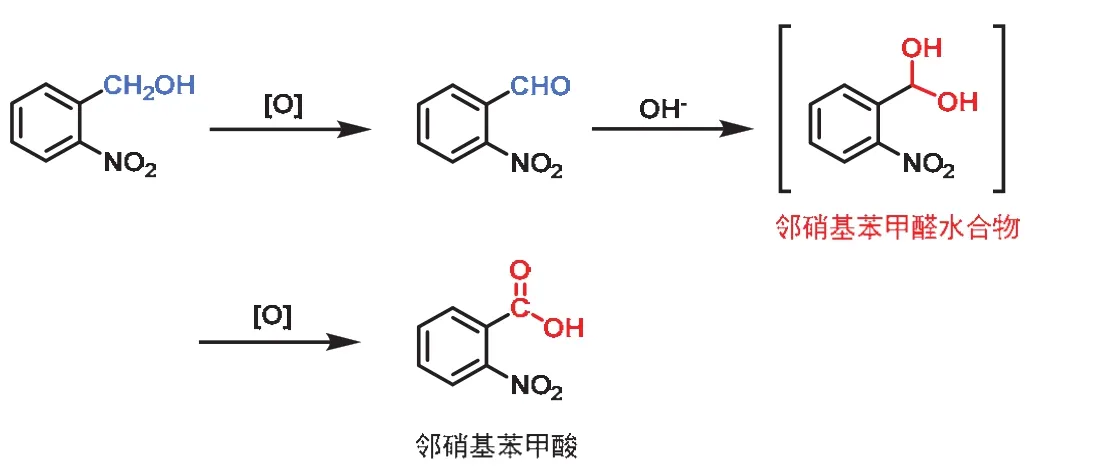
图3 邻硝基苯甲醛和邻硝基苯甲酸的形成过程
基于上述文献案例分析,我们不难发现产业界需求和所面临问题是重要的创新研究项目。对于邻硝基苯甲醛的制备,其中的科学问题亦逐渐明晰:1) 如何解决TEMPO残留的问题,是发展新的分离方法,亦或是设计更易与产物分离的TEMPO衍生物为催化剂?2) 如何更好固载金属催化剂防止流失,或者从源头上避免使用金属催化剂?3) 如何避免邻硝基苯甲酸的形成?
1.2 实验目的
1) 了解有机小分子催化反应;
2) 掌握两相反应设计的原理;
3) 掌握催化氧化合成邻硝基苯甲醛的反应机理;
4) 掌握邻硝基苯甲醛的制备、反应进度监测以及分离与精制方法;
5) 掌握核磁共振波谱仪、高效液相色谱等产物结构表征和纯度分析实验技术。
1.3 实验原理
根据相似相溶原理,TEMPO-COOH含有水溶性基团,应具有较好的水溶性,尤其在碱性条件下,其钠盐TEMPO-COONa水溶性更好。基于此,利用两相反应体系可实现邻硝基苯甲醛的选择性氧化合成。如图4所示,原料具有水溶性,TEMPO-COOH和次氯酸钠均在水相,氧化反应在水相中进行;所得产物水溶性差,进入有机相,有效避免了被氧化为酸,从而提高了邻硝基苯甲醛的收率。

图4 TEMPO-COOH催化氧化合成邻硝基苯甲醛(左)及其性状(右)
“照方抓药”式完成实验往往让学生失去了体会有机化学“创造”和“控制”的过程与乐趣。本实验教学中,学生可自主设计和引入变量,比如催化剂结构及用量,反应温度、溶剂、pH等。通过分组进行,比较各变量所导致的差异,并从原理上加以解释,共同体会有机合成方法学和工艺研究的巨大乐趣。
1.4 试剂和仪器设备
综合上述合成方案,实验所需要的主要试剂和仪器如表1和表2所示,其余物品包含:磁子、铁架台、漏斗、玻璃棒、100 mL圆底烧瓶、100 mL锥形瓶、25 mL量筒、100 mL分液漏斗、25 mL恒压滴液漏斗及1 mL注射器等。

表1 所需主要实验试剂

表2 所用主要实验仪器
1.5 合成实验步骤
本实验涉及目标产物邻硝基苯甲醛的合成、反应进度监测、分离与精制以及产物结构表征和纯度分析四个部分。
1.5.1 邻硝基苯甲醛的合成
1) 邻硝基苯甲醛的制备。
依次向100 mL圆底烧瓶中加入邻硝基苄醇(1.53 g,10 mmol),二氯甲烷(10.0 mL)和搅拌子(注:选取磁力足够大的搅拌子),搅拌使固体全部溶解。再依次加入TEMPO-COOH水溶液(1.0 mL,0.01 mmol,0.01 mol·L-1水溶液)和饱和碳酸氢钠溶液(13.0 mL,17 mmol)。将反应瓶放入15 °C水浴中,剧烈搅拌下用恒压滴液漏斗滴加NaClO水溶液(13.0 mL,20 mmol,10%水溶液),约10 min滴加完毕。滴加完毕后,继续在15 °C下反应40 min。
2) 反应进程监测。
停止搅拌,静置分层后取少量下层溶液,稀释后通过薄层色谱(TLC)监测反应进展。以原料和标准产品二氯甲烷溶液作为对照品,用石油醚和乙酸乙酯(V石油醚:V乙酸乙酯= 3 : 1)作为展开剂。展开后在254 nm的紫外灯下观察原料消耗情况和产物是否形成。
3) 产物分离。
反应完全后,将反应液倒入分液漏斗,分出有机层后,水相再用二氯甲烷(10.0 mL × 1)萃取。合并有机相,经无水硫酸钠干燥,过滤入已称重的圆底烧瓶中。滤液在旋转蒸发仪上浓缩得粗品。待恒重后,称重,收率为93%。
4) 产物精制。
粗品溶解在20.0 mL二氯甲烷中,加入10.0 mL饱和亚硫酸氢钠,常温下搅拌30 min,静置后分层(此处可用TLC监测)。分离得到水层,水层在冰浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重。
1.5.2 TEMPO及其衍生物催化活性和萃取回收率比较
参照上述标准实验步骤,可分组进行研究型实验,考察其他变量,如催化剂结构或用量,反应温度、溶剂等对该催化氧化反应的影响。
此处以比较TEMPO及其衍生物催化活性为例(结果见2.2小节)。为了进一步证明TEMPO-COOH的水溶性优势,我们设计了萃取回收率实验。分别取TEMPO、4-oxo-TEMPO、TEMPOL以及TEMPOCOOH各200.0 mg,溶解于50 mL饱和碳酸氢钠溶液中,并用二氯甲烷萃取(50 mL × 3)。合并有机相,无水硫酸钠干燥,过滤浓缩后称重,计算回收率。
1.5.3 结构表征与纯度分析
1) 结构表征。
取5.0 mg左右粗品或精制产物溶解在氘代氯仿中,测定产品核磁共振氢谱(1H NMR),解析数据,并与标准产品比对,确认产物结构。
2) 纯度分析。
取约1.0 mg粗品或精制产物溶解在色谱级正己烷/异丙醇(V正己烷:V异丙醇= 10 : 1)的混合溶剂中,用高效液相色谱仪(HPLC)分析产物纯度,并与标准产品保留时间比对。
2 结果与讨论
2.1 薄层色谱分析和精制后产品性状
如图5所示,在标准催化反应条件下,氧化反应完全,在紫外灯下未见明显副产物。计算得邻硝基苯甲醇Rf= 0.26,邻硝基苯甲醛Rf= 0.39。精制后所得产物为淡黄色粉末。

图5 TLC结果分析(左)和精制后产品性状(右)
2.2 TEMPO及其衍生物催化效果和萃取回收率比较
TEMPO和4-oxo-TEMPO结构类似,无额外亲水性基团,水溶性差,催化活性均较差;TEMPOL与TEMPO-COOH结构类似,含有亲水性基团,其催化氧化产率均在90%以上(图6)。萃取实验结果表明TEMPO-COOH相比TEMPOL更易溶于水,前者同时满足水相中氧化和易于分离的实验设计需求,从而可避免因催化剂残留在产品中所带来的基因毒性问题(图7)。

图6 TEMPO及其衍生物催化能力对比

图7 TEMPO及其衍生物萃取回收率比较
2.3 邻硝基苯甲醛结构表征及纯度分析
1) 邻硝基苯甲醛的结构表征。
对邻硝基苯甲醛分别进行核磁共振氢谱(1H NMR)表征,如图8所示,数据如下。

图8 邻硝基苯甲醛的1H NMR图谱
1H NMR (400 MHz, CDCl3):δ10.43 (s, 1H),8.12 (dd,J= 8.0, 1.6 Hz, 1H),7.96 (d,J= 7.8, 1.8 Hz,1H),7.82–7.74 (m, 2H)。
2) 邻硝基苯甲醛的纯度分析。
HPLC分析确认粗品纯度大于99%。分析条件:色谱柱为Luna 5μm Silica (2) 100 Å (1Å = 0.1 nm),柱温40 °C,流速为1.0 mL·min-1,洗脱液为V正己烷:V异丙醇= 10 : 1,检测波长为254 nm (图9)。

图9 邻硝基苯甲醛粗品(左)和精制产品(右)HPLC对比图
3 结语
本文紧扣邻硝基苯甲醛的合成工艺发展过程,将绿色催化氧化合成该醛的方法开发为有机化学基础实验,丰富了绿色氧化反应在实验教学中的应用。通过实验实践、实验拓展和结果分析,使学生深入理解催化氧化合成邻硝基苯甲醛的意义,熟练掌握其制备方法和实验过程。更为重要的是,该实验教学融入了以“科学问题为目标导向”的探究型实验模式、绿色化学理念和有机合成方法学研究的一般过程,在此教学基础上,学生对科学问题的解决与工艺技术的形成过程有了总体的了解。该新创实验所用试剂环境友好,安全性高,时长约3-4学时,非常适合用于有机化学基础实验教学,采用微课和实验教学相结合的教学方法,可促进学生理论知识学习与有机合成实践之间的有效互动,提高化学类专业人才培养质量。
4 创新性声明
1) 形成以“科学问题为目标导向”的探究型实验教学模式;
2) 采用微课和实验教学相结合的教学方法,并融入有机合成方法学研究的一般过程;
3) 采用物质的量分数0.1% TEMPO-COOH为催化剂,提高了氧化合成邻硝基苯甲醛的选择性。
