光学相干断层成像技术在龋病诊断中的研究进展
2022-07-29苏屹坤朱炳震伍韩雪卢倩倩王景云
苏屹坤,朱炳震,伍韩雪,卢倩倩,王景云
龋病是常见病、多发病,是牙体硬组织在细菌等多种因素作用下发生的慢性进行性破坏的感染性疾病[1]。第四次全国口腔健康流调显示,我国12岁儿童患龋率10年来由28.9%上升至38.5%,呈明显上升趋势[2]。龋病会引发疼痛,咀嚼障碍,引起牙髓、根尖周疾病甚至导致局部或全身感染[1]。对活跃性早期龋及时进行诊断和干预,降低治疗的生物学代价显得尤为重要[1,3-4]。临床检查(视诊和探诊)和影像学检查(根尖X线片和牙合翼片)是临床常规检测和诊断龋病的方法[3,5]。临床检查具有主观性,判断标准不一,影像学检查存在电离辐射的风险,而且对早期龋,尤其是早期窝沟龋的诊断敏感性差[6-7]。能够辅助诊断与治疗、追踪病变发展、无损、无创、敏感性高的龋病量化检查技术是非常有必要的。
光学相干断层成像(optical coherence tomography,OCT)是Huang等于1991年首次提出的一种无创、无辐射的获得生物结构高分辨率图像的技术[8-9]。OCT已广泛应用于眼科[10-11]、皮肤科[12-13]、心血管科[14-15]等疾病诊疗过程。1998年,Colston等[16]首次将OCT技术应用于口腔领域,他们设计的装置可以扫描到3 mm深的牙体硬组织以及1.5 mm深的软组织。同年,Feldchtein等[17]首次尝试将OCT应用于诊断牙体软硬组织病变。随着计算机、电子、图像处理分析等技术快速进步,OCT的成像速度、灵敏度和分辨率得到了迅速发展。OCT对于口腔软硬组织疾病诊断与监测有着良好的前景[6,18-21]。本文就OCT技术在龋病诊断中的研究进展作一综述。
1 OCT分类及其检测原理
1.1 时域OCT
常规OCT属时域OCT(time-domain OCT,TD-OCT),其原理类似于超声检查,但使用光波回波信号而非声波回波,OCT原理是将光波分束照射样本臂和参考臂,样本光检测样品组织,生物组织和参考臂对入射的低相干光的背向散射信号在迈克尔逊干涉仪内发生干涉,由探测器记录生成A-scan(深度)和B-scan(横截面图像),或创建三维(3D)图像以显示内部结构[16,20,22-23]。光源、成像透镜和检测单元的特性会影响OCT成像的深度、分辨率、视野和对比度[23]。更长波长的光源通常可以提供更深的成像深度[23]。高数值孔径成像透镜提供了更好的轴向分辨率和对比度,但景深较浅,视野较小,在口内应用受限于受试者微小运动引起的失焦[23]。大多数口腔OCT使用波长1 300 nm左右工作光源和低数值孔径成像透镜,这种条件下,OCT图像深2 mm,轴向分辨率10 μm,可以实现高分辨率牙釉质和牙本质组织微观结构成像[23]。
1.2 傅里叶域OCT
傅里叶域OCT(Fourier-domain OCT,FD-OCT),可通过将生物组织内部结构的干涉光谱经傅里叶变换获取信息,它分为扫频OCT(swept-source OCT,SS-OCT)和谱域OCT(spectral domain OCT,SD-OCT)。SS-OCT采用窄带高速可调谐激光光源,探测器为简单的二极管,通过快速扫描宽波长范围获取组织内部频谱,在每个波长处顺序测量干涉图案[23-24]。SD-OCT采用超宽带光源、分光计和线性扫描相机实现对干涉谱各分量的轴向深度扫描测量[6,23]。FD-OCT具有高成像速度、高相位稳定性和高信噪比的特点[20,25]。
1.3 功能OCT
OCT还能将干涉信号中的偏振等信息进行功能成像。健康釉质是双折射材料,可改变光在其中传播的偏振状态,传统OCT可能出现双折射条带伪影[23]。偏振敏感OCT(polarization sensitive OCT,PS-OCT)入射光为线性偏振光,分别收集两个正交极化状态,然后将其组合以生成没有条带伪影的图像,从而提供釉质组织的真实结构[23]。交叉极化OCT(cross-polarization OCT,CP-OCT)是在SS-OCT的基础上采用交叉极化模式检测,可以将牙齿表面的反射率降低20~30 dB,从而避免高反射的牙齿表面掩盖下方的牙齿结构,提高信噪比和对比度[20,26-27]。
2 OCT龋病检测原理
2.1 健康牙体组织OCT图像
牙冠硬组织由牙釉质组成外部,内部与牙本质相连,连接界面称为釉牙本质界(enamel-dentinal junction,EDJ)。健康釉质在近红外光波段1 310 nm左右的波长范围内几近透明,OCT检测轴向成像深度明显提高,可以捕获完整的釉质厚度和1~2 mm深的牙本质[28]。EDJ呈现为一条暗带,在OCT图像上容易区分牙釉质和牙本质(图1)[25,28-29]。

图1 SS-OCT对前牙进行实时横断面成像 [28]Fig.1 Real-time cross-sectional imaging was performed for the anterior tooth using SS-OCT [28]
2.2 龋病OCT图像
OCT检测中,龋病和正常组织的区别在于脱矿组织微孔隙增加引起的背向散射增加和脱矿组织对入射光的去极化[20,28]。硬组织脱矿引起牙釉质和牙本质孔隙度增大,微孔中微界面的局部反射差异引起反射增高,增加的背向散射在灰色图像中表现为白色亮区[28-29]。龋病侵及的EDJ可出现反射增强的亮线,表明该处牙釉质和牙本质受病变累及导致结构裂解,出现微间隙(图2)[29-30]。近红外光波段1 310 nm波长处,脱矿釉质光散射强度与健康釉质相差10~20倍,对比度高,因此OCT可以在脱矿早期区分病变组织[20]。
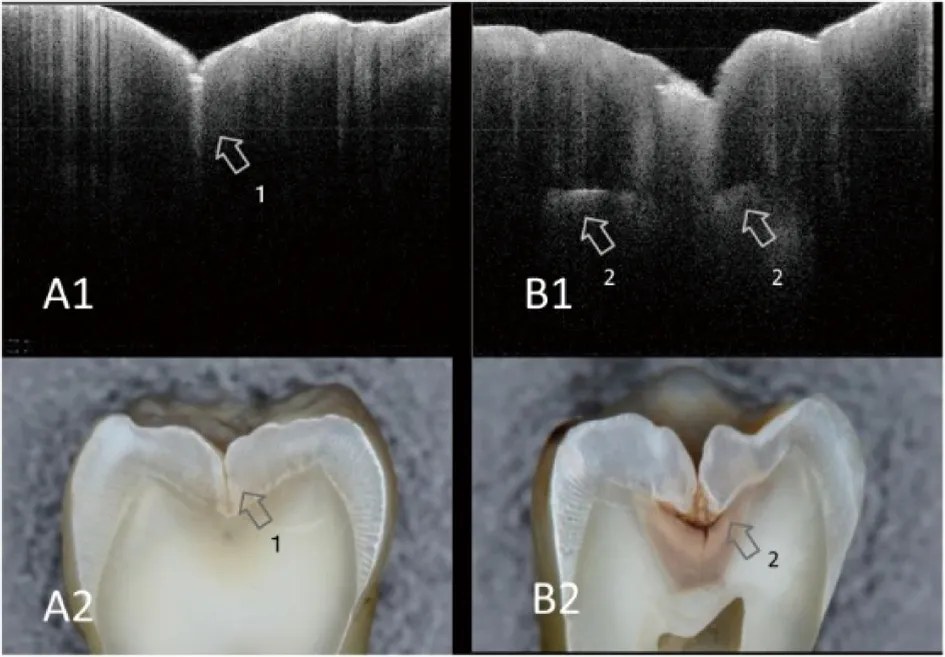
窝沟处的釉质脱矿表现为釉质深度内亮度增加(箭头1),沿着EDJ扩展的病变成像为一条亮线(箭头2)
2.3 OCT龋病检测的量化分析
丁江峰等[31]使用FD-OCT对牙本质龋进行检测,通过改良canny边缘提取法,计算测量位点的折射系数,高分辨率显微CT (micro-CT)检测矿化密度的改变,认为龋影响牙本质矿化密度测量值与折射系数间存在显著正相关性(r=0.78)。牙体组织光学特性改变和脱矿的相关性有可能定性和定量检测龋病范围和严重程度[31-32]。很多学者试图开发数学算法自动快速准确地测出龋病边缘[33-34],Chan等[33]使用CP-OCT获得口内平滑面釉质的交叉极化图像,通过整合正交轴或交叉极化图像的反射率来量化脱矿的严重程度,通过识别每个A-scan低于半峰宽阈值的第一个像素来将CP-OCT图像转变为病变深度。近年来,还有学者将深度学习应用在OCT图像分析领域,将卷积神经网络和OCT成像相结合,提取不同组织密度的牙齿OCT图像的特征,以更准确地识别病变组织[35-36]。
3 OCT应用于龋病诊断
3.1 平滑面龋
龋齿通常始于牙釉质表面及其下方,牙齿的晶体矿物结构在细菌代谢产生的有机酸作用下脱矿[1]。Tsai等[37]在体外通过37%磷酸酸蚀离体牙120 s模拟早期釉质脱矿, SD-OCT检测后,计算其平均散射系数由4.60 mm-1增加到了8.46 mm-1(P<0.001)。Park等[29]的体内试验中使用SS-OCT检测,将通过国际龋齿检测和评估系统(ICDAS)判断为完好釉质的50%检测位点诊断为早期龋,体外评估OCT和组织学检查对人离体牙平滑面龋的诊断结果,两种方法之间观察到中度显著一致性(κ=0.54),OCT可以作为平滑面龋视诊检查的补充,帮助判断病变程度。Vaswani等[38]在体外比较了PS-OCT和X线片检测龋病的敏感性和特异性, OCT的敏感性和特异性分别为0.90和0.69,高于X线的0.40和0.63,与组织学检查相比相关系数为0.68,呈相关度较好的正相关,AUC为0.80(95%CI=0.704~0.870),PS-OCT检查从脱矿和再矿化的角度评估早期龋损,辨别病变活动性,对决定是否采取再矿化治疗十分有意义[38]。
3.2 窝沟龋
Shimada等[28]使用离体牙进行窝沟龋的诊断试验,SS-OCT敏感性(0.98)与特异性(0.75)高于视诊(0.80、0.69),一些视诊看来刚有脱矿的病变实际上已经接近EDJ,而且牙齿单纯着色几乎不吸收近红外光[6],所以 OCT检查受窝沟着色影响小,对龋病的检测干扰小、准确性高。Luong等[39]的体外研究显示和X线检测相比(0.87),SS-OCT具有更好的敏感性(0.95),和较高的Az值, OCT在检查窝沟龋有良好性能。Zain等[40]评估了SS-OCT和偏振光显微镜诊断人前磨牙早期窝沟龋的一致性,OCT敏感性为0.98,特异性0.95,对于窝沟入口以上(宽度>200 μm),OCT进行病变深度测量与偏振光显微镜一致,但在窝沟入口以下(宽度<200 μm),OCT病变轴向深度测量平均值比偏振光显微镜小0.57 mm,并且与病变大小呈线性关系,这可能是由于复杂的窝沟结构增加了反射,并有可能导致对病变严重程度的估计不足。Simon等[41]使用了CP-OCT在体内对窝沟龋进行检测,认为与X线片相比,敏感度提高了50%以上。功能性OCT能否在深窝沟处获得准确的病变深度仍需进一步研究。
3.3 邻面龋
Erdelyi等[42]将SS-OCT和X线检查牙体组织效能进行对比,并使用Romexis Viewer图像软件进行评估分析,X线片上仅能观察到的第三磨牙近中邻面龋,在OCT中可以量化测量龋损深度,显示出优越的分辨率和对比度。Golde等[43]使用PS-OCT结合DOPU算法通过脱矿组织的去极化对比度来检测邻面龋,提高了对比度,能够更好界定龋病边界。Ei等[44]使用SS-OCT评估拔除前磨牙的邻面早期龋和微裂纹,认为牙釉质微裂纹的发生率与脱矿有关,这种微裂纹可能是邻面磨损和龋病进展的诱发因素。Xing等[26]在体外使用离体牙模拟牙列,使用CP-OCT从咬合面及水平面检测牙齿邻面龋,其中咬合面入路敏感性0.81,特异性1.00,Az值0.90,与水平面相比是更好的检测分析平面。Shimada等[30]使用SS-OCT从咬合面检测牙本质龋的敏感性(0.85)、特异性(0.97)高于X线(0.45、0.91)。AUC(0.94)与组织学检查的一致性(0.73)也高于X线(0.75、0.38)。OCT的诊断准确性高于X线片,为在三维图像上检测邻面龋提供了机会,从而克服传统二维方法的局限性。
3.4 继发龋
复合树脂粘接修复是最常用的龋病修复方式,牙体与复合材料之间密合性丧失,将产生微间隙,产生继发龋乃至修复失败[45]。复合材料散射OCT信号,在SS-OCT图像上呈白色。由于缺陷边界处的光折射,间隙的形成导致后向散射信号的信号强度分布出现峰值,在灰度图像中显示为明亮的簇,OCT可以检测出粘接间隙,监测间隙进展和定量界面间隙[46-47]。而修复体下方的牙本质呈黑色,可以明显区分开来[48]。Schneider等[6]通过口内SD-OCT成像可以看到复合树脂中存在气泡、增量线和各种不规则精细结构,以及边缘约7 μm的粘接剂分布不均匀,这些危险因素会增加继发龋的发生概率。Zhou等[46]在体外使用SS-OCT可以检测到树脂-牙本质粘接界面早期降解,在OCT图像中脱粘间隙呈亮簇状,脱矿的牙本质表现为刃状暗区和明亮的散在线,OCT结果和激光共聚焦显微镜结果显著相关(r=0.85)[46]。
4 展 望
OCT图像分辨率和辐射安全性明显优于X线片,能用于孕妇及幼儿[41],是一种有较高敏感性、特异性的龋病检测方法[3,41],可作为临床辅助工具支持常规检测手段和鉴别可疑病例。龋病检测评估系统与OCT相结合,有望提高龋病检测和评估的准确性和可重复性,从而有效和更精确地调整治疗策略[29]。治疗引导减少并发症和操作时间,监测治疗结果及病变发展,椅旁实时成像有利于医患之间的沟通。OCT探测深度、视场、图像信噪比和可靠性的提高,以及手持式口腔OCT设备开发和龋病定量检测算法将是今后研发的重点[26,47]。
