锂离子电池用V2O5正极材料研究进展
2022-07-25李鑫悦张晓民郎笑石蔡克迪
李鑫悦,张晓民,郎笑石,蔡克迪*,
(1.渤海大学 化学与材料工程学院,辽宁 锦州121013;2.辽宁省超级电容器工程技术研究中心,辽宁 锦州121013)
0 引言
锂离子电池(LIBs)因其循环寿命长、能量密度高和环境友好等特点已广泛应用于电动汽车(EV)、便携式电子设备及其他大型储能领域中.然而,目前商用锂离子电池的能量密度还不能满足能源汽车等领域对长续航能力的要求,其性能远落后于迅速发展的电子器件和电动汽车需求的提高[1-4].因此,为了更好的适应新技术的开发,下一代LIBs应具备高能量密度、出色的倍率性能、低成本和更好的安全性能等特点.
从材料的角度来看,电极材料的固有性能决定了电池的电化学储能能力,在整个电池系统中起着至关重要的作用.正负极材料的Li+存储能力和工作电压决定了锂离子电池的能量密度.研究发现,正极材料的低比容量已成为许多应用需求的瓶颈[5-7],因此亟需开发高性能的新型正极材料以促进锂离子电池技术的发展[8].与传统的单电子氧化还原体系相比,多个Li+的自由嵌入和脱嵌能够实现更高的比容量,从而提高能量密度,因此多电子反应电极是提高电池比容量和能量密度的有效途径.因钒具有丰富的价态(如V5+、V4+、V3+和V2+),所以钒基电极是一种能够进行多电子反应的重要电极.其中,五氧化二钒(V2O5)是具有层状结构的典型插层化合物,与常用的传统商业正极材料如LiCoO2(140 mAh/g)和LiFePO4(170 mAh/g)相比,V2O5具有294 mAh/g的高理论容量,可实现多个Li+的嵌入和脱嵌,其资源丰富且成本低,同时还具有特殊的物理和化学性质,这使其成为用于下一代高能LIBs的正极材料[9].然而,V2O5固有的缺点阻碍了其大规模的实际应用,包括较低的Li+扩散系数和电导率,以及由Li+嵌入/脱嵌过程中导致不可逆的结构变化等.
近年来,研究者为优化V2O5性能已开展了大量的研究工作,提出了许多方法对V2O5进行改性,包括阳离子掺杂、形貌控制和复合导电材料等方法.本文综述了V2O5的晶体结构及近期V2O5正极材料的研究进展.
1 V2O5的晶体结构
V2O5以其独特的晶体结构在锂离子电池中发挥着重要作用,V2O5是一种具有典型层状结构的插层化合物,其独特的层状排列结构使V2O5成为易于将Li+嵌入/脱出到其层间空间的良好主体[10].各层间通过较弱的范德华力连接在一起,且通常在Pmmn空间群的正交结构中结晶,晶格矢量a、b和c的长度分别为a=1.151 nm、b=0.356 nm和c=0.437 nm.图1[11]是正交晶系V2O5的晶体结构示意图,它是由共享棱角的层状方形棱锥组成.一个V2O5正交晶胞由双层构成,并且这种双层结构是由一系列具有扭曲顶点的[VO5]金字塔组成,这些金字塔共享棱角而形成锯齿形双链且沿(100)方向相互交联.在这种特殊结构中,钒原子周围有三种类型的氧中心,分别是末端或顶端单独配位的钒基氧原子O(1)、通过[VO5]金字塔共享角连接两个相邻钒原子的桥连氧原子O(2)及通过共享边连接三个钒原子的三配位链式氧原子O(3).O(1)与V仅形成一个键且键长较短,O(1)—V键长约为1.54 Å;O(2)与V形成两个V—O(2)—V键,相应的键长度约为1.77 Å;而O(3)形成三个键,其中两个O(3)—V键长约为 1.88 Å,另一个O(3)—V键长度约为2.02 Å.此外,各层金字塔顶端的O(1)与相邻层中的钒原子之间存在微弱的相互作用,形成了一个微弱的V—O范德华键,键长约为2.81 Å,这种垂直于c轴的层间相互作用起到了保持V2O5的层状结构的作用[12].由于相邻层之间的范德华力较弱,当锂离子进入到各层间时,V2O5会根据锂离子嵌入的程度伴随着一系列的相变(α、ε、δ、γ和ω相),进而导致晶体结构的改变,过量的离子嵌入会导致结构不可逆的转变和电化学性能的严重退化[13-15].为改善V2O5的结构稳定性和电化学性能,研究人员进行了深入研究.

图1 正交晶系V2O5的晶体结构
2 V2O5的改性研究
2.1 阳离子掺杂
阳离子掺杂是提高电极材料固有导电性及改善结构稳定性的有效途径,在V2O5晶格中引入阳离子会起到调节主体材料电子结构和离子占有率的作用,从而改善V2O5的电化学性能,包括(1)形成低价态V4+,提高材料导电性;(2)缓解Li+插层过程中V2O5的体积变化,提高材料稳定性;(3)改变V2O5形貌和晶粒尺寸等[16-18].
Li等[19]采用脉冲激光沉积(PLD)技术和退火工艺制备了V2O5-Au纳米复合薄膜,研究发现约 10 nm大小的Au纳米颗粒均匀地分布在165.3 nm的α-V2O5纳米片致密薄膜上,通过引入Au纳米粒子有效提高了材料的导电性和电池的容量.经计算得出纯V2O5和V2O5-Au纳米复合薄膜电极的Rct值分别为267.6 Ω和98.03 Ω.在0.5C下进行100次循环后分别增加了约536.8 Ω和176.27 Ω.这表明在V2O5薄膜中引入Au纳米颗粒可有效增强电荷转移过程,从而改善电池的循环和倍率性能.
在材料中引入氧空位是提高导电性的一种有价值的方法.阳离子掺杂或还原气体的热处理可有效引入氧空位.例如,Zhang团队[20]合成了一种Cu掺杂的棒状V2O5,在V2O5晶格中掺杂Cu引入了大量氧空位,使电子和离子在充放电过程中实现快速迁移.并且增大了晶胞的体积以缓解循环过程中V2O5的体积变化.除此之外,Hu等[21]进一步研究发现不同质量分数Cu2+的掺杂会影响V2O5·nH2O薄膜的形貌、钒的价态及其电化学性能.结果表明,当Cu2+的质量分数为1wt%时,V2O5·nH2O薄膜电极呈现独特的网状多孔纳米结构,有助于加快Li+的转移速率.其在250 mA/g下显示出344 mAh/g的高放电比容量,与纯V2O5·nH2O薄膜相比,掺杂材料表现出更优异的电化学可逆性.此外,Co掺杂已在改善 LiMnO2和LiNiO2等锂基材料性能中显示出明显优势.因此,Ji等[22]首次报道了通过水热法在Ti箔上成功制备了Co掺杂的V2O5纳米线阵列,V2O5纳米线可在Ti箔上分布均匀.与V2O5或Co3O4纳米线相比,Co掺杂V2O5纳米线具有更高的电化学储锂容量,在500 mA/g高电流密度下可达282.82 mAh/g的高可逆容量.人们发现,采用双离子掺杂策略能够更有效地改善电极材料性能.例如,Zhang等[23]制备Al/Mn共掺杂的V2O5·4VO2,并根据第一性原理计算得到Al/Mn-V2O5·4VO2晶体结构,如图2所示.Al3+和Mn2+插入到了V2O5·4VO2的层间位置,与V2O5·4VO2中的层间氧形成[AlO6]和[MnO6]八面体以稳定晶体结构并增加单胞的体积,此外,Al/Mn共掺杂会引入氧空位,为Li+的插入提供了更开放的结构.因此,Al/Mn共掺杂的V2O5·4VO2电极在0.1 A/g下表现出322.5 mAh/g的高初始容量以及50次循环后91.7%的高容量保持率.
稀土金属离子具有亲氧性和较大的半径,因此通常被用作掺杂剂以增加材料层间间距和导电性.Chen等[24]结合溶剂热法和煅烧工艺成功制备了Ce掺杂的V2O5微球.Ce0.1V2O5电极材料在5C下进行200次循环后的容量保持率约为88.93%,具备良好的结构可逆性和高容量保持性.此外,Hu等[25]制备了La掺杂V2O5·nH2O@OAB这种具有多层网络结构的无粘结剂薄膜正极.具有较大半径的稀土金属离子La3+和亲水碳氧化乙炔黑OAB发挥良好的协同优化作用,从而有效提高了V2O5·nH2O的电导率及循环和倍率性能.图3的实验过程为采用新型水热辅助溶胶-凝胶复合方法在ITO涂层玻璃基板上原位制备了一种自掺杂V4+-V2O5纳米薄膜[26].该研究发现不同退火条件对V2O5薄膜性能有所影响,V2O5晶格中引入氧空位的浓度由退火温度控制.与传统溶胶-凝胶方法制备的V2O5薄膜相比(30.28 mC/cm2),这种新型复合方法制备的薄膜其离子存储容量大大提高,其中300 ℃-V2O5薄膜的离子存储初始值高达112.25 mC/cm2,2 000次循环后仅下降2.4%.纳米薄膜优异的循环性能归因于梯度氧空位以及薄膜与基板之间良好结合力的协同效应.因此,通过一种或多种阳离子掺杂可获得富含丰富氧空位且更加开放的晶体结构,有利于提高V2O5的电化学性能.

图2 V2O5·4VO2和Al/Mn-V2O5·4VO2晶体结构
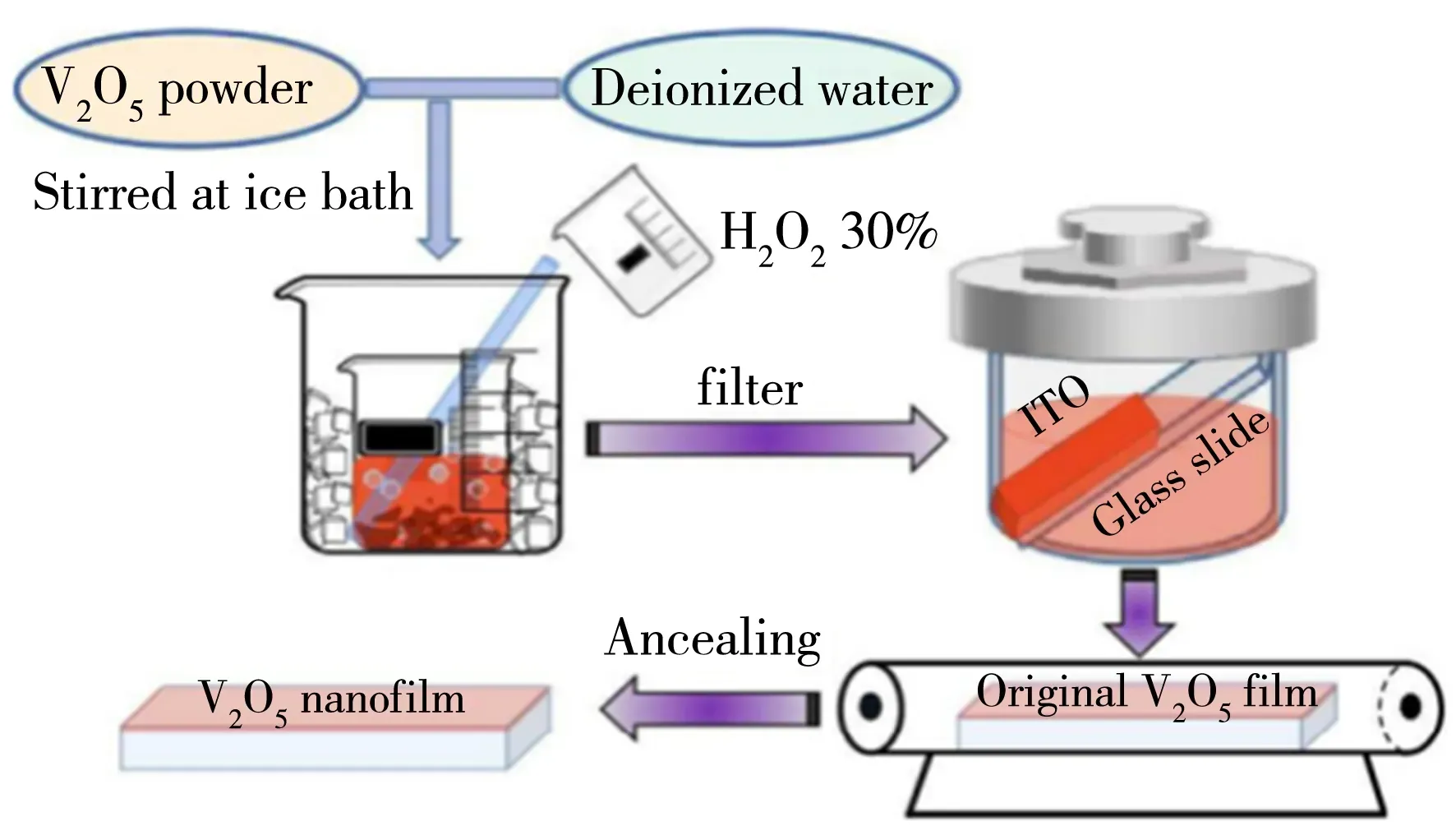
图3 制备V2O5薄膜的实验过程
2.2 形貌控制
通过设计电极材料微观形貌可增强与电解液的接触并降低极化电阻,从而改善材料电化学性能[27].为了提高V2O5的电化学性能,已合成各种具有不同形貌的V2O5材料,包括一维纳米线、二维纳米片以及三维空心纳米球等.
Huang等[28]制备了一种细长板状形态且具有斜方晶相的V2O5纳米晶体,该方法涉及硫酸钒在碱性溶液中的水解以及V2O5在含氢气氛下的退火过程,研究发现在300~400 ℃下进行退火可在不改变V2O5结构和形态的基础上产生大量氧空位.与原始V2O5纳米晶体相比,含氧空位的样品表现出增强的电化学性能,初始放电容量高达284 mAh/g,即使在10C下仍可达153 mAh/g,且在0.2C下循环50次后容量可保持在200 mAh/g左右.采用水热法和热处理过程可获得超薄分层V2O5纳米片,该材料的结构稳定性能优异,经高倍率循环后此V2O5纳米片在100 mA/g下的放电容量仍高达280 mAh/g[29].据报道,具有多孔结构的活性材料更有助于电解液渗透,从而显著提高锂储存及倍率性能.Dong团队[30]合成了两种具有巢状和球形的V2O5多孔微观结构,其独特的结构优势扩大了电化学反应的实际面积,具有更多的Li+存储活性中心,同时可起到缓冲应力和应变的作用并抑制团聚.类似的,具有分层多孔结构的巢状V2O5材料由平均长度约为100 nm的相互连接的纳米片组成.在100 mA/g下可提供330 mAh/g的初始放电比容量,经50个循环后仍可保持240 mAh/g的稳定放电容量[31].
电化学阳极氧化法可通过改变电压和时间等参数为制备各种纳米结构的V2O5提供一种简便且廉价的合成途径.Lee等[32]在钒箔上通过电化学阳极氧化和热退火过程制备了相位控制的多孔V2O5纳米材料,形成沿(001)面优先生长的V2O5薄膜,(001)面具有较低的活化能可增强Li+扩散和电子传导.其中400 ℃下退火得到的V2O5在快速充放电过程(1.5C)中显示出170.1 mAh/g的高放电容量和100次循环后91.4%的高容量保持率,显示出良好循环稳定性的同时可保持稳定的结构.通常,具有复杂中空内部的3D纳米结构可以缓冲体积膨胀,从而起到改善电极材料循环稳定性的作用[33-34].Ma等[35]制备的由纳米板组成的V2O5蛋黄-壳亚微球具有高可逆容量和大电流循环稳定性能.其在100 mA/g下可获得269.4 mAh/g的高可逆容量,在大电流1 200 mA/g下经80次循环后容量保持率可达78.31%.图4[36]为内部可调钒氧化物的形成过程示意图,该材料的优异电化学性能归因于具有多重双壁壳的V2O5中空微球与电解液的较大接触面积确保了电解液的有效渗透.此外,中空结构还能够更好地保持电极材料的结构完整性.

图4 内部可调钒氧化物的形成过程示意图
经研究发现,表面活性剂可通过发挥软模板作用来控制材料微观结构的特定形态.据此,Wu等[37]以聚氧乙烯-20-十六烷基醚作为表面活性剂,制备了一种分层剑麻状V2O5,该结构由具有(001)面取向生长和富氧空位的一维纳米带组成.V2O5中具有最低表面能和最稳定的(001)晶面可减少电极与电解质界面间的副反应.其在1C下循环400次后的容量保持率高达74.8%,容量衰减率仅为每周期0.06%.Hu等[38]探究了表面活性剂对V2O5形貌的控制,其中以十六烷基三甲基溴化铵(CTAB)作为表面活性剂得到的V2O5材料呈现出3D涡轮状微花和低维纳米颗粒组合的独特形态.这种独特的3D涡轮状分层结构是由超薄纳米片堆积形成,纳米片相互连接最终形成3D微米花状结构.此外,这些超薄纳米片中存在粒径约为300 nm的低维纳米颗粒.这种独特的结构有利于活性材料与电解质的有效接触并产生大量高活性位点,提供更高效的传输路径并加速反应动力学,在200 μA/cm2下获得237 mAh/g的高可逆比容量.由此可见,通过对V2O5的形貌控制不仅可保持其高容量和高倍率性能等优势,还在一定程度上提高了V2O5的结构稳定性.
2.3 复合导电材料
电导率和比容量是电极材料的关键性能参数,复合导电碳材料或聚合物的改性方法是提高电子导电性和缓解体积膨胀以及增强循环稳定性的最有效手段[39].
利用静电纺丝法和氧化铁催化作用相结合制备的石墨化碳纳米纤维(G-CNFs)网络的电导率比无定形碳纳米纤维增加了5 × 104倍,再利用水热法在G-CNFs上生长V2O5纳米片,以构建一种柔性的独立式复合电极V2O5@G-CNFs[40].该复合电极在0.1C时具有290 mAh/g的高比容量,在5C下进行700次循环后,容量保持率仍高达85.7%.研究发现,构建由低维纳米块组成的3D微/纳米结构是解决循环过程中材料团聚和粉化等问题的一种有前景的策略.Zhu团队[41]通过将三聚氰胺泡沫(MF)碳化形成碳泡沫(CF),以CF独特的3D结构作为骨架,通过一步水热法在CF上生长1D V2O5纳米针,得到V2O5@CF这种新颖的1D@3D纳米复合材料.该材料在经过5 000次连续充放电循环后可保持74.5%的初始容量,V2O5@CF材料具有优异电化学性能的原因是V2O5和碳纤维之间特殊的协同效应,3D碳纤维有助于V2O5纳米针阵列在其表面均匀、密集、垂直地生长,有效地防止了纳米针的团聚.Liu等[42]以葡萄糖为碳源成功合成了3D海绵状分层多孔V2O5@C微/纳米结构,它由堆叠组装的纳米片构成.如图5所示,V2O5@C和V2O5纳米带的放电比容量分别为232 mAh/g和190 mAh/g,经50次循环后,V2O5@C容量保持率比V2O5纳米带高18%,且在不同倍率下可提供更高的容量.此外,V2O5@C电极材料具有重叠良好的充放电曲线,符合其更高的可逆性和更好的容量保持性.V2O5@C复合材料丰富的介/微孔结构和导电碳框架能够起到缓冲锂化过程中大体积变化所产生的应力作用,确保整个微/纳米结构的坚固,有利于实现更好的电化学性能.

图5 V2O5@C和V2O5纳米带的电化学测量(a)100 mA/g电流密度下的循环性能比较;(b)V2O5@C在50 mA/g下的充放电曲线;(c)倍率性能比较;(d)锂化过程中体积变化示意图
结合阳离子掺杂和复合导电材料两种改性方法可获得性能更优异的电极材料.例如,碳包覆的Mn掺杂V2O5准球体(Mn0.1V2O5@C)是由均匀嵌入到多孔碳基质中的Mn0.1V2O5纳米棒构成,其多孔结构有助于形成3D传导网络[43].由于Mn掺杂和碳包覆,以5C倍率循环500次后仍可保留94%的初始容量.研究发现,掺杂金属离子Cu可以有效提高V2O5正极材料的储锂容量,但仍存在长期循环稳定性差等问题[20].因此,Zhang等[44]进一步将高导电性石墨烯(rGO)包裹在Cu-V2O5表面,制备得到的rGO/Cu-V2O5复合材料可在保持高储锂容量的同时,显示出显著增强的长期循环稳定性,rGO/Cu-V2O5复合材料在1C下循环200次后仍可保持初始容量的82.5%,比未复合的Cu-V2O5材料提高了23.5%.此外,Cu-V2O5和rGO/Cu-V2O5的电荷转移电阻(Rct)分别为93.6 Ω和57.9 Ω. rGO/Cu-V2O5具有较小阻值的原因是高导电性rGO的复合提高了整体材料的电导率,有利于液-固界面处的电子和离子传输.
聚3,4-乙烯二氧噻吩(PEDOT)是一种共轭高导电聚合物,在V2O5表面上均匀涂覆超薄的PEDOT可得到V2O5/PEDOT核壳纳米带,合成过程如图6[45]所示.这种核壳纳米带可有效地促进电子传输和Li+扩散并保持结构稳定性,避免V2O5的聚集并抑制粉化.因此与纯V2O5纳米带相比,V2O5/PEDOT核壳纳米带表现出更高的倍率性能,即使在10C下进行500次循环后,容量也可达到105 mAh/g.
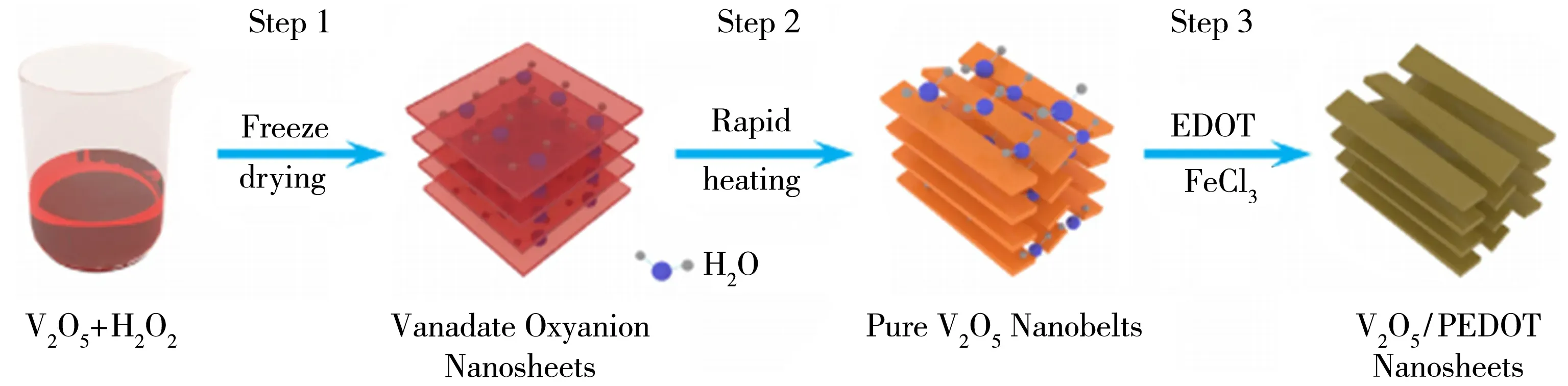
图6 V2O5/PEDOT核壳纳米带合成示意图
近年来,由于天然植物的多孔特性,人们已利用多种植物制备成低成本的多孔碳载体.例如,Tan等[46]通过高温碳化工艺和水热处理方法在天然微孔芦苇炭(PRC)表面上成功合成了类似杨桃状的V2O5纳米花阵列,合成过程如图7所示.V2O5纳米花可均匀分散并固定在大面积的光滑碳壁上,基于这种新颖的复合结构,其在0.2C下的初始放电容量高达285 mAh/g,接近于两个Li+插层的V2O5理论容量,即使在1.0C下进行500次循环后仍可保持在180 mAh/g左右,保留初始容量的87.5%.
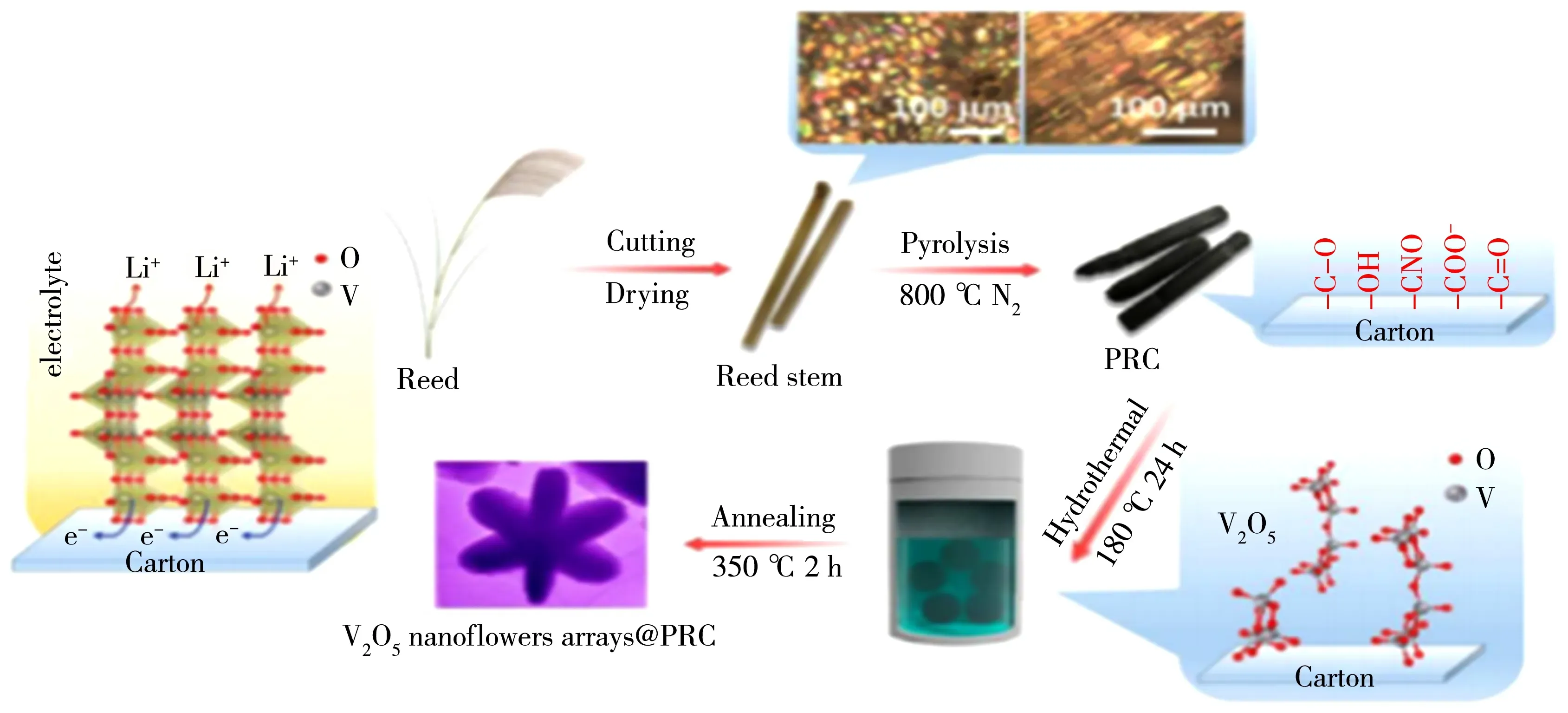
图7 V2O5@PRC复合正极材料合成工艺示意图
V2O5在电解液中的溶解严重影响了其循环稳定性,在V2O5表面包覆疏水性和高导电性的聚吡咯(PPy)层是一种有效的解决策略.因此,采用溶剂热法结合气相沉积法合成了聚吡咯(PPy)包覆具有核壳结构的V2O5纳米球[47].这种核壳结构的V2O5@PPy纳米球为Li+插层过程导致的活性材料体积变化提供了足够的缓冲区域,且介孔壳层有效地促进了电解液的渗透.此外,导电聚合物层和氧空位可提供高导电性以加快电荷转移动力学,并对钒氧化物的溶解起到抑制作用.大量研究表明,通过将碳纳米管(CNT)与纳米颗粒结合可获得用作电化学储能装置的高性能复合材料.Neto等[48]制备了V2O5·nH2O/CSCNT复合材料,首先将杯状堆积的碳纳米管(CSCNT)直接生长在碳纤维毡(CF)表面,然后将V2O5·nH2O电沉积在CF/CSCNT复合材料上.在1.5 V和4.2 V之间,负载34wt%的V2O5·nH2O可在0.5 A/g下提供633 mAh/g的比容量,进行300次充放电循环后具有较低的衰减容量.可见,通过复合导电材料可获得性能更优异的电极材料.
3 结论
V2O5是一种具有特殊晶体结构和电化学性能的新型正极材料,因其综合性能优良已成为正极材研究领域的热点.但其存在低电导率和扩散系数等固有问题限制了V2O5的大规模应用.本文总结了近年来国内外对应用于锂离子电池的V2O5正极材料的研究进展,通过阳离子掺杂、形貌控制和复合导电材料的改性方法使V2O5材料发挥出更好的性能.然而,未来的研究需关注不同改性方法之间的结合应用,同时还需关注V2O5的形成机理和晶体生长规律以及结构演变过程,进一步拓展V2O5在锂离子电池等储能领域的开发和应用.
