柴胡疏肝散精简方对慢性疼痛抑郁共病大鼠中缝核P2X7受体、Caspase-1及IL-1β表达的影响
2022-07-17许丽娥高雪松王安娜杜仪王永志赵静洁
许丽娥,高雪松,王安娜,杜仪,王永志,赵静洁,2
1.首都医科大学附属北京友谊医院,北京 100050;2.首都医科大学中西医结合学系,北京 100050
研究显示,慢性疼痛患者伴发重度抑郁的发生率约为52%,抑郁症患者伴发疼痛的发生率约为65%。抑郁症是一种以情绪低落和兴趣丧失为特征的慢性精神疾病,具有高患病率、高复发率及自杀倾向。临床上抑郁症患者除情绪症状外,还会出现不同程度和表现的躯体疼痛。疼痛和抑郁常共同发病,并有累加效应。因此,疼痛与抑郁共病受到越来越多的关注。疼痛抑郁共病属中医学“郁证”范畴,其病机为肝气郁滞,气机不畅,不通则痛,治疗以疏肝解郁、行气止痛为主,临床多用柴胡疏肝散加减治疗。
抑郁症发病机制至今尚未阐明,炎症假说近年备受关注。有学者认为,抑郁症是神经免疫炎症疾病,炎症介质诱导神经源性炎症反应,进而使外周感觉神经敏感性增强,传递痛刺激的感受器过度敏化,导致痛觉过敏。P2X7受体在中枢神经系统神经元及星型胶质细胞中高表达,其激活后可活化半胱氨酸天冬氨酸蛋白酶(Caspase)-1,进而促进白细胞介素(IL)-1β等促炎因子释放,在炎症反应及疼痛中发挥重要作用。既往研究表明,柴胡疏肝散有较好的抗炎效果,但其能否通过下调P2X7 受体进而调节Caspase-1/IL-1β信号通路发挥作用尚不清楚。本研究采用利血平致慢性疼痛抑郁共病大鼠模型,观察柴胡疏肝散精简方对P2X7受体及Caspase-1/IL-1β信号通路的调节作用,揭示其抗抑郁止痛的部分机制。
1 材料与方法
1.1 动物
SPF级健康雄性SD大鼠40只,体质量180~220 g,购于北京维通利华实验动物技术有限公司,动物生产许可证号SCXK(京)2014-0004,饲养于北京友谊医院实验动物中心,动物使用许可证号SYXK(京)2012-0023,温度(21±1)℃,湿度30%~40%,12 h昼夜节律,自由摄食饮水。
1.2 药物
柴胡疏肝散精简方(柴胡9 g,白芍15 g,枳壳9 g,香附9 g),免煎颗粒由北京康仁堂药业有限公司提供,用蒸馏水将免煎颗粒溶解,配制成浓度为1.6 g/mL混悬液。盐酸氟西汀分散片,苏州礼来制药有限公司,批号4145A,用蒸馏水配制成0.4 mg/mL溶液。利血平注射液,天津金耀药业有限公司,批号2020905,用蒸馏水配制成0.1 g/L溶液。
1.3 主要试剂与仪器
超纯RNA提取试剂、HiFi-MMLV cDNA第一链合成试剂盒、UltraSYBR Mixture(With ROX)、DNase1、5×RNA Loading Buffer(北京康为世纪生物科技有限公司,货号分别为CW0581、CW0744、CW0956、CW2090、CW0611A),总蛋白提取试剂盒(上海贝博生物科技有限公司,货号BB-3101),BCA蛋白浓度测定试剂盒(北京索莱宝科技有限公司,货号PC0020),IL-6、肿瘤坏死因子-α(TNF-α)抗体及IL-6、TNF-α ELISA试剂盒(英国Abcam公司,货号分别为ab233706、ab183218、ab234570、ab236712),β-actin抗体、辣根过氧化物酶标记羊抗兔二抗(美国Immunoway公司,货号分别为B1501、B0201)。分光光度计(美国赛默飞世尔科技公司,型号NANODROP 2000),荧光定量PCR仪(杭州博日科技股份有限公司,型号Line Gene 9600 Plus),冰冻切片机(德国Leica公司,型号CM1950),超速低温离心机(德国Sigma公司,型号Sigma-2K15),高通量组织研磨器(宁波新芝生物科技股份有限公司,型号SCIENTZ-48),电泳仪(北京市六一仪器厂,型号DYY-7C),涡旋震荡仪(上海其林贝尔仪器制造有限公司,型号VORTEX-6),转膜仪(美国Bio-Rad 公司,型号170-3940),智能热板仪(北京众实迪创科技发展有限责任公司,型号YLS-6B)。
1.4 分组、造模及给药
采用随机数字表法将40只大鼠随机分为空白组、模型组、氟西汀组和柴胡疏肝散精简方组(精简方组),每组10只,实验前适应性喂养1周。除空白组外,其余各组按0.3 mg/kg腹腔注射利血平制备慢性疼痛抑郁共病大鼠模型,空白组腹腔注射等量蒸馏水,每日1次,连续14 d。造模同时,按照成人与大鼠体表面积换算给药剂量,氟西汀组按2 mg/kg灌胃氟西汀溶液,精简方组按8 g/kg灌胃柴胡疏肝散精简方混悬液,灌胃体积5 mL/kg,空白组及模型组灌胃等量蒸馏水。
1.5 大鼠体质量检测
分别测量大鼠给药前后(实验第1日及第14日)体质量,计算体质量增量。
1.6 强迫游泳实验
给药结束后,将大鼠逐只放入高60 cm、直径30 cm透明玻璃桶内(水深40 cm、水温23~27 ℃),用摄像机记录大鼠10 min的游泳录像,由2位实验人员采用盲法观看游泳录像5 min(第3~8 min),计录大鼠强迫游泳不动时间,以四肢不动、漂浮于水面、仅头部露出水面呼吸为大鼠不动状态。
1.7 旷场实验
给药结束后,将大鼠置于100 cm×100 cm×40 cm的四面涂黑旷场中,利用软件将旷场分为4×4方格,摄像头记录大鼠行动轨迹,测定3 min内大鼠运动总距离及穿格次数。
1.8 热缩足阈值测定
给药结束后,应用智能热板仪检测大鼠热痛敏感阈值,热板仪温度设定为(55±1)℃,将大鼠右后足底置于热板仪上,以大鼠明显缩足回避为阳性反应,记录大鼠缩足时间,同法测定大鼠左后足缩足时间,以左右两侧平均值作为该大鼠热缩足阈值。
1.9 取材
1%戊巴比妥腹腔注射麻醉大鼠,快速断头,于冰上颈动、静脉混合取血,4 ℃静置4 h,3 000 r/min离心15 min,吸取血清,置于-80 ℃冰箱保存备用。冰上分离大脑,参照大鼠脑立体定位图谱定位中缝核并取出,放入干冰中预冷后,置于-80 ℃冰箱保存备用。
1.10 ELISA检测
采用ELISA 试剂盒检测血清IL-6、TNF-α 含量,严格按试剂盒说明书操作。
1.11 RT-PCR检测
超纯RNA提取试剂盒提取中缝核总RNA,进行RNA 电泳,用cDNA 合成试剂盒进行反转录,进行PCR扩增,扩增条件:95 ℃预变性10 min,95 ℃、15 s,60 ℃、50 s,共40个循环。以GAPDH为内参,2法计算mRNA相对表达量。引物序列见表1。

表1 各基因PCR引物序列
1.12 Western blot检测
中缝核组织剪碎后置于1.5 mL EP管中,预冷PBS漂洗2次;加入RIPA裂解液(含蛋白酶抑制剂和磷酸酶抑制剂),匀浆机匀浆后冰上裂解30 min;离心后取上清液,BCA法检测蛋白浓度;样品经上样、电泳、转膜、5%脱脂奶粉封闭、TBST洗膜后,分别滴加IL-6一抗(1∶1 000)、TNF-α一抗(1∶1 000)、β-actin一抗(1∶3 000),4 ℃孵育过夜;TBST洗膜4次,每次8 min;滴加相应二抗(1∶5 000),37 ℃摇床孵育2 h,TBST洗膜;ECL曝光后显影,采用Image J 1.8.0软件进行分析,以β-actin 为内参,计算目的蛋白相对表达量。
1.13 统计学方法
2 结果
2.1 柴胡疏肝散精简方对模型大鼠体质量增量的影响
与空白组比较,模型组大鼠体质量增量明显减少(<0.05);与模型组比较,氟西汀组和精简方组大鼠体质量增量明显增加(<0.05)。见图1。

图1 各组大鼠体质量增量比较(,每组10只)
2.2 柴胡疏肝散精简方对模型大鼠强迫游泳不动时间的影响
与空白组比较,模型组大鼠强迫游泳不动时间明显增加(<0.05);与模型组比较,氟西汀组和精简方组大鼠强迫游泳不动时间明显减少(<0.05)。见图2。
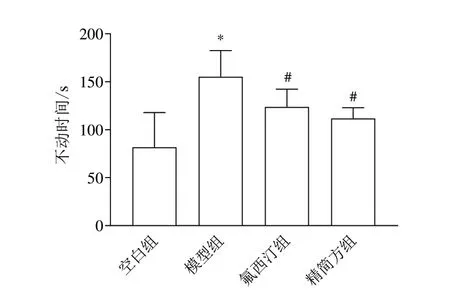
图2 各组大鼠强迫游泳不动时间比较(,每组10只)
2.3 柴胡疏肝散精简方对模型大鼠运动总距离及穿格次数的影响
与空白组比较,模型组大鼠旷场实验运动总距离及穿格次数明显减少(<0.05);与模型组比较,氟西汀组和精简方组大鼠运动总距离及穿格次数明显增加(<0.05)。见图3。
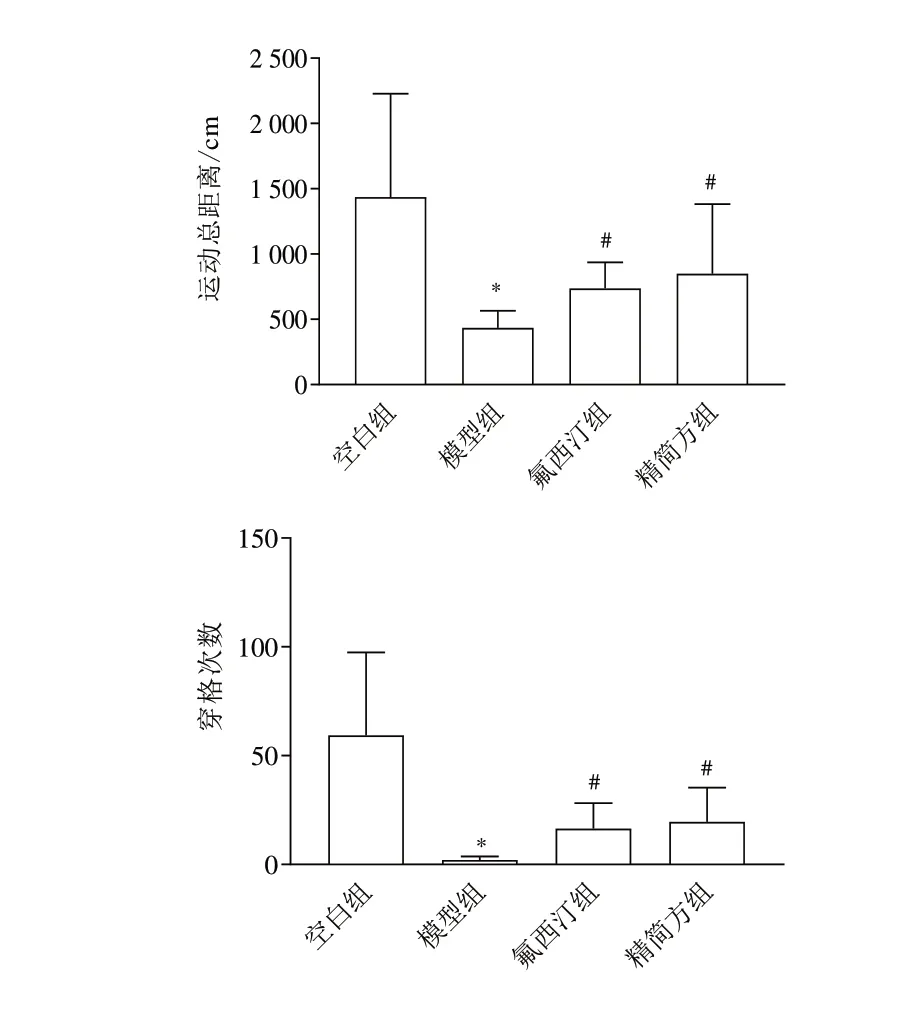
图3 各组大鼠旷场实验运动总距离和穿格次数比较(,每组10只)
2.4 柴胡疏肝散精简方对模大鼠热缩足阈值的影响
与空白组比较,模型组大鼠热缩足阈值明显降低(<0.05);与模型组比较,氟西汀组和精简方组大鼠热缩足阈值明显升高(<0.05)。见表2。
表2 各组大鼠热痛缩足阈值比较(,s)
2.5 柴胡疏肝散精简方对模大鼠血清白细胞介素-6、肿瘤坏死因子-α含量的影响
与空白组比较,模型组大鼠血清IL-6、TNF-α含量明显增加(<0.05);与模型组比较,氟西汀组和精简方组大鼠血清IL-6、TNF-α 含量明显减少(<0.05)。见图4。
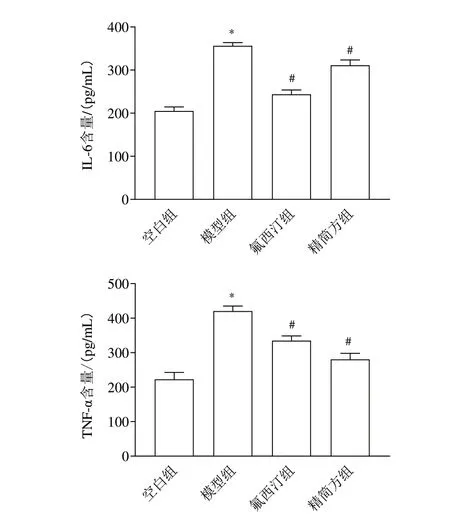
图4 各组大鼠血清IL-6、TNF-α含量比较(,每组10只)
2.6 柴胡疏肝散精简方对模大鼠中缝核P2X7 受体、Caspase-1及白细胞介素-1β mRNA表达的影响
与空白组比较,模型组大鼠中缝核P2X7 受体、Caspase-1 及IL-1β mRNA 表达明显升高(<0.05);与模型组比较,氟西汀组和精简方组大鼠中缝核P2X7受体、Caspase-1及IL-1β mRNA表达明显降低(<0.05)。见表3。
表3 各组大鼠中缝核P2X7受体、Caspase-1及IL-1β mRNA表达比较()
2.7 柴胡疏肝散精简方对模型大鼠中缝核白细胞介素-6、肿瘤坏死因子-α蛋白表达的影响
与空白组比较,模型组大鼠中缝核IL-6、TNF-α蛋白表达明显升高(<0.05);与模型组比较,氟西汀组和精简方组大鼠中缝核IL-6、TNF-α蛋白表达明显降低(<0.05)。见图5。

图5 各组大鼠中缝核IL-6、TNF-α蛋白表达比较(,每组10只)
3 讨论
目前关于抑郁症的发病机制尚不清楚,主要有单胺类神经递质假说、神经受体假说、神经营养和可塑性假说、神经内分泌假说、神经免疫炎症假说等。免疫炎症假说越来越受到关注。研究发现,抑郁症通常伴有炎症、自身免疫反应、氧化和亚硝化应激反应及神经退行性病变等,而这些反应部分是由IL-1水平升高引起。炎症因子可激活吲哚胺2,3 双加氧酶(IDO),IDO的激活又使合成5-羟色胺(5-HT)的原料色氨酸通过犬尿氨酸代谢通路消耗,从而降低5-HT的合成,进而出现抑郁样表现。P2X7受体是嘌呤受体的一个亚型,为ATP控制的离子通道,其在中枢神经系统表达丰富,被ATP激活后导致K外流和Ca内流,及非选择性膜孔形成,启动一系列信号途径如炎症小体NLRP3活化、Caspase-1和核因子-κB激活等,增强炎性细胞因子转录,介导IL-1β、IL-6、TNF-α等多种炎性因子释放,参与炎症发生发展。同时P2X7受体还参与疼痛的调节。
中医认为,疼痛抑郁共病基本病机为肝郁气滞,不通则痛,临床以疏肝类中药复方治疗,效果显著。柴胡疏肝散出自《景岳全书》,用于“治胁肋疼痛,寒热往来”,为经典疏肝理气剂,具有疏肝解郁、行气止痛功效。原方为“醋炒陈皮、柴胡各二钱,川芎、麸炒枳壳、芍药各一钱半,炙甘草五分,香附一钱半”,“水一盅半,煎八分,食前服”。柴胡疏肝散具有较好的抗炎作用,不仅可降低外周血炎症因子IL-6、TNF-α含量,还可减少中缝核IL-6、TNF-α蛋白表达,通过抑制炎症因子的释放抑制IDO 激活,从而促进5-HT合成,但其发挥抗炎作用的上游分子机制尚不清楚。P2X7受体作为启动炎症级联反应的关键蛋白,柴胡疏肝散是否通过影响该靶点发挥抗炎作用,目前缺少明确研究。本研究使用柴胡疏肝散精简方是根据原方进行化裁,由柴胡9 g、白芍15 g、枳壳9 g、香附9 g组成,增加君药柴胡剂量以增强疏肝解郁之功,增加枳壳、香附剂量而重理气,重用白芍以养血柔肝,同时去掉辛燥之川芎、理气之陈皮。本研究结果显示,精简方组大鼠中缝核P2X7 受体、Caspase-1、IL-1β mRNA及IL-6、TNF-α蛋白表达明显降低,提示柴胡疏肝散精简方可能通过抑制P2X7受体及Caspase-1/IL-1β表达,抑制中缝核炎症因子释放,从而发挥抗疼痛抑郁功效。
综上所述,柴胡疏肝散精简方可通过降低慢性疼痛抑郁共病大鼠中缝核P2X7受体mRNA表达,进而抑制Caspase-1/IL-1β 通路,降低中缝核及血清IL-6、TNF-α水平,减轻炎症反应,提高大鼠痛阈值及改善抑郁行为。
