基于模型荟萃分析5 个SGLT2 抑制剂在单用和联合用药治疗2 型糖尿病的临床疗效
2022-07-15盛兰兰李梓晴毕福林
曾 茗,盛兰兰,夏 宇,李梓晴,毕福林,杨 劲*
1 中国药科大学药学院,南京 211198;2 中国药科大学国际医药商学院,南京211198
糖尿病是常见的慢性疾病之一,其中患病率最高的是2 型糖尿病(type 2 diabetes mellitus,T2DM)[1]。口服降糖药钠-葡萄糖共转运蛋白2 抑制剂(sodium-glucose co-transporter-2 inhibitors,SGLT2i)通过选择性地抑制肾近曲小管中的SGLT2 受体,阻止葡萄糖的重吸收,增加葡萄糖在尿液中的排泄,从而改善人体血糖水平[2]。目前已批准上市SGLT2i 包括卡格列净[3]、达格列净[4]、恩格列净[5]、埃格列净[6]、依格列净[7]、鲁格列净[8]、托格列净[9]共7 种。
由于临床试验间存在异质性而产生偏差,不同试验结果受到试验样本量、受试人群、随访期、治疗剂量等因素的影响,而传统荟萃分析(meta-analysis)对数据的同质性要求较高。本研究基于模型的荟萃分析(model-based meta-analysis,MBMA)[10],选择糖化血红蛋白(hemoglobin A1c,HbA1c)相对基线变化值作为药效学指标,建立SGLT2i 以时间、剂量描绘的药物效应模型,定量分析不同SGLT2i 单用或SGLT2i 联合二甲双胍、联合二肽基肽酶-4 抑制剂(dipeptidyl peptidase-4 inhibitors,DPP4i)、联合DPP4i 和二甲双胍,探究四种治疗方式对于T2DM 的临床治疗效果,为制定临床用药方案、药物开发策略提供科学合理的证据。
1 资料方法
1.1 文献检索
在ClinicalTrials.gov(http://clinicaltrial.gov/)和Web of Science(MEDLINE)进行文献检索,检索时间截止至2021 年5 月。检索条件设置为英文发表的文献,检索表达式为(“targeted drugs”)AND(“diabetes”OR“diabetic”),其中“targeted drugs”包括已上市SGLT2i(卡格列净、达格列净、恩格列净、埃格列净、依格列净、鲁格列净、托格列净)的商品名、通用名和化合物代号,具体名称见表1。Clinical-Trials.gov 检索条件设置为已完成的、干预性临床Ⅱ期和Ⅲ期研究。此外,通过查阅美国食品药品监督管理局的药物审评报告、相关综述等,查验是否有缺漏文献。

表1 SGLT2 抑制剂的通用名、商品名和化合物代号
1.2 纳排标准
文献的纳入标准:(1)随机双盲临床试验;(2)研究人群为T2DM 患者;(3)由于运动饮食、服用降糖药或其他治疗方法而血糖控制不足,采用SGLT2i单用或SGLT2i 联用二甲双胍、联用DPP4i、联合DPP4i 和二甲双胍四种治疗方式;(4)以HbA1c 为临床终点指标;(5)可找到全文的英文文献。
文献的排除标准:(1)针对特殊人群的研究,包括青少年、肾功能衰竭患者;(2)伴随使用胰岛素以及胰岛素类似物、GLP-1RA、TZD、SU;(3)开放性研究、扩展阶段的观察性研究和临床Ⅳ期研究;(4)二次分析、汇总分析、重复发表等不相关的文章。
1.3 数据提取
从筛选得到的文献中提取以下信息:(1)各文献的基本信息,包括作者、发表时间;(2)给药方案,包括药物名称、剂量、给药方式、治疗维持时间和联合用药情况;(3)受试人群的样本量、人口统计学信息(年龄、性别和种族)、基线HbA1c 值、身体质量指数(body mass index,BMI)以及T2DM 患病持续时间;(4)主要疗效指标,即各时间点相对基线变化的HbA1c 平均值。使用GetDataGraph Digitizer(Version 2.2.5)将图中的数据转换为相应的数值。
不同研究对试验中缺失数据的处理方法不同,选择采用末次观测值结转法(last observation carried forward,LOCF)处理疗效缺失值的文献数据作为建模数据。
1.4 模型建立
选择相对基线HbA1c 的变化值作为药效学指标,基础模型由安慰剂效应和药物效应两部分组成,见式(1):

其中EFFHbA1c表示随时间变化HbA1c 相对基线的变化值,EFFplacebo和EFFdrug分别表示临床试验的安慰剂效应和药物效应。
由于安慰剂效应会随着治疗维持时间的变化而发生变化,考虑使用以下模型描绘安慰剂效应的变化情况,见式(2):

其中Pmax为最大安慰剂效应,kplacebo为指数模型的速率常数。
考虑使用以下模型描绘药物效应的变化情况,见式(3):

其中Emax为最大药物效应,ET50为达到50%最大药物效应(Emax)所需的时间,Dose 为药物的剂量,ED50为达到50%最大药物效应(Emax)所需的剂量。
随机效应包括研究间的变异和残差变异。其中研究间的变异通常考虑指数型模型(式4)、加和型模型(式5):

其中θi为个体i 的参数估计值,为参数的群体典型值为个体i 的参数θ 的研究间变异,具有个体的特异性,并且服从分布η~N(0,ω2)。
残差变异模型采用由样本量的平方根加权的加和模型,见式(6):

建立基础模型后进行协变量筛选,选择年龄、性别、种族、BMI、基线HbA1c 和T2DM 患病持续时间作为候选协变量,考察是否对基础模型参数产生影响。协变量模型考虑线性(式7)、指数型(式8)和幂型模型(式9):

其中P为基础模型中的参数,TVP 为该参数的群体典型值,θcov为该参数与协变量的关系系数,Cov 为协变量,Covmedian为协变量的中位数。协变量的纳入依据临床合理性和引入协变量后目标函数值(objective function value,OFV)的变化值。采用向前纳入法和向后排除法,显著性差异分别设定为0.01 和0.001。
使用NONMEM(Version7.5.0)建立模型,采用含个体间变异和残差变异交互作用的一阶条件估算法(first-order conditional estimation method with η-ε interaction,FOCE-I)进行参数估算,配合使用Perl-speaks-NONMEM(Version5.0.0)、工作平台Pirana(Version 3.0.0),以及使用R(Version 4.0.2)进行作图。
1.5 模型评价
最终模型采用拟合优度图(goodness of fit plots,GOF plots)进行综合评价,包括个体估计值(individual predictions,IPRED)-观察值图、群体估计值(population predictions,PRED)-观察值图、群体估计值-条件加权残差(conditional weighted residuals versus time,CWRES)图、时间-条件加权残差图,观察散点图是否分布均匀及是否呈现一定的趋势性。
采用可视化预测检验(visual predictive check,VPC),利用最终拟合的参数在原有数据基础上进行1000 次模拟,得到的95%置信区间与观察值作图,考察是否存在数据偏差。采用非参数自举法(bootstrap)进行1000 次自举拟合,模型估算参数成功率至少为80%,比较参数的拟合值和计算值。
1.6 模型模拟
基于最终模型结果,进行1000 次模拟,比较不同SGLT2i 在单用、或SGLT2i 联用二甲双胍、联用DPP4i、联合DPP4i 和二甲双胍四种治疗方式的降糖效果。
模拟SGLT2i 在推荐剂量下72 周随时间变化的效应变化曲线、第52 周各药的剂量效应曲线,以及基于各药ED50进行剂量校正后的量效关系曲线。
2 结果
2.1 数据特征
共检索得到652 篇文献,文献经筛选,最后纳入文献54 篇,其中卡格列净11 篇,达格列净17 篇,恩格列净12 篇,埃格列净7 篇,依格列净7 篇。鲁格列净和托格列净由于文献数量较少,未纳入后续的分析。在纳入文献中,与SGLT2i 联用的DPP4i 包括西格列汀、利格列汀、沙格列汀、替格列汀。综合所有的文献共涵盖167 组研究的24802 名受试者,其中57%为白种人,35%为亚洲人,黑种人和其他人种占8%。纳入文献的人群基线特征:平均年龄为56.36 岁(49.9 岁~64.3 岁),男性在人群的平均占比为58.1%(39.8%~83.1%),平均基线HbA1c值为8.03%(7.16%~9.03%),平均基线BMI 为29.34 kg·m-2(24.7 kg·m-2~33.6 kg·m-2),平均T2DM 患病持续时间为6.37 年(0.25 年~12.6 年)。
2.2 建立模型
汇总5 个SGLT2i 文献数据统一建立形成分析数据集,标识出不同药物,按照不同治疗方式分为5组:①因运动饮食血糖控制不足,采用SGLT2i 单药治疗组(简称SGLT2i 组);②因使用二甲双胍血糖控制不足,采用SGLT2i 联合二甲双胍治疗组(简称SGLT2i+MET 组);③因单用SGLT2i 或DPP-4i 血糖控制不足,采用SGLT2i 联合DPP4i 治疗组(简称SGLT2i+DPP4i 组);④因使用二甲双胍和DPP4i 血糖控制不足,采用SGLT2i 联合DPP4i 和二甲双胍治疗组(简称SGLT2i+DPP4i+MET(DPP4i+MET)组);⑤因使用二甲双胍血糖控制不足,采用SGLT2i联合DPP4i、二甲双胍治疗组(简称SGLT2i+DPP4i+MET(MET)组)。由此得以在不同治疗方式下对不同SGLT2i 分别拟合各自的模型参数。安慰剂模型描述不同治疗组的安慰剂效应随时间的变化情况,药效学模型描述不同药物随时间、剂量的变化情况,分别拟合SGLT2i 各药的模型参数。综合模型OFV 值、诊断图和参数拟合情况,研究间的变异采用加和型模型,最终模型见式(10):

其中Pmax,group为不同治疗组对应的最大安慰剂效应,Emax,drug、ET50,drug、ED50,drug为不同SGLT2i药物对应的最大药物效应、达到50%最大药物效应所需的时间、50%最大药物效应所需的剂量。
建立基础模型后考察潜在协变量对模型的影响,经向前纳入法和向后排除法依次筛选,未找到对模型参数产生显著性影响的协变量。最终得到一个以时间、剂量描绘的HbA1c 模型,模型参数结果见表2 所示,其中Emax,canagliflozin、Emax,empagliflozin、Emax,ipragliflozin的研究间变异值被固定为0,是因为出现收敛问题[11],使得估计值接近于0。
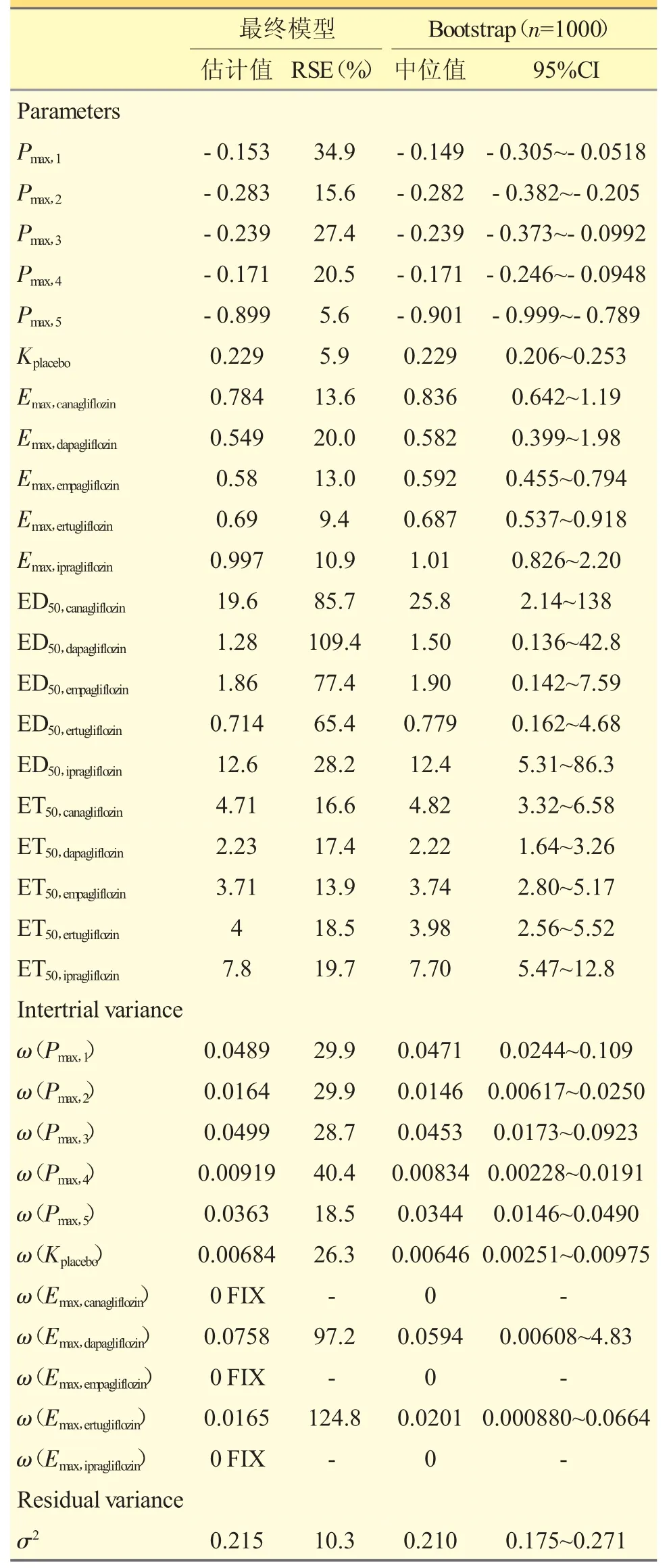
表2 最终模型参数估计值
2.3 评价模型
最终模型的GOF 诊断图如图1 所示,DVPRED 图和DV-IPRED 图的数据趋势线与对角线呈现出高度重合,表明模型能很好地描述数据的集中情况;Time-CWRES 图和PRED-CWRES 图各点均匀分布在X 轴两侧,且大部分处于±2 范围内,没有出现趋势性的偏倚。VPC 结果如图2 所示,大部分数据点落在95%置信区间内,说明模型具有良好的预测能力。结果如表2 所示,Bootstrap 重抽样1000 次,满足模型最小化成功率大于80%,所有参数的中位值均包含在95%的置信区间内,且与最终模型的参数估算值相近。

图1 最终模型的拟合优度图

图2 最终模型的可视化检验图
2.4 模拟结果
采用最终模型的参数结果,模拟安慰剂和治疗组72 周随时间变化的相对基线HbA1c 中位值变化,给药方案设为推荐剂量(即100 mg/300 mg 卡格列净,5 mg/10 mg 达格列净,10 mg/25 mg 恩格列净,5 mg/15 mg 埃格列净,50 mg/100 mg 依格列净)治疗72 周,每天给药一次。单用、二联、三联的模拟结果如表3 所示,72 周高剂量组卡格列净、达格列净、恩格列净、埃格列净、依格列净在SGLT2i 组的相对基线HbA1c 中位值分别为-0.84%、-0.63%、-0.67%、-0.78%、-0.95%,与之相比,SGLT2i+MET 组再降0.13%,SGLT2i +DPP4i 组再降 0.09%,SGLT2i +DPP4i+MET(DPP4i+MET)组再降0.02%,SGLT2i+DPP4i+MET(MET)组再降0.75%。模拟曲线如图3所示,综合考虑所有治疗方式,结果表明72 周内SGLT2i 各药按疗效由高到低排序为依格列净>卡格列净>埃格列净>恩格列净>达格列净。
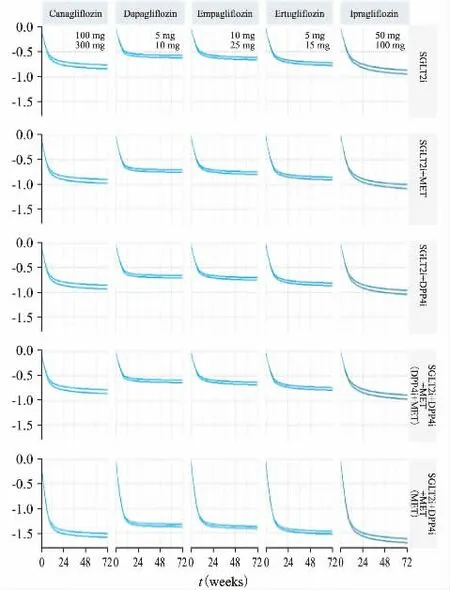
图3 SGLT2 抑制剂72 周相对基线HbA1c中位值随时间变化

表3 SGLT2 抑制剂第72 周在不同组的相对基线HbA1c 变化值
图4 为SGLT2i 在第52 周随剂量变化的经安慰剂校正的相对基线HbA1c 中位值变化。根据该量效关系曲线,目前所用的药物推荐剂量几乎已达到最大降糖效果。结果显示SGLT2i 存在剂量饱和现象,这提示继续加大剂量可能不会出现明显的降幅。

图4 SGLT2 抑制剂52 周经安慰剂校正的HbA1c 中位值随剂量变化
选择卡格列净作为参照药物,将各药推荐剂量通过ED50进行校正,在治疗第52 周随剂量变化的经安慰剂校正的相对基线HbA1c 中位值变化。结果如图5 所示,经剂量校正后SGLT2i 表现出一致的剂量HbA1c 效应关系,相比之下卡格列净和依格列净几乎已达到SGLT2i 的最大HbA1c 变化值。

图5 SGLT2 抑制剂52 周经安慰剂校正的HbA1c 变化值随用ED50 校正后剂量变化
3 讨论
基于模型的荟萃分析是在综合广泛数据的基础上,通过建立药效学模型,精确描述药物的剂量效应关系、时间效应关系,同时可考察多种因素(基线、人口学特征、试验特征等)对有效性或安全性的影响[12]。目前MBMA 已广泛应用于比较新化合物与新的或现有的治疗方案[13];将短期生物标志物反应与长期临床疗效、安全性终点联系[14];优化剂量选择和临床试验设计[15];综合评价上市后药物的有效性和安全性[16]。Gross JL 等[17]和Gibbs JP 等[18]用MBMA比较不同DPP4i 间的疗效差异,Inoue H 等[11]比较在二甲双胍基础上联用DPP4i、GLP-1RA、SGLT2i的疗效差异,Maloney A 等[19]比较6 类24 种治疗T2DM 药物在3 个T2DM 指标的差异。本研究针对SGLT2i 不同的治疗方式,建立时间、剂量与药物效应的关系,对SGLT2i 单药、二联、三联治疗方式在不同给药剂量和治疗时期作准确、定量分析。
本研究定量分析不同SGLT2i 单用、二联、三联治疗方式对T2DM 降糖效果的差异,得到SGLT2i按疗效排序依次为依格列净、卡格列净、埃格列净、恩格列净、达格列净,此结果与先前已发表研究[11,19]的结果相一致。SGLT2i+MET 组与SGLT2i+DPP4i 组72 周差异很小,但提示联合二甲双胍仍处于优势治疗地位。值得注意的是,三联用药组不同人群的HbA1c 基线差异大,对于已使用DPP4i+MET 而控制不足的患者,三联72 周降糖效果接近于SGLT2i+MET;但对于二甲双胍而控制不足人群,三联用药相比SGLT2i+MET、SGLT2i+DPP4i 两种二联用药仍有约0.6%的降幅。以上两个亚组,前者可能与联合用药的SGLT2i 固有降糖效果有关,后者则可能通过改善胰岛素抵抗情况以有效降低血糖水平[20]。本研究综合探究SGLT2i 安慰剂效应、药物效应以及变异性等因素对临床疗效终点的影响,有利于优化临床研究设计。由图3 时间效应曲线可知,SGLT2i在约36 周达到临床最大效应,这提示SGLT2i 临床研究的揭盲时间应至少为36 周以观察到最大临床获益。图4 剂量效应曲线表明,SGLT2i 目前的推荐剂量可接近最大临床疗效,这提示科学合理的剂量探索有利于成功开发SGLT2i 新品种。图5 则显示出卡格列净和依格列净几乎已达到该类药的最大HbA1c 变化值,这提示未来同类药物的开发可以以两者作为对照药物,衡量新化合物开发是否具有良好的临床优势性。
本研究也存在一定的局限性:一是T2DM 是一个动态发展的疾病过程,患者状态可能会伴随着β细胞功能障碍和胰岛素抵抗发生变化,每年HbA1c大约会升高0.2%,使得安慰剂效应会发生变化[18]。而现有的模型尚未考察这一影响因素,预测长期疗效可能出现一定的偏颇。二是由于仅能从已发表文献中的图表提取数据,而这些数据为群体均值,难以获得各研究每个受试者的原始个体数据。虽然本研究经筛选未发现协变量显著影响,但使用患者水平的数据对于理解协变量的影响将更具有参考价值[17],未来也需要通过大型的临床研究进一步确证。
综上所述,本研究采用MBMA 方法量化SGLT2i 在单用、二联、三联不同治疗方式的降糖作用,按药物疗效高低排序依次为依格列净、卡格列净、埃格列净、恩格列净、达格列净。未来同类药物的开发可以以卡格列净和依格列净作为对照药物,衡量新化合物开发是否具有良好的临床优势性。