g-C3N4/TiO2光催化材料的制备及其降解染料的实验研究
2022-07-14高雅伦陈广洲曹庆峰
高雅伦,陈广洲,曹庆峰,程 元,丁 健,吴 磊
(安徽建筑大学a.环境与能源工程学院;b.水污染控制与废水资源化安徽省重点实验室;c.环境污染控制与废弃物资源化利用安徽省重点实验室,安徽 合肥 230601)
印染废水具有三致效应,处理难度较大,且若处理不当会危害环境和人体健康[1]。光催化氧化法因具有可有效利用太阳光、彻底降解有机物和反应速率快等优点[2]而受到广泛关注,是极具应用前景的染料废水处理技术。因此,制备高效的光催化剂是目前研究的热点。光催化剂通常以固体半导体材料为主要成分,如氧化物TiO2等[3]和硫化物CdS 等[4]。TiO2是常用的半导体催化剂,具有无毒、价格低、光催化活性好等优点,但TiO2带隙较宽,单独使用时对太阳光利用率较低[5]。石墨相氮化碳(g-C3N4)是一种非金属半导体,拥有稳定的化学结构和独特的电子能带结构,光催化活性较高、对环境友好,但其比表面积较小、光生电子-空穴复合率高,致使其光催化效率偏低[6]。
目前,学者们研究将TiO2和g-C3N4复合形成g-C3N4/TiO2以提高材料的光催化活性。Peng 等[7]研究表明,无论g-C3N4和TiO2如何结合,g-C3N4/TiO2异质结构都可通过相应方式来提高光催化性能。Zhang 等[8-9]通过水热法分步制备TiO2/g-C3N4材料,材料形态比较均匀,但制备过程复杂;刘威等[10]采用热聚合法与溶胶法制备TiO2/g-C3N4材料,其对10 mg/L的MB染料能达到85%的降解率,但制备过程也比较复杂。在制氢应用方面,闫玉梅等[11]分别以硫脲、尿素和三聚氰胺作为前驱体制备g-C3N4,采用浸渍法和退火处理将g-C3N4负载在TiO2纳米花结构上制备出g-C3N4/TiO2复合材料,结果显示以三聚氰胺为g-C3N4前驱体制备的复合材料产氢性能最好。在染料降解应用方面,Li 等[12]通过在超薄g-C3N4片表面原位组装针状TiO2制备多孔g-C3N4/TiO2,其对酸性橙具有优异的光催化降解效果;Toghan 等[13]研究表明,TiO2@g-C3N4催化剂降解靛蓝胭脂红(IC)染料的速率比纯TiO2快7倍。综上,学者们对g-C3N4/TiO2复合材料的研究多集中于原料种类、制备方法、应用等方面;多采用两步法制备g-C3N4/TiO2光催化材料,多选用一种染料作为目标降解物,较少关注存在潜在致癌风险的孔雀石绿(MG)染料。基于此,以廉价易得的工业偏钛酸和三聚氰胺为原料,采用一步热处理法制备g-C3N4/TiO2复合催化材料,选取3种常用典型染料作为目标污染物进行光催化降解实验,探究复合材料的光催化降解性能。
1 实验材料与方法
1.1 试剂
三聚氰胺(C3H6N6)、工业偏钛酸(TiO(OH)2)、罗丹明B(C28H31ClN2O3,RhB)、亚甲基蓝(C16H18N3ClS,MB)、孔雀石绿(C23H25ClN2,MG)、乙二胺四乙酸二钠(C10H14N2Na2O8)、异丙醇(C3H8O)、对苯醌(C6H4O2)所有试剂均为分析纯(AR),购自上海麦克林生化科技有限公司。实验用水为去离子水。
1.2 实验方法
1.2.1 催化剂制备
g-C3N4的制备:称取5 g 三聚氰胺置于坩埚,再将坩埚加盖用锡纸包裹置于马弗炉,以10 ℃/min 的升温速率从室温升至500 ℃锻烧,保温1.5 h;自然冷却至100 ℃以下,取出焙烧后的淡黄色固体至研钵中研磨,得到g-C3N4粉末。
g-C3N4/TiO2复合催化材料的制备[14]:将三聚氰胺与工业偏钛酸按质量比(1∶2,1∶1)称取后分别置于坩埚,超声均匀分散5 min,制备成前驱体;将坩埚加盖用锡纸包裹置于马弗炉,以10 ℃/min的升温速率从室温升至500 ℃锻烧,保温1.5 h;自然冷却至100 ℃以下取出,研磨得到粉体材料备用,分别标记为0.5-g-C3N4/TiO2,1.0-g-C3N4/TiO2,0.5与1.0代表三聚氰胺与工业偏钛酸的质量比值。
1.2.2 催化降解实验
以MB,MG,RhB 染料溶液为目标降解对象,加入光催化剂,釆用300 W 氙灯模拟太阳光照射,在光催化反应器中进行降解实验。取10 mg 制备的复合催化材料与50 mL 染料废水充分混合后置于反应容器中,溶液质量浓度分别为10,20 mg/L。打开光源前将反应体系置于避光处,暗吸附60 min,使之达到吸附-脱附平衡。反应过程中,每隔30 min 取样3~4 mL,以3 000 r/min 速率离心分离后,取上层清液在紫外-可见分光光度计特定波长(664,620,550 nm)处测定其吸光度,依据标准曲线计算对应的质量浓度,绘制光降解效率曲线,光催化降解时长为150 min。设置一组对照组,将其置于避光条件下进行相同实验。采用反应前后染料质量浓度变化评价其光催化性能,降解率η= (1-ρ/ρ0)× 100%,ρ0为溶液的初始质量浓度,ρ为t时刻溶液的质量浓度。
1.2.3 催化剂性能表征与机理测试
采用日本理学Smartlab 型X 射线衍射仪(X ray diffraction,XRD)分析光催化剂的晶相结构;采用美国热电Nicolet iS1 型傅里叶变换红外光谱仪(Fourier transform infrared spectrometer,FT-IR)分析样品的结构和化学基团;采用日本日立高分辨冷场发射Regulus 8100 型扫描电子显微镜(scanning electron microscope,SEM)与JEM-2100F 型高分辨透射电子显微镜(transmission electron microscope,TEM)表征催化剂的微观形貌;采用美国麦克ASAP2460 全自动比表面积及孔径分析仪测定样品吸附-脱附等温线与比表面积;采用美国PerkinElmer 公司LAMBDA 950 型紫外-可见光分光光度计测定催化剂的紫外-可见漫反射光谱(UV-Vis diffuse reflection spectra,UV-Vis DRS)。
分别以乙二胺四乙酸二钠(EDTA-2Na)、异丙醇(IPA)和对苯醌(BQ)作为空穴h+、羟基自由基·OH、超氧自由基的捕获剂,将其加入到初始质量浓度为10 mg/L 的MB,MG 和RhB 反应体系中进行自由基捕获实验。捕获剂浓度为0.5 mmol/L,光催化剂的用量均为10 mg 1.0-g-C3N4/TiO2材料,实验步骤同1.2.2节。
2 结果与讨论
2.1 催化剂的性能表征
2.1.1 物相分析
g-C3N4和复合材料的XRD 图谱见图1。由图1可得:位于12.9°和27.4°处的是g-C3N4的特征衍射峰;0.5-g-C3N4/TiO2和1.0-g-C3N4/TiO2在12.9°和27.4°处的峰强有所降低,这是TiO2使g-C3N4表面受到覆盖,结晶度降低[15]所致。对比文献[15]中纯TiO2的XRD 图 谱 可 得,0.5-g-C3N4/TiO2和1.0-g-C3N4/TiO2中 含 有TiO2的 所 有 特 征 峰,在25.3°,37.6°,47.8°,54.0°,54.8°,62.4°,70.0°,75.1°处均与锐钛矿相TiO2标准PDF卡片(JCPDS:21-1272)一致。
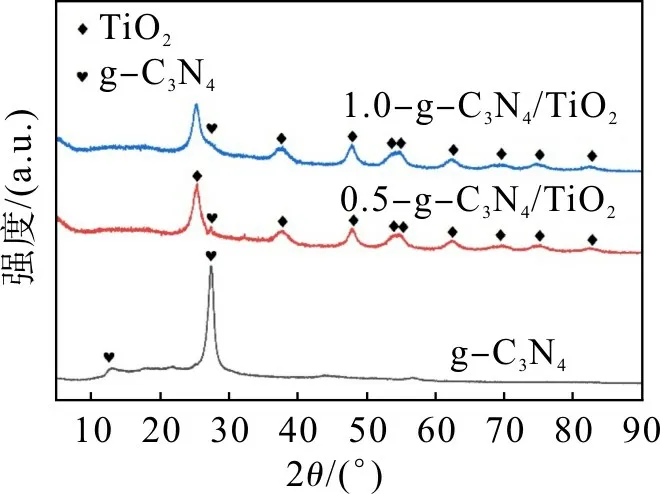
图1 g-C3N4和g-C3N4/TiO2的XRD图谱Fig.1 XRD patterns of g-C3N4 and g-C3N4/TiO2
2.1.2 FT-IR分析
g-C3N4与复合材料的FT-IR光谱见图2。由图2可得:复合材料中出现g-C3N4的特征吸收峰,且在808 cm-1以下范围吸收峰增强,对应3-S-三嗪结构的键振动[16];复合材料中也出现了TiO2的特征吸收峰[17],在3 300~3 500 cm-1范围内对应TiO2表面的O--H 伸缩振动,600 cm-1附近对应键的伸缩振动[18];复合材料中,3 000~3 300 cm-1对应g-C3N4表面N--H 基团的特征峰减弱,表明复合过程中该基团和TiO2表面O--H 基团发生缩合反应,形成异质结构[19],两者的杂化使g-C3N4的骨架结构发生变化,这也是复合材料催化活性提高的关键。
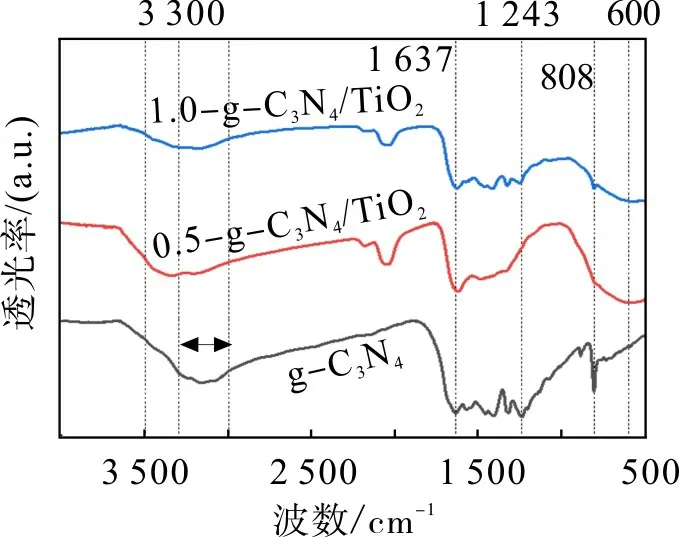
图2 g-C3N4和g-C3N4/TiO2样品的FT-IR图谱Fig.2 FT-IR spectrum of g-C3N4 and g-C3N4/TiO2
2.1.3 形貌与比表面积
g-C3N4与复合材料的形貌结构见图3。由图3可得:g-C3N4结构呈片状,复合材料颗粒呈球状,TiO2粒子分散负载在g-C3N4片状结构上,可有效增大染料分子和催化剂的接触面积,利于降解效率的提高;1.0-g-C3N4/TiO2的TEM 图显示TiO2粒子有团聚现象,但团聚不明显,g-C3N4的存在会抑制团聚,利于光的吸收[14];图3(f)显示具有明显晶格的TiO2粒子负载在g-C3N4上。

图3 g-C3N4和g-C3N4/TiO2的SEM及1.0-g-C3N4/TiO2样品的TEM照片Fig.3 SEM images of g-C3N4 and g-C3N4/TiO2,TEM images of 1.0-g-C3N4/TiO2
图4为g-C3N4和1.0-g-C3N4/TiO2的N2吸附-脱附与孔径分布曲线。图中V为吸附量,d为孔径。
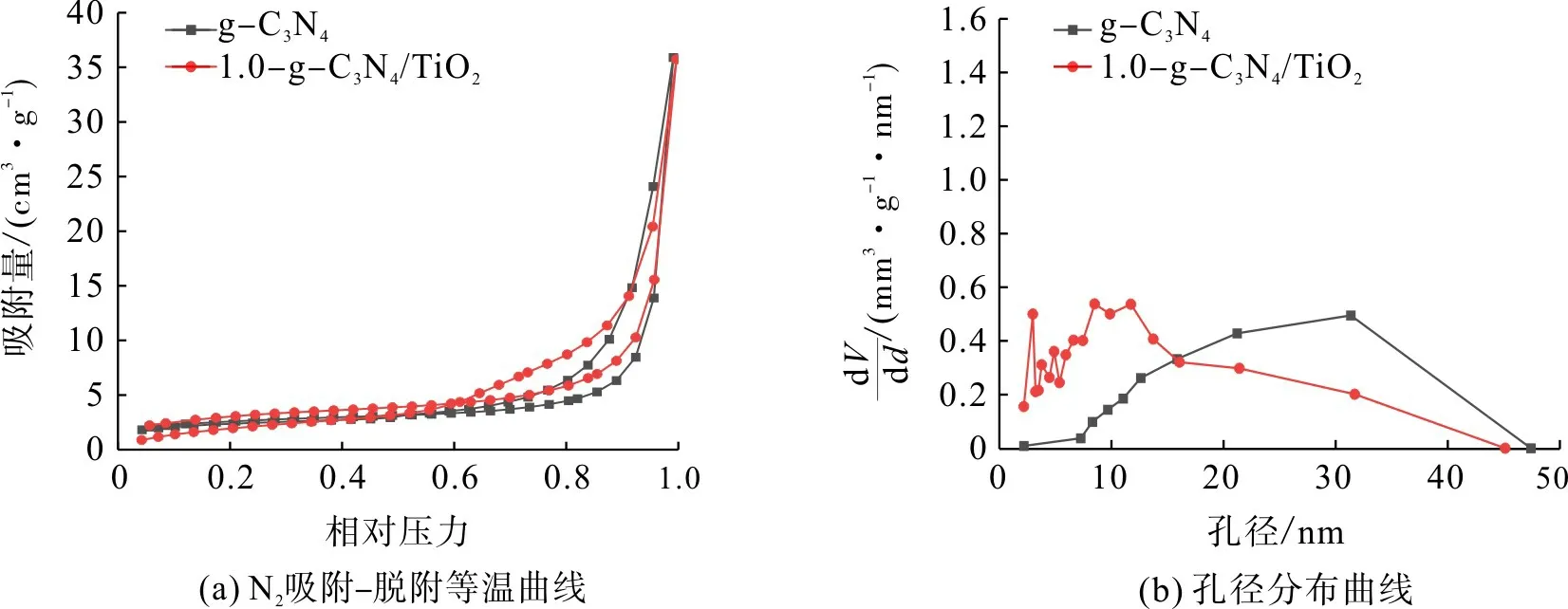
图4 g-C3N4和1.0-g-C3N4/TiO2的N2吸附-脱附等温曲线和孔径分布曲线Fig.4 Adsorption-desorption isotherms and pore size distribution curves of g-C3N4 and 1.0-g-C3N4/TiO2
图4 显 示:1.0-g-C3N4/TiO2属 于IUPAC 分 类法[20]中的IV 型等温线,为H3 型滞后环,说明样品具有介孔结构;g-C3N4的孔径主要分布在20~30 nm 范围,而1.0-g-C3N4/TiO2存在大量10 nm 左右的孔。结合表1 可得出,复合材料平均孔径有所减小、比表面积有所增加,利于复合材料对染料的吸附。

表1 样品的比表面积、孔容积、平均孔径Tab.1 Surface area,pore volume and average pore diameter of the samples
2.1.4 光吸收性能
g-C3N4与复合材料的紫外-可见光漫反射吸收光谱见图5。由图5 可得:g-C3N4与复合材料在可见光范围均具有吸收能力,复合材料的吸收波长发生红移,拓宽了可见光吸收范围,光吸收性能增强;复合材料具有TiO2的紫外光响应性能和g-C3N4的可见光响应性能,有效结合了两者的特点。对图5曲线进行微分找到极值点,过极值点做截线,取该截线在吸光度为0 时的波长阈值λg,通过公式Eg=1 240/λg[21]计 算 出g-C3N4,0.5-g-C3N4/TiO2和1.0-g-C3N4/TiO2的禁带宽度Eg分别为2.75,2.32,2.14 eV。由此可见,复合材料的禁带宽度明显变窄,光生电子容易转移,从而表现出更强的光催化性能。
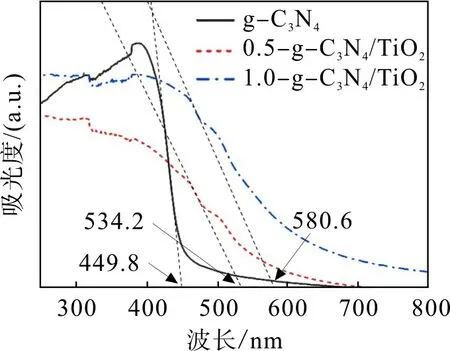
图5 g-C3N4和g-C3N4/TiO2的紫外-可见光漫反射吸收光谱Fig.5 UV-Vis DRS of g-C3N4 and g-C3N4/TiO2
2.2 催化剂的光催化降解性能
2.2.1 原料配比的影响
图6为复合材料g-C3N4/TiO2对MB,MG和RhB染料的光催化降解曲线。3种染料的初始质量浓度为10 mg/L。由图6 可得:对于MB 溶液,光照150 min后降解率均能达97%以上,但采用1.0-g-C3N4/TiO2复合材料的降解速度更快、效率更高;对于MG 溶液,光照150 min 采用1.0-g-C3N4/TiO2为催化剂时的降解率达96.60%,采用0.5-g-C3N4/TiO2为催化剂时的降解率仅71.54%;对于RhB 溶液,采用1.0-g-C3N4/TiO2与0.5-g-C3N4/TiO2光照150 min 后的降解率分别为92.72%,43.72%,差异明显。
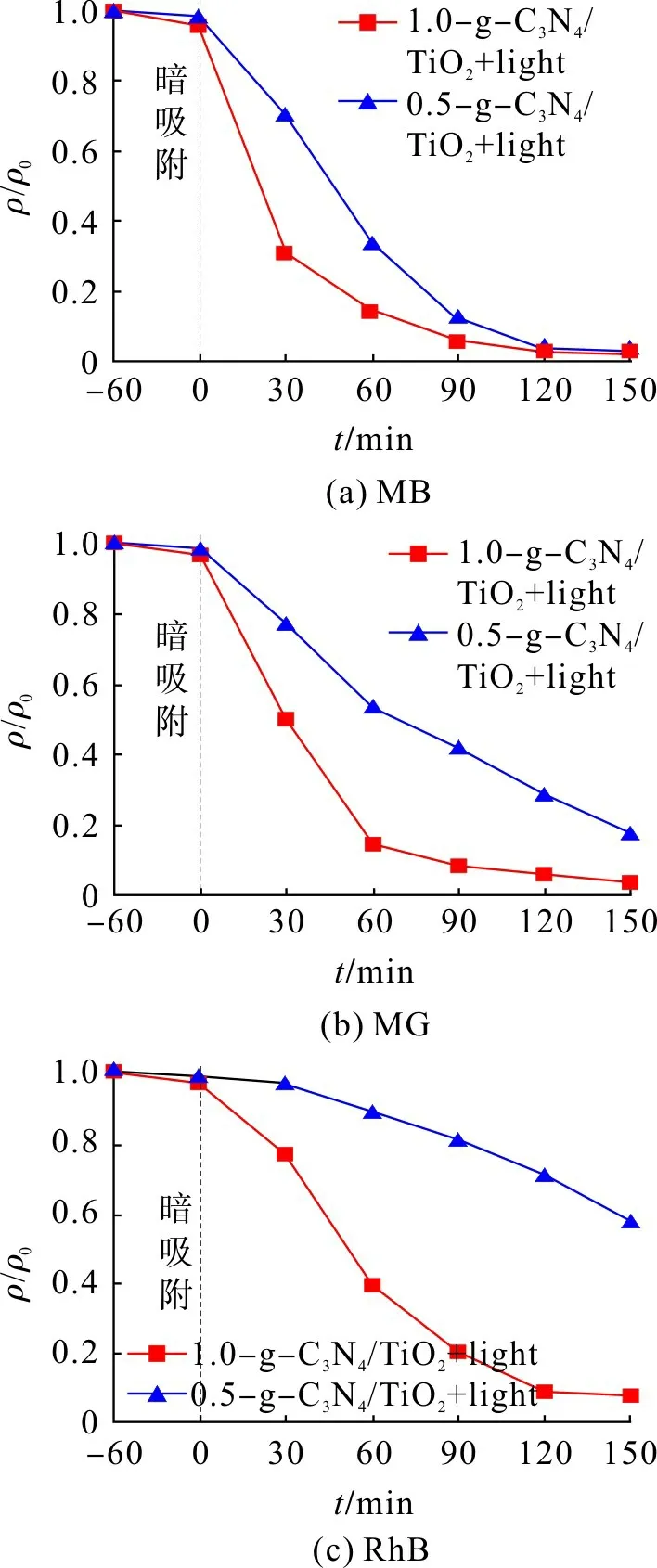
图6 两种原料配比下的MB,MG,RhB溶液降解曲线Fig.6 Degradation curves of MB,MG and RhB solutions under the ratio of two raw materials
比较分析可知:复合材料1.0-g-C3N4/TiO2的降解效果优于0.5-g-C3N4/TiO2,这是因为1.0-g-C3N4/TiO2材料中的g-C3N4含量较多,对可见光的响应增强,光催化性能得到提升。但文献[21]的研究表明:g-C3N4/TiO2复合材料中g-C3N4含量不能过多,过多的g-C3N4会产生光生载流子复合中心,反而会导致光催化活性下降。此外,g-C3N4含量增大会产生更多的电子转移至TiO2的导带,促进光生电子和空穴的分离,但含量过大会导致有限的TiO2难以接收g-C3N4产生的光生电子[22]。
2.2.2 光照的影响
不同光照条件下1.0-g-C3N4/TiO2对MB,MG和RhB 染料的降解曲线见图7。3 种染料的初始质量浓度为10 mg/L。图7表明:在1.0-g-C3N4/TiO2体系避光反应条件下MB 有微量吸附,降解率最终稳定在15.00% 左右,光照150 min 后降解率为97.20%;在1.0-g-C3N4/TiO2体系避光条件下,MG达到11.30% 的降解率,光照150 min 后降解率达96.60%;在1.0-g-C3N4/TiO2避光条件下,RhB 溶液光照 150 min后降解率为92.70%。
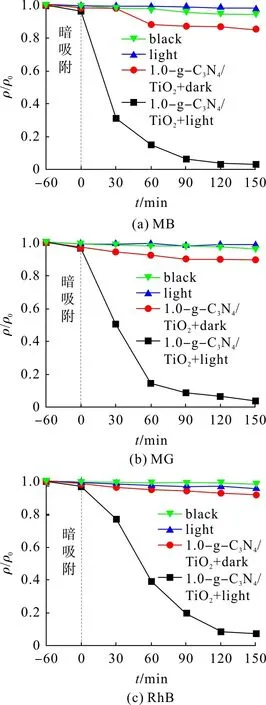
图7 不同光照条件下MB,MG,RhB溶液降解曲线Fig.7 Degradation curves of MB,MG,RhB solutions under different lighting conditions
对于3种染料,光照和催化剂是影响其降解率的重要因素。在无催化剂仅光照的条件下,染料基本没有降解;在有催化剂无可见光照条件下,复合催化剂会吸附部分染料,但吸附量有限,达到一定程度时保持不变;复合催化剂经可见光照射后,降解效果明显。在可见光照射下,g-C3N4吸收可见光后激发产生的电子转移到TiO2的导带中,致使电子与空穴分离,利于提高光催化活性[23];由于TiO2的结晶性下降,在TiO2表面出现更多缺陷,更易捕获从g-C3N4转移的电子,可有效促进光生载流子的分离,实现g-C3N4和TiO2协同作用[24]。
2.2.3 染料初始浓度的影响
为考察染料初始浓度对复合材料降解效果的影响,设置染料MB,MG 和RhB 的初始质量浓度为10,20 mg/L,1.0-g-C3N4/TiO2对3种染料的降解曲线见图8。
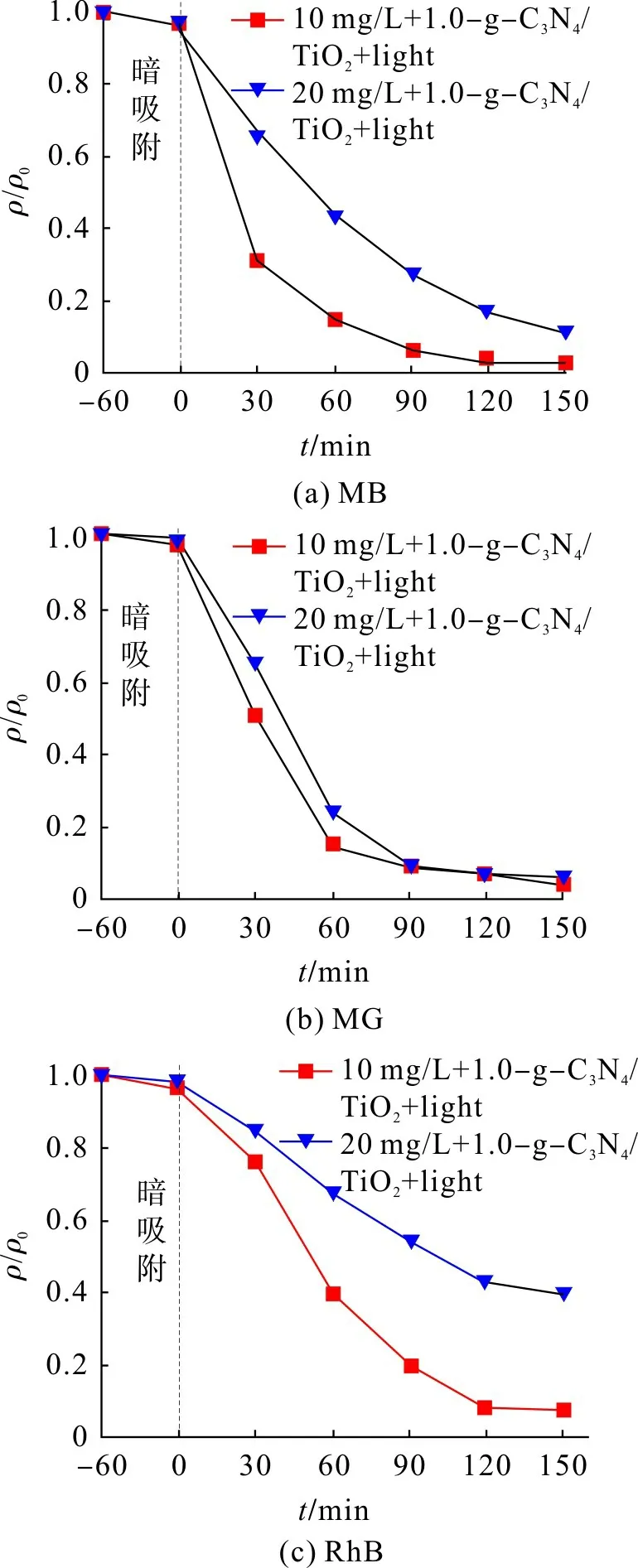
图8 不同初始浓度MB,MG,RhB溶液降解曲线Fig.8 Degradation curves of MB,MG,RhB solutions under different initial concentrations
由图8 可得:在1.0-g-C3N4/TiO2体系下,初始质量浓度为10,20 mg/L MG 溶液的降解率相近;针对MB与RhB溶液,初始质量浓度10 mg/L的降解率大于20 mg/L的降解率。这是因为相同量的复合催化剂活性位点相同,浓度高的废水含更多染料分子,导致有效反应降低,降解效果减弱;且浓度升高,催化剂表面被染料分子遮盖,导致光利用率降低[25]。
2.3 催化剂的稳定性及反应机理
以初始质量浓度为10 mg/L MB 溶液的光催化降解为例,研究1.0-g-C3N4/TiO2的可重复利用性,图9 为1.0-g-C3N4/TiO2降解MB 溶液的循环利用测试结果。由图9 可看出:第一次降解效果最好,降解率为97.20%;之后每次降解率略有下降,5次循环反应后,仍具有较高的降解率,达93.20%,表明该复合催化材料光催化性能稳定。

图9 MB的循环降解实验结果Fig.9 Cyclic degradation experiment results of MB
为探讨复合材料的光催化反应机理,加入3 种捕获剂进行捕获实验,结果见图10。由图10 可得:当IPA 存在时,MB 的降解率为23.40%,与不加入捕获剂相比,复合材料对MB 的催化活性明显降低,IPA 消耗了较多的·OH,反应受到较大抑制,表明在MB 溶液中起作用的活性物质主要是·OH,h+与次之;在MG 和RhB 溶液中加入3 种捕获剂时,MG和RhB 的降解率均有不同程度的下降,抑制作用最大的是BQ,表明在MG和RhB反应体系中起作用的的活性物质主要是。
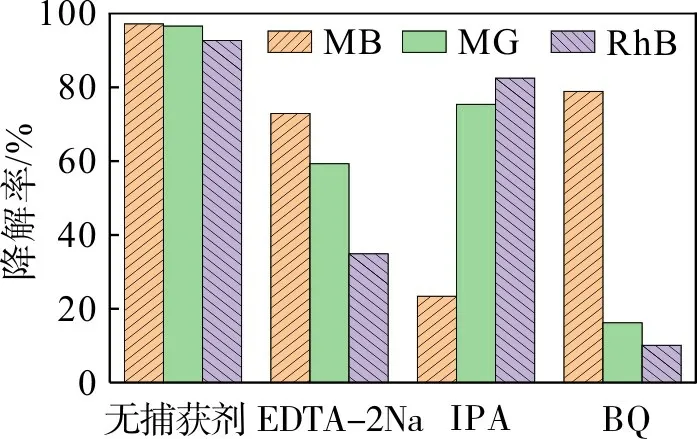
图10 添加不同捕获剂的染料降解率Fig.10 Degradation rates of dyes under different capture agents
3 结 论
1)g-C3N4/TiO2复合材料的物相、结构及形貌表征结果表明:g-C3N4与TiO2的杂化使g-C3N4的骨架结构发生变化,致使复合材料在可见光区域响应范围增大,吸光性能增强,具有更好的光催化性能。
2)1.0-g-C3N4/TiO2复合材料在可见光下催化降解染料的效果更佳,在光照150 min 的条件下,初始质量浓度为10 mg/L MB,MG,RhB 溶液的降解率分别达97.20%,96.60%,92.72%。1.0-g-C3N4/TiO2复合材料对初始质量浓度为10,20 mg/L MG溶液的降解效果差别较小;对于MB和RhB两种染料,其对初始质量浓度为10 mg/L 溶液的降解率大于初始质量浓度为20 mg/L溶液的降解率。
3)重复使用1.0-g-C3N4/TiO2复合材料5次后,MB 的光催化降解率仍能达到93.20%,复合材料表现出良好的稳定性和可重复利用性。该复合材料在可见光下降解3 种染料时,活性物质h+,·OH,均起积极作用,降解MB溶液过程中起主要作用的是·OH,降解MG和RhB溶液过程中起主要作用的是。
