成型Ru/PAC催化剂催化葡萄糖加氢制备山梨醇
2022-07-12向珏贻彭子康梁金花
向珏贻,彭子康,赵 晶,梁金花
(1.江苏德纳化学股份有限公司,江苏 南京 211599;2.南京工业大学 生物与制药工程学院,江苏 南京 211800)
作为化石燃料替代品的生物质衍生物在满足人们日益增长的能源需求及高附加值产品方面具有巨大的潜力[1-2]。据文献[3]报道,每年全球超过90%的生物质未被使用,而这些生物质可以用来作燃料或化学品。山梨醇是由6个C原子和6个羟基组成高附加值的糖醇,广泛运用于食品、医药和化妆品行业。主要用途是作为甜味剂、保湿剂、分散剂、增稠剂、生产维生素C,也可以生产山梨醇[4]、乙二醇[5]、丙二醇[6]、甘油[7]、戊二醇[8-9]、5-羟甲基糠醛[10]及各种聚合物的单体。
山梨醇可以通过葡萄糖加氢、生物技术及电还原技术制得,葡萄糖加氢是工业上使用最多的工艺,因为该产品的生产和加工步骤简单、反应温度和压力较温和,用于该工艺的镍基催化剂价格低廉。但该工艺的镍基催化剂在反应过程中Ni容易浸出到溶液中形成螯合物,增加了产品的净化提纯步骤,而且该催化剂催化葡萄糖制得的山梨醇选择性还有待提高,目前该反应工艺的核心仍然是寻找绿色高效且可循环的催化剂[11-13]。因此需要开发新的催化剂来替代镍基催化剂。已有文献[14]报道,糖类加氢催化剂的活性由大到小顺序是Ru、Ni、Rh、Pd。
为了替代镍基催化剂,研究者们开发了一系列贵金属催化剂如钌基催化剂,该类催化剂尽管成本较高,但葡萄糖的转化率及山梨醇的选择性好,而且在热稳定性、力学稳定性和催化剂的循环使用性较好;文献报道以Ru为催化剂、H2O为溶剂,可以提高糖类加氢的转化率[15-16],催化剂载体如C、SiO2及Al2O3是催化剂活性成分的分散剂、黏结剂及负载体,它们在不同反应条件下均可保持长期化学及力学稳定性。MCM载体的催化剂可以允许葡萄糖分子扩散及金属分散更好,这样可以使反应压力降低,底物的转化率及产品的选择性更高。Zhao等[4]、Wang等[17]、李洪波等[18]分别用Ru/Al2O3、Pd/Al2O3及Ru/MCM-41为催化剂,考察葡萄糖加氢制备山梨醇均取得较好的催化效果,这表明非贵金属Ru对葡萄糖加氢制山梨醇有较好效果。徐三魁等[19]采用Ru/C催化剂在0.5 MPa、120 ℃测得葡萄糖加氢生成山梨醇的催化活性、山梨醇选择性较好。
碳材料碳含量丰富、环境友好且价格低廉,有较大的比表面积,作为载体化学稳定性较好[20]。因此,活性炭因其具有大的比表面积而被选作科研及工业生产用的催化剂载体,为此,本研究从工业应用角度出发,首先在成型柱状活性炭上聚合高分子化合物,然后通过化学配位法将Ru负载到载体上制备成型Ru/PAC催化剂,然后考察该催化剂催化葡萄糖加氢制备山梨醇的催化性能及重复使用性能。
1 实验部分
1.1 实验试剂与仪器
苯乙烯(质量分数为99%,化学纯)、二乙烯苯(质量分数为80%,化学纯)、顺丁烯二酸酐(分析纯) 、浓盐酸(质量分数为36.5%,分析纯)为上海凌峰化学试剂有限公司;氨水、无水葡萄糖、无水乙醇、甲醇、过氧化苯甲酰、均为分析纯,购于国药集团化学试剂有限公司;水合氯化钌(Ru质量分数≥37.5%)、二乙烯苯(异构体混合物质量分数为80%)购于上海阿拉丁生化科技股份有限公司,成型活性炭载体(比表面积>1 000 m2/g、直径2 mm)购于福建鑫森炭业股份有限公司。
高效液相色谱(Prominence UFLC),日本岛津公司;电热鼓风干燥箱(DHG-9070A),上海一恒科学仪器有限公司;调温加热包(500 mL),温州市申通电热器厂;电子天平(EL204),天津大马衡量仪器有限公司;分析天平(METTLER TOLEDO),梅特勒-特利多仪器(上海)有限公司;高压釜(GSA-0.15L),威海威化机械厂。
1.2 催化剂的制备
1.2.1 活性炭载体处理
将具有一定的比表面积、孔径及直径的活性炭放入蒸馏水中超声去除孔道里的灰尘,烘干备用。根据文献[21-22],活性炭载体的处理方法如下:按照m(苯乙烯)∶m(过氧化苯甲酰)∶m(二乙烯苯)∶m(马来酸酐)=200∶1∶20∶200的质量比配制聚合液,将处理过的活性炭在聚合液中浸泡4 h,取出活性炭沥干,置于烘箱内,程序升温78 ℃ 2 h、85 ℃ 1 h、90 ℃ 1 h、110 ℃ 2 h,在活性炭表面形成聚苯乙烯-二乙烯苯-马来酸酐高聚物外壳;将聚合后的活性炭放入45 ℃氨水溶液中氨解2 h,静置后取出活性炭,用1 mol/L稀盐酸中和至中性,烘干后得到表面包裹氨解过的聚苯乙烯-马来酸酐活性炭载体(PAC)。载体的处理程序见图1。

图1 载体的处理流程Fig.1 Carrier preparation processing
1.2.2 Ru/PAC的制备
将PAC载体加入质量分数为0.5% RuCl3乙醇溶液(载体质量计),78 ℃浸渍回流14 h。滤渣放入高压反应釜中,在120 ℃、4 MPa H2压力下还原2 h,得到Ru/PAC催化剂,将还原得到的催化剂用去离子水冲洗至无Cl-滤出,烘干后的催化剂Ru/PAC。载体的处理和负载反应方程式如式(1)—(3)所示。

(1)

(2)

(3)
1.3 催化剂表征
BET(Brunauer-Emmett-Teller)测试可用于测量颗粒的比表面积、孔容、孔径分布。试样经过200 ℃真空脱气处理后,在北京精微高博科技有限公司出品的JW-BK122W型比表面及孔径吸附仪-196 ℃ N2吸附测定。比表面积和孔径分别通过BET和BJH(Barrett-Joyner-Halenda)方法计算得出;透射电子显微镜(TEM)是以极短波长的电子束作为光源,电子束可以穿透非常薄的载体,电子与试样中原子发生碰撞因其方向发生改变,从而产生了立体角散射,透射电子具有比扫描电镜更大的放大倍数、更高的分辨率,可以观察到材料的微观结构、晶体结构。本实验中,先将几毫克催化剂粉末通过超声分散在2 mL的乙醇中,然后将其滴在覆盖有50 μm多孔碳膜的Cu网上,通过JEOL JEM 2100F 显微镜以200 kV的加速电压下进行TEM分析。X线衍射(XRD)可以分析材料的晶体结构、晶胞大小等。本实验采用的是日本Rigaku公司生产的Rigaku Smartlab TM 9 kW的衍射仪,使用的是以Cu kα线作为激发源(λ=0.154 2 nm),电压为40 kV,电流为100 mA,角度范围为5°~60°;傅里叶红外光谱仪能测定有机分子官能团结构。本实验采用的是美国赛默飞公司生产 Nicolet iS5型号红外光谱仪,通过将所测催化剂与KBr混合压片来制备试样,测试范围为400~4 000 cm-1。
1.4 葡萄糖加氢实验
将质量分数为10 % 100 mL葡萄糖水溶液和1.5 g催化剂加入150 mL高压反应釜中,密闭,用H2置换3次以上保证釜内没有空气残留。调节稳压阀至4.0 MPa,打开加热炉电源,调节电压至50 V、搅拌器转速调至100 r/min,当温度升至130 ℃时,搅拌器转速调成500 r/min,加氢反应开始计时(加氢反应方程式见图2)。3.0 h后反应结束,静置冷却,打开反应釜,过滤出催化剂,洗涤催化剂,105 ℃真空烘干过夜以备下次使用,得到的滤液用岛津LC-20AD高效液相色谱分析成分,检测器为示差折光检测器,液相色谱柱为SC1011,柱温80 ℃,流动相为超纯水。葡萄糖的转化率和山梨醇的选择性分别如式(4)和式(5)所示。
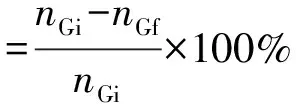
(4)

(5)
式中:nGi为葡萄糖初始摩尔量;nGf为葡萄糖反应后摩尔量;nS为反应后山梨醇摩尔量。

图2 葡萄糖加氢制备山梨醇Fig.2 Glucose hydrogenation to sorbitol
2 结果与讨论
2.1 催化剂表征
2.1.1 催化剂的BET表征
图3和表1分别为聚合前后吸附-脱附曲线、孔径分布和比表面积变化。从图3(a)可以看出,所有试样吸附脱附等温线均为Ⅰ型和Ⅳ型等温线。当处于低压区(0
0.4)时,随着压力增大,吸附量增大,出现了明显的滞后环,表明出现了毛细凝聚现象,表明材料中介孔和微孔同时存在[23-24]。表1表明,当活性炭聚合一层高聚物外壳后,比表面积骤然变小(从1 065.0降至508.0 m2/g),这可能是由于高聚物的高流动性使得吸附能力下降。当负载金属Ru后,发现滞后环明显缩小,这可能是由于加入金属会使PAC载体的介孔含量减少,从而导致比表面积下降。从图3(b)中还可以看出,无论是聚合还是负载金属,材料依然保持介孔(2~50 nm)结构。

图3 载体负载前后及催化剂的N2等温吸附(脱附)曲线及孔径分布Fig.3 N2 isotherm adsorption (desorption) curves and pore size distribution of carriers before and after polymerizing and catalyst

表1 活性炭聚合前后和金属负载前后比表面积、孔径和孔容
2.1.2 催化剂的TEM表征
图4是催化剂Ru/PAC的TEM图以及Ru金属簇的粒径分布图。由图4(b)可知,金属Ru的平均粒径为4.4 nm。图4(a)结果表明,Ru在载体PAC上分布均匀、粒子尺寸均一且粒径较小,没有团聚现象,说明PAC在浸渍过程中充分吸收了RuCl3乙醇溶液中的Ru离子,经过H2还原金属Ru具有良好的分散性,这有利于氢化反应的进行。这是由于核壳结构的载体有利于Ru纳米分散均匀,而且聚合物中引入的氨基和聚合物表面的羟基能与金属之间产生配位键,聚合物形成的网格状结构不仅为金属提供了稳定的支撑[17,25],提高了催化剂的力学强度和热稳定性。
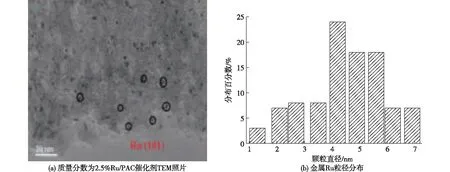
图4 质量分数为2.5% Ru/PAC催化剂TEM照片及金属Ru粒径分布Fig.4 TEM image and the corresponding Ru size distribution of mass ratio 2.5% Ru/PAC catalyst
2.1.3 载体和催化剂的XRD表征
测定聚合前后及Ru负载后的结构见图5。从图5可以看出,XRD图谱中的模糊峰表明宏观多孔的活性炭低结晶性,以及被聚苯乙烯-马来酸酐包裹的低结晶性。在AC、PAC及Ru/PAC试样中,可以观察到在24.7°左右出现C的衍射峰,属于活性炭特征峰,负载Ru之后特征峰呈弥散状,由于Ru的负载量小通常被载体所覆盖,无法观察到明显的Ru衍射峰,本实验选用负载质量分数为2.5%金属Ru, Ru/PAC仅在43.6°左右出现1个小峰[26],对应Ru(0)的[101]晶面,这表明Ru已经成功负载在PAC载体上。

图5 载体和催化剂的XRD表征Fig.5 XRD pattern of supporter and catalyst
2.1.4 Ru/PAC催化剂的红外表征

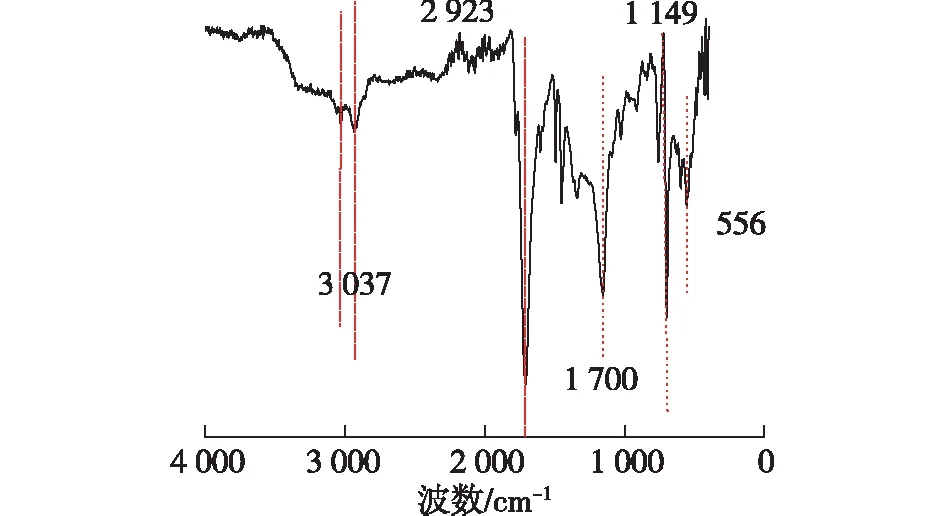
图6 Ru/PAC催化剂的红外光谱Fig.6 FT-IR spectrum of Ru/PAC catalyst
2.2 葡萄糖加氢工艺考察
2.2.1 不同金属催化剂对葡萄糖加氢的影响
本实验考察不同金属催化剂对质量分数为10%的葡萄糖加氢的影响,反应条件:反应温度为120 ℃、反应压力为3.0 MPa、转速为600 r/min,结果见表2。

表2 不同金属催化剂对葡萄糖加氢的影响
从表2可以看出,Ni催化剂催化葡萄糖加氢时,几乎无山梨醇产生,Pt催化剂和Pd催化剂用于葡萄糖加氢时,其产物山梨醇的选择性和葡萄糖的转化率都较Ru催化剂的活性要低,所以本实验优选Ru催化剂来研究催化剂量、反应温度及反应时间等单因素条件对葡萄糖加氢的影响。
2.2.2 不同催化剂量对葡萄糖加氢的影响
本实验是在研究催化剂量对质量分数为10%的葡萄糖加氢效果的影响,反应条件:反应温度120 ℃、反应压力为3.0 MPa、反应时间为3.0 h、转速500 r/min,结果如图7所示。

图7 催化剂量对葡萄糖加氢的影响Fig.7 Effects of different catalyst dosage on hydrogenation of glucose
从图7可以看出,在该反应条件下催化剂量会影响到葡萄糖的转化率,将催化剂的用量从0.5 g提高到2.0 g时,转化率从73%上升到86%。但再增加催化剂的用量至2.5 g时,转化率反而会逐渐下降至81%。这是由于增加催化剂的量时,反应物与催化剂上附着的反应基团的碰撞概率增加,转化率上升。但是催化剂用量过多,可能会导致搅拌不充分,催化剂聚集黏合在一起,使活性基团不能与反应物接触,从而引起转化率的降低。因此,本实验经分析后认为最佳催化剂用量为2.0 g。
2.2.3 反应温度对葡萄糖加氢的影响
由阿伦尼乌斯方程可知,温度对反应的影响很大。随着反应温度的增加,反应物分子之间碰撞的概率增大,化学反应的速率也随之增强,而糖液对温度很敏感,所以选择合适的反应温度显得尤为重要。
配制质量分数为10% 100.0 g葡萄糖水溶液并取2.0 g催化剂置于150 mL反应釜中,控制H2压力为4.0 MPa、搅拌器转速为500 r/min、反应4.0 h的条件下,考察温度对葡萄糖H2反应的影响,结果如图8所示。

图8 反应温度对葡萄糖加氢的影响Fig.8 Effects of different reaction temperature on hydrogenation of glucose
由图8可知,随着温度的增加,葡萄糖转化率迅速上升,温度到达130 ℃时,葡萄糖的转化率最高,可达91%。此时产物山梨醇的选择性一直保持在95%左右,之后再提高反应温度,葡萄糖的转化率及山梨醇的选择性急剧降低,这是由于高温使得糖液结焦(反应后试样液也变黄)导致葡萄糖的转化率和山梨醇的选择性下降。因此,本实验最佳反应温度为130 ℃,后续实验选取反应温度为130 ℃,对其他单因素进行考察。
2.2.4 反应时间对葡萄糖加氢的影响
配制质量分数为10%的葡萄糖水溶液100.0 g并取2. 0 g催化剂置于150 mL反应釜中,控制反应温度为130 ℃、H2压力为4.0 MPa、搅拌器转速为500 r/min的条件下,考察反应时间对葡萄糖加氢反应的影响,结果如图9所示。

图9 反应时间对葡萄糖加氢的影响Fig.9 Effects of different reaction time on hydrogenation of glucose
从图9可以看出,随着反应时间增加,葡萄糖转化率上升,当反应时间到达4.0 h时,葡萄糖的转化率最高可达91%,产物山梨醇的选择性一直保持在95%左右,之后再增加反应时间,葡萄糖的转化率缓慢降低。这是由于随着反应时间的延长,葡萄糖的异构化越发严重,导致葡萄糖的转化率下降。因此,本实验最佳反应时间为4.0 h,后续实验选取反应时间为4.0 h,对其他单因素进行考察。
2.2.5 反应压力对葡萄糖加氢的影响
配制质量分数为10% 100 g葡萄糖水溶液,再取催化剂2.0 g一同置于150 mL间歇反应釜中,控制搅拌器转速为500 r/min、反应温度为130 ℃、反应4.0 h的条件下,探究反应压力对葡萄糖加氢反应的影响,结果如图10所示。
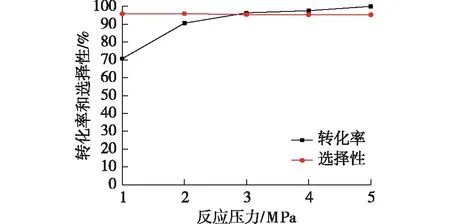
图10 不同反应压力对葡萄糖的转化率及山梨醇选择性的影响Fig.10 Effects of different reaction pressure on conversion of glucose and selectivity of sorbitol
由图10可知,当反应压力为2.0 MPa以下时,葡萄糖转化率较低,可能是溶解氢的压力过低影响了反应分子在活性位点上的碰撞。而当反应压力达到2.0 MPa以上,反应转化率较高,压力达到4.0 MPa以后,葡萄糖的转化率增加不是很明显,而山梨醇的选择性比较稳定[29],在此H2压力下,葡萄糖的转化率和山梨醇的选择性分别为91%和95%。综上所述,本实验中所选用的压力为4.0 MPa较好。
2.2.6 葡萄糖质量分数对葡萄糖加氢的影响
为了探究葡萄糖质量分数对催化反应的影响,配制了不同质量分数的葡萄糖来考察质量分数对葡萄糖加氢的影响,结果如图11所示。

图11 不同w(葡萄糖)对山梨醇收率的影响Fig.11 Effects of w(glucose) on the yield of sorbitol
从图11中不难发现,当葡萄糖的质量分数从10%上升到20%,底物的转化率和产物的选择性得到了提升,继续提高葡萄糖的质量分数,底物的转化率从95%下降到79%,山梨醇的选择性也随之下降。当葡萄糖的质量分数为20%时,葡萄糖的转化率和山梨醇的选择性达到最大。这是因为葡萄糖在Ru/PAC上的吸附差异造成的[30],在较低质量分数下,加氢速率随着质量分数的增加而增加,这是因为催化剂表面吸附无法达到饱和,当葡萄糖质量分数增至20%时,吸附达到饱和,底物的转化率和产物的选择性达到最大。当底物质量分数继续增加时,催化剂上吸附的葡萄糖过饱和,阻碍了H2在催化剂表面的吸附,导致葡萄糖的转化率降低及其山梨醇的选择性也降低。
因此,本实验的最佳底物质量分数为20%,此时的葡萄糖转化率为95%,山梨醇的选择性达到98%。
2.3 催化剂重复使用性能的考察
由以上所有结果可知,成型的Ru/PAC催化剂拥有良好的催化活性,实验还配制了质量分数为20%的葡萄糖在4.0 MPa、130.0 ℃、反应时间5.0 h的条件下考察催化剂工业应用的另一重要指标——催化剂的重复使用性能。每次葡萄糖催化加氢结束,对催化剂进行过滤、水洗,用于下一次使用,实验结果如图12所示。
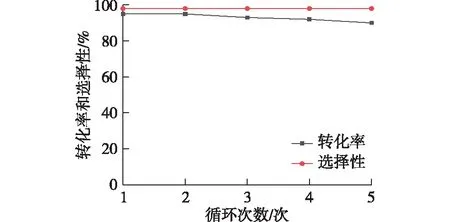
图12 催化剂重复使用对葡萄糖加氢的影响Fig.12 Effects of recycling times on hydrogenation of glucose
从图12可以看出,在该催化剂套用5次时,催化活性保持稳定,尽管有搅拌桨搅动球体催化剂,表面依然保持了较好的耐磨性能,葡萄糖的转化率及山梨醇的收率基本维持不变。由此可知,该类催化剂具有一定的稳定性,并具有潜在的工业应用价值。
3 结论
采用工业成型活性炭进行聚合处理,制备得到Ru/PAC,考察了该催化剂的最佳加氢工艺,结果表明该催化剂在4.0 MPa、130 ℃、反应时间5 h的最佳条件下,质量分数为20%葡萄糖的转化率及山梨醇的选择性分别为95%和98%,且该催化剂5次的重复使用表明,葡萄糖的转化率及山梨醇的选择性无明显降低,催化剂具有一定的稳定性,并具有潜在的工业应用价值。
