HPLC-ELSD 测定桔贝合剂中桔梗皂苷D 含量
2022-07-11洪挺章瑛周志强陈丹丹杨毅生
洪挺,章瑛,周志强,陈丹丹,杨毅生
1.江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029;2.江西中医药大学,江西 南昌 330004
桔贝合剂处方来源于重庆市中医研究所(原重庆市第一中医院)的院方制剂——桔贝糖浆,后改为合剂,但为了矫味,处方中仍保留了20%的糖量。桔贝合剂的处方主要由桔梗、浙贝母、苦杏仁、麦冬、黄芩、枇杷叶、甘草七味药材组成,具有润肺止咳的功效,临床上主要用于肺热咳嗽、痰稠色黄、咳痰不爽等[1]。据文献报道,桔贝合剂联合布地奈德治疗小儿支气管炎、肺炎的痊愈率与有效率均有提高[2]。桔梗作为处方中的君药之一,主归肺经,具有宣肺、利咽和排痰之功效。临床主治痰多、咳嗽,胸闷不畅,喉咙痛,声音嘶哑,肺痈吐脓等症状[3]。桔梗药材的主要化学成分为皂苷类、酚酸类、黄酮类、甾醇类等,而大量文献均报道桔梗皂苷D 是其主要活性成分,具有祛痰止咳、抗肿瘤、抗炎、护肝、杀精、抗动脉粥样硬化、免疫调节等良好的药理活性[4-10]。桔贝合剂现行标准为《卫生部药品标准·中药成方制剂》(第二册),该标准仅有性状与检查项,标准非常简单,亟须提高。经查阅文献发现目前对桔贝合剂的研究主要集中在浙贝母、黄芩的含量测定和枇杷叶的薄层鉴别研究,而对君药桔梗的研究未见报道[11-13]。本研究参照《中国药典》2020年版一部中桔梗药材的含量测定方法及有关文献报道[3,14-17],采用HPLC-ELSD 法对桔梗皂苷D 进行含量测定研究,以便更好地控制桔贝合剂的质量并保证其疗效的发挥。
1 仪器与试药
仪器:安捷伦1260Infinity Ⅱ型HPLC 色谱仪(美国安捷伦公司);ELSD 检测器(奥泰公司);Sartorius BT25S 电子天平(十万分之一,德国赛托利斯公司)。
试剂:乙腈为色谱纯,其余试剂均为分析纯。
对照品:桔梗皂苷D(批号:111851-201103,含量以96.9%计,中国食品药品检定研究院)。
样品:36 批次桔贝合剂(A 公司20 批次,B 公司9 批,C 公司7 批)。
2 方法与结果
2.1 溶液的配制
2.1.1 对照品溶液的制备 取桔梗皂苷D 对照品适量,精密称定,加甲醇溶解后,制成0.3 mg/mL 的溶液,即得。
2.1.2 供试品溶液的制备 精密量取桔贝合剂样品溶液20 mL,用水饱和正丁醇萃取4 次,每次30 mL,合并正丁醇液,用正丁醇饱和的氨试液洗涤2 次,每次40 mL,取正丁醇层,蒸干,残渣加甲醇适量使溶解,转移至5 mL 量瓶中,再用甲醇稀释至刻度,摇匀,即得。
2.1.3 阴性对照溶液的制备 取缺桔梗的其他药材,按处方工艺制成阴性样品,再按“2.1.2”的方法制备阴性对照溶液。
2.1.4 空白溶液的制备 取甲醇溶液,即得。
2.2 色谱条件与系统适用性试验
色谱柱:Phenomenex C18(250 mm×4.6 mm,4 μm);流动相:乙腈-水(25:75);柱温:20 ℃;ELSD 检测器,漂移管温度100 ℃;气体流速2.5 mL/min。理论板数按桔梗皂苷D 峰计算应不低于3 000。
精密吸取上述供试品溶液、对照品溶液、阴性对照溶液及甲醇的空白溶液各10 μL,按上述色谱条件测定,比较对照品溶液、供试品溶液、阴性样品溶液及空白溶液的色谱图,结果阴性样品及空白均无干扰,见图1。

图1 HPLC色谱图:A.桔梗皂苷对照品;B.供试品;C.阴性样品;D.空白
2.3 线性关系的考察
精密称取10.46 mg 桔梗皂苷D 对照品,置10 mL 量瓶中,加甲醇超声溶解后,再稀释至刻度,摇匀,作为对照品母液。再精密吸取该母液1、2、3、5 mL,分别置10 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品稀释液,精密吸取对照品稀释液和母液各10 μL 进样测定,以Y(Lg 峰面积)为纵坐标,X(Lg 进样量)为横坐标,作回归方程,桔梗皂苷D 回归方程为Y=1.581 7X+2.295 3,r=0.999 9。结果见表1。结果表明桔梗皂苷D 进样量在1.013 6~10.135 7 μg 之间与峰面积呈良好对数线性关系。

表1 桔梗皂苷D线性关系测定结果
2.4 精密度试验
取对照品溶液,按“2.2”项下HPLC 条件,连续进针6 次,结果桔梗皂苷D 峰面积相对标准偏差为3.5%,符合实验测定要求。
2.5 重复性试验
取样品(C 公司,批号:19090030)6 份,照“2.1.2”项下方法制备成供试品溶液,测定,结果桔梗皂苷D 的平均含量为0.18 mg/mL,相对标准偏差为0.1%,表明该方法重现性良好。
2.6 稳定性试验
取同一份供试品溶液,按“2.2”项下HPLC 条件,按间隔时间要求进样,结果桔梗皂苷D 色谱峰面积在24 h 内无明显变化,相对标准偏差为0.6%,表明桔梗皂苷D 在24 h 内稳定性良好。
2.7 回收率试验
采用加样回收试验,精密量取重复性项下已经测定含量的本品(C 公司,批号:19090030,含桔梗皂苷D 0.18 mg/mL)6 份,每份10 mL,分别置分液漏斗中,精密加入桔梗皂苷D 对照品溶液(浓度1.013 6 mg/mL)2 mL,再按“2.1.2”项下方法萃取4 次,每次30 mL,其余步骤同法操作,计算回收率,结果详见表2。

表2 桔梗皂苷D回收率试验结果
2.8 耐用性试验
取样品,照“2.1.2”项下方法,分别采用Phenomenex C18 柱(250 mm×4.6 mm,5 μm)、Thermo-C18 柱(250 mm×4.6 mm,5 μm),Sunfire-C18 柱(250 mm×4.6 mm,5 μm)3 种不同品牌的色谱柱进行耐用性考察,结果桔梗皂苷D 在上述色谱柱中均分离良好,桔梗皂苷D 测定结果相对标准偏差为2.5%,桔梗皂苷D 含量差异无统计学意义,耐用性符合要求。
2.9 样品测定
取样品36 批,照前述方法制备和测定,从测定结果可知,不同企业样品中桔梗皂苷D 含量差异巨大,其中A 公司样品桔梗皂苷D 含量普遍偏低,且批间差异大。测得不同企业桔梗皂苷D 所测含量最高值比最低值高11 倍。测定结果见表3。
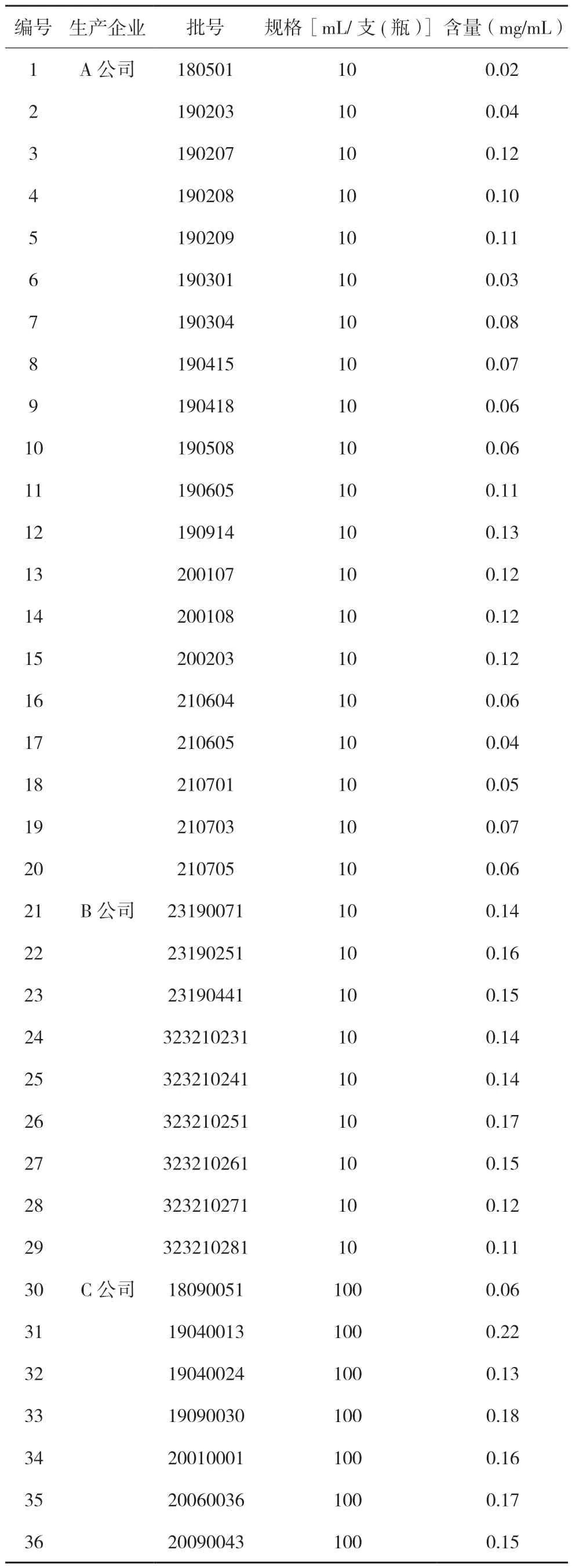
表3 桔贝合剂样品测定结果
3 讨论
桔梗作为桔贝合剂处方中的君药之一,对其质量进行控制存在必要性,而桔梗皂苷D 又是桔梗的主要活性成分,选用其作为含量测定指标,研究意义大且专属性较好。本研究在前期对桔梗皂苷D 进行紫外扫描,发现其紫外吸收弱,因为桔梗皂苷D 没有共轭基团,只有一个碳碳双键[18],故而不能用紫外检测器进行检测。ELSD 检测器不依靠被检测样品的光学特性,对无紫外或紫外吸收较弱的样品均可检测,且ELSD 的响应值是与样品质量成正比[17,19]。所以本研究选用HPLCELSD 方法对桔梗中的桔梗皂苷D 进行含量测定。经过多次色谱条件及样品前处理等条件的摸索,最终选择以乙腈-水(75∶25)为流动相进行等度洗脱、以水饱和的正丁醇作为提取媒介,ELSD的漂移管温度100 ℃,气体流速2.5 mL/min,此时的基线平稳、峰形对称、主峰与其他峰无干扰、杂质峰较少。
从测定结果可知,不同企业样品中桔梗皂苷D含量差异巨大,其中A 公司样品桔梗皂苷D 含量普遍偏低,且批间差异大。测得不同企业桔梗皂苷D 含量最高值比最低值高11 倍。桔梗药材在处方工艺中仅经水煎煮,工艺简单,造成桔梗皂苷D 含量差异大,可能是不同企业所用桔梗药材质量差异造成的。由此可见,对桔梗药材的质量进行控制有一定的必要性与紧迫性。
