高炉块状带喷吹页岩气化学反应热力学研究
2022-07-08秦跃林高绪东胡景兰
李 鑫 秦跃林 高绪东 胡景兰
(重庆科技学院 冶金与材料工程学院, 重庆 401331)
0 前 言
在31个制造业中,钢铁业的碳排放量最大,承担着较大的减排压力,钢铁企业低碳转型的任务迫在眉睫[1-2]。我国钢铁业吨钢CO2排放量约为 1.7~1.8 t,高炉炼铁及前端所产生的CO2占整个钢铁业的80%[3]。为了更好地实现高炉减排,研究人员提出了由“碳冶金”过渡至“氢冶金”的技术路线[4]。在这一过程中存在一个过渡状态 —— 富氢冶金,此过程通过碳氢元素的共同作用实现高炉内的化学反应[5-6]。天然气是北美钢铁企业常用的还原剂,但我国天然气价格相对昂贵,无法大规模应用于工业。页岩气与天然气成分相近,且我国页岩气储量丰富,因此未来页岩气有望应用于高炉生产[7]。
为探究还原气体对还原过程的影响,提出一种仅由CO、H2、CH4还原Fe2O3的简化炼铁模型。在反应温度为900 ℃的条件下,通过气体利用率、还原气体使用量、反应能耗等指标,综合评价不同还原气体对Fe2O3的还原效果。
1 基本原理
1.1 基本定义
生产能耗,是指在一定温度和足量反应物的条件下,生产1 mol Fe的能耗。
最佳气体还原量(nBR),是指在一定条件下生成1 mol Fe所需的还原气体量,此时的气体利用率为还原气体的实际有效利用率(ηI)。
1.2 炼铁模型
建立CH4、H2、CO还原Fe2O3的简化炼铁模型,模型假设条件如下:
(1) 忽略反应及传热过程的动力学影响,仅探讨反应方向和限度。
(2) 忽略实际炼铁过程中灰分、碱金属等物质对还原过程的影响。
在等压封闭体系中,能量变化等于相应的焓变,如式(1)所示:
(1)

在最小吉布斯自由能模型的基础上对平衡组分进行计算,还原系统的初始和平衡状态如图1所示。
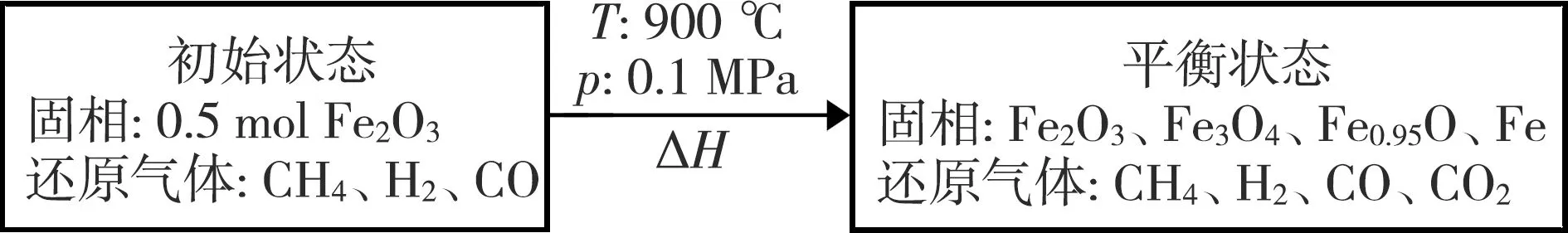
图1 还原系统的初始和平衡状态
单一还原气体的利用率,是指还原气体对应的氧化产物与反应后气相各组分之和的比值[8-9],如式(2) — 式(4)所示:
(2)
(3)
(4)
当CO、H2、 CH4共同参与反应时,其利用率可表示为:
(5)
式中:ηCO、ηH2、ηCH4分别表示CO、H2、CH4的利用率,%;η(CO+H2+CH4)表示 CO、H2、CH4混合条件下的综合利用率,%;φCO、φCO2、φH2、φH2O、φCH4分别表示平衡状态下CO、CO2、H2、H2O、CH4的体积分数,%。
1.3 实验条件
本次研究的实验条件是:压力为0.1 MPa;反应温度为900 ℃;还原气体包括CO、H2、CH4,气体增量为20%;初始固相Fe2O3为0.5 mol。实验目的是研究不同还原气体对还原产物、气体利用率和能耗等指标的影响。
2 实验结果分析
2.1 单一气体对还原反应的影响
采用单一CO、H2、CH4气体,分别对Fe2O3进行还原。初始还原气量对Fe2O3还原反应的影响,如图2所示(图中nH表示还原产物物质的量;nCO、nH2、nCH4分别表示CO、H2、CH4物质的量)。根据初始还原气量与平衡产物之间的关系,将整个还原过程划分为α、β、γ等3个阶段。

图2 单一CO、H2、CH4初始量对Fe2O3还原反应的影响
α阶段:当初始还原气量较少时,还原产物为Fe2O3和Fe3O4。随着初始还原气量的增加,Fe2O3的含量逐渐减小为0,Fe3O4含量逐渐增至最大值。随着初始还原气量持续增加,Fe3O4向固溶体(FeO+Fe2O3)转变,固溶体中Fe2O3含量先增加后减少,当FeO含量达到最大值时,α阶段结束。α阶段存在2个气体利用率平台:第1个气体利用率平台对应的物质转变为Fe2O3→Fe3O4;第2个气体利用率平台对应的物质转变为Fe3O4→固溶体。
β阶段:此阶段的含铁产物包含了Fe和固溶体。随着初始还原气量的增加,当固溶体逐渐减少为0,Fe含量由0逐渐增大至最大值时,β阶段结束。β阶段存在第3个气体利用率平台,其对应的物质转变为固溶体→Fe。此时气体利用率为还原气体的实际有效利用率(ηI),对应的还原气体量为最佳气体还原量(nBR)。
γ阶段:此阶段含铁产物中仅含有单质Fe,且含量恒定。随着初始还原气量的增加,气体利用率逐渐下降。
由图2可知,不同还原气体的利用率变化情况大致相同:当还原气量极少时,气体利用率接近100%;当还原过程处于第1个气体利用率平台时,CO、H2、CH4的利用率分别为80.98%、84.24%、83.15%;α、β、γ阶段所需的还原气量由大到小依次为CO、H2、CH4。
当还原气体为CO时,其气体利用率变化情况如图2a所示。当β阶段结束时,ηI-CO=30.26%,nBR-CO=4.97 mol。当CO物质的量为0~0.21 mol时,Fe2O3逐渐被还原为Fe3O4;当CO物质的量为0.22~0.43 mol时, Fe3O4向固溶体进行转变,含铁产物中再次出现少量的Fe2O3,此阶段的ηCO=80.98%;当CO物质的量为0.43~4.97 mol时, Fe2O3与FeO的摩尔比为定值,nFe2O3∶nFeO=0.05∶0.95。
当还原气体为H2时,其气体利用率变化情况如图2b所示。β阶段结束时,ηI-H2=35.19%,nBR-H2=4.26 mol。与CO相比,H2的利用率提高了4.93%。
当还原气体为CH4时,其气体利用率变化情况如图2c所示。β阶段结束时,ηI-CH4=33.53%,nBR-CH4=0.74 mol。与CO和H2相比,CH4作为还原剂时有以下特点:
(1) Fe2O3转化为Fe3O4时,所需的气体量大幅减少,α阶段大幅缩短。
(2) 固溶体分解阶段的反应更加剧烈,受气体浓度的影响也更大。
(3) 在γ阶段,CH4参与反应的程度高。
2.2 2种气体混合对还原反应的影响
如图3所示,当CO和H2按不同比例混合,各反应阶段的变化趋势大致相同。β阶段随着H2比例的增加而缩短,按照H2占比由大到小(nCO∶nH2分别为2∶8、4∶6、6∶4、8 ∶2)的顺序,混合气体的ηI依次为34.18%、33.17、32.19%、31.21%,混合气体的nBR依次为4.39、4.53、4.67、4.82 mol。这表明增大H2比例,可以提高混合气体的利用率、提升气体的还原能力。

图3 CO和H2混合气体初始量对还原反应的影响
如图4所示,CO和CH4按不同比例混合,各反应阶段的趋势大致相同。β反应阶段的跨度随CH4比例增加而缩短,按CH4占比由大到小(nCO∶nCH4=2∶8、4∶6、6∶4、8∶2)的顺序,混合气体的ηI分别为33.28%、32.93%、32.44%、31.62%,混合气体的nBR分别为0.91、1.14、1.53、2.34 mol。这表明增大CH4比例,可以提高混合气体的利用率,强化气体的还原能力。
如图5所示,CO、H2、CH43种气体按不同比例混合,各反应阶段的变化趋势大致相同。按nCO∶nH2∶nCH4为2∶2∶6、2∶4∶4、2∶6∶2、4∶2∶4、4∶4∶2、6∶2∶2的顺序,混合气体的ηI依次为33.76%、33.53%、33.77%、32.99%、32.07%、32.23%,nBR依次为0.98、1.50、1.52、2.27、2.31 mol。通过CO、H2、CH4这3种气体对比分析发现,气体利用率并不是按照气体比例的变化而变化的,其利用率存在相互耦合的关系。
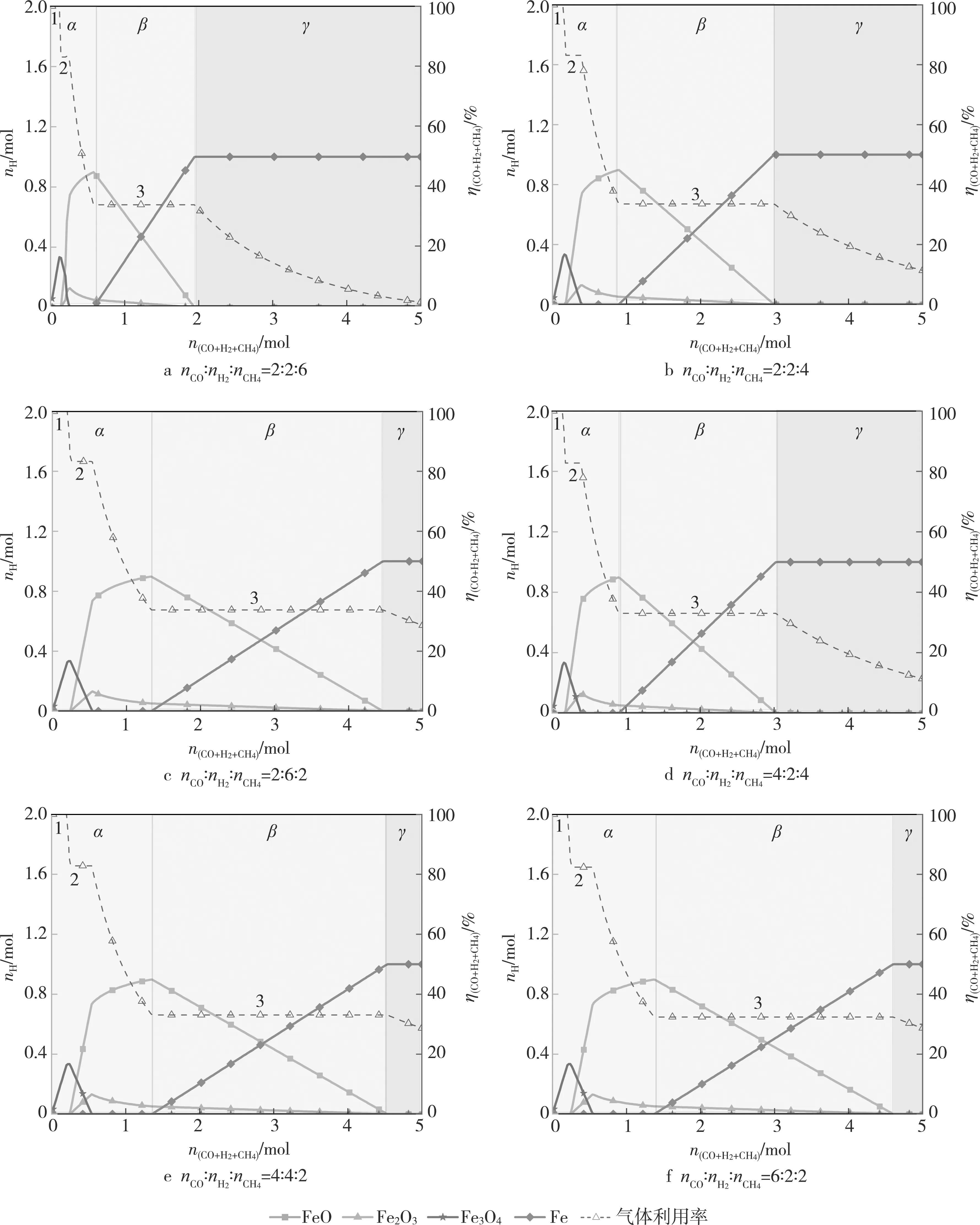
图5 CO、H2和CH4混合气体初始量对还原反应的影响
3 还原气体最佳配比的确定
首先,采用Equip模块计算反应前后的气相成分;然后,采用Reaction模块计算反应的焓变,结果如表1所示。

表1 还原气体在不同条件下的参数
3.1 不同混合条件下的耦合关系
通过Equip模块,计算还原气体在不同配比条件下的ηI、nBR,记为ηI-c、nBR-c;采用纯气体加权的方式,计算出还原气体在不同配比条件下的ηI、nBR,记为ηI-t、nBR-t。以ηI为例,若ηI-c优于ηI-t,则说明不同气体之间存在相互促进的耦合关系,反之则说明不同气体之间存在相互抑制的耦合关系。气体利用率提升比例(R)的计算公式如式(6)所示:
(6)
不同混合条件下,气体的耦合关系如图6所示。当CO和H2混合时,R为负。这表明CO和H2存在相互抑制的耦合关系,随CO占比的增加抑制关系逐渐增强,但R仅为0~-0.5%,影响不大。当CO和CH4混合时,R为正,且R随CH4占比的增大而增大,当nCH4∶nCO=4∶6时,R达到最大,这表明CH4和CO存在相互促进的耦合关系。当CO、H2、CH4混合时,气体最大利用率为32.19%~33.61%,R存在正负波动。这表明当CO、H2、CH4混合时,不同配比下的耦合关系不同。当nCO∶nH2∶nCH4=2∶4∶4时,R接近0,表明此时气体之间的促抑制关系相互抵消最多。

图6 还原气体不同混合条件下的耦合关系
混合气体初始量对其利用率的影响,如图7所示。还原过程中的3个阶段,重点在α和β阶段。
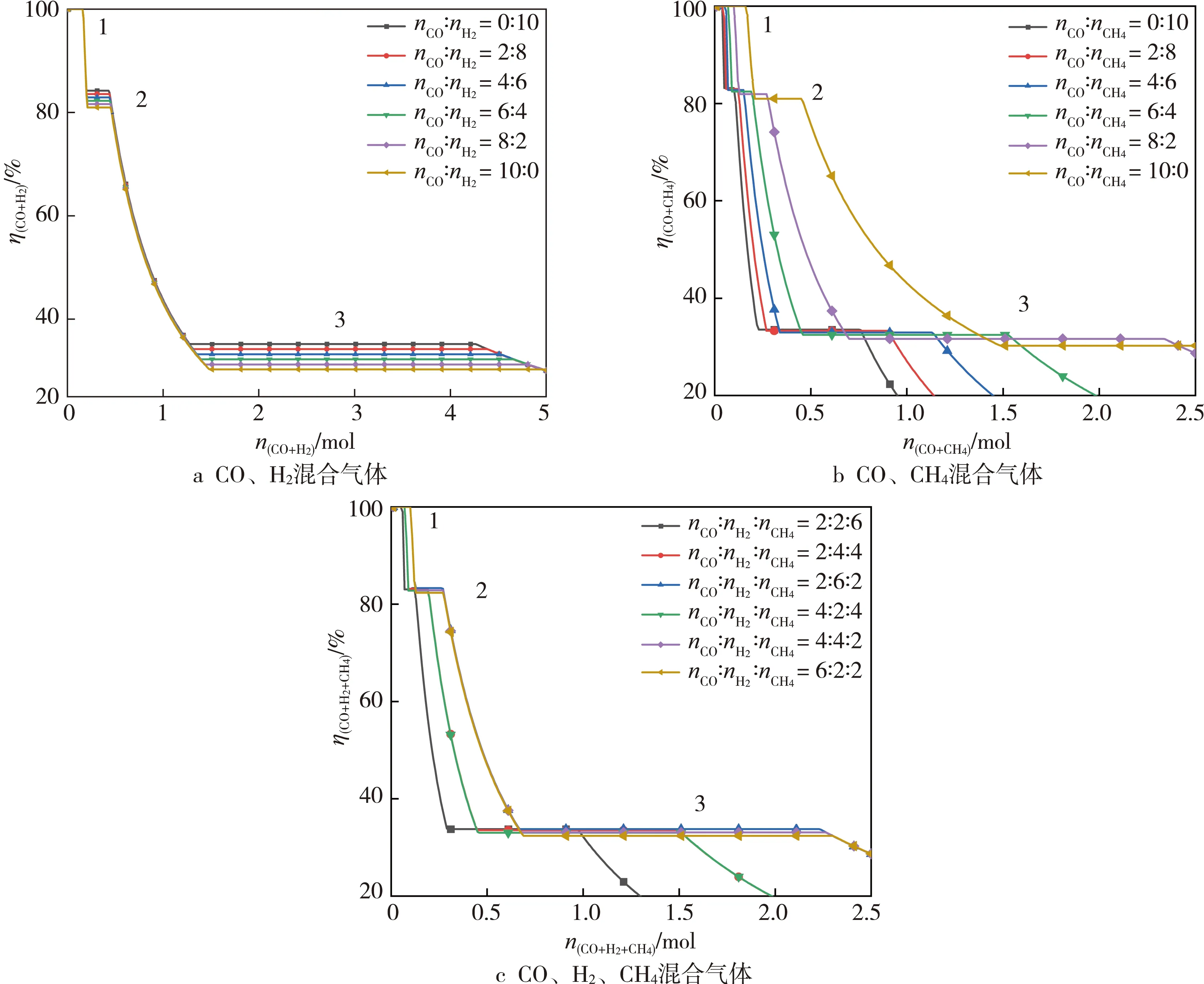
图7 混合气体初始量对气体利用率的影响
当CO和H2混合时, 非还原反应阶段出现明显的重叠,这表明CO和H2含量不会影响此阶段的气体利用率。第2、3利用率平台相互平行,混合气体的利用率随H2占比的增大而逐渐增大。
当CO和CH4混合时,非还原阶段出现明显分离,且CH4含量越多气体利用率变化越明显,这说明CH4含量对还原反应影响较大。
6种配比方案中, CH4占比相同的曲线在非还原阶段的气体利用率出现重合,而CO和H2比例变化对此并无影响。这表明在此条件下,CH4含量是气体利用率变化的决定性因素,CH4含量越多,气体利用率的变化越明显。
3.2 不同混合条件下的焓变
CO、H2和CH4按不同比例混合,其焓变情况如图8所示。当反应温度为900 ℃时,1 mol焦炭燃烧生成CO所释放的热量为113.2 kJ。根据最低碳耗理论可知[10],吨铁生产过程中的最低碳耗点rd为20%~30%。本次研究取rd=25%,此时,间接还原可获得的热量为28.3 kJ,图中矩形A区域的配气方案可以满足该条件。符合条件的配气方案为:纯CO;nCO∶nH2为8∶2、6∶4、4∶6;nCO∶nCH4为8∶2;nCO∶nH2∶nCH4为6∶2∶2。
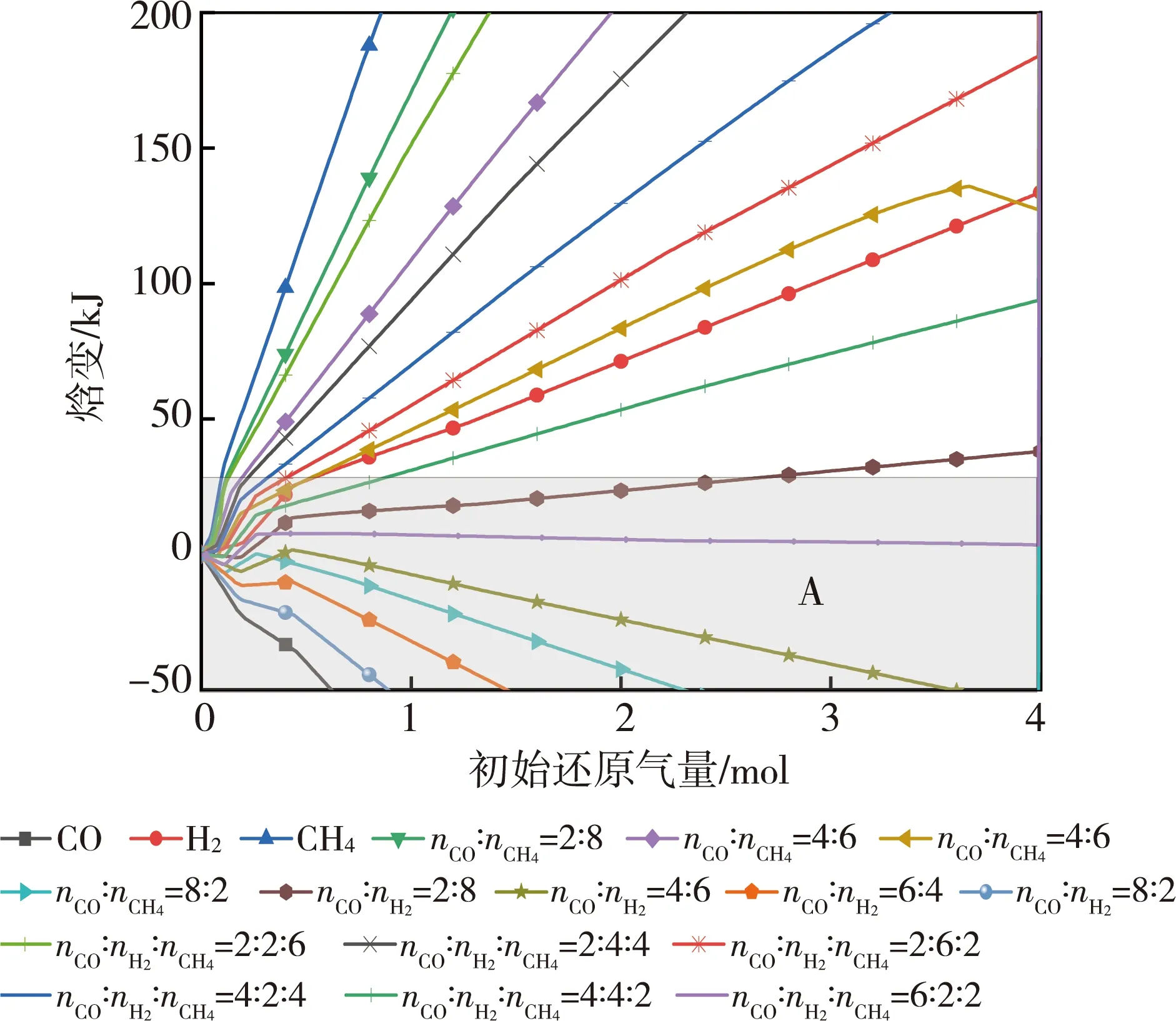
图8 还原气体能耗分析
4 结 语
在还原反应的α阶段,H2和CO的利用率不随混合气体配比的变化而变化。向炉内加入CH4,可以在一定程度上提升气体利用率,有效减少还原气体的使用量。当反应温度为900 ℃时,还原气体利用率之间的促抑制关系微弱。在最低碳耗理论基础上分析可知,符合条件的配气方案为:纯CO;nCO∶nH2为8∶2、6∶4、4∶6;nCO∶nCH4为8∶2;nCO∶nH2∶nCH4为6∶2∶2。
