UiO系列金属-有机骨架材料在重金属离子去除中的应用1
2022-07-06赵瑞明叶代杰高梓翔洪远哲孙瑜李岭领龙清华
赵瑞明,叶代杰,高梓翔,洪远哲,孙瑜,李岭领,3,龙清华
(1.广东石油化工学院,广东 茂名 525000;2.景德镇陶瓷大学 材料科学与工程学院,江西 景德镇 333403;3.广东广油华丰科技研究有限公司,广东 潮州 515700)
重金属污染日益成为一个全球性的环境问题[1]。与沉淀法、膜分离法、混凝/絮凝法、光催化法、反渗透法、氧化/还原法、生物处理法等各种水净化技术相比,吸附法由于其具有设计灵活、操作方便、成本低、易再生等优点,被认为是去除重金属最有效、简便的方法。
与传统的沸石和活性炭吸附材料相比,金属-有机框架材料(MOFs)具有其无法比拟的独特优势。首先,由于MOFs是由无机金属簇和有机配体经配位键桥连组成,无机金属簇和有机配体[2]以及它们之间配位方式的多样性决定了MOFs结构的多样性;其次,多数经典MOFs具有很高的比表面积(1000~10000 m2/g)[3],远超过传统多孔材料;更为重要的是,MOF材料易于进行功能化修饰且其孔道结构和孔尺寸具有可设计性和调控性的特点。这些独特性质使得MOFs在吸附分离、催化、分子识别、药物控释、电化学等诸多领域有广阔的应用前景。近年来,由UiO-MOFs(UiO-66, UiO-67, UiO-68, UiO-69)构建的三维多孔纳米复合材料,因其具有相对均匀、大孔径、高比表面积、强稳定性等特性,得到了广泛的研究和应用。
1 UiO-MOFs介绍
在MOFs的大家族中,从2008年起陆续报道的以锆为金属中心、芳香族多羧酸化合物为有机配体的锆基MOFs(Zr-MOFs)表现出丰富的结构类型和独特的性质,尤其是优于绝大多数MOFs的热稳定性(450 ℃左右)、化学稳定性(耐水、苯、丙酮等有机溶剂)以及机械稳定性,使它受到了研究者们极大的重视与关注[4]。
UiO-MOFs是由Zr4+和二羧酸配体构成的三维多孔材料,图1总结了代表UiO-MOFs结构(a)和共同UiO-MOFs合成有机配体(b)。Zr6O4(OH)4分别与十二配体配位,形成一个由一个八面体中心孔笼和八个四面体构成的三维结构。由于Zr—O键的结合能力较强,UiO-MOFs的合成逐渐集中在功能化或配体长度的变化上,以期对UiO-MOFs的物理/化学性质、孔径和形貌进行调控。到目前为止,相关研究人员已经报道了多种不同的UiO-MOFs合成方法,如溶剂热法、微波法、挥发法、扩散法、模板法、超声波法和机械搅拌法等。
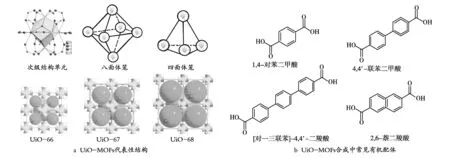
图1 UiO-MOFs结构和配体
2 UiO-MOFs及其复合材料的合成、应用
虽然MOFs具有很强的吸附重金属离子的能力,但原始MOFs中的有机配体往往缺乏活性官能团,导致其吸附能力和选择性不理想。而且MOFs的吸附能力在很大程度上取决于其官能团和可控的孔道结构,其中,官能团是影响其对重金属离子的吸附能力的关键因素[5]。因此,增加MOFs表面的官能团是提高其吸附性能的有效途径之一。通过对合成过程的调控赋予其更多的功能性活性位点,在成本方面具有优势;相比之下,对原始MOF进行功能化修饰,使其具有所需的活性官能团,使其更容易获得螯合位点进一步加速了MOFs对重金属络合的吸附能力。
2.1 后合成改性UiO-MOFs
UiO-66被认为是具有较多修饰性的最稳定的MOFs之一。赵旭东等[6]在UiO-66的基础上,合成了一系列具有不同官能团的水稳定的UiO-66-X(其中X为H、Br、NH2、NH-(CH2)2-SO3H、2COOH)对水溶液中的Cu2+进行选择性去除。由于两个羧基对相邻有机配体独特的螯合作用以及Jahn-Teller效应,在文献报道的10种吸附剂中,UiO-66-(COOH)2对Cu2+/Ni2+的选择性最高,达到27左右,且去除速度快,稳定性和可再生性好。
赵旭东等还报道了一系列羧基接枝的金属-有机框架材料(UiO-66-(COOH)n,其中n=0、1、2、4)用于Pb2+去除并探究羧基在Pb2+中的重要作用[7]。UiO-66-(COOH)2在pH=4.8时对Pb2+的最大吸附量为420.2 mg/g,远远高于UiO-66、UiO-66-COOH以及UiO-66-(COOH)4对Pb2+的最大吸附量。通过FT-IR、XPS和DFT理论计算表明,羧基和合适的孔结构的协同作用在Pb2+的捕获中起着关键作用。
鉴于NH2-UiO-66易于功能化的特点,暴露的氨基可以作为与其他配体连接的反应位点,通过后合成改性的方式可以进一步提高其对重金属离子的吸附能力和选择性。
王仕兴课题组针对NH2-UiO-66进行了一系列的修饰改性[8],以获得对不同重金属离子的吸附能力。用1,4-苯二羧酸盐与ZrCl4在DMF和HCl的混合溶液中反应,获得NH2-UiO-66纳米颗粒,再用DMTD对其进行改性,通过引入硫化氢基团[8]来增强其对Hg2+的吸附能力(见图2a)。经过DMTD修饰的NH2-UiO-66(DMTD-UiO-66)对Hg2+的吸附量从145.1 mg/g增加到670.5 mg/g。
该课题组[9]利用间苯二甲酸RSA修饰NH2-UiO-66,通过醛胺缩合选择性去除Pb2+(见图2b)。RSA的主要目的是增加NH2-UiO-66中的羟基数目,对Pb2+的实际最大吸附量从46.9 mg/g提高到189.8 mg/g,去除率由29.8%提高到78.9%。
该课题组[10]又利用L-半胱氨酸修饰NH2-UiO-66,制备Cys-UiO-66用于选择性去除Hg2+(见图2c)。得到的Cys-UiO-66纳米颗粒对Hg2+的吸附量为350.14 mg/g,远高于未经改性的NH2-UiO-66(112.68 mg/g)。
最近,该课题组又采用硫辛酸对NH2-UiO-66(TA-UiO-66)进行改性,以增强其对废水中Au离子的承载能力[11](见图2d);TA改性使最大Au3+吸附量从158 mg/g提高到372 mg/g。TA-UiO-66对Au3+具有较高的选择性,吸附量大,原因可能是S/N与Au之间存在两种螯合作用。随后该课题组通过巯基-1,3,4-硫代二唑(MTD)修饰Zr-MOFs[12],以提高其对Au3+(见图2e)的吸附能力和选择性。MTD-UiO-66的最大吸附量为301.5 mg/g。以GD-UiO-66为中间体,该课题组[13]还与6-氨基硫脲嘧啶功能化合成了TA-UiO-66用于吸附Pb2+。在上述改性中,醛氨基缩合起着重要作用,由此表明醛氨基缩合反应也用于MOFs后合成改性的修饰。
2.2 MOF基微米/纳米复合材料
基于协同效应,复合材料通常表现出优异的性能。将其他材料(如金属氧化物和/或纳米颗粒)掺入MOFs中可以对其功能和表面积起到调控作用。同样,研究人员也找到了将MOFs与其他功能材料结合的方法,以增强其吸附和分离能力。
黄理金等[14]采用原位生长的方法,在纳米尺度的Fe3O4@SiO2核(约15 nm)表面包覆一层Zr-MOFs(约5 nm)壳层。Fe3O4@SiO2@UiO-66-NH2对Pb2+最大容量为102 mg/g,可能是NH2基团的引入提供了更多的吸附位点,而且可以通过螯合作用与Pb2+相互作用增强吸附。
綦鹏飞等[15]设计并制备了磁性核壳结构Fe3O4@TA@UiO-66微球吸附剂。Fe3O4@TA@UiO-66对As3+和Sb3+具有良好的吸附性能,吸附量分别为50.3 mg/g和97.8 mg/g。
MOF@MOF结构由于可调节的孔隙和丰富的表面活性位点,在吸附方面非常有应用前景。李林澄等[16]设计了一种表面活性剂功能化的磁性MOF@MOF吸附剂(Fe3O4@UiO-66@UiO-67/CTAB),并将其用于吸附水中Cr6+。结果表明,虽然Fe3O4掺入和CTAB功能化均降低了孔体积和比表面积,却会使材料孔隙增大。Fe3O4@UiO-66@UiO-67/CTAB的大孔径可能更有利于Cr6+吸附。
通常一种优秀的吸附剂应该能够同时去除多种重金属离子。CeO2纳米粒子对各种重金属离子具有良好的吸附活性,但与其他无机纳米颗粒一样,其实际应用也受到溶液中易团聚的限制。将纳米颗粒固定在另一种基质上成为一种替代方法[17]。Olivera等设计制备了一种含CeO2的UiO-66-(SH)2纳米吸附剂,CeO2/UiO-66对Pb2+、Cu2+、Hg2+、(Cr3+、Cr6+)、Cd2+、(As5+、As3+)的去除率分别为3%、0%、1%、(35%、62%)、0%、(99%、24%);UiO-66-(SH)2对Pb2+、Cu2+、Hg2+、(Cr3+、Cr6+)、Cd2+、(As5+、As3+)的去除率分别为97%、99%、91%、(99%、57%)、97%、(88%、26%);CeO2/UiO-66-(SH)2对Pb2+、Cu2+、Hg2+、(Cr3+、Cr6+)、Cd2+、(As5+、As3+)的去除率分别为99%、99%、98%、(93%、93%)、87%、(56%、56%)。
2.3 3DMOF在重金属离子去除中的应用
作为一种优异的重金属离子吸附剂,MOFs在去除水溶液中污染物方面的功能得到了广泛的关注。然而由于其材料自身的结晶性使它多以粉末形式存在,不利于回收利用。将MOFs与适当基底材料(如金属板、泡沫和多孔管)结合,是实现其功能化回收再利用的一种有效方法。
雷超等[18]以纤维素气凝胶CA为基底材料,通过简单的原位生长,制备得到了金属-有机框架材料@纤维素气凝胶复合材料(UiO-66@CA、UiO-66-NH2@CA)。UiO-66@CA和UiO-66-NH2@CA对Pb2+的平衡吸附容量分别为81.30 mg/g和89.40 mg/g,对Cu2+的平衡吸附容量分别为31.23 mg/g和39.33 mg/g。纯的CA对Pb2+和Cu2+的吸附能力非常低,分别为5.62 mg/g和5.85 mg/g。所获得的MOFs@CA复合材料可以很容易地从废水中分离,没有任何二次污染。这种优异的可重复使用性和易分离性能使MOFs@CA复合材料成为去除废水中重金属离子的理想选择。
Jamshidifard等[19]通过微波加热法制备了PAN/chitosan/UiO-66-NH2(PAN代表聚丙烯腈)复合纳米纤维,可通过吸附和膜过滤去除Pb2+、Cd2+和Cr6+离子。当MOF质量分数为10% 时,PAN/chitosan/UiO-66-NH2纳米纤维中吸附位点(UiO-66-NH2中具有功能化官能团如羧基、氨基以及最高比表面积)的增加导致其对Pb2+、Cd2+和Cr6+离子的最大吸附量为441.2,415.6,372.6 mg/g。研究发现当纳米纤维膜厚度为50 μm、UiO-66-NH2质量分数为10%时,PVDF/PAN/chitosan/UiO-66-NH2膜在18 h内具有较高的水通量和高金属离子去除能力。
3 结语与展望
与传统多孔材料相比,以UiO-66为代表的复合材料具有良好的力学和热稳定性、可调的孔道结构、合成可调控和高比表面积等优点,作为吸附剂在去除中金属离子应用中得到广泛研究,并取得了良好的吸附效果,可以为重金属污染治理提供有效的新途径,改善生态环境安全。
然而,UiO-MOFs粉体吸附剂在应用于重金属离子吸附方面仍存在巨大的挑战。(1)绿色合成方法:MOFs传统合成方法多为水热合成,反应需要消耗大量溶剂,对环境造成威胁;(2)工业吸附应用:UiO-MOFs粉体吸附剂不易回收,存在诸如二次污染的产生或分离困难的问题,易于堵塞设备造成处理效率下降,无法大规模工业应用;(3)MOFs的特定功能改性:材料的吸附能力依赖于其结构内的配位点的数量,单一的 MOF 吸附材料的吸附容量普遍较低。因此,需要通过后合成技术进一步开发新型功能化的MOF材料,以提高其吸附性能。(4)再生成本等。未来MOFs作为吸附剂还需要在合成化学稳定性更高、选择性好、具有超强吸附特性的新型MOFs方面进行大量的研究。此外,还需解决由实验室规模向中试规模和工业规模的转变,如经济成本制约、吸附剂的再生循环和有机化学品的高效利用等问题。
