放化疗联合贝伐珠单抗靶向治疗晚期卵巢癌患者的临床效果
2022-06-30邓颖慧
邓颖慧
统计调查显示:卵巢癌病发率已经位居女性生殖系统癌症疾病第三位,卵巢癌致死率已经位居妇科恶性肿瘤疾病的第一位[1-2]。肿瘤细胞减除术联合术后铂类药物化疗是卵巢癌患者的主流治疗方案,对提高患者肿瘤细胞减灭率、改善患者临床缓解率均有积极效果[3]。但一方面多数卵巢癌患者确诊时均已发展至晚期,难以耐受手术治疗或手术疗效不够理想;另一方面放化疗对晚期卵巢癌患者治疗效果有限,长期放化疗亦会导致患者面临耐药风险[4]。贝伐珠单抗是一种具有抗血管生成功能的靶向抗体药物,临床研究显示:贝伐珠单抗能有效抑制人体内血管内皮因子的表达水平,具有抗肿瘤细胞侵袭及转移等功能,可用于癌症疾病的治疗中[5]。此前亦有研究显示贝伐珠单抗能有效提升晚期卵巢癌患者的治疗效果及生活质量[6]。基于此,本次研究将针对放化疗联合贝伐珠单抗靶向治疗晚期卵巢癌患者的临床效果进行研究,现报告如下。
1 资料与方法
1.1 一般资料
设计研究时间为2016年1月-2018年1月,研究对象为首都医科大学石景山教学医院住院治疗的晚期卵巢癌患者共60例,纳入标准:(1)影像学、病理学诊断结果确诊为晚期卵巢癌;(2)预计生存时间≥6个月。排除标准:(1)本次研究前伴有其他放化疗史,或其他肿瘤手术史;(2)体质对本次研究药物不耐受,或为过敏性体质;(3)伴有肿瘤疾病、血液系统疾病、精神系统疾病,以及脏器功能障碍、凝血功能障碍及其他影响治疗障碍。采用随机数字表法分为观察组(n=30)与对照组(n=30)。观察组年龄35~75岁,平均(55.26±6.28)岁;组中疾病依据文献[7]国际妇产科联盟FIGO分期标准分期,包括Ⅲ期21例,Ⅳ期9例;病理分型包括浆液型20例,黏液型8例,内膜样1例,透明细胞样1例。对照组年龄35~75岁,平均(55.49±6.07)岁;组中疾病分期包括Ⅲ期22例,Ⅳ期8例;病理分型包括浆液型21例,黏液型6例,内膜样2例,透明细胞样1例。两组患者临床资料比较,差异无统计学意义(P>0.05),有可比性。本次研究已得伦理委员会批准,患者及家属知情同意。
1.2 方法
对照组予以放化疗。放疗方式:使用6MV-X线全腹盆腔外照射放疗,视野集中于患者横膈与骨盆中间位置。照射过程中患者直肠、膀胱区域使用铅遮挡照射,设置DT:40 Gy/4周。待剂量至40 Gy后缩小照射视野至患者肿瘤组织周围2~3 cm区域,此时DT调整至10~20 Gy/1~2周。放疗期间患者血常规检测1~2次/周,有恶心、呕吐等不良反应患者对症治疗。化疗方式:使用紫杉醇联合卡铂化疗方案。化疗第1天:紫杉醇(辰欣药业股份有限公司生产,国药准字 H20057404,5 ml∶30 mg)175 mg/m2与 0.9%氯化钠注射液500 ml混合后静脉滴注,持续3 h。卡铂注射液(齐鲁制药有限公司生产,国药准字H20020180,10 ml∶100 mg)曲线下面积 5.0 mg/ml静脉滴注。本组患者以3周为1个疗程,2个疗程间隔时间为3周,治疗共6个疗程。
观察组予以放化疗联合贝伐珠单抗靶向治疗。本组患者在对照组放化疗的基础上,同时予以贝伐珠单抗(齐鲁制药有限公司生产,国药准字S20190040,100 mg∶4 ml)5 mg/kg 静脉滴注,持续30~90 min。贝伐珠单抗治疗1次/周,持续6周为1个疗程。第1个疗程结束后改为2次/周,治疗共6个疗程。
两组患者均予以3年随访,随访方式为电话随访。
1.3 观察指标及评价标准
(1)于疗程结束后次日评价治疗效果。疗效标准,完全缓解(CR):所有靶病灶消失,无新病灶出现,肿瘤标志物检测结果正常,持续时间≥4周;部分缓解(PR):靶病灶最大直径总和减少幅度≥30%,持续时间≥4周;疾病稳定(SD):靶病灶最大直径总和减少幅度<30%,增长幅度<20%;疾病进展(PD):靶病灶最大直径总和增长幅度≥20%,或出现新病灶[8]。治疗有效率=(CR+PR)/总例数×100%。(2)于疗程内统计毒副反应。参考文献[9]常见不良事件评价标准,统计两组患者毒副反应发生率,包括消化道反应、皮肤黏膜出血、骨髓抑制等。(3)随访期内生存率。统计两组患者1年内、3年内生存率。(4)于治疗前、治疗后次日检测血清肿瘤标志物。选择血管内皮生长因子(vascular endothelial growth factor,VEGF)、白介素-6(interleukin-6,IL-6)、血清甲胎蛋白(alpha fetoprotein,AFP)、 癌 胚 抗 原 -125(carbohydrate antigen 125,CA125)作为两组患者血清肿瘤标志物检测指标。其中VEGF、IL-6使用酶联免疫吸附法进行检测,AFP、CA125使用化学免疫分析法进行检测。VEGF正常参考值:<294 ng/L;IL-6正常参考值:56~150 pg/ml;AFP 正常参考值:<20 μg/L;CA125 正常参考值:<35 kU/ml。
1.4 统计学处理
采用SPSS 22.0统计学软件进行数据分析,计量资料用(±s)表示,两组间比较采用t检验;计数资料采用率(%)表示,组间比较采用χ2检验。等级资料使用秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗效果的比较
观察组治疗有效率高于对照组,差异有统计学意义(P<0.05),见表1。
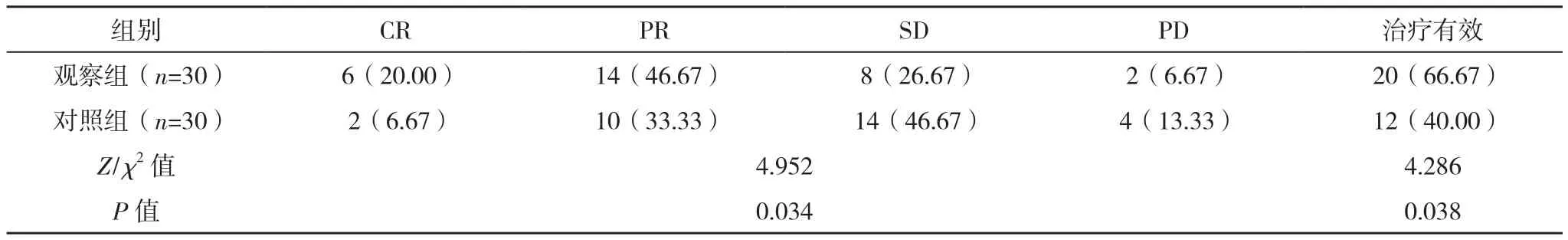
表1 两组治疗效果比较[例(%)]
2.2 两组毒副反应发生率比较
两组毒副反应发生率比较,差异无统计学意义(P>0.05),见表2。
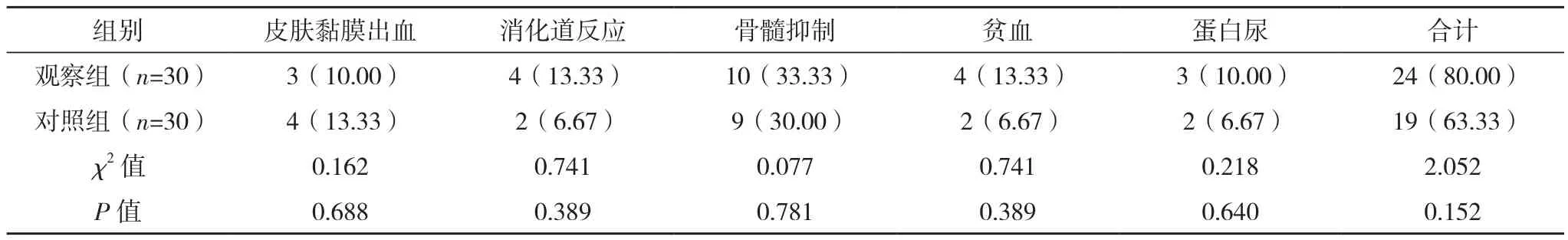
表2 两组毒副反应发生率比较[例(%)]
2.3 两组随访期内生存率比较
观察组随访1、3年内生存率高于对照组,差异均有统计学意义(P<0.05),见表3。

表3 两组随访期内生存率比较[例(%)]
2.4 两组治疗前后血清肿瘤标志物水平比较
治疗前,两组VEGF、IL-6、AFP、CA125水平比较,差异无统计学意义(P>0.05);治疗后,观察组VEGF、IL-6、AFP、CA125水平低于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组治疗前后血清肿瘤标志物水平比较(±s)

表4 两组治疗前后血清肿瘤标志物水平比较(±s)
组别 VEGF(ng/L)IL-6(pg/ml)AFP(μg/L)CA125(kU/ml)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=30)520.63±52.41 305.11±30.27 166.92±8.45 102.38±20.12 5.42±0.51 2.41±0.16 215.44±18.26 16.22±1.64对照组(n=30)521.74±50.68 382.41±38.47 164.45±9.42 133.57±22.26 5.53±0.48 2.98±0.27 216.53±18.85 33.41±3.68 t值 0.083 8.649 1.069 5.693 0.860 9.948 0.227 23.370 P值 0.467 0.000 0.145 0.000 0.197 0.000 0.410 0.000
3 讨论
卵巢癌本身可分为上皮性卵巢癌、卵巢性索间质肿瘤、卵巢恶性生殖细胞肿瘤等多种类型,该病病情发展将会造成患者生理与病理多重伤害。由于卵巢癌本身早期缺少临床症状,部分患者即使存在临床症状但本身并无特异性,当前临床亦缺少标准筛查方案,因此大部分患者于临床确诊时多以晚期卵巢癌为主,病灶存在明显转移的情况下单纯手术治疗效果有限。在此情况下只能通过非手术方案缓解患者临床症状,延长患者生存时间。本次研究中对照组所用的放化疗联合方案,即为当前临床较为常用的非手术治疗方案。其中放疗使用6MV-X线全腹盆腔外放疗仪器,能在尽量保护患者卵巢周围组织的基础上通过射线灭杀患者卵巢内肿瘤组织;化疗使用紫杉醇+卡铂的TC基础化疗方案,两项药物协同使用能有效改善患者临床症状,控制肿瘤组织生长[10]。但对于晚期卵巢癌患者而言,TC化疗方案效果有限,患者耐药性问题频发,多数患者不能保持长期疗效,总体生存率较低[11]。因此仍需联合其他治疗方案以进一步提高晚期卵巢癌患者的治疗效果。本次研究中即尝试贝伐珠单抗靶向治疗联合放化疗的方案治疗晚期卵巢癌患者,取得较好效果。
在肿瘤疾病的发生发展中,肿瘤新生血管的出现与形成在其中起到了非常重要的作用。而VEGF对肿瘤新生血管的出现与形成具有重要作用。VEGF能够与受体结合,提升肿瘤新生血管的产生速度,提高人体腹膜血管通透性[12]。因此阻断晚期卵巢癌患者体内VEGF与受体的结合进程和相互作用,一者能够阻断患者体内新生肿瘤血管的新生进程,另一者能够有效抑制肿瘤组织血液供应,最终达到缩小肿瘤组织、杀灭肿瘤细胞的目的。贝伐珠单抗作为一种单克隆抗体,对VEGF与受体的结合进程和相互作用具有显著的抑制作用。研究证实:贝伐珠单抗能有效抑制卵巢癌患者体内VEGF的增殖进程,抑制患者体内肿瘤新生血管形成,具有良好的抗肿瘤效果。同时贝伐珠单抗还能有效调整肿瘤血管趋向,增强此前所用化疗药物对肿瘤组织的种种灭杀功效[13]。本次研究结果亦证实:观察组治疗有效率高于对照组,差异有统计学意义(P<0.05)。与张善存等[14]研究结果相近。充分说明放化疗联合贝伐珠单抗靶向治疗晚期卵巢癌患者能有效提高患者治疗效果;两组毒副反应发生率比较,差异无统计学意义(P>0.05)。说明贝伐珠单抗靶向治疗并不会对晚期卵巢癌患者放化疗方案的安全性造成不利影响;治疗后,观察组VEGF、IL-6、AFP、CA125水平低于对照组,差异均有统计学意义(P<0.05)。从血清肿瘤标志物方面证实放化疗联合贝伐珠单抗靶向治疗晚期卵巢癌患者的良好效果,患者体内多种卵巢癌血清肿瘤标志物水平均有明显降低,代表患者体内肿瘤细胞凋亡数量显著增加;观察组随访1年内、3年内生存率高于对照组,差异均有统计学意义(P<0.05)。说明放化疗联合贝伐珠单抗靶向治疗能有效晚期卵巢癌患者的3年内生存率。相关研究亦证实:放化疗联合贝伐珠单抗靶向治疗能有效延长晚期卵巢癌患者生存时间,提高患者免疫功能[15]。但需要注意的是,本次研究亦存在样本数量较少的问题,后续需增加研究样本以进一步提升研究结果的标准性和规范性。
综上所述,放化疗联合贝伐珠单抗靶向治疗晚期卵巢癌效果良好,能有效提高患者近期生存率且安全性较好,同时患者VEGF、IL-6等血清肿瘤标志物水平明显下降,值得临床推广。
