MXenes的制备、性质及其在肿瘤诊疗中的研究进展
2022-06-29白志强白云峰
白志强,赵 璐,白云峰,冯 锋
(1.山西师范大学 化学与材料科学学院,临汾 041004;2.山西大同大学 化学与化工学院,化学生物传感山西省重点实验室,大同 037009)
二维(2D)纳米材料的尺寸从几纳米到几百纳米不等,一般为单原子层或多原子层结构,2D 纳米材料可以是元素的同素异形体或化合物,其层内的原子可通过共价键牢固地结合,层间的原子则通过范德瓦尔斯力连接[1-2]。常见的2D 纳米材料有石墨烯(Graphene)[3]、过渡金属二硫化物(TMDs)[4]、共价有机框架(COFs)[5]、六方氮化硼(h-BN)[6]、金属有机框架(MOFs)[7]、层状双氢氧化物(LDHs)[8]、2D 元素纳米片[9]等。二维过渡金属碳化物、氮化物或碳氮化物(MXenes)是一种新型的2D 纳米材料[10]。Gogotsi课题组[11]报道了世界上第一种MXenes 材料Ti3C2,他们使用氢氟酸(HF)刻蚀 Ti3AlC2成功制备出Ti3C2。制备MXenes 主要是将层状金属陶瓷(MAX)材料中的A 层选择性刻蚀掉。MAX 的分子式为Mn+1AXn,其中M 是过渡金属元素(如Ti,Sr,V,Cr,Ta,Nb,Zr,Mo 等),A 通常是第三或四主族的元素(如Al,Ga,In,Si,Ge 和Ga),X 表示碳或(和)氮元素,n从1 到3 变化,因此MXenes 的结构为M2X、M3X2和M4X3[12-13]。到目前为止,已经在实验室中成功制备了近30 种MXenes(图1),然而计算模拟预测却有100 多种MXenes[14]。MXenes 具有优异的表面化学性能、电子传递性能、机械和热力学性能,在电化学储能[15-16]、海水淡化[17-19]、电磁屏蔽[20-21]、催化[22]、传感器[23-26]等诸多领域具有广阔的应用前景。
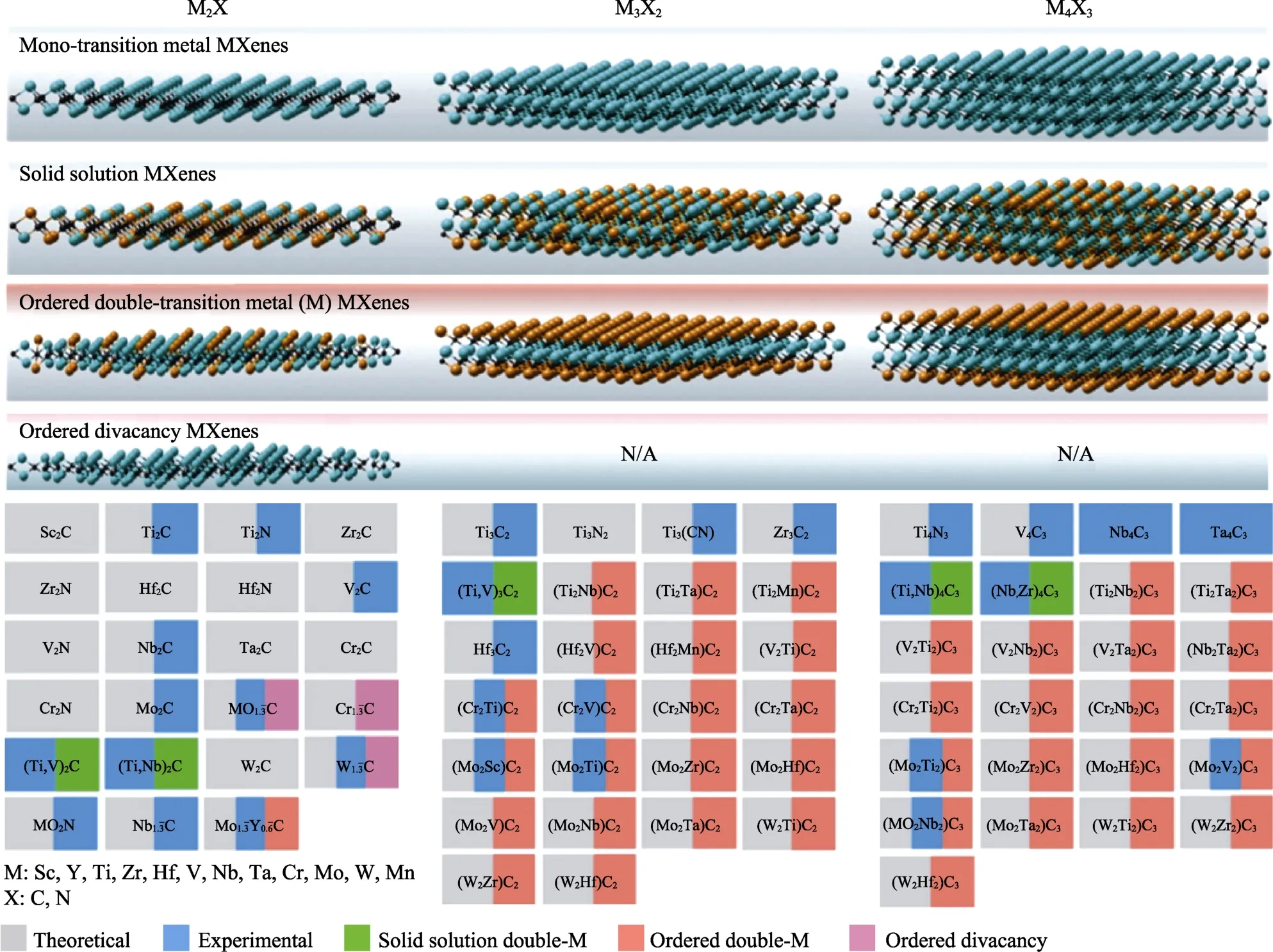
图1 MXenes 组成示意图[14]Fig.1 MXenes schematic composition[14]
随着对MXenes 研究的日益深入,这一新兴的2D纳米材料已被证实可应用于肿瘤治疗领域[27-29]。MXenes 具有很强的近红外光(Near infrared,NIR)吸收能力和光热转换性能,可用于肿瘤光声(Photoacoustic,PA)成像和光热治疗(Photothermal therapy,PTT)[28,30]。由于MXenes 具有优异的光电性能,可以作为光敏剂产生活性氧(Reactive oxygen species,ROS)用于光动力治疗(Photodynamic therapy,PDT)[29,31]。MXenes还具有高比表面积和低毒性的特点,可用于药物分子的装载和运输[29,32]。然而,MXenes 表面缺乏足够的化学基团与药物分子结合[33]。另外,肿瘤微环境(Tumor microenvironment)中氧含量较低,缺氧会影响PDT 效果,而MXenes 通过PTT 方法对肿瘤治疗效果有限。
为了提高MXenes 的肿瘤治疗效果,研究人员开发了多种基于MXenes 的联合治疗新方法。本文简要总结MXenes 的制备方法,重点介绍其在肿瘤治疗中的应用研究,包括PTT 和联合治疗等,最后阐述MXenes 在肿瘤治疗应用中存在的挑战以及未来发展前景。
1 MXenes 的制备
随着对MXenes 制备方法的深入研究,到目前为止实验室已经制备出近30 种MXenes[14,34]。总体来说,MXenes 的制备方法包括自上而下法和自下而上法。
1.1 自上而下法
自上而下法是将较大尺寸的MAX 材料选择性刻蚀掉A 层制备成MXenes,根据刻蚀方法的不同,主要分为HF 刻蚀法、氟盐刻蚀法、熔融盐法和碱辅助水热法。
1.1.1 HF 刻蚀法
通过使用HF 选择性刻蚀MAX 材料中的A 层是最经典的MXenes 制备方法。在MAX 材料中M-A键是金属键,其化学活性较高;而M-X 键同时具有金属键和共价键,比M-A 键更强,因此可以通过HF 选择性刻蚀掉MAX 材料中A 层[35]。该方法主要采用以下步骤完成MXenes 制备。
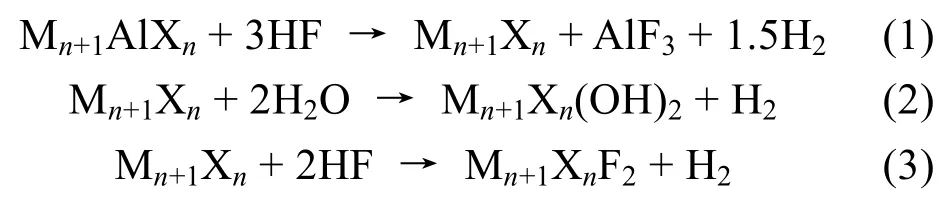
2011年,Gogotsi 课题组[11]通过HF 刻蚀法制备手风琴状结构的2D Ti3C2层状材料(图2(a)),并将该材料命名为MXenes。另外,利用该方法还可以制备Ta4C3[27]、Nb2C[28]等。
HF 刻蚀法制备的MXenes 在M 层末端具有高表面能,通过吸附溶液中的羟基、氧或氟等基团或离子可形成稳定的表面官能团,从而降低M 层的末端表面能[12]。此外,通过二甲基亚砜、四甲基氢氧化铵等有机试剂对制备的MXenes 进行处理,并在液相超声作用下可制备单层或少层MXenes 纳米片[28,32]。
1.1.2 氟盐刻蚀法
将氟化物盐(如NaF、KF 或LiF)与硫酸或盐酸混合,可取代具有强腐蚀性的HF,其制备机理与HF 刻蚀法相同。为避免MXenes 制备反应后处理危险的HF,2014年人们首次利用HCl 和LiF 混合液在低温下刻蚀Ti3AlC2制备得到Ti3C2[36],该方法可以制备黏土状结构的Ti3C2。相比于HF 刻蚀法,该方法在制备MXenes 过程中更为安全。(NH4)HF2也可作为刻蚀剂制备MXenes。Gogotsi 课题组[37]采用(NH4)HF2作为刻蚀剂制备了Ti3C2,发现(NH4)HF2通过阳离子的电化学嵌入来刻蚀Al 元素,同时NH4+还会进入Ti3C2的层间空间,提高分层效率,其反应条件更为温和,制备过程更加安全,还可根据实际需要合理地替换氟盐中的阳离子。该方法主要有以下反应步骤:
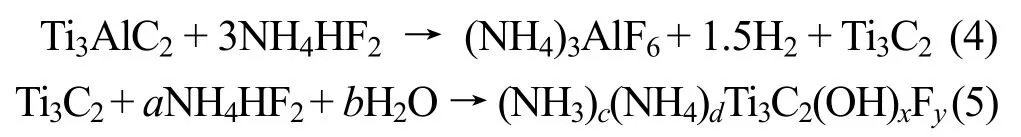
1.1.3 熔融盐法
虽然HF 刻蚀法和氟盐刻蚀法可以成功制备碳化物或碳氮化物的 MXenes,但无法制备氮化物MXenes。Tin+1AlNn中的Ti-Al 键比Tin+1AlCn中的Ti-Al 键更加牢固,制备Tin+1Nn需要更高的能量,而Tin+1Nn的稳定性较低,在HF 中容易溶解。熔融盐法采用低熔点盐作为助熔剂,在合成过程中有液相出现,可以提高离子扩散速率。Gogotsi 课题组[19]开发出熔融盐法制备MXenes(图2(b)),他们采用KF、NaF 和LiF 混合盐与Ti4AlN3反应,通过去除Al 层制备Ti4N3,成功制备出氮化物MXenes。此后,黄庆课题组[38]建立了一种路易斯酸熔融盐制备MXenes 的通用策略。该方法可采用多种路易斯酸氯化物熔盐(如ZnCl2、FeCl2、CuCl2等)制备MXenes,并且对多种MAX 材料(如A 元素为Al、Zn、Si、Ga 等)均可刻蚀,极大拓展了MXenes 的制备途径。
1.1.4 碱辅助水热法
采用含氟刻蚀剂制备MXenes,可能存在氟离子引发的安全性问题。碱与两性元素Al 的结合能力很强,理论上可以作为制备Mxenes 的刻蚀剂,但MAX 材料内部金属层限制了含铝氧化物或氢氧化物与溶液中羟基反应生成可溶解的Al(OH)4-,只有更高的温度和碱浓度才有助于Al(OH)4-生成,促使MXenes 制备过程持续进行。Zhang 课题组[39]采用高浓度NaOH 溶液刻蚀MAX 材料制备MXenes(图2(c)),全程未使用含氟试剂。虽然NaOH 处理无法去除整个MAX 材料的Al 原子,但是该制备方法也为无氟刻蚀剂制备MXenes 开辟了一条安全的新途径。
1.2 自下而上法
自下而上法是使用单个无机原子或分子作为前体,通过化学合成的方法制备MXenes[40]。Ren 课题组[41]首次通过化学气相沉积法(Chemical vapor deposition,CVD)制备α-Mo2C(图2(d)),得到横向尺寸超过100 μm 的高质量α-Mo2C 超薄MXenes。与自上而下法相比,自下而上法的优点是节省原材料,而且可以精确控制MXenes 的元素组成、尺寸大小及表面基团,但在大尺寸MXenes 制备方面较为困难。
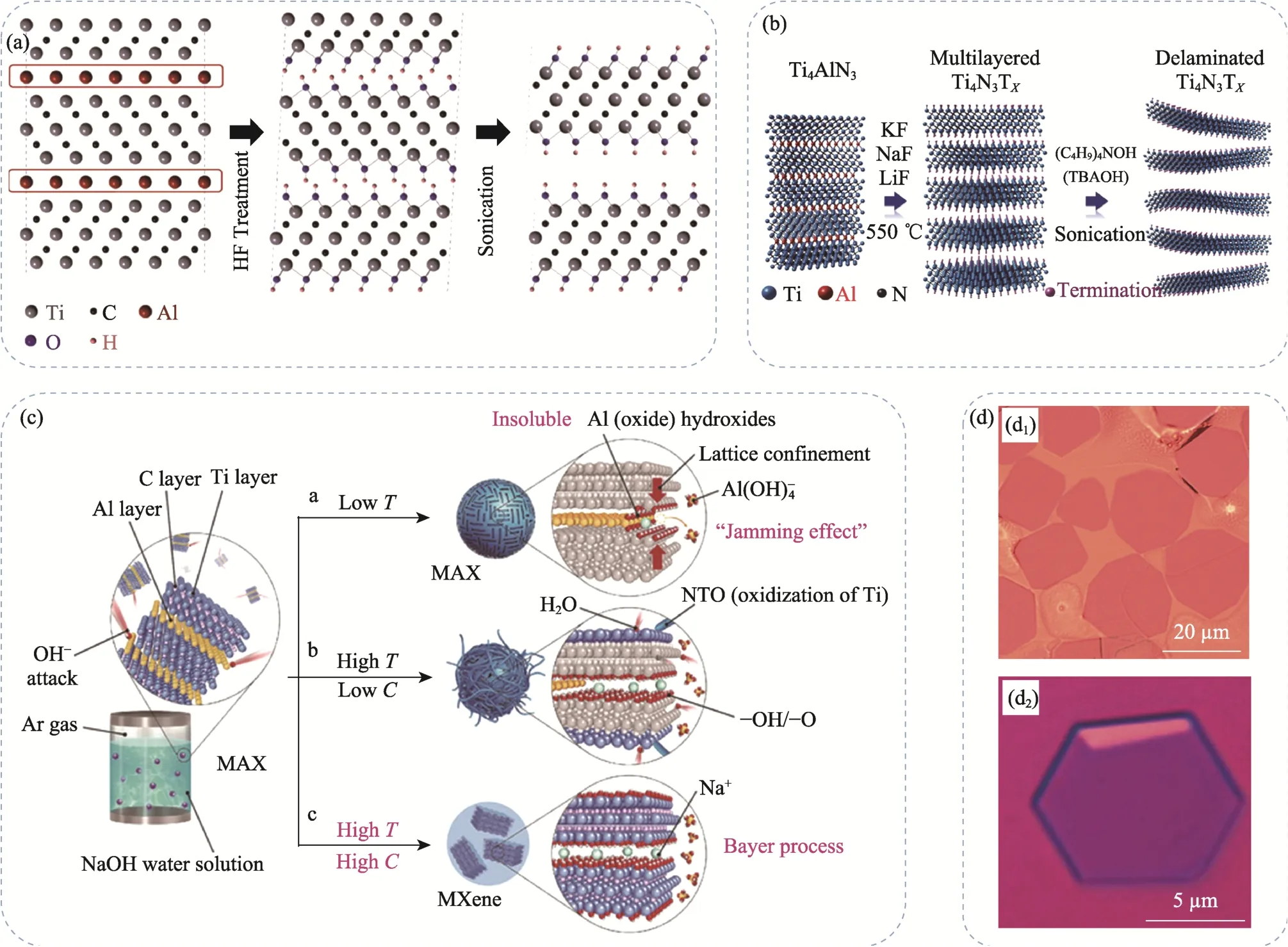
图2 MXenes 制备方法示意图及化学气相沉积法制备的产物Fig.2 Schematic preparation methods for MXenes and products prepared by chemical vapor deposition
目前报道的MXenes 大多采用自上而下法制备,采用自下而上法的报道较少。不同的制备条件对MXenes 的物理结构和表面基团影响不同,自上而下法对MXenes 表面化学、物理结构和缺陷的控制较差,而自下而上法虽然能够有效控制以上参数,但其合成极为困难[35]。上述方法的优缺点见表1。
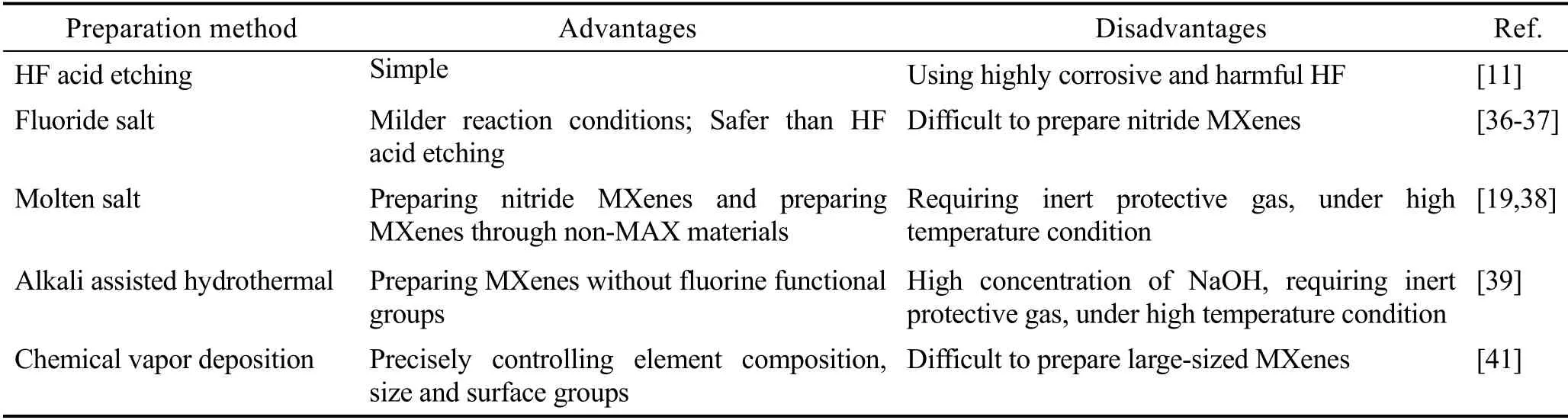
表1 MXenes 的制备方法总结Table 1 Summary of preparation methods of MXenes
2 MXenes 的性质
MXenes 的性质与其元素组成、层状结构堆叠顺序和纳米材料横向尺寸大小有关。目前大量制备高纯度MXenes的技术问题还没有解决,因此MXenes的性质研究是通过理论计算方法进行预测的,主要包括MXenes 的稳定性质、机械性质、光学性质和电学性质。
2.1 稳定性质
晶体材料的稳定性与晶格能相关,晶格能越负则晶体越稳定。Ivanovskii 课题组[42]通过密度泛函理论(Density functional theory,DFT)的第一性原理能带结构对MXenes 的晶格能进行理论计算,结果显示MXenes 的晶格能为负值,可以稳定存在。通过计算结合能(Ecoh)也可以预测MXenes 的稳定性,Ecoh是化合物总能量减去每个原子能量的差值,Ecoh的绝对值越大,MXenes 的结构稳定性越高。Tin+1AlCn结构中的Ti-C 键同时具有金属键和共价键,比Ti-Al金属键更强。随着n增大,Tin+1AlCn结构中的Ti-C键数量超过Ti-Al 键,其稳定性也越高[43]。
2.2 机械性质
通过DFT 的第一性原理对Ti2C、Ti3C2和Ta3C2等MXenes 材料进行计算[44],发现以上MXenes 材料沿着参考基准面进行拉伸时,弹性模量均高于500 GPa,力学性能均大于相同厚度的多层石墨烯。研究还发现MAX 材料的弹性模量远低于其对应的MXenes,比如M2AX 弹性模量与相应的MXenes 相比降低了近40%,而M3AX2和M4AX3弹性模量与相对应的MXenes 相比则降低了近70%。
2.3 光学性质
MXenes 与光量子相互作用时,如果MXenes 的光学带隙与光量子能量相对应,则可以吸收光量子。DFT 的第一性原理计算表明,调整MXenes 表面基团成分和含量可以改变其光学带隙范围[40]。MXenes 在NIR 有很强的光吸收能力,可用于肿瘤PTT 和PA 成像。然而,MXenes 的光热转换机理目前尚未完全清楚,Dong 课题组[29]认为Ti3C2具有类似于金纳米粒子的局域表面等离子体共振(Localized surface plasmon resonance,LSPR)效应,所以在近红外(NIR)光区具有光热转换能力。Wang 课题组[45]认为MXenes 在NIR 具有光热转换能力是因为其自身具有优异的电磁干扰屏蔽效应,以及与贵金属纳米粒子类似的LSPR 效应。
2.4 电学性质
MXenes 的电学性质与其内部金属原子有序排列有关,金属原子使MXenes 具有导体或半导体性质。不同方法制备的MXenes 表面基团不同,导致电子吸引能力有所差异,会显著影响其电学性能。MXenes 在制备过程中所形成的表面缺陷增多,则限制了电子的自由运动,导致金属层内电子密度分布不平衡,会显著影响其电学性质[40]。MXenes 在热或光等外部刺激下,可产生活性电子,利用这一电学性质,Dong 课题组[29]采用NIR 照射使Ti3C2产生ROS,从而增强对肿瘤细胞的杀伤效果。
3 MXenes 在肿瘤诊疗中的应用
MXenes 在肿瘤诊疗中的应用主要包括:1)通过PTT 方法在肿瘤部位产生热量杀死肿瘤细胞;2)联合PTT、PDT 和化学疗法(Chemotherapy,CHEMO)实现多模式肿瘤治疗,构建MXenes 表面介孔材料负载化疗药物或连接靶向剂对肿瘤进行联合治疗;3)基于多功能MXenes 复合材料建立诊断-治疗一体化平台。
3.1 光热治疗
PTT 是依靠光热转换剂(Photothermal transducing agen,PTA)在肿瘤内积累并将光能转化为热能,通过产生热量而杀死肿瘤细胞,比传统肿瘤治疗方式的副作用小[46-51]。外界光照射和PTA 是决定PTT效果的主要因素[52]。对于PTA 来说,有两个基本参数影响其PTT 效果: 一个是PTA 对光的吸收能力,由消光系数决定;另一个是在外界光照射下PTA 产生热量的能力,由光热转换效率决定[40,53]。
Geng 课题组[54]将Ti3C2纳米片作为PTA 用于肿瘤治疗研究,其制备的Ti3C2纳米片在808 nm NIR光照射下质量消光系数为29.1 L·g-1·cm-1。随着NIR功率增大,4T1 鼠乳腺癌细胞存活率急剧下降。结果显示,Ti3C2纳米片是一种性能良好的PTA,通过PTT 可有效抑制肿瘤细胞生长。
2017年Shi 课题组[30]首次研究了Ti3C2纳米片在小鼠体内的PTT 效果(图3(a))。制备的Ti3C2纳米片在808 nm NIR 光下质量消光系数为25.2 L·g-1·cm-1,光热转换效率为30.6%。对4T1 肿瘤模型的荷瘤裸鼠静脉注射Ti3C2后进行PTT,结果显示裸鼠肿瘤组织在PTT 后凋亡或坏死。
MXenes 除了能够在NIR-I 下对肿瘤进行PTT,还可以在NIR-II 区域进行PTT,且NIR-II 比NIR-I有更深的组织穿透深度和更大的组织允许曝光量[28]。Shi 课题组[28]将Nb2C 在NIR-I 和NIR-II 照射下研究PTT 效果(图3(b)),发现Nb2C 在NIR-I 和NIR-II 照射下光热转换效率分别为36.5%和46.65%。Nb2C在NIR-II 照射下对肿瘤细胞和荷瘤裸鼠有更优异的PTT 效果,且Nb2C 具有良好的生物相容性和生理稳定性,在体内外均无明显毒性。
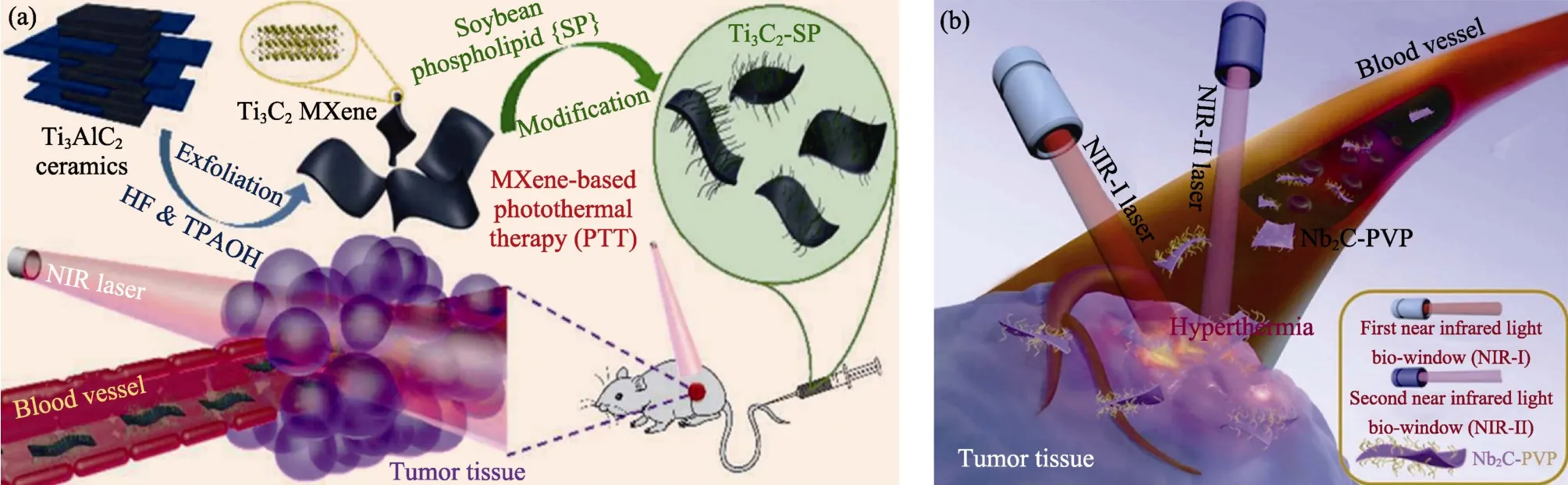
图3 (a)Ti3C2 纳米片对4T1 肿瘤模型的荷瘤裸鼠PTT 的示意图[30]和(b)Nb2C 纳米片在NIR-I 和NIR-II 下进行体内PTT 的示意图[28]Fig.3 (a) Schematic diagrams of Ti3C2 nanoparticles on PTT in 4T1 tumor bearing nude mice[30] and(b) Nb2C nanosheets for PTT in vivo under NIR-I and NIR-II[28]
以上研究结果说明MXenes 具有较高的光热转换效率,通过PTT 可有效抑制肿瘤生长。除了Ti3C2和Nb2C,目前已经有7 种MXenes 用于肿瘤PTT,表2中将应用于肿瘤PTT 的一些MXenes 及其关键参数作了汇总。
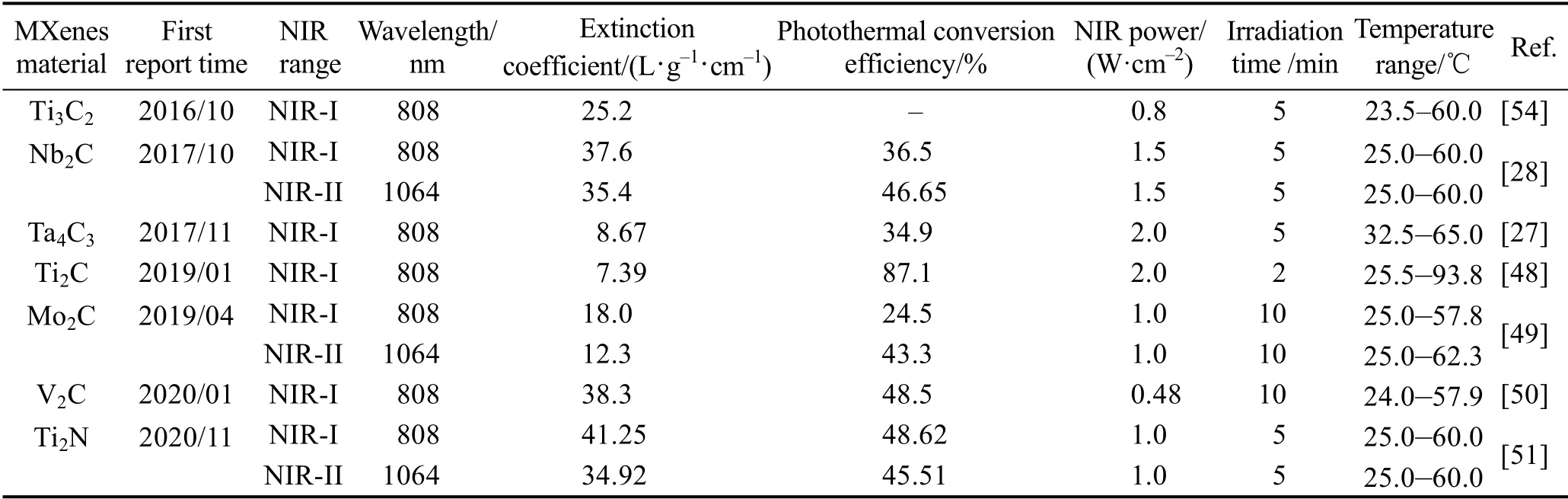
表2 MXenes 首次应用于肿瘤PTT 的结果总结Table 2 First application of MXenes in PTT on tumor
3.2 联合治疗
MXenes 通过PTT 方法对肿瘤的治疗效果有限,为了提高肿瘤治疗效果,研究人员开发了多种基于MXenes 的联合治疗新方法,主要集中在以下几个方面:1)通过PTT、PDT 和CHEMO 等方法对肿瘤进行多模式联合治疗;2)构建MXenes 表面介孔并负载化疗药物,依靠较大的孔体积提高载药能力,并实现化疗药物的可控释放;3)通过主动靶向技术提高MXenes 对肿瘤的治疗效果,同时减少毒副作用。
3.2.1 多模式联合治疗
PDT 主要依靠活化的光敏剂将激光照射能量转移给周围的氧分子产生ROS,之后生物大分子与ROS 发生氧化反应,可对肿瘤细胞产生毒性作用,导致肿瘤细胞受损或死亡[55-56]。MXenes 单独采用PDT 方式进行肿瘤治疗研究非常少,大多数都是联合PTT 或CHEMO。环境中氧含量直接影响PDT效果,而缺氧是肿瘤微环境的一个主要特征,因此MXenes 如何在缺氧环境下发挥PDT 的效果仍需进一步研究。
CHEMO 是一种重要的肿瘤治疗方法,主要通过抗肿瘤药物抑制肿瘤细胞增殖和转移[56]。MXenes独特的2D 平面结构具有高比表面积的特点,有利于负载药物[29,31]。另外,MXenes 表面存在羟基或氟基团,带有负电荷,可以通过静电相互作用负载带正电荷的药物[13]。
2017年,Dong 课题组[29]首次利用Ti3C2纳米片进行多模式肿瘤治疗研究(图4(a)),Ti3C2纳米片通过静电相互作用负载抗肿瘤药物阿霉素(Doxorubicin,DOX),负载率达到84.2%,之后通过透明质酸包被负载DOX 的Ti3C2纳米片。肿瘤细胞内的透明质酸酶可降解透明质酸,释放DOX,肿瘤微环境酸性条件和PTT 可加速DOX 释放,而且Ti3C2纳米片在NIR-I 照射下可产生ROS。因此,PTT/PDT/CHEMO多模式联合治疗大幅提高了Ti3C2纳米材料对4T1肿瘤细胞的杀死率。
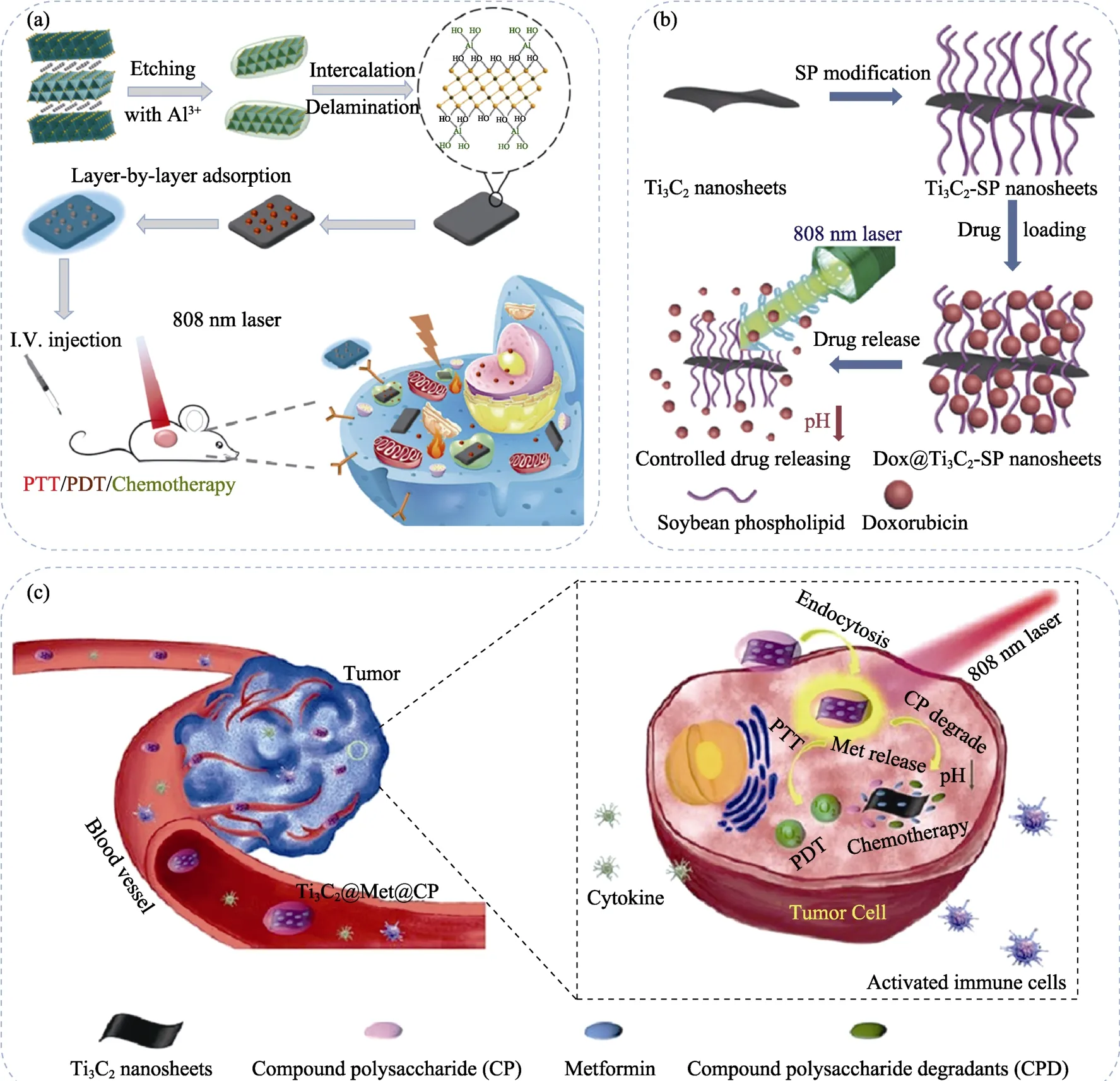
图4 (a)Ti3C2 纳米材料负载DOX 用于肿瘤PTT/PDT/CHEMO 联合治疗[29]、(b)DOX@Ti3C2-SP 纳米材料用于肿瘤PTT/CHEMO 联合治疗[32]和(c)Ti3C2@Met@CP 纳米材料用于肿瘤PTT/PDT/CHEMO 联合治疗[57]示意图Fig.4 Schematic diagrams of (a) Ti3C2 nanomaterials loaded with DOX for tumor PTT/PDT/CHEMO combined therapy[29],(b) DOX@Ti3C2-SP nanomaterials for tumor PTT/CHEMO combined therapy[32],and (c) Ti3C2@Met@CP nanomaterials for tumor PTT/PDT/CHEMO combined therapy[57]SP: Soybean phospholipid
为了使Ti3C2纳米片负载更多DOX 以提高联合治疗效果,2018年,Chen 课题组[32]首先在Ti3C2纳米片表面修饰大豆磷脂(Soybean phospholipid,SP)以增加生物相容性,再通过静电相互作用负载DOX(图4(b))。经SP 修饰的Ti3C2纳米片DOX 载药量高达211.8%,而且DOX 释放具有pH 和温度依赖性。体内和体外实验结果均表明PTT 和CHEMO 联合治疗效果优于单一治疗模式。
MXenes 除了可负载抗肿瘤药物,还可以同时负载激活机体自身免疫功能的药物提高联合治疗效果。2020年,Hou 课题组[57]在Ti3C2纳米片表面通过层层吸附二甲双胍(Metformin,Met)和复合多糖(Compound polysaccharide,CP)的方法建立了Ti3C2@Met@CP 多模式联合治疗系统,Met 具有抗肿瘤功效,CP 是由香菇多糖、茯苓多糖和银耳多糖组成的一种新型免疫调节剂,可激活机体自身免疫功能(图4(c))。因而 Ti3C2@Met@CP 具有 PTT/PDT/CHEMO 多模式联合治疗作用,可通过激活免疫系统杀死肿瘤细胞并抑制肿瘤复发和转移。
上述研究表明,相比于单一治疗模式,通过PTT、PDT 和CHEMO 等方法对肿瘤进行多模式联合治疗可以提高肿瘤治疗效果。MXenes 在多模式联合治疗中扮演重要角色,其具有良好的生物相容性和较大的比表面积,可负载不同抗肿瘤药物及免疫调节剂,对肿瘤进行 CHEMO,而其本身具有良好的PTT 和PDT 效果。采用多模式联合治疗对于一些耐药性肿瘤细胞可以实现更为理想的治疗效果。
3.2.2 MXenes 表面介孔负载化疗药物的体系
MXenes 要实现理想的肿瘤治疗效果需进行表面功能化修饰,但是MXenes 表面缺乏足够的化学基团结合生物分子或功能性纳米粒子[33]。为解决这一问题,可在MXenes 表面构建介孔二氧化硅层。介孔二氧化硅层具有低毒性的特点,在其表面容易进行表面功能化修饰,便于结合生物分子和功能性纳米粒子[58-61]。而且,MXenes 表面构建的介孔二氧化硅层具有较高的比表面积和较大的孔体积,可提高载药能力并实现化疗药物的可控释放[33]。
Yang 课题组[58]通过十六烷三甲基氯化铵(CTAC)在Ti3C2表面构建介孔二氧化硅层,成功制备了Ti3C2@mMSNs 复合材料(图5(a)),介孔二氧化硅层的孔结构增强了复合材料在生理溶液中的亲水性和分散性,还可以使复合材料按需释放DOX 药物。
另外,CTAC 也是一种有效杀死肿瘤细胞的药物分子,Chen 课题组[59]在构建Nb2C 介孔二氧化硅纳米复合材料时,创新性地将CTAC 保留在纳米复合材料中(图5(b)),从而避免了去除纳米复合材料中残留的CTAC 的繁琐步骤[58]。CTAC 在PTT 作用下有效释放,进一步增强了肿瘤治疗效果。
芬顿(Fenton)反应可催化H2O2分子转化为高毒性羟自由基(·OH),但是肿瘤是一个低氧微环境,这限制了Fenton 反应等氧依赖性方法的治疗效果。2,2′-氮杂双(2-咪唑啉)二盐酸盐(AIPH)是一种水溶性分子,具有热敏性,受热可分解产生自由基,而且自由基产生水平与环境内氧水平无关。2019年Chen 课题组[60]又在Nb2C 纳米材料的介孔二氧化硅层中孔内负载AIPH,所构建的A@Nb2C@Si 复合纳米材料经PTT 可促使AIPH 快速释放并分解产生自由基,同时实现了自由基的可控生成和释放(图5(c))。该方法在低氧微环境中可促进肿瘤细胞凋亡,是一种在肿瘤微环境内与氧无关的肿瘤联合治疗方法。
高含量的NO 可以通过抑制肿瘤细胞修复以及对线粒体和DNA 造成损伤等途径抑制肿瘤生长。然而,NO 在体内半衰期短,容易与生物大分子和自由基发生反应,因此NO 很难在肿瘤部位实现有效富集。为进一步利用介孔二氧化硅层的孔结构,Xu课题组[61]将S-亚硝基硫醇(RSNO)负载到介孔二氧化硅层的孔结构内,构建了一种Nb2C-MSNs-SNO复合纳米材料,PTT 产生的热量促进RSNO 的S-NO键断裂从而产生NO(图5(d))。这种光热触发方式可以使复合纳米材料在肿瘤部位按需产生NO,有效抑制肿瘤生长。
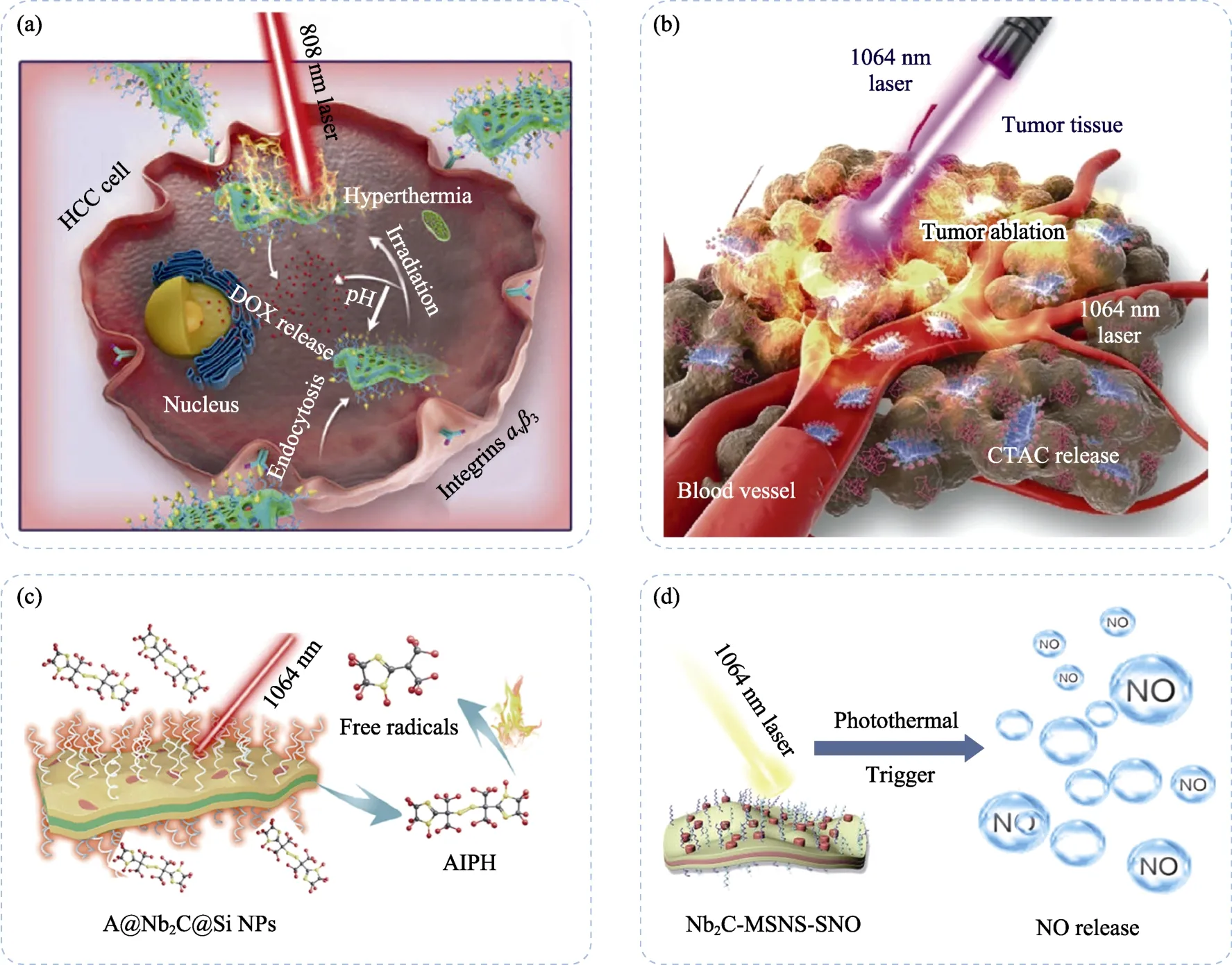
图5 (a)DOX@Ti3C2@mMSNs-RGD 复合纳米材料[58]、(b)CTAC@Nb2C-MSN-PEG-RGD 复合纳米材料在PTT 下释放CTAC 对肿瘤的联合治疗[59]、(c)A@Nb2C@Si 复合纳米材料在PTT 下产生自由基[60]和(d)Nb2C-MSNs-SNO复合纳米材料在PTT 下释放NO 对肿瘤联合治疗[61]的示意图Fig.5 Schematic illustrations for (a) combined therapy on HCC cells as assisted by DOX@Ti3C2@mMSNs-RGD at the cell level[58],(b) CTAC@Nb2C-MSN-PEG-RGD composite nanomaterials releasing CTAC under the action of PTT for combined treatment of tumor[59],(c) AIPH@Nb2C@Si composite nanomaterials generating free radicals under the action of PTT[60],and(d) Nb2C-MSNs-SNO composite nanomaterials releasing NO under the action of PTT for combined treatment of tumor[61]
构建MXenes 表面介孔的设计策略不仅可以增强MXenes生物相容性,同时还提高了MXenes表面化学性能,为进一步表面修饰功能性纳米离子提供了便利。MXenes 表面介孔是一种性能优异的药物分子载体,不仅满足了高剂量药物分子的负载需求,最为重要的是实现了药物分子在肿瘤部位的可控释放,显著提高了化疗药物在肿瘤治疗中的精度和功效。
3.2.3 MXenes 主动靶向治疗
MXenes 主要依靠高渗透长滞留效应(Enhanced permeability and retention,EPR)在肿瘤部位进行被动积累,也称为被动靶向。采用主动靶向可以更有效地将MXenes 纳米材料运送到肿瘤部位[30,55]。目前MXenes 主动靶向已报道两种方法: 一种是利用透明质酸与CD44+(CD44 是一种细胞膜蛋白,在细胞之间起连接、整合作用,下文αvβ3和αvβ5也属此类)进行特异性识别;另一种是利用含三个氨基酸短肽的精氨酸-甘氨酸-天冬氨酸(Arginine-glycineaspartic acid,RGD)与肿瘤细胞表面整合素αvβ3和αvβ5进行特异性结合[29,58]。
2017年,Dong 课题组[29]首次在Ti3C2纳米材料表面包覆透明质酸,利用透明质酸与肿瘤细胞上过表达的CD44+进行特异性识别,提高了Ti3C2纳米材料主动靶向性能,使其更容易在肿瘤部位富集,从而在肿瘤细胞内释放更多DOX。
2018年,Yang 课题组[58]为实现MXenes 复合纳米材料对肝癌细胞(HCC)的主动靶向作用,在Ti3C2@mMSNs 复合材料表面共价连接RGD,因为αvβ3和αvβ5在肝癌细胞表面特异性表达,而在正常肝细胞表面不表达,所以修饰RGD 的Ti3C2@mMSNs 纳米复合材料可以通过小鼠血液循环系统运输并主动靶向至肿瘤部位。Ti3C2@mMSNs 复合纳米材料经RGD功能化不仅提高了对HCC 的靶向性,还减少了纳米材料的毒副作用,同时对HCC 有更好的抑制效果。
主动靶向策略可以增强MXenes 在肿瘤部位的选择性聚集,上述研究也为MXenes 在主动靶向肿瘤治疗方面提供了研究基础和技术积累。然而,这些研究使用的主动靶向剂还不能对任一类型的肿瘤实现主动靶向治疗,未来需要开发更多的靶向策略以满足不同类型肿瘤的主动靶向需求。
3.3 MXenes 诊断-治疗一体化平台
较高原子序数的过渡金属元素(如Ta 和W)有良好的X 射线衰减能力,因此一部分MXenes 可以作为计算机断层扫描(Computed tomography,CT)成像造影剂[27,62]。MXenes 如果存在顺磁性过渡金属元素(如 Cr 和 V),则还可用作磁共振(Magnetic resonance,MR)成像造影剂[63]。为了提高肿瘤治疗效果,可以制备多功能MXenes 复合纳米材料用于放射治疗(Radiotherapy,RT),具有MR 和CT 成像能力,建立MXenes 诊断-治疗一体化平台。
为了使Ti3C2纳米材料具有MR 成像能力,Chen课题组[64]在Ti3C2表面原位生长氧化锰(MnOx)纳米粒子,成功构建MnOx/Ti3C2复合纳米材料(图6(a))。Mn-O 键在肿瘤微环境弱酸性条件下容易断裂,因此MnOx/Ti3C2复合纳米材料具备MR 成像能力,可以实现PA 和MR 双模成像。MnOx/Ti3C2复合纳米材料具有优良的光热转换性能,通过PTT 可有效杀死肿瘤细胞。
Ta4C3因含有高原子序数(Z=73)的Ta 元素而具有CT 成像能力,为使Ta4C3纳米材料同时具有MR成像能力,Chen 课题组[62]在Ta4C3纳米材料表面原位生长超顺磁性氧化铁纳米粒子(Superpara-magnetic iron oxide nanoparticles,IONP),构建的Ta4C3-IONP复合纳米材料具有CT 和MR 成像性能(图6(b)),通过PTT 可杀死肿瘤。另外,IONP 作为Fenton 反应试剂,可催化H2O2分子转化为高毒性·OH。为了在肿瘤细胞内部产生H2O2分子,他们将天然葡萄糖氧化酶(Glucose oxidase,GOD)固定在 MXene-IONPs@ PEG 表面,以催化肿瘤内的葡萄糖产生大量H2O2分子[65]。随后IONPs 催化H2O2分子转化为高毒性·OH,实现肿瘤治疗目的(图6(c))。结合PTT,肿瘤部位温度升高可以进一步加速Fenton 反应,提高肿瘤治疗效果。
为了使Ti3C2纳米材料同时具备MR 和CT 成像能力,Chen 课题组[66]将多金属氧酸盐(Polyoxometalates,POMs)与Ti3C2结合,成功构建了GdW10@Ti3C2复合纳米材料(图6(d))。该复合纳米材料因为存在Gd元素,实现了MR 成像,而因存在高原子序数的W(Z = 74)元素,又可实现CT 成像。GdW10@Ti3C2复合纳米材料在MR 和CT 成像技术引导下,对肿瘤实现实时诊断,并通过PTT 实现良好的肿瘤治疗效果。
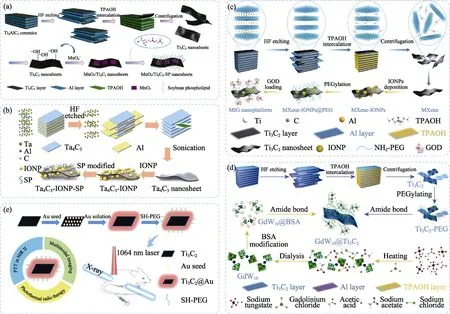
图6 用于肿瘤诊疗的多功能MXenes 复合纳米材料(a)MnOx/Ti3C2[64]、(b)Ta4C3-IONP[62]、(c)MIG[65]、(d)GdW10@Ti3C2[66]和(e)Ti3C2@Au[67]的模式图Fig.6 Schematic diagrams of (a) MnOx/Ti3C2[64],(b) Ta4C3-IONP[62],(c) MIG[65],(d) GdW10@Ti3C2[66],and(e) Ti3C2@Au[67] composite nanomaterials in tumor theranostics
以往构建的Ti3C2纳米材料只能在NIR-I 进行PTT,Cheng 课题组[67]通过种子生长法制备出Ti3C2@Au纳米复合材料,在NIR-II 下具有优异的光热转换能力(图6(e))。复合纳米材料不仅可以对肿瘤进行PTT和RT 联合治疗,还具有CT 成像能力,在体内外均可有效杀死肿瘤细胞。
由这些研究可见,MXenes 除了具有良好的肿瘤治疗效果之外,还具有良好的光热转换能力,能对肿瘤作PA 成像诊断,虽然成像性能无法与CT 和MR 相比。近年来研究人员开发了多种基于MXenes材料的肿瘤诊疗方法[68-80],表3是这些MXenes 材料在肿瘤诊疗领域应用情况的总结。从表3可见,近年的研究一方面不断开发新MXenes 用于肿瘤诊疗,另一方面也在构建多功能MXenes 复合纳米材料,以此获得诸如医学成像、主动靶向和药物可控释放等性能。
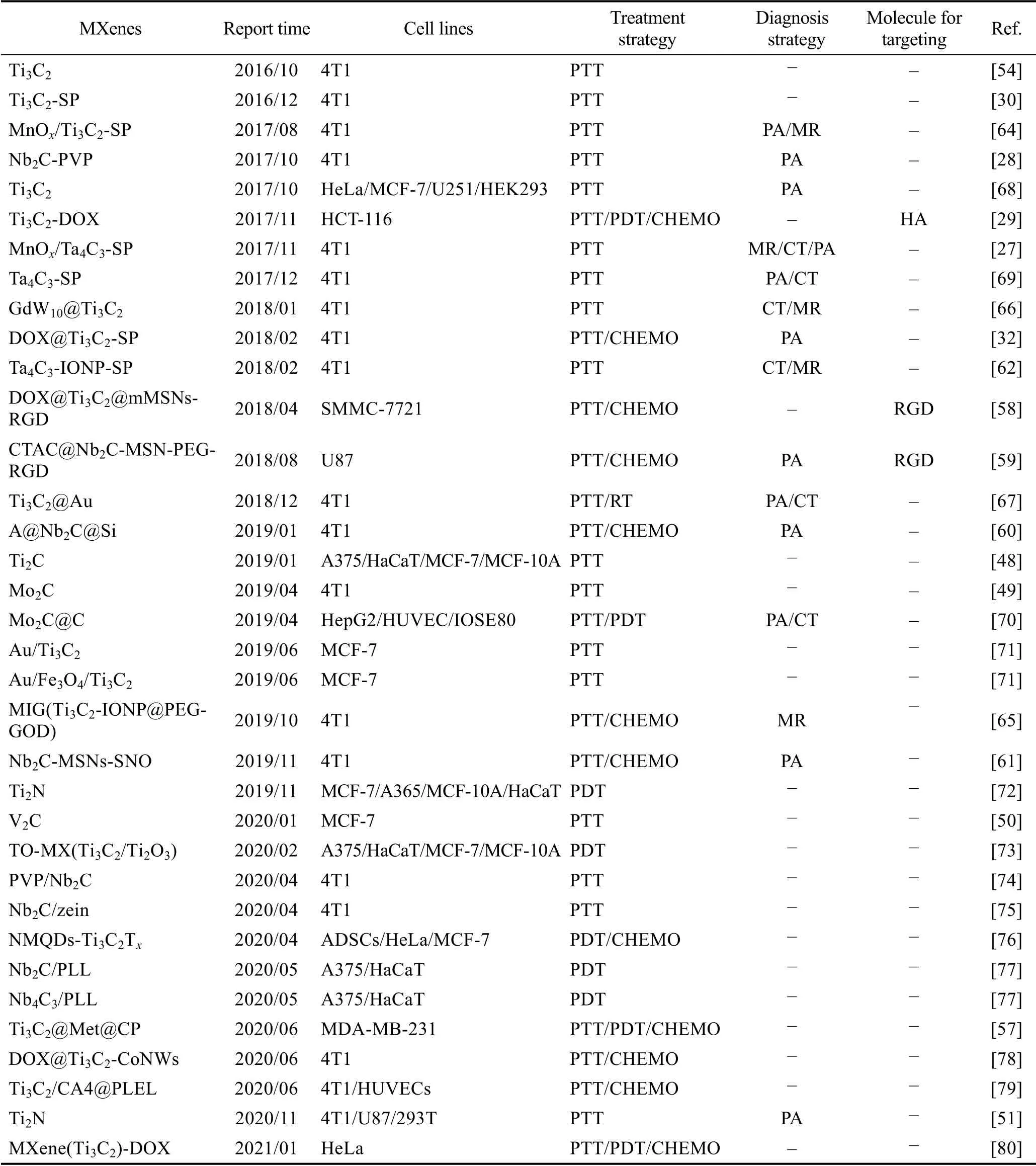
表3 应用于肿瘤诊疗的MXenesTable 3 MXenes for application in tumor theranostics
4 MXenes 辅助肿瘤诊疗的其他性能及应用
MXenes 不仅在肿瘤诊疗领域显示出巨大的应用潜力,在生物传感、药物递送、骨组织工程和抗菌等生物医学领域中也展现出优异的性能,都有可能较好地辅助肿瘤靶向治疗。
生物传感利用固定在电极上的生物分子与被检测生物物质进行特定结合,所产生的生物化学信号可通过生物传感器转换成电信号,被检测生物物质浓度与电信号大小相关。Zhang 课题组[81]利用Ti3C2构建了一种检测骨桥蛋白(Osteopontin,OPN)的生物传感器(图7(a)),固定在MXenes 复合材料表面的配体蛋白可与OPN 特异性结合,配体蛋白构象发生改变,从而产生电信号用于检测OPN 浓度,其最低检测限为0.98 fg/mL,性能优异,可重复使用。这一灵敏的特异性结合特点也可为特异性表达OPN 的肿瘤构建载药诊疗MXenes 提供思路。
MXenes 有独特的2D 平面结构,有较大的比表面积,纳米级的材料尺寸使其更容易在人体血液中运输,是一种良好的药物递送载体。Chen 课题组[32]通过SP 修饰的Ti3C2纳米片对DOX 载药量高达211.8%。
MXenes 具有良好的生物相容性,部分MXenes材料在生物体内可降解,因此在骨组织工程中具有重要应用价值。Chen 课题组[82]将Nb2C 与骨生物材料复合,用3D打印制备了一种复合生物支架(图7(b)),在NIR-II 下可有效治疗杀死骨肿瘤细胞,同时,Nb2C降解释放的Nb 元素具有促进血管生成和骨再生能力,从而修复因手术切除骨肉瘤后的大面积骨缺损。而且,Nb2C 在NIR-II 下产生的热量可促进骨生物支架降解,为骨骼重塑提供了足够的空间。
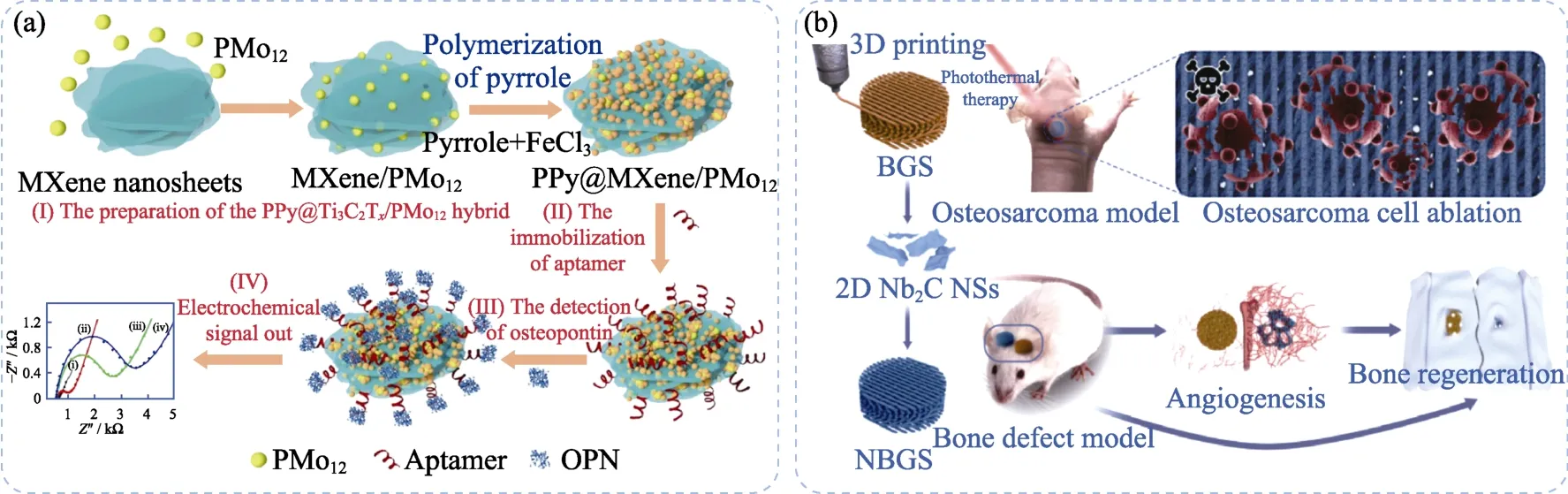
图7 MXenes 纳米材料在(a)生物传感[81]和(b)骨组织工程中的应用示意图[82]Fig.7 Schematic diagrams of the application of MXenes nanomaterials in (a) biosensing[81] and (b) bone tissue engineering[82]
此外,MXenes 表面基团具有良好的亲水性,可以增强与细菌细胞膜的相互作用,并与细菌细胞膜脂多糖分子形成氢键,从而阻止细菌摄取营养物质,抑制细菌生长[13]。MXenes 的这一抗菌性能亦有利于肿瘤手术后的伤口抗菌。
5 总结与展望
自2016年首次报道Ti3C2纳米片用于肿瘤治疗研究以来,研究人员一直致力于MXenes 的制备和表面功能化,以适用于PTT 和联合疗法的研究。尽管MXenes 在肿瘤诊疗领域显示出巨大的应用潜力,但在实现临床应用之前,还存在一些问题没有完全解决,主要包括以下三个方面。
1)MXenes 可控制备问题。MXenes 的可控制备研究尚不够深入,目前在肿瘤治疗领域使用的MXenes 主要通过HF 刻蚀法和氟盐刻蚀法制备,缺乏对制备过程条件的精确调控手段,以致MXenes终产物的纳米粒径、层数分布和表面基团等难于控制。另外,规模化制备是进一步商业化应用所不可或缺的,许多复杂因素会影响规模化制备高质量的MXenes,而目前MXenes 的制备仅停留在实验室阶段。研究人员需要探索MXenes 的规模化生产方法并进行工艺优化,这是保障MXenes 能够用于肿瘤临床治疗的前提条件。
2)生物安全性问题。MXenes 的临床应用须经过系统的生物安全性评估。虽然研究人员已在动物体内开展了多种MXenes 的短期毒性和器官残留分布研究,证实MXenes 有理想的短期生物安全性,但缺乏长期生物安全性研究,尚没有对遗传毒性、免疫毒性和生殖毒性的研究报道。此外,表面改性和构建复合纳米材料过程是否对MXenes 的生物安全性造成影响也需要进一步阐明。
3)靶向性问题。目前大多数研究表明MXenes依靠EPR 效应在肿瘤部位被动靶向积累,之后再可对肿瘤进行PTT 或联合治疗,但是被动靶向在肿瘤部位的积累效率较低。虽然理论上MXenes 主动靶向积累效率较高,但相关研究开展较少。未来需要开发更多的靶向策略,设法提高MXenes 的主动靶向治疗效果,减少对正常细胞的毒副作用。此外,针对不同肿瘤类型还需设计不同的靶向策略以提高治疗效果,真正实现有实际疗效的精准医疗。
虽然MXenes 在肿瘤诊疗领域的临床应用还面临诸多问题,但近五年来对MXenes 肿瘤诊疗研究已经有了诸多突破,未来有望在以下四个方面取得实质进展。
1)不同过渡金属元素构成的MXenes 的理化性质探索。目前实验室成功制备的MXenes 约有30 种,根据计算模拟结果来看,还有更多新型MXenes 材料有待实验合成、探索其理化性质、开发其在肿瘤诊疗领域的应用。
2)MXenes 的可控制备方法探索。目的是要面向临床应用,实现对MXenes 终产物在尺寸、表面官能团和层数等参数的精确调控,以及在此基础上规模化制备高质量MXenes。
3)新型空间结构的MXenes 探索。目前MXenes纳米片在肿瘤诊疗领域应用研究较多,未来有必要进一步制备MXenes 纳米管、纳米球、纳米笼等其他形貌的MXenes 材料,并应用于肿瘤诊疗,发掘此类应用的最佳空间结构。
4)MXenes 与其他纳米材料的复合探索。已证实MXenes 结构上负载其他纳米材料可提高MXenes自身的理化特性,赋予MXenes 复合材料光学及电磁学等特性。因此开发基于MXenes 与其他无机和/或有机材料复合的纳米材料,有望进一步提高MXenes 肿瘤诊疗性能。
随着化学、材料学、生物学和医学的发展以及各学科之间的互相合作,相信MXenes 在未来肿瘤诊疗领域将有更加光明的应用前景。
