CRISPR/Cas系统在新型冠状病毒肺炎快速诊断中的应用
2022-06-27吴永彬
吴永彬,李 凌
(1.广西壮族自治区南溪山医院检验科, 广西桂林 541002; 2.南方医科大学基础医学院,广州 510515)
规律成簇间隔的短回文重复序列(clustered regularly interspaced short palindromic repeats, CRISPR)及其相关蛋白(CRISPR-associated protein, Cas)相互协同,构成原核生物中CRISPR/Cas自适应免疫系统的基础。近年来,该系统被开发成为一种高效的分子诊断工具[1-2],并在感染性疾病的诊断领域取得重大突破[3-6],严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus-2,SARS-CoV-2)及其变异株[7-8]引起的新型冠状病毒肺炎(coronavirus disease 2019, COVID-19)作为一种新的传染病,其导致的疫情仍在全球肆虐,快速、便携、准确的诊断方法是及时发现病原体,防止疫情扩散的重要手段。为此,本文将关注现有和正在研究的CRISPR/Cas系统用于COVID-19快速诊断的潜在能力,并重点探讨其在临床中的应用和面临的挑战,以期为新一代分子诊断技术的研究和SARS-CoV-2等病原体的检测提供借鉴和参考。
1 CRISPR/Cas系统工作机制
1.1 CRISPR/Cas系统简介 CRISPR/Cas系统由四部分组成,分别为CRISPR簇、前导序列、重复序列、以及一系列保守的CRISPR相关基因。最初发现于原核生物的基因组中,包括细菌和古细菌[9],随着Cas的发现和重组DNA技术的应用,科学家又发现CRISPR/Cas系统还是原核生物防御系统对病毒的自适应免疫基础,其通过俘获一段外源DNA序列,找出其原间隔序列邻近基序(protospacer adjacent motif, PAM),表达并加工CRISPR RNAs(crRNA),当噬菌体二次感染时,crRNA与Cas蛋白复合物相互作用,形成一个具有特殊功能的复合物crRNP(crRNA-Cas ribonucleoprotein),靶向干扰入侵核酸的合成,特异性地阻止噬菌体感染,见图1。近年来,经过重新设计的Cas扩展了CRISPR/Cas系统的功能和应用,也丰富了CRISPR/Cas系统的进化分类[10],即类别一(包含I, III和IV型)和类别二(包含II, V和VI型)。CRISPR/Cas系统常用的Cas蛋白为II型(Cas9等)、V型(Cas14, Cas12a, Cas12b等)和VI型(Cas13a,Cas13b等)效应蛋白[11-12]。其中Cas12和Cas13在COVID-19快速诊断中的应用越来越受到重视[13-15],包括近期SARS-CoV-2新变异株的诊断[16-17]。
1.2 CRISPR/Cas12系统工作机制 Cas12具有RNA核糖核苷酸酶(RNA ribonuclease, RNase)和DNA核糖核苷酸酶(DNA ribonuclease, DNase)活性,可激活独立的crRNA生物反应[18],无需反式激活crRNA(trans-activating crRNA, tracrRNA)的协助。在CRISPR/Cas12a系统中,Cas12a(或称Cpf1)特异性地识别DNA靶标内的5'-TTTV-3'PAM,使crRNA间隔区片段特异性地与靶标DNA碱基配对[19],实现DNA双链切割,形成黏性末端,见图1。基于该特性,CHEN等[20]人开发了一种新型的分子诊断工具,即DNA内切酶靶向的CRISPR反式报告系统(DNA endonuclease targeted CRISPR trans reporter, DETECTR)。在该系统中,Cas12a利用自身的核酶功能域对crRNA的表达阵列进行剪切,并与荧光淬灭法结合起来实现基因编辑。同时,通过重组酶聚合酶扩增(recombinase polymerase amplification, RPA)技术来提高检测系统的灵敏度,进一步提升了其整体检测优势和临床应用价值。
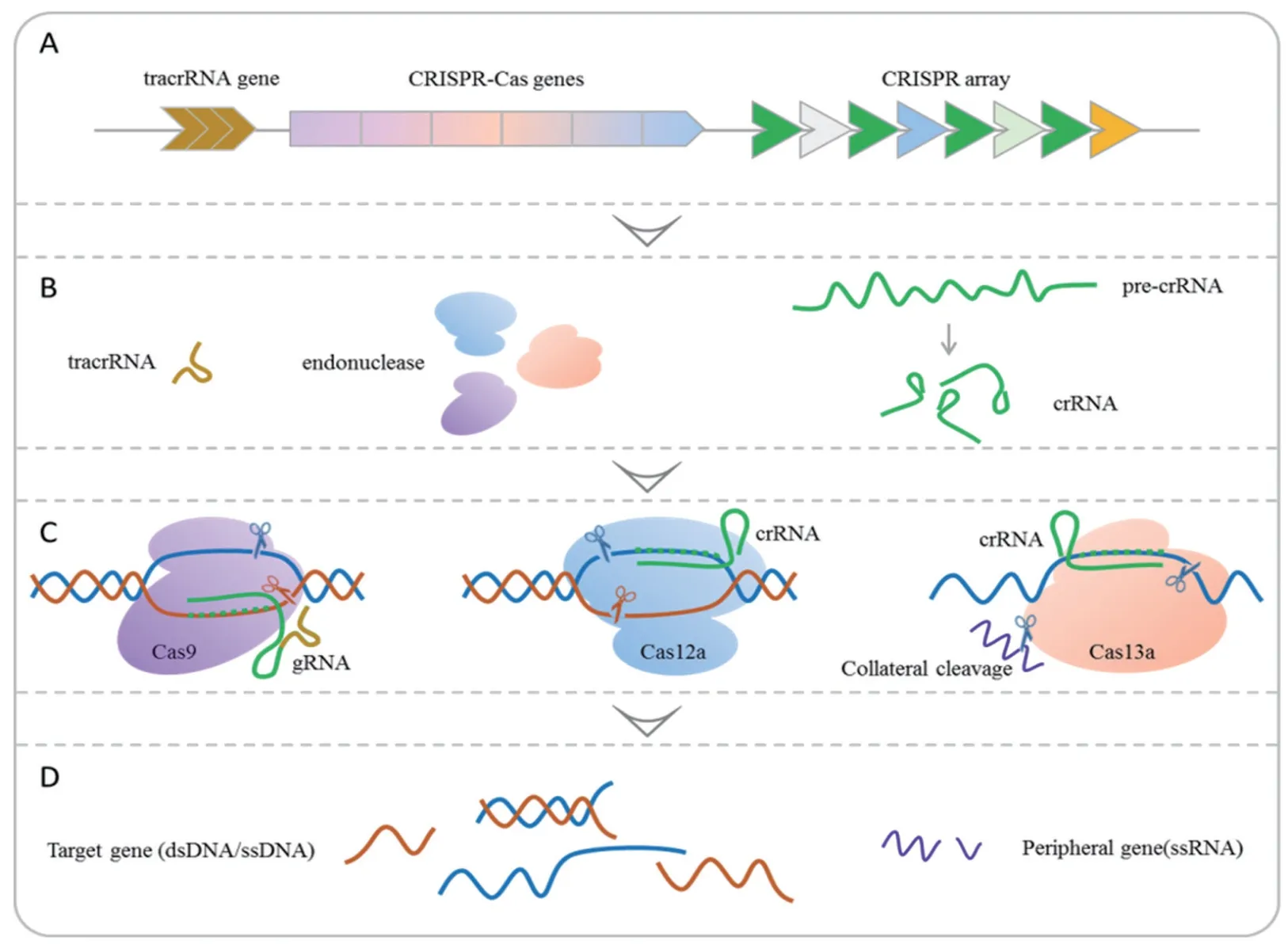
图1 CRISPR/Cas系统工作机制
1.3 CRISPR/Cas13系统工作机制 与其他Cas不同的是,Cas13a(或称C2c2)具有双重核酸酶特性[21],一方面专一靶向RNA进行剪切靶序列,另一方面又非特异性地对附近的RNA片段进行无差别的“附带剪切”[22]。其工作机制是:先募集由重复茎环结构和间隔序列构成的向导RNA(guide RNA, gRNA)片段,再由gRNA-Cas13复合物通过RNA-RNA配对识别靶RNA并切割靶向区域,此过程中Cas13需要前间隔序列侧翼位点(protospacer-flanking site, PFS)来协助锁定目标RNA,见图1。基于该特性,另一种新型的分子诊断工具,即特异性高灵敏度酶促解锁系统(specific high-sensitivity enzymatic reporter unLOCKing, SHERLOCK)由MYHRVOLD等[4]人建立起来,其借助RPA恒温扩增技术对样本中核酸进行扩增,产物经T7核糖核酸聚合酶介导转录后再通过Cas13a工具进行检测。目前,该系统通过不断优化,引入辅助性CRISPR相关酶Csm6,已实现更高灵敏度的定量检测[23]。
2 CRISPR/Cas系统在COVID-19快速诊断中的应用
目前,COVID-19的常见诊断分子技术主要有逆转录PCR(reverse transcription-polymerase chain reaction, RT-PCR)、恒温扩增[如:重组酶聚合酶扩增(recombinase polymerase amplification, RPA)、环介导等温扩增(loop-mediated isothermal amplification, LAMP)、重组酶介导扩增(recombinase-aided amplification, RAA)等]、微滴数字PCR、微流控芯片等,基于CRISPR/Cas系统开发的快速诊断平台见表1。与传统分子诊断技术比较,其具有以下几点优势:①快速,现有的技术平台均可在1h左右完成,快速综合核酸酶串联检测(fast integrated nuclease detection in tandem, FIND-IT)甚至可缩短至20min内完成。②便携,无需大型和专用的设备,如FIND-IT,使用CRISPR酶Cas13和Csm6放大荧光信号,而不用借助扩增仪来完成。③准确,以SHERLOCKv2技术为例,其灵敏度高至10-21摩尔水平。④廉价,如SHERLOCKv2试纸只需几美元、DETECTR单次检测成本不到一美元。⑤多通路,基于不同的Cas和酶的组合,CRISPR/Cas系统可实现多通路检测,如Cas12a,Cas13与Csm6的组合。上述特点充分展现了CRISPR/Cas系统在COVID-19快速诊断中的优势。其中,DETECTR和SHERLOCK,尽管他们仍处于初期研发阶段,但可能是临床应用最有潜力的两种技术平台[24-26]。
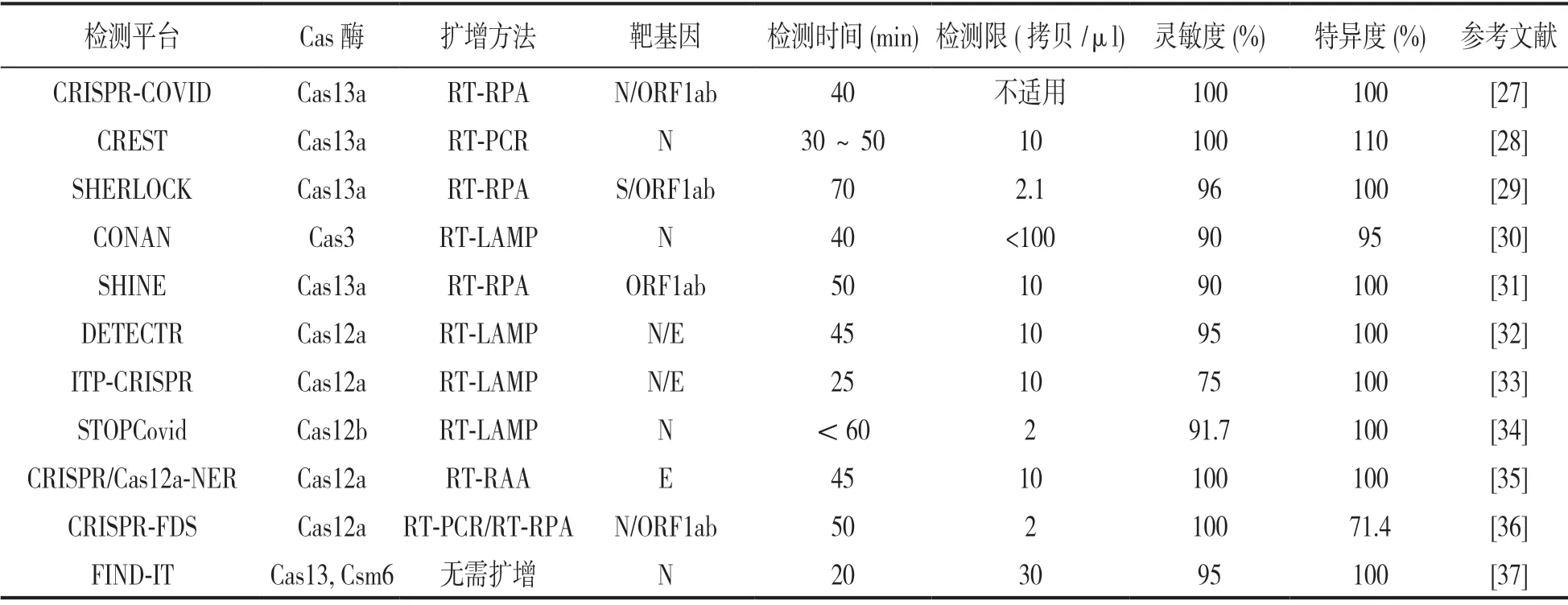
表1 基于CRISPR/Cas系统快速诊断COVID-19的主要技术平台
2.1 DETECTR快速诊断COVID-19 DETECTR平台已用于实验室和临床环境中的大量病毒的诊断。基于等温扩增与CRISPR/Cas12系统相结合的DETECTR技术可特异性地检测SARS-CoV-2的N基因和E基因,且在30min左右获得结果[38-39],这节省了基于Cas13a检测所需的体外转录步骤花费的时间[40]。而且DETECTR可以同时使用不同的gRNA来避免由于N基因突变引起的假阴性结果[40]。此外,相较于其他人源性冠状病毒,DETECTR检测SARS-CoV-2的特异度可达100%[39]。因此,无需特殊设备的DETECTR技术可作为RTPCR技术的有效补充[41]。
2.2 SHERLOCK快速诊断COVID-19 SHERLOCK是最早基于CRISPR/Cas系统应用于COVID-19快速诊断的技术平台[42-43],并得到不断的优化和升级[44]。在crRNA的引导下,Cas13识别并结合SARS-CoV-2两个靶基因S和ORF1ab,同时激发了Cas13对周围ssRNA分子的“附带剪切”,系统将淬灭荧光的ssRNA报告基团添加到反应中,当激活的Cas13切割RNA后,收集检测信号以示目标核酸的存在。同时,通过RPA或RT-RPA扩增目标DNA或RNA,再与T7转录相结合,将扩增后的DNA转化为RNA,以利于后续的Cas13检测,最终使其检测灵敏度可及10-18摩尔水平,特异度更是达到单碱基错配,且在不到1h内无需特殊设备条件下完成检测。
2.3 FIND-IT快速诊断COVID-19 基于CRISPR/Cas系统快速诊断COVID-19的主要技术平台几乎都是建立在基因扩增的基础上设计,见表1归纳的前10种技术平台。根据最新研究,LIU等[37]人开发了一种不依赖于恒温扩增技术的FIND-IT技术,即通过RNA引导的Cas13和Csm6与化学稳定激活剂相结合,可以使用紧凑型探测器检测从呼吸道拭子样本中提取的SARS-CoV-2,并在20min内实现对每微升RNA标本约30个拷贝进行稳定检测的能力[37]。该方法特别适合于标准实验室之外的场地开展,如临床床旁和资源有限的偏远地区。
3 CRISPR/Cas系统在COVID-19快速诊断中的局限
新兴的基于CRISPR/Cas系统的诊断工具在SARS-CoV-2等病原体的检测中也存在一些局限:①CRISPR/Cas系统自身在病原体检测优势还未充分体现 :(a)需借助其他分子诊断技术辅助进行,(b)需利用多个不同的Cas实现多重病原体检测,(c)需结合预扩增环节提高检测灵敏度;②CRISPR/Cas系统在对RNA靶标进行编辑时存在易脱靶情况;③CRISPR/Cas系统在真核细胞中进行有效的ssRNA切割时可能存在毒性;④CRISPR/Cas12系统存在较低的基因组覆盖率和较低的靶向效率等缺点[45-47];⑤CRISPR/Cas13系统在多步核酸扩增环节中存在可能影响精确定量的缺陷。其中,针对常见的脱靶效应带来的问题,目前解决的策略主要是从预测脱靶位点,优化sgRNA设计及修饰Cas蛋白结构等途径入手[48]。
4 总结与展望
CRISPR/Cas技术革新了分子诊断领域的研究模式,尤其是在感染性疾病的诊断上具有广阔的应用前景。本文重点论述了其在COVID-19快速诊断中的潜在应用,尽管诸如DETECTR和SHERLOCK等技术尚未完全实现商业化,但CRISPR/Cas系统的精确度和易操作程度目前在其他分子诊断工具中是无法实现的。现有的COVID-19诊断技术仍由数十年前的RT-PCR技术所主导,其昂贵的专用设备和严苛的实验环境限制了其在体外诊断的施展空间,尤其是近期出现的SARS-CoV-2新型突变体,给全球持续紧张的疫情防控带来了新的挑战。目前,相同的突变体已在不同国家独立出现[49],新的突变位点可能会增加SARS-CoV-2的传染性,甚至对现有的治疗和疫苗接种人群构成重大威胁[50-51]。从长远而言,开发高效的且同时覆盖病原体多个靶基因位点的新型分子诊断工具更具临床价值。另外,鉴于CRISPR/Cas系统本身的局限性,可以预见的是,未来的CRISPR/Cas技术平台仍离不开其他技术的支持,除前述的各类PCR,恒温扩增外,后期还会有更多的新兴材料与技术加入到CRISPR/Cas系统中,开发出更为实用和智能的诊断工具,这将为COVID-19等感染性疾病的快速诊断带来新的希望和契机。
