老年自发性脑叶反复出血一例
2022-06-27李占稳东潇博宋光荣蔡旭刘慧敏
李占稳,东潇博,宋光荣,蔡旭,刘慧敏
(北京中医药大学东方医院:1病理科,2脑病科,北京 100078)
老年自发性脑叶出血是不同于高血压脑出血的一类自发性脑出血疾病。随年龄增长,该类疾病发病率越来越高。高复发率是自发性脑叶出血的临床治疗难点,本文通过分析1例典型脑叶反复出血病例,结合文献复习,探讨自发性脑叶出血的病因、预防及治疗特点。
1 临床资料
患者女性,83岁,主因“咳嗽、咳痰加重半天”于2016年5月10日收入北京中医药大学东方医院呼吸科。入院症见:咳嗽、咳痰,痰色灰白、质黏、量少,不易咳出,咽痒,无发热,无喘息憋气,无夜间呼吸困难,无鼻塞流涕,口干口苦,纳眠可,小便调,大便可。入院查体:听诊双肺呼吸音粗,双下肺可闻及少许湿啰音,未闻及干啰音及双肺摩擦音。心脏叩诊向左下扩大。心率78次/min,率齐,心音有力,各瓣膜听诊区未闻及病理性杂音。患者长期卧床,高血压病史10年,冠心病史5年,长期口服阿司匹林0.1 g/d抗血小板聚集。入院诊断:肺部感染,高血压3级(极高危组),冠状动脉粥样硬化性心脏病。入院后予抗感染、化痰治疗。同时发现患者血D-二聚体升高(4.99 mg/L),血栓形成风险高,待除外肺栓塞。给予皮下注射低分子肝素钠(4 100 U,1次/12 h)进行抗凝治疗。患者否认家族性遗传性疾病史。
3次脑出血情况及诊疗过程患者于2016年5月13日早晨约6:00起床后发生剧烈咳嗽,继而出现头痛、头晕、恶心、呕吐、言语不利及左侧肢体活动不利。我院急诊科行头颅CT检查示,右侧颞顶枕大脑皮层下大量出血(图1A),遂给予脱水、止血治疗。完善检查后考虑患者意识状况进行性恶化,左侧肢体肌力下降进行性加重,随时有脑疝可能,遂以“脑出血”转入脑病科行“右颞枕开颅,脑内血肿清除,去骨瓣减压术”。术中见右侧颞、枕、顶叶蛛网膜下腔出血,脑组织出血、肿胀、张力高。于脑表面出血中心部位切开皮层,进入血肿腔内,见血凝块质韧、与脑组织界限不清,分块切除血凝块及周边部分混杂脑组织,标本送病理检查(图2),诊断为病理学支持的很可能的脑淀粉样血管病(cerebral amyloid angiopathy,CAA)。术中未见畸形血管团、占位性病变及动脉瘤。术后患者曾出现一过性血压升高,达180/105 mmHg(1 mmHg=0.133 kPa)。采用静脉推注持续泵入10 mg/h乌拉地尔控制血压,直至血压恢复至120~138/60~80 mmHg,心率至80~97次/min,逐渐减停降压药物。患者麻醉未清醒,带气管插管返回病房。术后6 h患者仍未清醒。
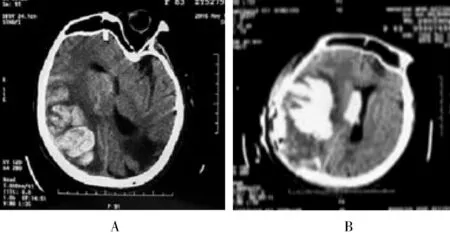
图1 患者脑出血CT图像Figure 1 CT images of patients with intracerebral hemorrhageA: first cerebral hemorrhage; B: second cerebral hemorrhage.

图2 手术切除的血管组织病理检查Figure 2 Histopathological examination of surgically removed vascular tissueA: hematoxylin-eosin staining showed damaged vascular wall and homogenous powdered amyloid (×400); B: immunohistochemical staining showed positive β protein deposition in the vascular wall (×200).
术后20 h复查头颅CT见脑内原出血灶周围皮层下第2次大量出血(图1B)。患者家属拒绝再次开颅手术,遂给予脱水、止血、稳定血压、持续呼吸机辅助呼吸、监测并控制血糖、维持酸碱及电解质平衡、脑保护及营养支持等治疗。患者于术后第3天自主呼吸部分恢复,呼吸机改为压力支持模式。术后第7天患者生命体征逐渐平稳,第11天拆除切开缝线,伤口愈合良好。此时患者出现一过性血压升高(达180/100 mmHg)及反流性肺炎导致的全身炎症反应,均给予对症治疗,同时进行胃肠道管理,改善患者的舒适度。
术后第13天凌晨1∶00患者双瞳孔逐渐散大,对光反应消失,头颅右颞枕减压窗张力较前明显增高,考虑为颅内第3次出血,紧急给予脱水及止血治疗。1∶20患者自主呼吸消失,切换呼吸机模式为容量控制,并增加呼吸机给氧浓度。因患者家属拒绝行头颅CT检查,未取得颅内再出血的影像学证据。最终患者逐渐出现心率下降,血压下降,经抢救无效死亡。死亡原因考虑为脑出血、脑疝、脑干功能衰竭。
2 讨 论
CAA是老年人一种独立的脑血管病,其病理特点为大脑皮质及软脑膜小血管壁内的中层和弹力层有淀粉样物质沉着,从而导致血管壁坏死、出血。CAA发病机制未明,目前认为β-淀粉样蛋白的产生和清除之间的不平衡及“朊病毒假说”可能是该疾病的诱因[1]。CAA的诊断标准经多次改进,现广泛使用改良的Boston诊断标准[2],该标准包括了病理学及影像学的特征表现。本例患者首次以肺部感染就诊,后发脑出血症状,遂手术进行血肿清除,结合临床症状、影像及手术活检病理,诊断为病理学支持的很可能的CAA。
CAA临床表现复杂,早期可能不表现出任何临床症状,因此识别潜在的CAA患者较为困难,但仍然有部分患者出现一些特征性的端倪。主要表现为以下3点:(1)反复和(或)多发性脑叶出血。在老年人非外伤性脑出血中,CAA是继高血压之后的第二常见病因。高血压患者的出血灶多在基底节区、丘脑、脑室、小脑及脑干,因此,当临床上老年人出现多发性和复发性脑叶出血时,应考虑CAA的可能。(2)短暂性局灶性神经系统发作(transient focal neurological episodes,TFNE)。CAA与短暂性脑缺血发作均可表现为TFNE,具有一定迷惑性,但CAA更多与出血(特别是浅表皮质铁质病或局灶性蛛网膜下腔出血)、而不是缺血有关[3]。因此,切勿将CAA误诊为短暂性脑缺血发作而给予抗栓治疗。(3)认知功能障碍、快速进展性痴呆。有研究显示,部分CAA患者在脑出血前已存在认知功能障碍,出血后比例继续增加[4]。此外,CAA与阿尔茨海默病在病理和临床表现上相互重叠,2者常伴发[5]。因此,痴呆也是CAA的一种诊断信号。CAA发生率随着年龄增加不断升高,当老年患者出现上述特征性表现时,临床医师应提高警惕,必要时进行磁敏感加权成像检查,以识别CAA早期的微出血病灶。本例患者在诊断CAA前患有肺部感染及高血压疾病,很容易在治疗现有具有明显症状的疾病时忽略CAA,但此患者有脑叶出血表现,为诊断CAA提供了线索。
目前没有治疗CAA的特异性方法,CAA患者治疗的重点在于降低反复发生的出血风险。对于合并高血压的CAA患者,严格控制血压可降低出血风险[5]。若CAA合并心房颤动或血管闭塞等疾病,在使用抗凝药物和他汀类药物时要尤为谨慎[6,7],因其在治疗老年人缺血性疾病的同时,也增加了出血的风险。临床医师需权衡利弊,制定个体化的治疗方案。本例患者有高血压病史且出现一过性血压升高,并在入院初期因血D-二聚体升高,为降低血栓风险而使用了肝素,这些都可能和脑出血的复发相关。CAA出血后是否清除血肿,需要根据出血量、出血部位及患者的生命体征综合判断[8,9]。本例患者因有脑疝形成故行紧急手术,但术后复发出血。因此,更精确的手术适应证需要更多临床研究进行验证。此外,采取手术治疗的患者术后应将清除的血肿常规送检病理科以及时确诊CAA。
综上所述,本文报道了1例脑叶反复出血的病例。该患者前期应用抗凝药物及手术治疗未获得相对好的治疗效果。但本例给予我们的启示是,对于临床上潜在的CAA相关脑叶出血患者,应根据现有症状综合判断,早期识别及诊断CAA,积极控制脑出血复发的已知危险因素。围手术期血压管理是防止脑内再出血的有效措施,同时应特别注意谨慎使用溶栓抗凝药物。
