心脏起搏器谐振式无线供能LCL-LCL的集成
2022-06-25陈伟华宋邑玮闫孝姮
陈伟华 宋邑玮 闫孝姮
心脏起搏器谐振式无线供能LCL-LCL的集成
陈伟华 宋邑玮 闫孝姮
(辽宁工程技术大学电气与控制工程学院 葫芦岛 125000)
为减小植入式心脏起搏器无线充电系统的体积及电磁干扰,该文设计一种工作频率为150kHz的两端串并联(LCL-LCL)补偿集成式磁耦合谐振式无线供能系统。将谐振线圈取代电感集成到主线圈上;首先建立线圈模型并进行优化,分析匝数与匝间距对线圈互感的影响规律,设计一种耦合系数最佳的圆角方形线圈;然后对比集成式与非集成式结构系统的传输效率,验证了此结构在效率和体积更具优势;最后通过模拟三维人体组织,计算比吸收率和温升以及电磁场强度,进一步评估植入式充电系统的可行性和安全性。实验结果表明,在线圈中心对齐相距8mm的条件下,系统传输效率可达73%,比非集成式结构提升了15%,最大温升仅为1.2℃。
心脏起搏器 集成线圈 三维人体 安全评估
0 引言
目前,国内外针对有源植入式医疗设备无线电能传输技术开展了广泛的研究,以降低二次手术更换电池可能导致的感染风险[1-4];然而若要实现其成功应用,必须着重考虑效率、植入和安全等问题,因此供能效率、拓扑结构及安全性成为近年来的研究热点[5-13]。
为实现高效率传输能量,国内外众多专家学者已提出许多性能优越的拓扑结构,文献[14]中,T. Campi等对四种基础拓扑串联-串联(Series-Series, SS)、串联-并联(Series Parallel, SP)、并联-并联(Parallel-Parallel, PP)和并联-串联(Parallel- Series, PS)做了简要的分析,其中PP和PS两种拓扑一次侧电路并联补偿的电压值过高,当补偿拓扑输入电压的极性变化时,发射端并联补偿电容(PS和PP补偿中的第一个P对应的补偿电容)的电压会迅速上升到电源电压,此后该电容中不再有电流流过,除非输入电压极性发生变化,该电容已经失去了无功补偿的作用。而SS和SP拓扑由于谐振匹配灵敏度过高,导致系统的不稳定性,也会限制传输效率。相较于以上四种低阶补偿拓扑,双端LCL拓扑结构由于具有输出电流恒定以及传输性能高的优点[15],因此就传输性能而言较适合应用于植入式医疗[16]。
然而对于双端LCL补偿拓扑,植入侧结构复杂,谐振电感的存在将导致植入体积较大,不利于植入,因此需要采取措施将植入侧电路结构优化以减小植入体积;对于高阶补偿拓扑,众多专家学者针对其结构提出了许多优化方法[17-19]。A. N. Laskovski等提出了一种用于植入式医疗的新型无线传输线圈,该线圈采用方形螺旋结构,通过将四个线圈串联叠加在一起,有效地减小了植入所需体积,但线圈间的串联导致了系统阻抗的增大,降低了系统的传输效率[20]。S. H. Ahn等设计了一种应用于近距离的双端LCC(LCC拓扑, LCC topology)无线电能传输系统,该系统对发射端与接收端各自的电容和电感元件进行了集成,发射线圈由一个多匝的方形线圈和位于其中心的方形金属板组成,该设计利用线圈产生涡流以减小互感的变化,实现了系统的小型化并提高了传输效率,但对于方形金属板设计要求极其严格[21]。K. Sadeque等针对四线圈串联拓扑,提出了一种平面四线圈集成优化方法,其将源线圈与负载线圈分别集成于发射线圈与接收线圈之中,该方法有效地简化了系统电路结构,但集成线圈间的错位将会降低系统的传输性能[22]。
由于该系统应用于人体,因此必须保证其安全性,目前针对植入式心脏起搏器的安全性研究,T. Campi等建立了二维轴对称模型进行安全评估,但只是简单地将人体简化为三层组织结构,并未细化到三维模型[23]。Xiao Chunyan等虽然建立了三维人体模型,但只是在发射线圈上直接施加电流激励,并未考虑到场路耦合这一因素,未加场路耦合而直接给定施加激励源等同于给定一个均匀场,由于电路拓扑复杂,而引入电路可以与实际的模型结合起来,更加准确地模拟实际情况[24]。
综上所述,为减小植入式心脏起搏器无线充电系统的体积以及电磁干扰,本研究设计了一种工作频率为150kHz[14]的双端LCL集成式磁耦合谐振式无线供能系统。建立线圈模型并进行优化,分析匝数与匝间距对线圈互感的影响规律,并搭建了实验系统对比集成式与非集成式结构系统的传输效率。构建了一个考虑场路耦合的三维人体模型,通过模拟人体组织,计算比吸收率和温升以及电磁场强度,评估了充电系统的可行性和安全性,减小了人体接收端器件的体积,并提高了传输效率。
1 基于磁耦合谐振的双端LCL补偿电路拓扑
1.1 双端LCL补偿电路模型
如图1所示为双端LCL补偿电路,该模型基于磁耦合谐振原理,图中,为交流电压,p和s分别为发射线圈和接收线圈的电感,p和s为其内阻;f和r分别为两侧谐振电感,f和r为其内阻;f和s分别为发射端和接收端的补偿电容,1为发射线圈与接收线圈之间的互感,为负载。
针对植入式心脏起搏器体积以及效率的问题,本文采用了集成式双端LCL补偿电路结构,建立在传统非集成式电路模型的基础上,如图1所示,利用谐振线圈来替代发射端与接收端的谐振电感,使其电路的互感增多。设2为发射线圈与发射端谐振线圈之间的互感,3为发射线圈与接收端谐振线圈之间的互感,4为发射端谐振线圈与接收线圈之间的互感,5为发射端谐振线圈与接收端谐振线圈之间的互感,6为接收线圈与接收端谐振线圈之间的互感。该集成模型考虑了线圈的内阻,其中接收单元只需使用一个电容元件来补偿谐振线圈的电感,有效地减小了植入所需体积,此外该结构通过植入线圈的电流较小,因此适用于植入人体。
1.2 双端LCL网络的阻抗匹配
对于非集成式双端LCL网络,其互感仅有一个,即发射线圈与接收线圈之间的互感1,非集成式双端LCL补偿系统的谐振条件为

式中,为频率。
互感1表达式为

式中,1为耦合系数。
考虑其内阻,系统二次侧等效输入阻抗x为

当系统发生谐振时s=r,x化简为

折射到一次侧的等效阻抗y为


其中

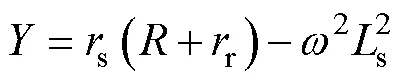

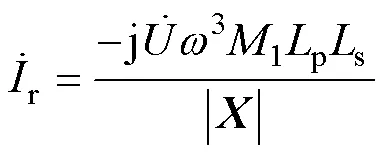
可以看出,当逆变输出电压保持恒定时,输出电流也保持恒定。
对于集成式双端LCL网络,如图1所示,补偿电路存在6个互感,由基尔霍夫电压定律得方程组为

由克莱姆法则求取非齐次线性方程组得行列式为


传输效率表达式为

式中,out为输出功率;in为输入功率。
2 磁耦合机构优化设计
2.1 磁耦合机构分析
本文采用的集成式线圈耦合结构如图2所示,系统采用双端LCL补偿,发射端与接收端结构对称。从上到下依次为发射端谐振线圈f、铁氧体层、发射线圈p、接收线圈s、铁氧体层、接收端谐振线圈r;其中发射与接收线圈结构相同呈圆角方形,尺寸相同;由于双端LCL拓扑参数的唯一性,已知发射与接收线圈的大小,在谐振状态下就确定了唯一的谐振线圈电感大小;两侧谐振线圈呈DD(Double D series)形,同尺寸空间角度旋转90°;各侧的谐振线圈与主线圈共用铁氧体层。

图2 集成式磁耦合机构模型
当两侧谐振线圈集成到各侧的主线圈上时,由图1可以看出,四个线圈中存在6个耦合系数,ps为一次侧主线圈p与二次侧主线圈s间的耦合系数,pf为一次侧主线圈p与其谐振线圈f之间的耦合系数,sr为二次侧主线圈s与其谐振线圈r之间的耦合系数,fr为两侧谐振线圈之间的耦合系数,fs与pr分别为异侧主线圈与谐振线圈之间的耦合,无线充电系统的功率传输效果主要依赖于发射与接收线圈之间的耦合系数ps,异侧耦合会增加传能系统的无功功率,导致系统传输效率降低,因此对线圈结构进行集成时,应使发射与接收线圈之间的耦合达到最佳状态,同时使异侧线圈耦合系数降低到最小。
以接收端为例,由于DD形谐振线圈r结构特殊,根据电流流向以及右手定则的判断,线圈左右两侧产生大小相等、方向相反的磁通密度r1与r2,即r1=-r2,当磁场穿过接收线圈s时,所产生的磁通量可表示为r1s和r2s,穿过的总磁通量即为r1s+r2s=0,即

式中,rs为谐振线圈r穿过接收线圈s的总磁通;r1和r2分别为DD线圈左右两侧的磁通密度;s为接收线圈r的面积,由于rs=0,故rs=0,即接收线圈与谐振线圈间的互感系数rs为

由于二次侧与一次侧对称,同理,发射线圈与谐振线圈间耦合系数fp=0,此外由发射线圈p穿过谐振线圈r的总磁通为0,由接收线圈s穿过谐振线圈f的总磁通量也为0,即异侧耦合系数pr=0、sf=0,同理fr=0。
2.2 磁耦合机构优化
所建立的主线圈结构为圆角方形耦合线圈,即发射线圈和接收线圈,主线圈模型如图3所示,参照文献[14, 25]所设计的线圈参数,本文所选取的主线圈尺寸为35mm×35mm×0.3mm,外径已定,线径为双股0.3mm,通过线圈匝数与匝间距两个变量对线圈进行参数化扫描优化,采用有限元仿真软件COMSOL Multiphysics对线圈变量进行分析,从而确定最佳线圈匝数与匝间距,在自变量匝数与匝间距的变化过程中,内径=-2[(+)-]相当于因变量也随之变化,内径的变化已被隐含在线圈的控制变量关系中;主线圈设计与优化流程如图4所示。首先给定主线圈尺寸以及两线圈之间的距离=0.8cm,通过建立线圈模型并控制线圈匝数(=1~23,步长为1)和匝间距(=0~0.15mm,步长为0.05mm)这两个变量来优化线圈结构,确定出最佳的匝数与匝间距,直至优化出耦合系数最佳的线圈结构。

图3 主线圈模型
对以上两个变量进行同步优化,匝数、匝间距与耦合系数关系如图5所示,在匝间距不变的前提下,随着线圈匝数的增多,耦合系数先增加后减小;在匝数为21匝,匝间距为0mm(线圈紧凑)时,得到发射线圈与接收线圈的耦合系数最佳。

图4 主线圈优化流程
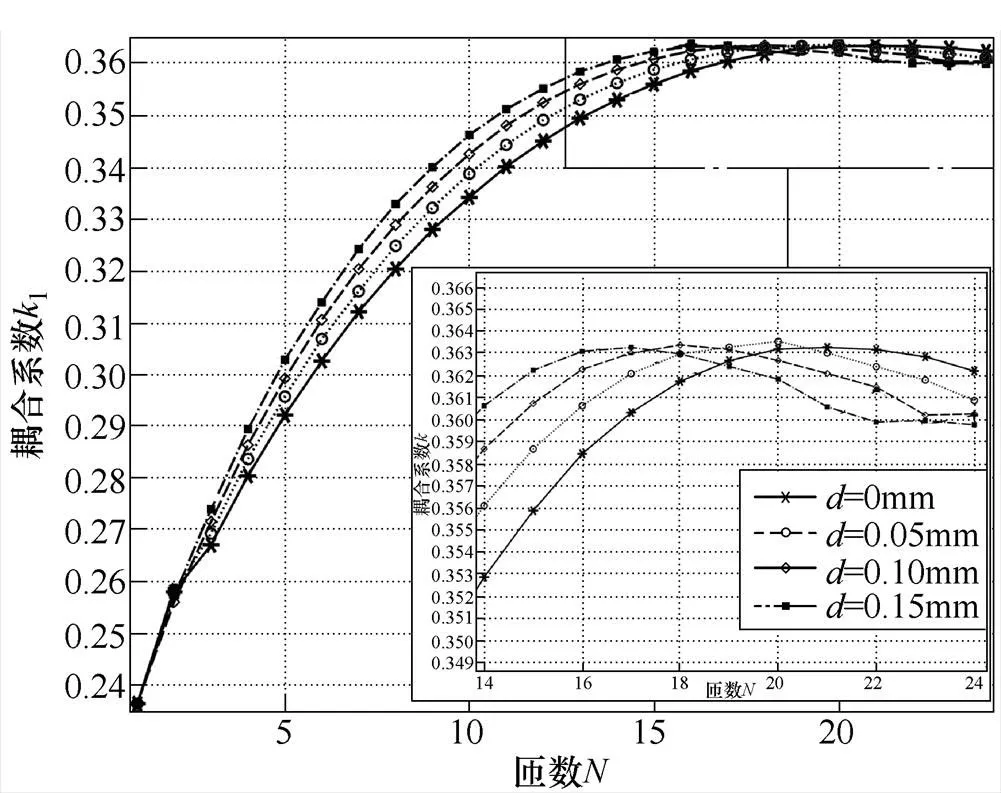
图5 匝数、匝间距与耦合系数关系
图6为空间旋转90°的DD形谐振线圈模型,所选取的线圈外围尺寸为35mm×35mm×0.3mm,线径为单股0.3mm,由于双端LCL补偿拓扑的谐振特性,可知谐振线圈与主线圈的电感量相同。通过COMSOL Multiphysics仿真得出匝数为19,匝间距为0mm时满足谐振线圈的电感量需求,此时系统可达到谐振状态。

图6 谐振线圈模型
3 安全性评估
3.1 指南和标准
根据国际非电离辐射防护委员会(International Commission on Non-Ionizing Radiation Protection, ICNIRP)指南相关准则[26],基本人体暴露于150kHz电磁场时,需要考虑内部电场和比吸收率的大小。根据限制电磁场暴露导则推出,频率为150kHz时内部的电场限值为87V/m,磁通密度限值为6.25mT,受控情况下全身平均比吸收率(Specific Absorption Rate, SAR)峰值为0.08W/kg,等效平面波功率密度可以忽略不计。
3.2 仿真
对于安全性评估,文献[19, 24]分别采用了Ansys和COMSOL有限元对具体工作进行了分析,计算精度符合实际需要,本文采用的是后者;人体模型如图7所示,所建立的仿真模型由躯干、心脏组成。仿真中重建了一个提取STL格式简化的躯干模型,建立了二次侧接收端线圈、起搏器外壳和铁氧体薄膜的几何模型引入人体躯干区域,同时建立了体外自由空间发射端线圈模型。

图7 人体模型
忽略内阻,利用节点电压法将双端LCL拓扑分为6个节点,给定初始电压5V,设定谐振电容以及负载的参数,对发射线圈(接收线圈)引入外部vs.(外部电流引入节点,通过线圈产生电压,相当于电压源)充当电压源,其电压值取自于电路耦合,并将电路引入磁场接口,与磁场(Magnetic Field, MF)模块的线圈进行匹配,将电路与电磁场、温度场进行多物理场耦合,激励线圈的电流由电压源提供的电压经过电路模型所产生。而文献[24]中未引入电路,则是直接在线圈两端施加给定的电流,场路耦合这一好处在于仿真情况更加贴切实验。利用COMSOL Multiphysics建模和场路耦合对人体安全特性进行分析。
图7模型中,①为线圈,②为铁氧体,③为部分人体组织,④为起搏器外壳,其中人体组织包括1mm厚的皮肤,2mm厚的脂肪和5mm厚的肌肉组织;铁氧体薄膜尺寸为35mm×35mm,钛合金外壳尺寸为50mm×50mm×16mm,在150kHz频率下人体组织参数见表1[27]。
表1 人体组织参数

Tab.1 Human tissue parameters
表1中,r为介电常数,为电导率,为组织密度,为组织的比热容,为导热系数,b为血液灌注,为传热速率,为产热速率。
3.3 人体组织的安全评估
3.3.1 电磁场强度
仿真中人体内的电磁场为

式中,为磁通密度;为电场;0、r分别为自由空间磁导率和相对磁导率;为磁矢势;s为源电流密度;为电动势;p为复电导率,表达式为
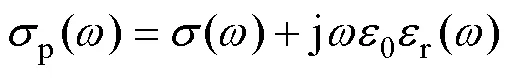
式中,0为自由空间介电常数;r()为相对介电常数;()为电导率。
在150kHz频率下采用频域有限元法对上述方程进行数值求解,以下分析了人体内电场强度与磁通密度的分布情况,并截取了距离起搏器外壳上端1mm的平行截面,该截面介于接收端谐振线圈和起搏器外壳之间,对局部分布情况做了分析。
电场强度如图8所示。图8a中,仿真结果表明,在胸部组织中,电场强度峰值为6.205 18V/m,远低于电场限值标准87V/m;图8b为距离起搏器外壳1mm的平行截面,介于接收端谐振线圈和起搏器外壳之间,可以看出,表面最大电场强度为0.71V/m;符合人体安全规范标准。
磁通密度如图9所示。图9a中,仿真结果表明,磁通密度峰值约为2.28mT,低于磁通密度限值标准6.25mT;图9b为距离起搏器外壳1mm的平行截面,可以看出,表面最大磁通为0.38mT;符合人体安全规范标准。
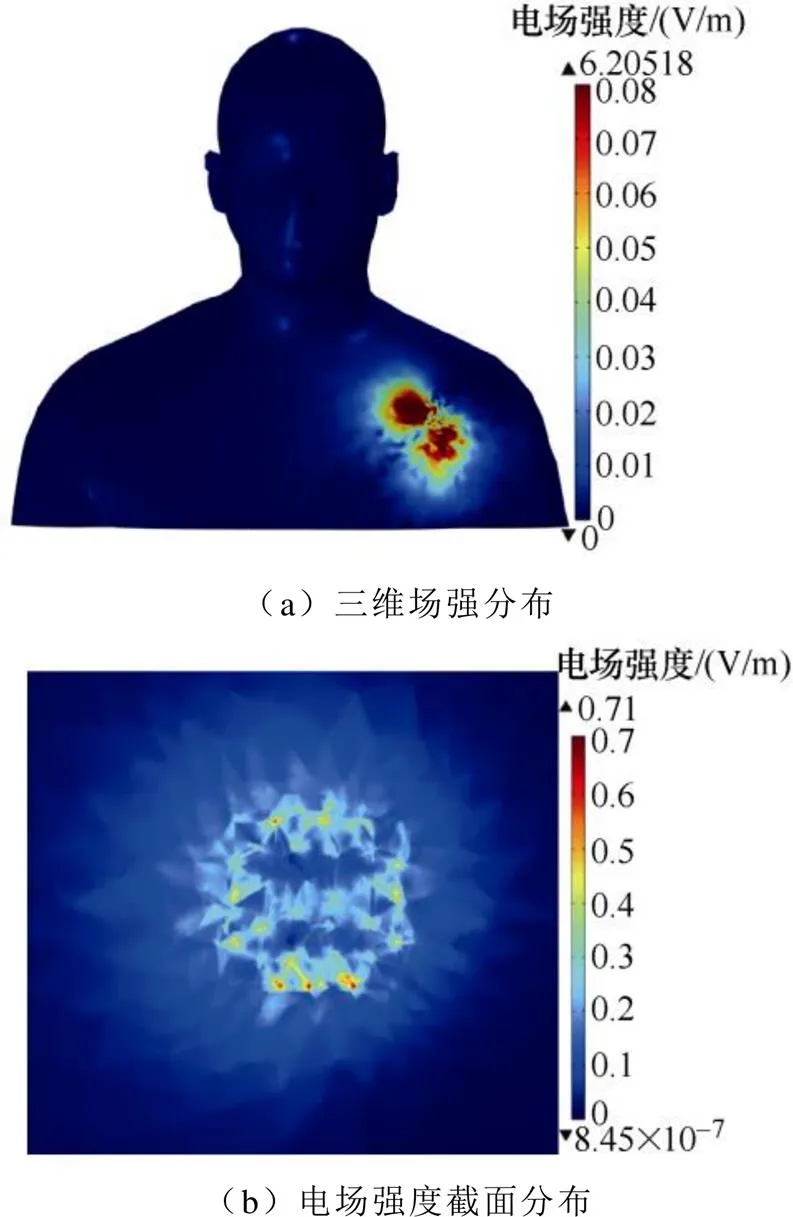
图8 电场强度
3.3.2 组织的温升
生物热方程[28]用于计算暴露在电磁场下人体组织内部的瞬态温度分布。式(19)是由广义的人体热平衡方程得到的,考虑了组织内部热量的产生和交换。

图9 磁通密度
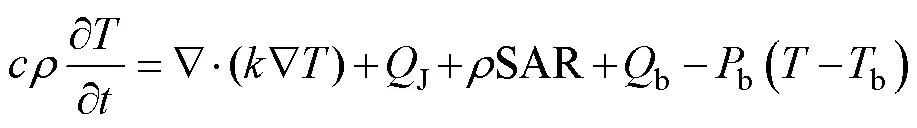
式中,为未知温度;为比热容;热源由焦耳效应的热量J、组织热量SAR、血液热量b给出,血液灌注b为仿真中初始温度设置为b=36.2℃下从体内产生热量,通过对流换热散布外部组织。仿真中,封闭域的求解需要满足热边界条件,即

式中,D、N分别为狄利克雷边界和诺伊曼边界;为已知的热流;为对流换热系数;D和N为已知的温度。
人体温度变化如图10所示。仿真的初始温度设置为309.351K(36.2℃),从图10a可以看出,在充电时间为18min时,局部温度最高上升到310.19K(37.04℃),温度最高上升了0.84℃,从图10b结果可以看出,在充电时间为30min时,局部温度最高上升到310.478K(37.33℃),温度最高上升了1.13℃;远低于温度的限制,不会导致蛋白质变性和一些神经机制发生障碍,对人体组织不会造成伤害,符合人体安全规范标准。

图10 人体温度变化
3.3.3 SAR值
本文的工作频率为150kHz,基于国际标准工频超过100kHz时,就需要考虑比吸收率对人体安全的影响。比吸收率主要与组织电导率、质量密度和所处电场强度有关,计算式为
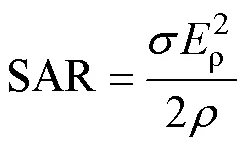
式中,为电导率;r为电场峰值的模;为组织密度。
SAR值分布如图11所示。仿真结果如图11a所示,可以看出,组织中SAR值最大约为0.007W/kg;低于全身平均SAR峰值0.08W/kg,图11b为距离起搏器外壳上端1mm的平行截面,此时SAR值表达式中肌肉组织的电导率=0.371S/m,肌肉组织的质量密度=1 090kg/m3,可以看出表面局部比吸收率峰值为8.76×10-5W/kg,符合人体安全规范标准。

图11 SAR值分布
4 实验
4.1 植入式心脏起搏器无线充电系统模型
植入式心脏起搏器无线充电系统模型如图12所示,起搏器的外壳使用了厚度为0.8mm的钛合金材料,其几何尺寸为50mm×50mm×16mm。植入式心脏起搏器的无线充电模型主要包括以下三部分:电源逆变电路、线圈传能单元和整流部分。电源提供5V直流电压通过全桥逆变输出交流150kHz电压,在双端LCL补偿拓扑的谐振阻抗匹配下,发射线圈向相距8mm的接收线圈传递能量,为模拟人体组织,距离8mm的空间由1mm猪皮+2mm脂肪+ 5mm瘦肉填充;通过逆变电路以及发射端线圈与接收端线圈之间的耦合,对接收线圈接收到的感应电压进行整流,负载采用12W的功率电阻进行替代。为了模拟人体条件进行充电测温实验,使用厚度为2mm的亚克力板搭建了一个尺寸为60cm×20cm× 20cm的近乎密闭的空间。

图12 实验平台
4.2 耦合线圈以及谐振补偿网络参数
磁场对起搏器外壳产生的涡流会影响接收线圈的感应电压,为了提高心脏起搏器无线供电系统的效率与适用性,设计了两组集成线圈,并采用了铁氧体薄膜以提供电磁屏蔽,采用该种集成可有效地减小涡流并增加耦合强度,不仅提高了系统的传输效率,而且减小了植入设备的体积。本文所选择的线圈参数见表2,接收单元由接收线圈、铁氧体薄膜和谐振线圈组成,位置固定于心脏起搏器的外壳之上。主线圈间的互感1=5.764mH,耦合系数1= 0.54;同侧互感为0.7mH,异侧主线圈与谐振线圈互感数量级极小,可忽略不计,谐振电容为106.3nF。在临床实践中,为了避免直接接触引起生物反应,在接收线圈和组织之间需要填加导电性差的材料。
表2 线圈参数

Tab.2 Coil parameters
4.3 实验分析
对不同的线圈结构做了以下三组实验:第一组为采用的集成式圆角方形主线圈和DD形谐振线圈;第二组为非集成式线圈;第三组为集成式圆角方形主线圈和圆角方形谐振线圈。

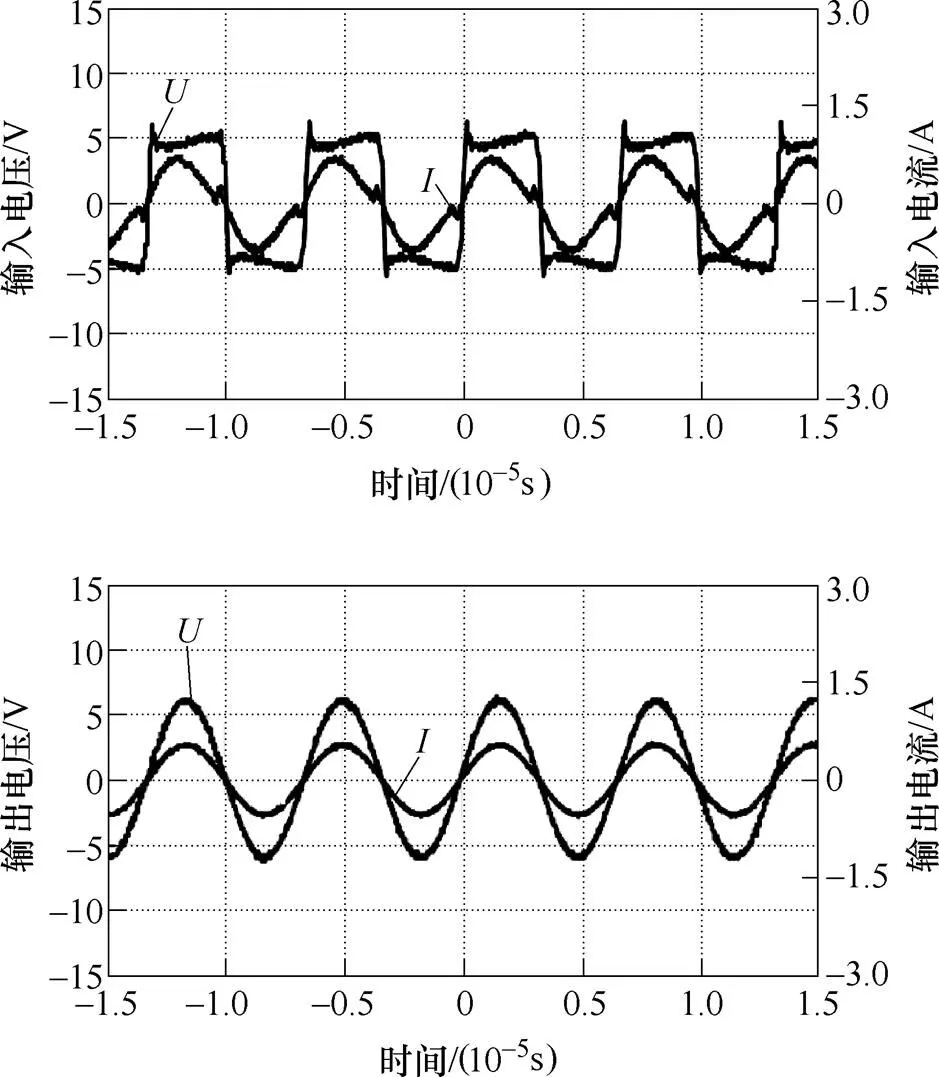
图13 第一组实验输入(输出)电压(电流)波形
效率对比如图16所示。从图16可以看出,在线圈中心对齐相距8~20mm的情况下,本文提出的集成式圆角方形线圈与DD形线圈的解耦结构在三组传能实验中效率最高,远高于其他两组的传输效率。
4.4 温度检测
在植入式心脏起搏器无线充电系统模型上罩着一个厚度为2mm亚克力板搭建的密闭的空间,尺寸为60cm×20cm×20cm;温度传感器用小块的双面胶贴合在接收线圈和肌肉组织之间的接触面上,该接触面是温度升高最快的位置,显示屏记录着温度时刻的变化。
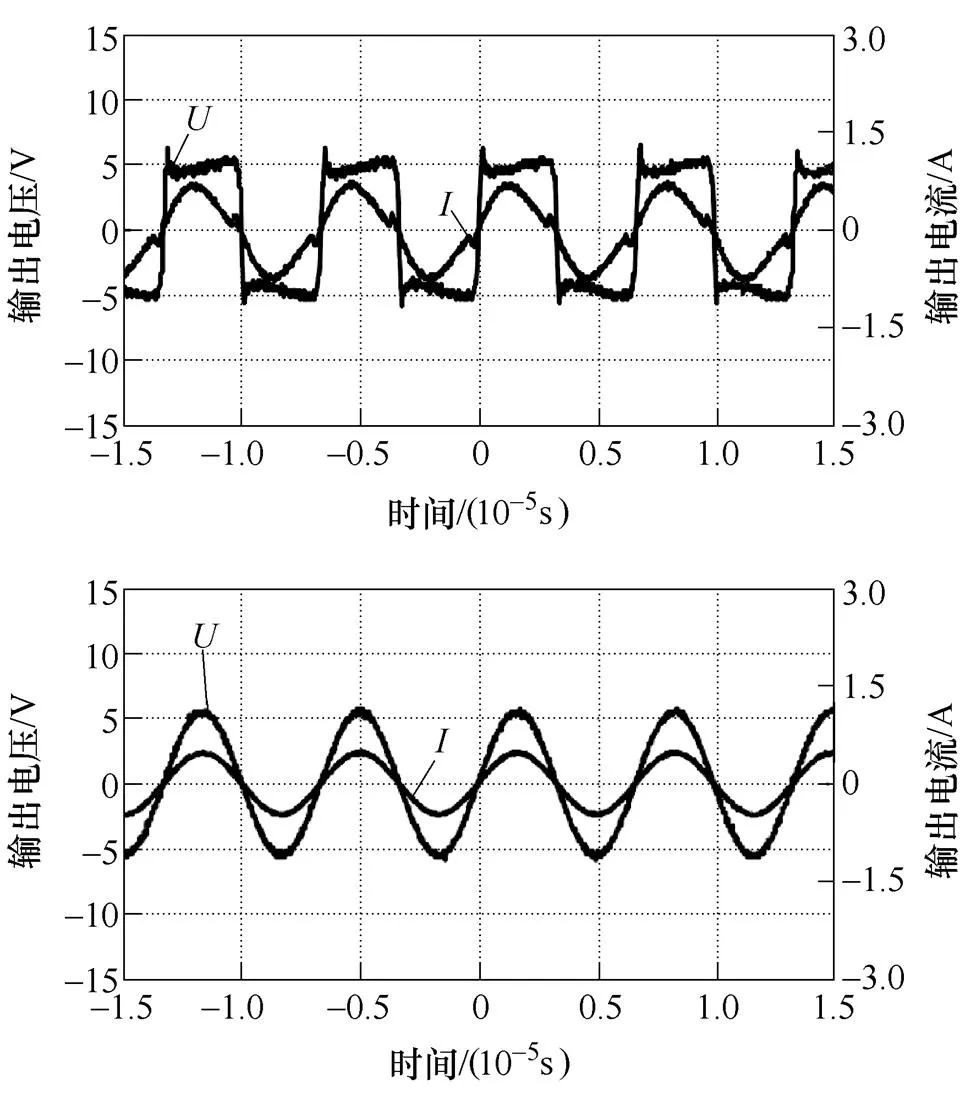
图14 第二组实验输入(输出)电压(电流)波形

图15 第三组实验输入(输出)电压(电流)波形
表3 8mm距离的实验结果

Tab.3 Experimental results of 8mm distance

图16 效率对比
30min温度变化如图17所示,第一组实验充电时起初温度为26.9℃,随着充电时间的增加,温度逐渐升高,最终在30min时温度达到28.1℃,温度升高了1.2℃。第二组起初温度为28.3℃,在30min时温度达到29.8℃,温度升高了1.5℃。第三组起初温度为28.4℃,在30min时温度达到29.8℃,温度升高了1.4℃。可以看出,三组实验温升差距不大,第一组的温升最低,第二组的温升最高。

图17 30min温度变化
人体温度过高会导致蛋白质变性和一些神经机制发生障碍,温度超过40℃会严重危害人的生命安全[24],在本研究中使用40℃作为人体的温度极限,实验测得局部组织的最高温升1.2℃,不会对人体造成损伤。考虑到实验和真实人体所处环境的不同,实验中的热量理论上比人体中的要高,其中一个原因是因为实验使用的是部分猪肉组织而不是人体内血液流动组织,因为血液组织流动会导致对流换热,因而温度偏低;其次实验系统外层罩着一块隔热性能良好的亚克力板,与人体组织不同,阻止了热量的散失。
5 结论
本研究设计了一种应用于植入式心脏起搏器的无线充电系统,该系统基于磁耦合谐振原理,为了进一步减小植入体积,采用集成的方法将二次侧补偿电感集成到谐振线圈之上,有效地简化了植入电路结构。通过建立相应的线圈模型,分析匝数和匝间距对互感的影响来优化线圈结构,对比了集成式与非集成式结构系统的传输性能,验证了集成结构在传输性能和体积方面更具优势。此外,还建立了三维人体模型对该系统进行了相应的安全评估,模拟计算了无线充电过程中比吸收率、温升以及电磁场强度在人体的分布情况,最后进行了相应的温升实验进一步验证了该系统的安全性。结果表明,所设计的磁耦合机构用于该系统是可行的,本文的主要工作和结论如下:
1)采用了一种集成式的双端LCL补偿电路拓扑结构,推导了其谐振阻抗匹配参数;为了将二次侧补偿电感集成于接收线圈之上,设计了一种集成线圈解耦结构,主线圈为圆角方形,谐振线圈为DD形,通过对匝数和匝间距进行参数化扫描来优化磁耦合机构,成功的实现了集成,有效地减小了植入体积。
2)建立了三维人体模型对系统的安全性进行了评估,并考虑了场路耦合,结果表明,充电30min过程中,比吸收率峰值为0.007W/kg;温升峰值为1.13℃;电场强度和磁通密度峰值分别为6.2V/m和2.28mT,同时温升实验表明,局部组织的温升峰值为1.2℃,皆符合安全标准,验证了该系统的安全性。
3)搭建了集成结构与非集成结构实验系统,进行了传输性能实验验证,实验结果表明:在频率为150kHz时,非集成结构在供电功率为2.19W时接收到了1.27W功率,传输效率为58%,而集成结构在供电功率为2.11W时接收到了1.54W功率,传输效率可达73%,相较于非集成结构效率提高了15%,有效的提升了系统的传输性能。
4)本设计还未实现活体植入,进一步的研究还需要在活体动物身上进行实验,最后进行临床试验,以便于将其引入到实际应用中。
[1] Xiao Chunyan, Wei Kangzheng, Cheng Dingning, et al. Wireless charging system considering eddy current in cardiac pacemaker shell: theoretical modeling, experiments, and safety simulations[J]. IEEE Transa- ctions on Industrial Electronics, 2017, 64(5): 3978- 3988.
[2] Kim Sanghoek, Ho John S, Poon Ada S Y. Wireless power transfer to miniature implants: transmitter optimization[J]. IEEE Transactions on Antennas and Propagation, 2012, 60(10): 4838-4845.
[3] Abiri P, Abiri A, Packard R, et al. Inductively powered wireless pacing via a miniature pacemaker and remote stimulation control system[J]. Scientific Reports, 2017, 7(1): 6180-6188.
[4] 谢文燕, 陈为. 全方向无线电能传输技术研究进[J]. 电力系统自动化, 2020, 44(4): 202-215.
Xie Wenyan, Chen Wei. Research progress of omni- directional wireless power transfer technology[J]. Automation of Electric Power Systems, 2020, 44(4): 202-215.
[5] 薛明, 杨庆新, 章鹏程, 等. 无线电能传输技术应用研究现状与关键问题[J]. 电工技术学报, 2021, 36(8): 1547-1568.
Xue Ming, Yang Qingxin, Zhang Pengcheng, et al. Application status and key issues of wireless power transmission technology[J]. Transactions of China Electrotechnical Society, 2021, 36(8): 1547-1568.
[6] 赵军, 徐桂芝, 张超, 等. 磁耦合谐振无线能量传输系统头部植入线圈对人体头部电磁辐射影响的研究[J]. 中国生物医学工程学报, 2012, 31(5): 649-654.
Zhao Jun, Xu Guizhi, Zhang Chao, et al. Electro- magnetic radiation to head from head implantable coil powered via magnetic coupling resonance wireless energy transmission[J]. Chinese Journal of Biomedi- cal Engineering, 2012, 31(5): 649-654.
[7] 宫飞翔, 魏志强, 丛艳平, 等. 植入式医疗设备电磁共振无线能量传输系统天线对人体电磁辐射安全影响的研究[J]. 中国生物医学工程学报, 2016, 35(4): 497-501.
Gong Feixiang, Wei Zhiqiang, Cong Yanping, et al. Research on the effects of antenna electromagnetic radiation to human body safety for implantable medical device wireless energy transmission system based on magnetic resonance[J]. Chinese Journal of Biomedical Engineering, 2016, 35(4): 497-501.
[8] Barretto E C S, Chavannes N, Douglas M. Challenges in safety and compliance assessment in wireless power transfer applications using numerical analysis: guidelines and solutions[C]//10th European Con- ference on Antennas and Propagation (EuCAP), Davos, Switzerland, 2016: 5-9.
[9] 沈栋, 杜贵平, 丘东元, 等. 无线电能传输系统电磁兼容研究现况及发展趋势[J]. 电工技术学报, 2020, 35(13): 2855-2869.
Shen Dong, Du Guiping, Qiu Dongyuan, et al. Research status and development trend of electro- magnetic compatibility of wireless power trans- mission system[J]. Transactions of China Electro- technical Society, 2020, 35(13): 2855-2869.
[10] Gong Feixiang, Wei Zhiqiang, Cong Yanping, et al. Analysis of SAR distribution in human head of antenna used in wireless power transform based on magnetic resonance[J]. Technology and Health Care, 2016, 25(4): 387-397.
[11] 吴旭升, 孙盼, 杨深钦, 等. 水下无线电能传输技术及应用研究综述[J]. 电工技术学报, 2019, 34(8): 1559-1568.
Wu Xusheng, Sun Pan, Yang Shenqin, et al. Review on underwater wireless power transfer technology and its application[J]. Transactions of China Electro- technical Society, 2019, 34(8): 1559-1568.
[12] 张波, 疏许健, 吴理豪, 等. 无线电能传输技术亟待解决的问题及对策[J]. 电力系统自动化, 2019, 43(18): 1-12.
Zhang Bo, Shu Xujian, Wu Lihao, et al. Problems of wireless power transmission technology urgent to be sloved and corresponding countermeasures[J]. Auto- mation of Electric Power Systems, 2019, 43(18): 1-12.
[13] 罗成鑫, 丘东元, 张波, 等. 多负载无线电能传输系统[J]. 电工技术学报, 2020, 35(12): 2499-2516.
Luo Chengxin, Qiu Dongyuan, Zhang Bo, et al. Wireless power transfer system for multiple loads[J]. Transactions of China Electrotechnical Society, 2020, 35(12): 2499-2516.
[14] Campi T, Cruciani, Palandrani F, et al. Wireless power transfer charging system for AIMDs and pacemakers[J]. IEEE Transactions on Microwave Theory & Techniques, 2016, 64(2): 633-642.
[15] 刘帼巾, 白佳航, 崔玉龙, 等. 基于双LCL变补偿参数的磁耦合谐振式无线充电系统研究[J]. 电工技术学报, 2019, 34(8): 1569-1579.
Liu Guojin, Bai Jiahang, Cui Yulong, et al. Double- sided LCL compensation alteration based on MCR- WPT charging system[J]. Transactions of China Electrotechnical Society, 2019, 34(8): 1569-1579.
[16] 李洪宇, 王茜, 苗雨润, 等. LCL补偿型浮标感应耦合电能传输系统特性[J]. 仪器仪表学报, 2018, 39(2): 122-129.
Li Hongyu, Wang Qian, Miao Yurun, et al. Characteristics of LCL compensation inductively coupled power transmission system for buoy[J]. Chinese Journal of Scientific Instrument, 2018, 39(2): 122-129.
[17] Hernandez Sebastian N, Villa Villasenor N, Renero- Carrillo F J, et al. Design of a fully integrated inductive coupling system: a discrete approach towards sensing ventricular pressure[J]. Sensors, 2020, 20(5): 1525-1534.
[18] Seo D W, Lee J H, Lee H, et al. Integration of resonant coil for wireless power transfer and implantable antenna for signal transfer[J]. Inter- national Journal of Antennas & Propagation, 2016, 1(1): 1-7.
[19] Liu Chunhua, Jiang Chaoqiang, Song Jingjing, et al. An effective sandwiched wireless power transfer system for charging implantable cardiac pacemaker[J]. IEEE Transactions on Industrial Electronics, 2019, 66(5): 4108-4117.
[20] Laskovski A N, Yuce M R, Dissanayake T. Stacked spirals for use in biomedical implants[C]//Asia Pacific Microwave Conference, Singapore, 2009: 389-392.
[21] Ahn S H, Lee W S. A compact module-integrated wireless power transfer system with a square metal plate[J]. Microwave and Optical Technology Letters, 2019, 61(5): 1235-1239.
[22] Sadeque K, Goangseog C. Analysis and optimization of four-coil planar magnetically coupled printed spiral resonators[J]. Sensors, 2016, 16(8): 1219-1225.
[23] Campi T, Cruciani S, Santis V D, et al. EMF safety and thermal aspects in a pacemaker equipped with a wireless power transfer system working at low frequency[J]. IEEE Transactions on Microwave Theory & Techniques, 2016, 64(2): 375-382.
[24] Xiao Chunyan, Cheng Dingning, Wei Kangzheng. An LCC-C compensated wireless charging system for implantable cardiac pacemakers: theory, experiment and safety evaluation[J]. IEEE Transactions on Power Electronics, 2017, 33(6): 4894-4905.
[25] Abiri P, Abiri A, Packard R, et al. Inductively powered wireless pacing via a miniature pacemaker and remote stimulation control system[J]. Scientific Reports, 2017, 7(1): 6180-6188.
[26] Zhou Yujing, Liu Chunhua, Huang Yongcan. Wireless power transfer for implanted medical application: a review[J]. Energies, 2020, 13(11): 2837-2866.
[27] Hasgall P A, Neufeld E, Gosselin M, et al. IT'IS database for thermal and electromagnetic parameters of biological tissues[J]. Journal of Cell Biology, 2012, 93(1): 170.
[28] Pennes, Harry H. Analysis of tissue and arterial blood temperatures in the resting human forearm[J]. Journal of Applied Physiology, 1948, 1(2): 93-122.
Integration of Resonant Wireless Energy Supply LCL-LCL for Cardiac Pacemaker
(Faculty of Electrical and Control Engineering Liaoning Technology University Huludao 125000 China)
In order to reduce the volume and electromagnetic interference of the wireless charging system of the implantable pacemaker, a wireless power supply system with a series parallel (LCL-LCL) compensation integrated coupling structure and working frequency of 150kHz was designed based on the principle of magnetic coupling resonance. The resonant coil was integrated into the main coil instead of the inductance. Firstly, the coil model was established and optimized, and the influence of turn number and turn spacing on coil mutual inductance was analyzed. Accordingly, a rounded square coil with the best coupling coefficient was designed. Then, the transmission efficiency of the integrated system and the non- integrated structural system was compared, and the advantages of this structure in efficiency and volume were verified. The feasibility and safety of the implantable charging system were further evaluated by simulating three-dimensional human tissue, calculating the specific absorption rate, temperature rise and electromagnetic field intensity. The experimental results show that the transmission efficiency of the system can reach 73% when the coil center is aligned 8mm apart, which is 15% higher than that of the non integrated structure, and the maximum temperature rise is only 1.2℃.
Pacemaker, integrated coil, 3D human body, safety assessment
10.19595/j.cnki.1000-6753.tces.210790
TM724; TN99
2020年辽宁省教育厅科学研究青年科技人才“育苗”项目(LJ2020QNL019)和2019年辽宁省教育厅科学技术研究创新团队项目(LT2019007)资助。
2021-06-01
2021-08-30
陈伟华 男,1980年生,博士,副教授,研究方向为无线电能传输。 E-mail: fxlgd@163.com
闫孝姮 女,1984年生,博士,副教授,研究方向为无线电能传输。 E-mail: xiaohengyan@163.com(通信作者)
(编辑 陈 诚)
