北山新场BS34钻孔岩样在不同温度下的水岩作用
2022-06-23李亚楠周志超季瑞利赵敬波
李亚楠,苏 锐,周志超,*,季瑞利,赵敬波
1.核工业北京地质研究院,北京 100029;2.国家原子能机构高放废物地质处置创新中心,北京 100029
水岩作用是近地表环境演化的主要驱动力之一,以流体、地下水和岩石之间存在的化学或同位素的不平衡为前提,是一个非平衡地球化学过程[1]。它基本经历了一个从水-岩相互作用,到水-岩-有机物相互作用,最后到水-岩-气-有机物-微生物相互作用研究的发展历程[2]。近年来,水岩作用室内实验研究越来越多,Ilgen等[3]研究了在页岩-盐水-CO2相互作用过程中,富碳酸盐岩页岩盖层的长期稳定性。Phan等[4]研究了Marcellus地球化学演化中的水-岩相互作用。刘宁[5]采用高温高压反应釜研究了陆相沉积盆地砂岩储层CO2地质封存流体运移和水岩相互作用。王开然[6]采用ML-0.3型高温高压反应釜研究了煤层系统CO2-水-煤(岩)地球化学作用。田海龙[7]采用KDSF-Ⅱ型高温高压反应釜研究了CO2-咸水-岩相互作用对盖层封闭性影响。李娜娜[8]开展了钠基膨润土-北山地下水-岩作用实验研究。上述研究对本工作的研究可以起到很好的参考作用。
地下水是放射性核素迁移的最主要媒介,在放射性核素迁移过程中,会与水岩发生相互作用,这类作用通常能够起到阻滞核素迁移的效果,其程度取决于地下水的化学性质。因此地下水的化学性质对高放废物安全处置具有重要意义。目前,国内外公认的最经济安全的高放废物处置方式是深地质处置。深地质处置过程中,高放废物因核素的衰变,会向周围局部地质环境中释放大量的热量,废物罐表面温度可达90 ℃左右[9-13]。本工作拟使用新场场址原状地下水与深部花岗岩岩样,开展不同温度室内水岩作用实验,探究不同温度对新场场址深部地下水化学环境的影响,旨在为我国高放废物安全处置提供依据。
1 研究区概况
新场场址位于甘肃河西走廊以北北山地区,距离嘉峪关约135 km,海拔标高1 670~1 730 m,地形相对较为平缓,地表为典型岩漠戈壁景观,年平均降水量为60~80 mm,年平均蒸发量为3 200 mm,属典型的大陆性气候[9-10]。研究区位置示于图1。

(a)——研究区在甘肃省位置图,(b)——新场周边地理位置图,(c)——BS34钻孔在新场位置图,(d)——BS34钻孔岩心照片图1 研究区及取样钻孔位置图Fig.1 Location map of study area and sampling boreholes
2 实验部分
2.1 实验仪器和样品
X’Pert PRO X射线衍射仪(XRD),荷兰PANalytical公司;ICS-1100离子色谱仪,美国赛默飞;883 Basic IC plus离子色谱仪,瑞士万通;AT-510滴定仪,日本KEM京都电子;TU-1901紫外可见分光光度计,北京普析。
本研究使用新场场址内BS34钻孔517~520 m破碎段花岗岩岩样与BS34钻孔内深部原状地下水进行水岩作用实验。原状地下水保存于密闭的不锈钢罐体(定制)内。其中花岗岩岩样为灰白色花岗闪长岩,岩心照片如图1(d)所示。实验前,采用文献[14]的检测方法对实验岩样进行XRD分析,分析测试单位为核工业北京地质研究院。测试得到其主要矿物的质量分数为:石英,47.7%;斜长石,34.0%;钾长石,11.0%;黏土矿物,7.3%。XRD谱图示于图2。实验后,将90 ℃下固体样品烘干,进行XRD测试,样品中黏土矿物质量分数为11%,高于反应前样品的数值(7.3%),说明反应后,固体样品黏土矿物含量有所增加。实验前,测试BS34钻孔原状地下水水样的主要化学组分[15-16],结果列入表1。

图2 实验前岩样XRD谱图Fig.2 XRD spectrum of rock sample before test
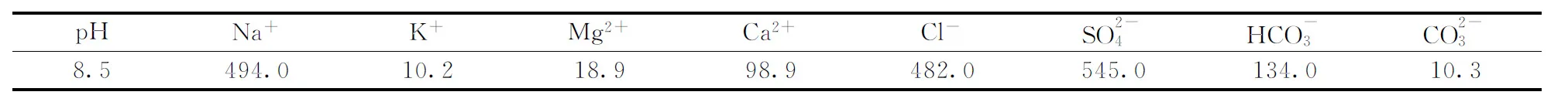
表1 BS34钻孔原状地下水样品主要化学组分分析Table 1 Analysis of chemical components of undisturbed groundwater samples from BS34 borehole mg/L
2.2 实验步骤
(1) 将采集的BS34钻孔破碎段岩心样品制备成粒径140~200 μm的岩粉。
(2) 按照液固比10∶1配制反应溶液:称取30 g已经制备好的破碎段岩粉20份,装入20个锥形瓶,用量筒量取300 mL原状地下水样品20份,倒入上述20个锥形瓶中,在液面处做好标记,振荡搅拌30 min后用锡箔纸封口,用高温皮筋密封,以减少反应过程中的蒸发,反应后期可通过添加去离子水至标记处,来保持反应液体积恒定。
(3) 将上述样品放入恒温恒湿箱中进行反应,因废物罐表面温度可达90 ℃左右[9-13],所以选取最高反应温度为90 ℃,其他反应温度分别为25(室温)、30、60 ℃,反应时间分别为1、3、7、14、28 d。
(4) 反应结束后,将反应液冷却,取上清液离心,装入聚乙烯取样瓶中,经核工业北京地质研究院分析测试中心测试反应液的水化学组成[15,17-19]。
2.3 分析测试方法

3 结果与讨论
3.1 水溶液主要化学组分变化趋势
(1) pH值、TDS
不同温度水溶液pH值、TDS变化趋势示于图3。由图3可知:水溶液pH值随温度变化不明显,但随反应时间(t)有一定的变化,从开始反应到实验结束,水溶液pH值介于6.4~8.5之间,随着反应时间增加先减小,后逐渐趋于稳定;反应温度为25~60 ℃时,水溶液TDS为1 653.9~1 750.1 mg/L,随着反应温度的升高,表现为下降的趋势,且随着反应时间的增长,变为先减小后逐渐趋于稳定的趋势;反应温度为90 ℃时,水溶液TDS介于1 677.5~1 759.6 mg/L,随着反应时间的增长,表现为先减小后增大的趋势。

■——25 ℃,△——30 ℃,◆——60 ℃,□——90 ℃图3 不同温度水溶液pH值、TDS变化趋势Fig.3 pH and TDS variation of aqueous solutions at different temperatures
(2) 主要阳离子
不同温度水溶液主要阳离子质量浓度变化趋势示于图4。由图4可知:反应温度为25~60 ℃时,温度对水溶液中Na+含量影响不大,随着反应时间的增长,Na+质量浓度整体表现为逐渐增大的趋势,为485.0~512.0 mg/L,当升高到90 ℃时,Na+含量快速增大,且随着时间的增长,也表现出增大的趋势,其质量浓度为494.0~535.0 mg/L,说明温度从60 ℃到90 ℃时,加快了水溶液含钠矿物的溶解;随着温度升高,K+含量表现为逐渐增大的趋势,且随着反应时间增加,K+含量先快速增大,后逐步趋于稳定,其质量浓度为10.2~31.2 mg/L;Mg2+含量表现为随温度升高、逐渐减小的趋势,且随着反应时间增加,其质量浓度逐渐减少,为0.2~19.0 mg/L;温度对Ca2+含量影响不大,随着反应时间增加,Ca2+质量浓度先快速减小,后逐步趋于稳定,为59.9~98.9 mg/L。

■——25 ℃,△——30 ℃,◆——60 ℃,□——90 ℃(a)——Na+,(b)——K+,(c)——Mg2+,(d)——Ca2+图4 不同温度水溶液主要阳离子质量浓度变化趋势Fig.4 Main cations mass concentration variation of aqueous solutions at different temperatures
(3) 主要阴离子


■——25 ℃,△——30 ℃,◆——60 ℃,×——90 ℃图5 不同温度水溶液主要阴离子质量浓度变化趋势Fig.5 Main anions mass concentration variation of aqueous solutions at different temperatures
(4) Al3+、SiO2
选取90 ℃下反应后的水溶液,分析其中Al3+、SiO2的含量,其结果示于图6。由图6可知,随着反应时间的增加,Al3+、SiO2含量先增加,后趋于稳定,最大值分别为0.35、52.3 mg/L。

图6 90 ℃下水溶液中Al3+(a)、SiO2(b)含量变化趋势Fig.6 Al3+(a), SiO2(b) content variation of aqueous solutions at 90 ℃
3.2 水化学模拟研究
为明确岩样与原状地下水之间的相互作用,需确定水溶液中不同矿物的反应状态,通常通过矿物饱和指数(saturation index, SI)来判断其反应状态。当某矿物SI>0时,该矿物在水溶液中处于过饱和状态,会沉淀析出;当某矿物SI<0,该矿物在水溶液中未饱和,可以继续溶解;当某矿物SI=0,该矿物处于饱和状态,此时既不溶解也不沉淀。本研究选取90 ℃下,采用PHREEQC计算水溶液中不同矿物的矿物饱和指数,其结果示于图7。由图7可知:水溶液中钠长石、钾长石、钙长石的矿物饱和指数SI均小于0,处于未饱和状态,可以继续溶解;钙蒙脱石和高岭石的矿物饱和指数SI前3天小于0,处于未饱和状态,随着反应的进行,不断有钙蒙脱石和高岭石生成,导致其饱和指数SI大于0,在水溶液中沉淀析出。

●——钠长石,×-——钙长石,▼——钙蒙脱石,■——钾长石,▲——高岭石图7 90 ℃下水溶液中主要矿物的矿物饱和指数Fig.7 Saturation index of main minerals in aqueous solution at 90 ℃
3.3 水溶液主要离子来源分析
BS34钻孔破碎段岩样与原状地下水反应后,水溶液化学成分发生了变化,下面对水溶液中主要离子的来源进行分析。
(1) Na+的来源
反应后,水溶液中Na+含量的增加可能主要来源于钠长石的溶解、阳离子交换作用,反应如下:

(2) K+的来源
反应后,水溶液中K+含量的增加可能主要来源于钾长石的溶解,反应如下:

水溶液中Na+、K+增加的同时,SiO2的含量也在增加,推断为Si(OH)4分解成SiO2,反应方程式如下:



钙长石的溶解:

CaCO3、CaMg(CO3)2的沉淀:

通过该水岩作用实验可知,反应后水溶液中部分钠长石、钙长石、钾长石等可能溶解生成了高岭石、蒙脱石等黏土矿物[25-27]。
4 结 论

(2) 反应温度高于60 ℃时,对地下水组成的影响较为显著,尤其表现为随着反应温度的升高,水溶液中的钾长石溶解越多,方解石、白云石沉淀析出越多。
(3) 钠长石、钾长石、钙长石等的溶解可能生成高岭石、蒙脱石等黏土矿物,这些生成的黏土矿物对封堵处置库近场的裂隙、阻滞放射性核素的迁移可能有一定作用。
