下肢深静脉血栓后综合征患者中静脉支架的中期通畅率及高危因素回归分析
2022-06-23范隆华刘坚军王晓俊黎力梦董智慧
汪 涛 范隆华, 刘坚军△ 李 旭 陶 悦 王晓俊 黎力梦 董智慧
(1复旦大学附属中山医院青浦分院血管外科 上海 201700;2复旦大学附属中山医院血管外科 上海 200032)
下肢深静脉血栓后综合征(post-thrombotic syndrome,PTS)是下肢深静脉血栓形成(deep venous thrombosis,DVT)的远期并发症,主要包括患肢水肿、沉重感、疼痛、继发性静脉曲张、色素沉着,甚至形成静脉性溃疡,严重影响患者的生活质量[1-2]。Enden 等[3]报道接受保守单纯抗凝治疗的DVT 患者PTS 发生率高达50%。近年来随着血管腔内技术的快速更替,PTS 腔内介入治疗因创伤小、疗效肯定和并发症少等优点得到国内外临床医师的认可[4]。
PTS 病变部位好发于髂静脉和股静脉,通过球囊扩张联合支架植入术,可恢复血流通畅,一次性处理疾病,减少相关并发症。随着静脉内支架在PTS 的广泛应用,相应问题也随之出现。国内学者报道PTS 静脉支架植入术后,短期内(3~6 个月)支架通畅率为92.4%,但中远期支架通畅率研究尚少,且影响支架通畅率的因素仍不明确[5-7]。复旦大学附属中山医院青浦分院自2015 年开始开展下肢PTS 静脉腔内支架植入术,本研究主要探讨静脉支架在下肢PTS 患者的中期通畅率,并进行相关高危因素的筛查,为临床治疗策略提供参考。
资料和方法
一般资料纳入2015 年8 月至2019 年3 月在复旦大学附属中山医院青浦分院就诊的124 例PTS患者,随访2 年,最终纳入102 例下肢PTS 患者(图1)。登记患者详细信息,主要包括现病史,既往史,伴随症状,体重指数,血栓位置,疼痛、瘙痒和沉重感主诉,下肢水肿、压痛和色素沉着等体征的Villalta 评分,超声或CT 静脉造影评估的支架通畅率。纳入标准:(1)PTS 诊断明确;(2)既往有下肢静脉血栓病史;(3)具有典型慢性下肢静脉功能不全症状。排除标准:(1)年龄<18 或>70 岁;(2)下肢静脉造影或超声提示股总静脉远端狭窄或闭塞;(3)既往行下肢静脉球囊扩张行或静脉支架植入;(4)预期寿命少于1 年的恶性肿瘤患者;(5)双侧发病;(6)因其他终末期疾病、意外死亡或患有精神类疾病不能配合的。统计PTS 术后2 年时支架通畅率,分为支架堵塞组和支架通畅组。本研究获复旦大学附属中山医院青浦分院伦理委员会批准,所有研究对象知情同意并签字。

图1 患者纳入排除流程图Fig 1 Flow chart of patients through inclusion and exclusion criteria
治疗方法所有入组患者接受髂股病变静脉球囊扩张和支架植入成形术,术前根据彩超或磁共振静脉造影检查结果,选取股静脉入路,逆行穿刺股静脉,导丝配合导管通过病变静脉进入下腔静脉,再次造影确认导管末端位于下腔静脉。血管开通过程中操作应轻柔,避免出现穿透血管壁引起出血或血肿。首先选用较小直径(6~8 mm)的球囊扩张病变血管,然后根据造影结果选择合适直径的球囊充分预扩病变静脉,每次球囊完全充起维持2 min。髂静脉病变段首选Bard Luminexx 支架,股静脉段病变首选Boston Wallstent 支架,支架直径根据术中静脉造影以及球囊扩张情况选择,支架长度应完全覆盖血管病变部位,若病变血管植入2 枚支架,重叠区域至少10 mm。手术完毕压迫穿刺点10 min。所有PTS 患者围手术期皮下注射低分子肝素抗凝(100 U/kg,qd),出院后继续足量全程抗凝治疗至少12 个月,口服利伐沙班片(10 mg,qd)或华法林[ 需维持国际标准化比值(international normalized ratio,INR)在2~3],同时服用拜阿司匹林(100 mg,qd)抗血小板治疗,并辅以弹力袜支持治疗。合并高血压、糖尿病或心肺肾功能不全的患者接受相应治疗。
手术疗效评价及随访手术技术成功率指支架完全覆盖病变血管。患者分别于术后1、6、12 和24 个月进行门诊随访,随访截止时间是出院后2 年。临床缓解:患者24 h 内患 肢沉重感、肿胀减轻[8]。Villalta 评分:通过9 项评分累加对PTS 患者临床症状进行评估。静脉通畅率:通过下肢静脉血管造影评估髂股静脉通畅情况。若存在下肢静脉性溃疡,评估伤口愈合情况。
变量赋值根据不发生为0、发生为1 进行二分类数据量化,计量数据BMI、年龄和血栓病程时间采用自然数编码(表1)。

表1 各研究因素的赋值结果Tab 1 Assignment results of each study factor
统计学分析采用SPSS 15.0 进行统计分析,连续变量采用±s表示,分类变量采用率的形式表示。影响通畅率危险因素采用单因素和多因素非条件二元Logistic 回归分析,并建立回归模型。P<0.05 为差异有统计学意义。
结 果
术后患者情况纳入的102 例患者均成功接受静脉球囊扩张+支架植入手术治疗(图2),技术成功率100%。术后24 h 内95 例(93.1%)患者患肢沉重感、疼痛、水肿明显缓解,溃疡加速愈合。出院时患者Villallta 评分较术前明显降低(6.7±2.5vs.13.3±2.5,P=0.032)。围手术期无穿刺点出血、血肿等严重并发症发生。随访2 年的支架通畅率为85.3%。
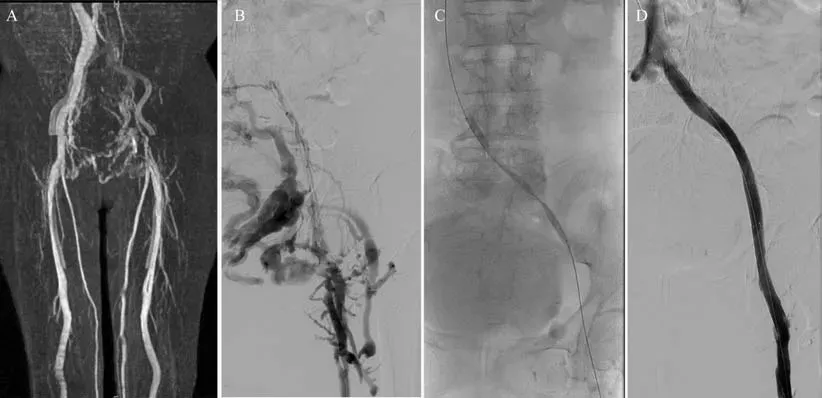
图2 典型PTS 患者介入手术图片Fig 2 Images of interventional surgery in typical PTS patients
影响PTS 术后支架通畅率危险因素的单因素分析结果对12 个因素进行单因素回归分析(表2),在α=0.1 水平上筛出5 个影响PTS 术后支架通畅性的危险因素,分别为BMI(P<0.001)、抗血小板治疗(P<0.001)、支架数量(P<0.001)、血栓堵塞位置(P=0.001)和弹力袜支持治疗(P<0.001)。

表2 影响PTS 术后支架通畅率危险因素的单因素分析结果Tab 2 Single-factor analysis of the stent patency after PTS surgery
影响PTS 术后支架通畅率的多因素回归分析结果对单因素分析筛出的5 个有意义的变量进行多因素二元Logistic 回归分析,在α=0.05 水平上筛出4 个影响PTS 术后支架通畅率的危险因素(表3):BMI(OR=1.999,95%CI:1.145~3.489)、抗血小板治疗(OR=0.005,95%CI:0.003~0.932)、植入2个支架(OR=41.033,95%CI:1.346~1250.940)和弹力袜治疗(OR=0.018,95%CI:0.001~0.622)。由此建立的Logistic 回归模型为:Y=-18.463+0.693X2-3.001X8+3.714X9-4.003X12。
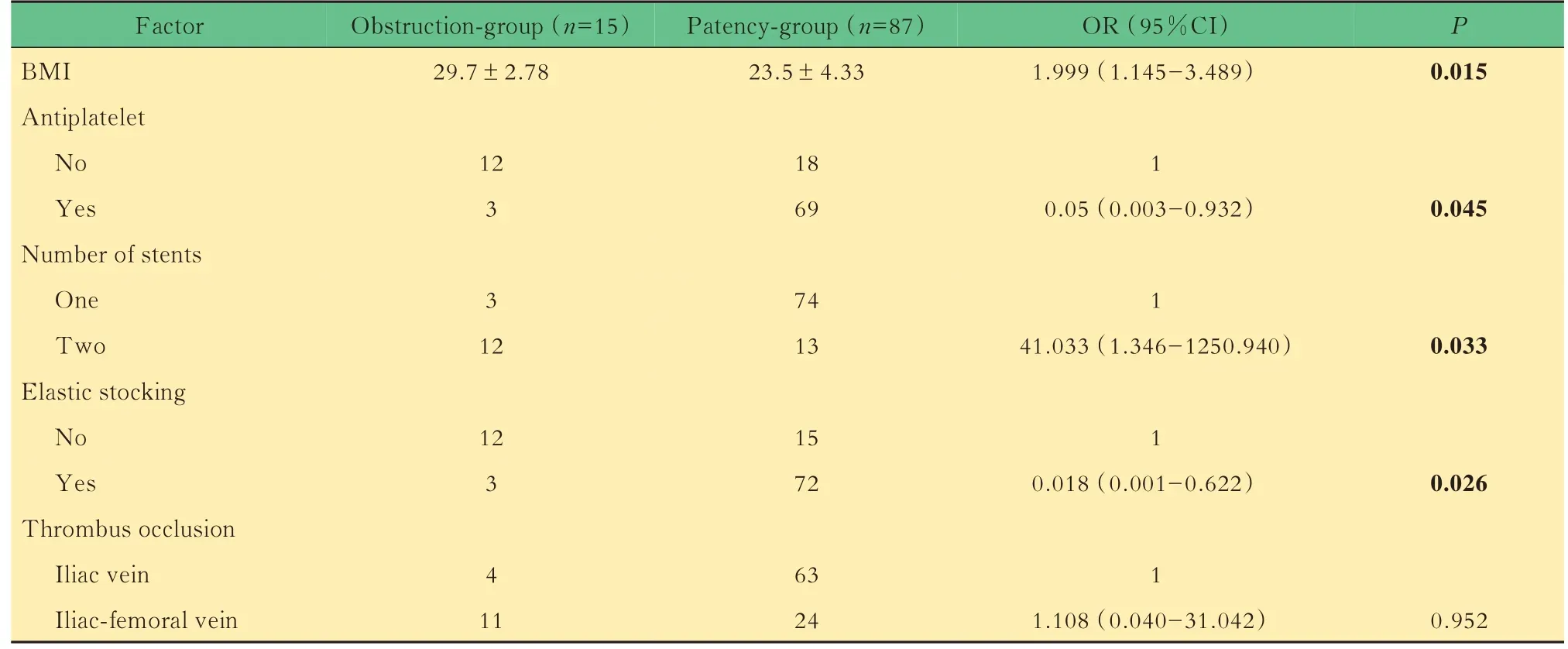
表3 影响PTS 术后支架通畅率的多因素Logistic 回归分析Tab 3 Multi-factor Logistic analysis of the stent patency after PTS surgery
讨 论
随着外周血管腔内技术的迅猛发展,血管腔内介入治疗已成为PTS 的首选。PTS 腔内治疗具有创伤小、耐受性好和恢复快等优势[4]。但目前该技术在临床使用存在最大挑战是:植入静脉支架远期通畅率如何提高?尚缺乏临床大样本远期随访评估。本研究分析了静脉支架植入在PTS 患者临床治疗效果,静脉支架植入成功率100%,通过开通PTS 闭塞段血管,术后患者临床缓解率高达93.1%,疗效显著,且围手术期无出血等严重并发症。可见一期支架植入能即刻维持静脉回流通路,快速缓解患者临床症状,与国内外等报道一致。Michael 等[9]纳 入79 例 下 肢 深 静 脉PTS 患 者,经 球囊扩张联合支架植入术后,临床缓解率达86.4%,2年支架通畅率为95.5%。国内相关文献报道较少,类似研究结果提示在下肢深静脉血栓形成伴髂静脉压迫患者中,球囊扩张联合支架植入术后1 年支架通畅率为92.15%[10]。本研究通过Logistic 多因素回归分析总结出肥胖、未规范抗血小板治疗、长段支架以及未予弹力袜支持治疗是PTS 术后支架堵塞的危险因素。
肥胖是心血管等众多疾病发生发展的重要致病因素。本研究回归分析发现PTS 合并肥胖体质患者术后支架通畅率明显低于非肥胖患者,这可能与肥胖增加患者下肢静脉压有关,引起下肢静脉反流,减少静脉血流回流。同时肥胖患者缺乏锻炼,小腿肌肉泵功能下降,进一步影响下肢静脉血液回流,致使支架内血流缓慢,血小板边集及黏附能力增强,可能引起相应血栓或内膜的增生。Galanaud等[11]报道过类似结果,在纳入的急性DVT 患者中,BMI≥30 时PTS 发生率是对照组2 倍,由此推断肥胖既是PTS 发生的高危因素,也是引起术后支架堵塞的高危因素。
本研究结果提示长段支架是PTS 术后发生支架堵塞的危险因素。球囊对病变静脉管腔进行扩大,髂股静脉管腔压力低且易塌陷,同时生理性压迫仍然存在,球囊扩张后静脉管腔形态难以保持。因此,PTS 患者经球囊扩张后需植入静脉支架来维持静脉管腔形态,既能恢复正常的解剖通道,又能解除下肢回流障碍。国内专家共识认为,PTS 腔内治疗推荐使用自膨式静脉支架[12]。自膨式支架柔顺性高,目前主要包括激光雕刻型和编织型支架。以E-Luminexx 为代表的激光雕刻型支架具有较佳的定位性能和柔顺性,但抗断裂性能不足;以Wallstent 为代表的编织型支架具有较佳的抗断裂性和柔顺性,但径向支撑力若和定位不准确[13]。长段支架是PTS 术后发生支架堵塞的可能原因是,长段的支架植入预示着髂股静脉长段狭窄闭塞,下肢静脉回流阻力增大,相对于短段闭塞,下肢静脉高压的发生率更高。另外髂股静脉有瓣膜,长段病变静脉血管血栓机化过程中,释放更多的炎症介质破坏瓣叶结构和功能,引起PTS 术后支架通畅率下降[5,14]。
本研究结果提示未规范抗血小板治疗是PTS术后发生支架堵塞的危险因素,可能原因是:PTS患者术中球囊扩张过程中,对静脉内膜的刺激引起新血栓形成及内皮增生,术后存在内膜增生或急性血栓形成,髂静脉受髂关节活动影响,静脉支架受到牵连及扭曲等作用力,刺激静脉内膜内皮细胞增生[15]。同时支架对于机体来说是外来物质,会激活凝血因子,启动外源性凝血途径,引起微小附壁血栓,而血小板在血液中的激活和边集对血栓的形成具有重要的促进作用[16]。
本研究结果提示未规范弹力袜支持治疗是PTS 术后发生支架堵塞的危险因素。压力支持治疗目前是PTS 最有效的无创治疗方法,下肢静脉高压在PTS 进展过程中有着关键作用,站立时踝部静脉压可达80~100 mmHg,而压力支持治疗可通过增加外部静脉压促进静脉回流[17]。未规范弹力袜支持治疗导致外部静脉压的缺失,患者日常活动时下肢静脉渗出增多,引起下肢水肿,同时导致下肢静脉血液回流缓慢,严重时甚至血液回流停滞[18]。血液停滞是静脉血栓形成Virchow 三联征始发因素之一,可激活静脉血栓形成[19],由此可能引起静脉血液回流缓慢,影响支架通畅率。
综上所述,PTS 患者静脉支架植入术后2 年支架通畅率为85.3%。肥胖、未规范抗血小板治疗、长段支架以及未规范弹力袜支持治疗是影响PTS 术后支架通畅率的危险因素。本研究的不足之处在于:纳入病例数不多;非多中心病例对照研究,仅纳入复旦大学附属中山医院青浦分院病例,属于单中心前瞻性病例对照研究;随访时间相对较短,影响支架通畅率的远期危险因素尚未确定,仍需进一步研究。
作者贡献声明汪涛 论文构思和撰写,数据整理和分析。范隆华 研究设计。刘坚军 研究设计,论文修改。李旭 数据统计和分析。陶悦数据解释。王晓俊,黎力梦 数据收集。董智慧实验指导。
利益冲突声明所有作者均声明不存在利益冲突。
