椎间孔镜双侧入路与大通道内镜下椎板间单侧入路双侧减压治疗重度中央型腰椎管狭窄症的对比研究
2022-06-21胡源孔清泉张斌冯品黄章恒刘俊麟马骏松舒翔
胡源 孔清泉 张斌 冯品 黄章恒 刘俊麟 马骏松 舒翔
退变性腰椎管狭窄症 ( lumbar spinal stenosis,LSS ) 系各种腰椎退变导致的椎管空间狭窄,椎管内神经及血管有效空间受压减少,进而产生的臀部或下肢疼痛,伴或不伴腰背痛等一系列临床综合征。它是引起老年人下肢疼痛最常见的原因之一,可显著影响患者的生活质量,治疗首选保守治疗,但如果保守治疗失败,严重影响日常生活则需手术减压治疗,这种情况在重度的腰椎中央管狭窄症患者中较为多见。此类患者的双侧腰椎小关节突增生明显、黄韧带肥厚,可合并有椎间盘退变钙化、侧隐窝及椎间孔区域狭窄等改变,在腰椎 MRI上表现为横断面硬膜囊面积 ( dural sac crosssectional area,DSCA ) < 75 mm,按形态学定性分级 ( morphological grading,MG ) 为 C、D 级。既往手术治疗腰椎中央管狭窄主要采用传统开放椎板减压、腰椎减压固定融合、微创椎间盘镜减压及通道辅助下椎管减压等方式,椎板切除减压术后可能出现腰椎不稳及慢性腰痛,减压固定融合在老年高龄患者中则面临手术创伤大、术后不融合、内固定松动等诸多并发症问题。
近年来,随着脊柱微创外科的不断发展,经皮脊柱内镜减压技术已逐步应用于腰椎中央管狭窄症的治疗中。由于腰椎重度中央管狭窄的病理特征,常需在脊柱内镜下进行双侧充分减压 ( 去除背侧及腹侧等诸多致压因素 ),目前已有经双侧椎间孔入路双侧减压技术及经椎板间单侧入路双侧减压技术应用于不同程度的腰椎中央管狭窄症治疗中,并取得了较满意疗效的报道,但还没有文献对上述两种术式在治疗重度中央型 LSS 上进行对比。笔者所在的脊柱微创外科团队对腰椎中央管狭窄症的治疗具有丰富经验,除常规采用大通道内镜下椎板间单侧入路双侧减压技术外,早期也采用双侧椎间孔入路双侧减压的方式进行治疗,故通过回顾性分析 2017 年 2 月至 2020 年 5 月采用上述两种技术治疗的腰椎中央管狭窄症患者的临床资料,对比两种技术的疗效及优缺点,为手术方式选择提供参考,现报道如下。
资料与方法
一、纳入标准与排除标准
1. 纳入标准:( 1 ) 症状、体征及辅助检查明确诊断为单节段重度中央型 LSS 者;( 2 ) 严格保守治疗 3 个月以上无效后,采用上述两种手术方式之一治疗者;( 3 ) 术后随访时间 > 12 个月且临床资料完善者;( 4 ) 同意纳入本研究并提供所有随访资料者。
2. 排除标准:( 1 ) 重度腰椎中央管狭窄内镜手术治疗困难,术中中转开放或合并其它手术治疗技术者;( 2 ) 术后随访,原手术节段因其它原因 ( 骨折、肿瘤、结核等 ) 再次接受手术者;( 3 ) 术后随访时间 < 12 个月、临床资料不完善或失访者。
二、一般资料
本组共纳入 81 例,根据手术方式不同,分为大通道内镜下经椎板间单侧入路双侧减压组 ( A 组,= 31 ) 和椎间孔镜双侧入路双侧减压组 ( B 组,= 50 )。其中,A 组男 19 例,女 12 例;年龄 53~83 岁,平均 ( 67.3±8.7 ) 岁;受累节段:L22 例,L~S9 例;随访 13~25 个月,平均( 18.6±4.0 ) 个月。B 组男 29 例,女 21 例;年龄49~84 岁,平均 ( 66.8±9.1 ) 岁;受累节段:L36 例,L~S14 例;术后住院时间 2~5 天,平均( 2.6±0.8 ) 天;随访 13~25 个月,平均 ( 19.4±3.9 )个月。所有患者均具有典型的间歇性跛行症状,伴有双侧臀部和 ( 或 ) 下肢疼痛,且以臀部和下肢疼痛为主 ( 腰痛影响程度较轻 )。术前 X 线片示腰椎退变明显,但无明显腰椎不稳及重度滑脱;CT 检查示腰椎双侧关节突增生内聚、黄韧带肥厚 ( 合并钙化等 )、椎管狭窄明显、呈三叶草形;MRI 检查示腰椎间盘退变、突出 ( 非巨大 ) 伴椎管狭窄,马尾神经受压 / 显示不清,硬膜囊外侧脂肪消失等。所有患者术前均符合重度单节段腰椎中央管狭窄诊断标准。
三、手术方法
1. 手术适应证与禁忌证:所有重度腰椎中央管狭窄病例均根据下述标准评估是否适合全脊柱内镜双侧减压治疗。适应证:( 1 ) MRI 检查提示单节段重度腰椎中央管狭窄:DSCA < 75 mm,按 MG为 C、D 级;( 2 ) 具有典型的间歇性跛行症状,双侧臀部和 ( 或 ) 下肢疼痛为主 [ 伴 / 不伴腰痛,但腰痛影响甚小,疼痛视觉模拟评分 ( visual analogue scale,VAS ) < 3 分 ];( 4 ) 严格保守治疗 3 个月以上无效;( 5 ) 可以耐受手术;( 6 ) 患者及家属同意并签署手术知情同意书。禁忌证:( 1 ) 患者存在明显腰痛影响生活 ( VAS 评分 > 3 分 );( 2 ) 单纯腰椎间盘突出症或合并巨大腹侧腰椎间盘突出、腹侧骨化引起的椎管狭窄;( 3 ) 腰椎不稳,退变性腰椎滑脱Meyerding Ⅱ 度及以上;( 4 ) 伴有腰椎感染、结核、肿瘤、骨折;( 5 ) 责任节段有手术史,预判瘢痕组织增生有严重粘连;( 6 ) 全身情况差,不能耐受手术,存在手术禁忌证。
2. A 组手术方法:俯卧位,气管插管全身麻醉。麻醉成功后患者取俯卧位于脊柱手术垫上,腰部垫起形成腰桥,克氏针置放于皮肤表面定位手术节段并作好标志标线,腰背部常规消毒铺巾;透视定位手术节段,正中线旁开 1 cm 取长约 1 cm 的手术切口,以软组织扩张器分离至上位节段椎板下缘和黄韧带交接处,置入大通道工作套管及内镜;内镜监视下使用镜下环锯、椎板咬骨钳、镜下骨刀切除同侧及对侧部分下关节突及上关节突,咬除部分棘突根部;切开黄韧带,暴露神经根及硬膜囊边缘,镜下骨刀、椎板咬骨钳减压双侧侧隐窝,神经剥离器游离并松解双侧神经根。予射频电极充分术野内止血;再次探查,双侧神经根及硬膜囊减压后搏动良好;退出工作套管及内镜,皮内缝合手术切口。
3. B 组手术方法:俯卧位,静脉麻醉 + 局部麻醉,患者取俯卧位于脊柱手术垫上,腰部垫起形成腰桥,克氏针置放于皮肤表面定位手术节段,并作好标志标线,腰背部常规消毒铺巾;距离腰椎后正中线侧方 11~13 cm 及手术目标间隙平面上方 3 cm处双侧进行皮肤及穿刺路径深部组织麻醉,从双侧向手术目标节段椎间孔穿刺,以 0.5% 利多卡因分层局部浸润麻醉。取长约 7 mm 切口,透视下导棒插入手术目标节段双侧椎间孔区域,定位位置满意,顺导棒依次导入扩张器、工作套管,限深环锯切除双侧部分上关节突,扩大椎间孔成形。导入内镜。内镜下以初次环锯成形后的锯痕为参考,清理、止血、显露上关节突腹侧、外侧及与椎弓根移行处,更换为可视环锯配套工作套管并置入镜外可视环锯,在内镜监视下对关节突关节行二次成形;使用椎板咬骨钳、镜下骨刀去除增厚、骨化黄韧带以及增生的关节突,同时将突起的纤维环附着点咬平,彻底松解双侧行走根。探查双侧行走根减压充分,彻底减压后见硬膜囊膨隆,搏动良好。退出工作套管及内镜,皮内缝合手术切口。
四、术后处理及评估指标
两组术后均不需要放置引流管,不需要预防性使用抗菌药物,常规给予对症消肿止痛及预防下肢深静脉血栓处理。术后复查腰椎 CT 平扫 + 三维重建、腰椎 MRI 平扫后佩戴有支撑性和限制性的腰围下床活动。
记录手术相关评价指标:手术时间、术中透视次数、并发症 ( 硬膜囊撕裂、术后下肢麻痹无力、麻木 / 疼痛不缓解或加重、手术切口感染等 ) 发生情况。记录患者术前、术后 1 个月、末次随访时的臀部及下肢痛 VAS 评分及 Oswestry 功能障碍指数( oswestry disability index,ODI )。末次随访时行改良 MacNab 标准评估临床疗效,优:症状完全消失,恢复原来的工作和生活;良:有轻微症状,活动轻度受限,对工作生活无影响;可:症状减轻,活动受限,影响正常工作和生活;差:治疗前后无差别,甚至加重。
五、统计学处理
结 果
两组患者的年龄、性别、术后住院时间差异无统计学意义 (> 0.05 )。A 组手术时间和透视次数均少于 B 组,差异有统计学意义 (< 0.05 ) ( 表 1 )。
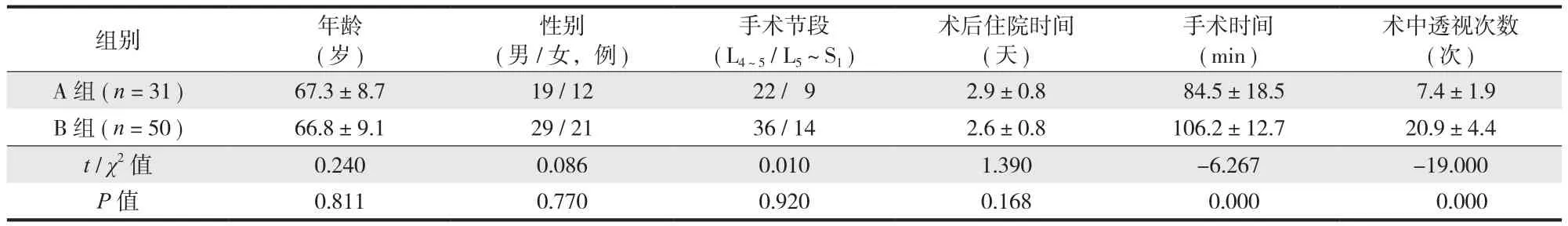
表1 两组一般资料和手术相关指标比较Tab.1 Comparison of general information and surgery-related indicators between the two groups
两组患者术后 1 个月、末次随访时 VAS 评分和 ODI 评分较术前均有明显降低,差异有统计学意义 (< 0.05 )。组间比较,两组患者术前、术后 1 个月、末次随访 VAS 评分和 ODI 评分差异均无统计学意义 (> 0.05 ) ( 表 2 )。
表2 两组术前、术后 1 个月、末次随访 VAS 评分、ODI 评分比较 ()Tab.2 Comparison of VAS and ODI between the two groups before surgery, 1 month after surgery, and at the last follow-up ( )
并发症发生情况:A 组 1 例 ( 3% ),为术后麻木加重,B 组 3 例 ( 6% ),1 例为硬膜囊撕裂,2 例为术后麻木加重。1 例硬膜囊撕裂患者术后严密缝合,术后未发生脑脊液漏等不良结果,3 例麻木加重患者术后予以脱水、营养神经等治疗,均在术后3 个月内麻木程度轻于术前。末次随访时采用改良MacNab 标准评定疗效,A 组优 22 例、良 8 例、可1 例,优良率为 96.8%;B 组优 35 例,良 13 例,可2 例,优良率为 96.0%。典型病例见图 1、2。
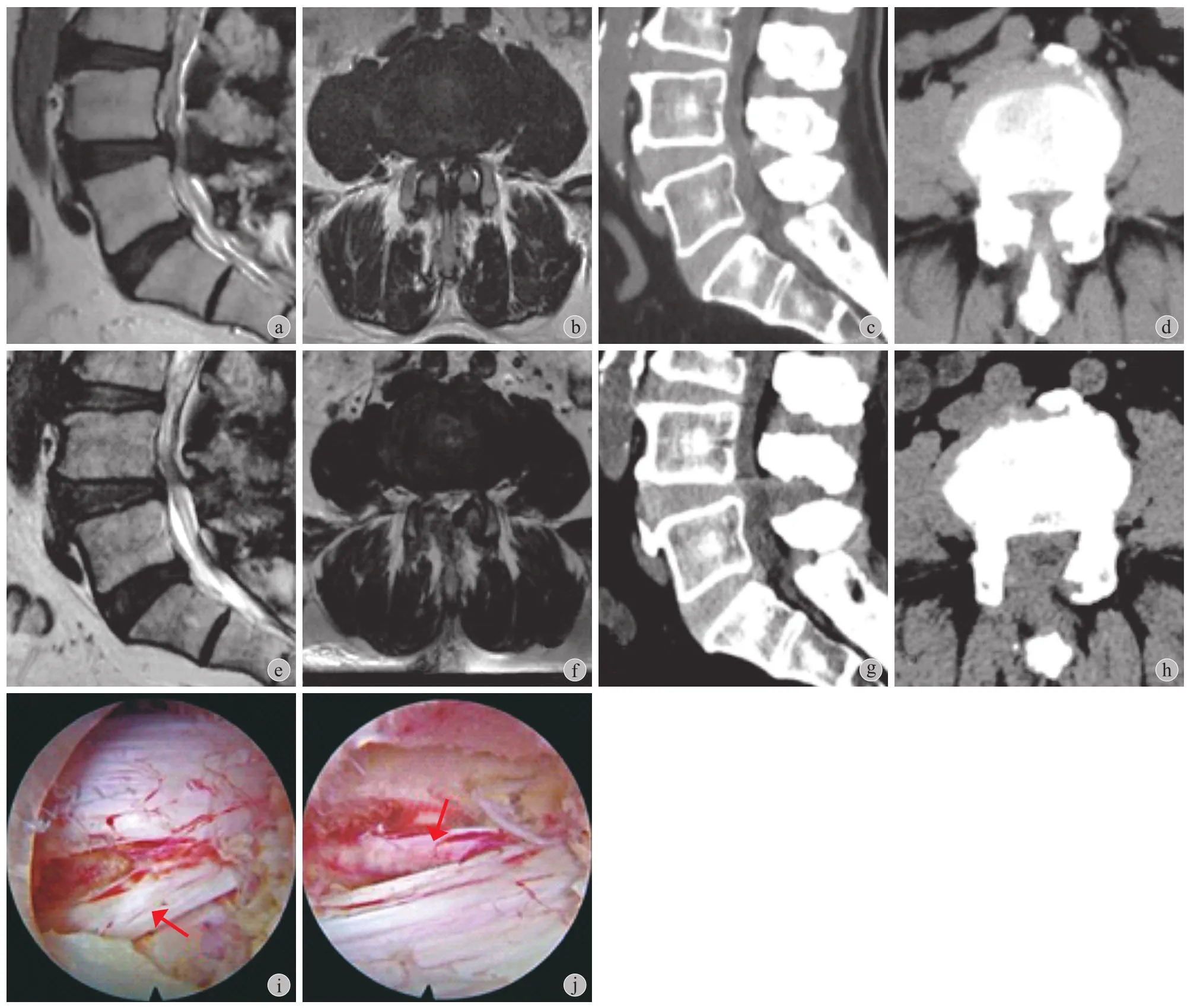
图1 A 组患者,男,83 岁,L4~5 重度中央型椎管狭窄,采用大通道内镜单侧入路双侧减压 a、b:术前 MRI 示 L4~5 中央椎管重度狭窄,椎间盘突出伴黄韧带肥厚;c、d:术前 CT 示关节突关节增生、内聚,中央椎管及双侧侧隐窝狭窄;e、f:术后16 个月 MRI 示中央椎管区域明显减压、容积扩大;g、h:术后16 个月 CT 示背侧骨性结构去除,中央椎管扩大、减压,双侧侧隐窝减压;i:减压后右侧神经根 ( 箭头 );j:减压后左侧神经根( 箭头 )Fig.1 A patient in group A, male, 83 years old, severe lumbar central spinal stenosis of L4-5. The patient was treated with large channel endoscopic unilateral approach for bilateral decompression a - b: Preoperative MRI revealed L4-5 disc herniation, severe central spinal canal stenosis and ligamentum flavum hypertrophy; c - d: Preoperative CT images showed articular process hyperplasia, central spinal canal and bilateral lateral recess stenosis; e - f: MRI showed remarkable decompression of central spinal canal 16 months after surgery; g - h: 16 months after surgery, CT showed the dorsal bony structures were removed, the central spinal canal was enlarged and decompressed, and the bilateral lateral recess were decompressed; i: The right nerve root after decompression ( arrow ); j: The left nerve root after decompression ( arrow )
讨 论
一、两种手术方式的有效性
手术治疗 LSS 的原则是在尽量保护脊柱稳定性的基础上,充分对狭窄的椎管及神经根管进行减压,扩大椎管内神经及血管的有效容积,进而缓解临床症状,提高生活质量。在对中央型腰管狭窄症的手术治疗上,既往常选经后方入路减压,包括开放手术 ( 椎板切除 / 开窗,减压固定融合 ) 及微创手术 ( 微创椎间盘镜减压、通道辅助下椎管减压 )等,但随着脊柱内镜技术的不断发展,手术器械的改进及手术流程的优化,可在对周围组织产生最小影响的前提下,对狭窄的中央椎管进行充分减压,其疗效也得到认可。
目前大通道辅助下经椎板间单侧入路双侧减压是治疗重度 LSS 的常规手术,因其使用大通道内镜 ( 10 mm ) 相比普通内镜 ( 7 mm ) 具备更宽的工作通道,能使用更大的减压器械,具有微创且效率高的特点,受到脊柱外科医师的青睐。一方面,因该手术只需要单侧入路且相比椎板开窗减压创伤更小,可以最大限度地减少对后方结构的医源性损伤;另一方面,大通道内镜通过椎板间入路可直接减压硬膜囊背侧结构,更容易处理位于背侧的肥厚韧带组织及侧方内聚增生的关节突,可以有效扩大中央椎管及双侧骨性侧隐窝空间,实现双侧神经根和硬膜囊的充分减压,保证了手术减压效果。本研究中采用该术式治疗重度腰椎中央管狭窄的患者VAS 评分、ODI 评分与术前相比有显著改善,末次随访 MacNab 优良率达 96.8%,其有效性与既往该类手术报道相似。
既往有学者研究认为,经皮椎间孔镜减压技术不适合腰椎中央管狭窄的治疗,因其减压范围主要在椎间孔及侧隐窝区域。但随着微创手术技术的不断发展,经椎间孔入路治疗中央型 LSS 的有效性也已经被一些临床研究所证实。笔者也在临床中应用孔镜双侧入路双侧减压治疗重度中央型 LSS,并取得满意临床疗效。因经孔镜双侧入路双侧减压范围包括双侧椎间孔、侧隐窝和中央椎管,可以充分有效地扩大整个椎管容积,实现双侧神经根和硬膜囊的充分减压,也可以保证手术效果。本研究中 B组患者的 VAS 评分、ODI 评分与术前相比有显著改善,末次随访时采用改良 MacNab 标准评价疗效也取得 96.0% 的优良率,略优于其它经椎板间入路减压的临床研究效果。
在两种手术方式治疗重度中央型 LSS 均取得满意临床疗效的前提下,大通道内镜手术具备手术时间短、术中 C 型臂 X 线机射线暴露时间短的优势,更适合应用于治疗腰椎小关节增生、内聚,黄韧带肥厚、钙化等引起的重度中央型 LSS。但对于影像学显示在硬膜囊腹侧椎间盘突出、后纵韧带钙化或骨化的同时存在背侧致压因素的重度中央型 LSS,则建议选择经孔镜双侧入路双侧减压治疗。因为大通道内镜工作通道直径粗大,难以对腹侧进行有效彻底的减压,而强行推挤、牵拉硬膜及神经张力过大可能会使术后下肢麻木加重,甚至增加术后神经麻痹等并发症的发生概率,而经皮椎间孔镜直径较小,可以在对硬膜、神经刺激较小的情况下对腹侧进行更直接、彻底的减压。
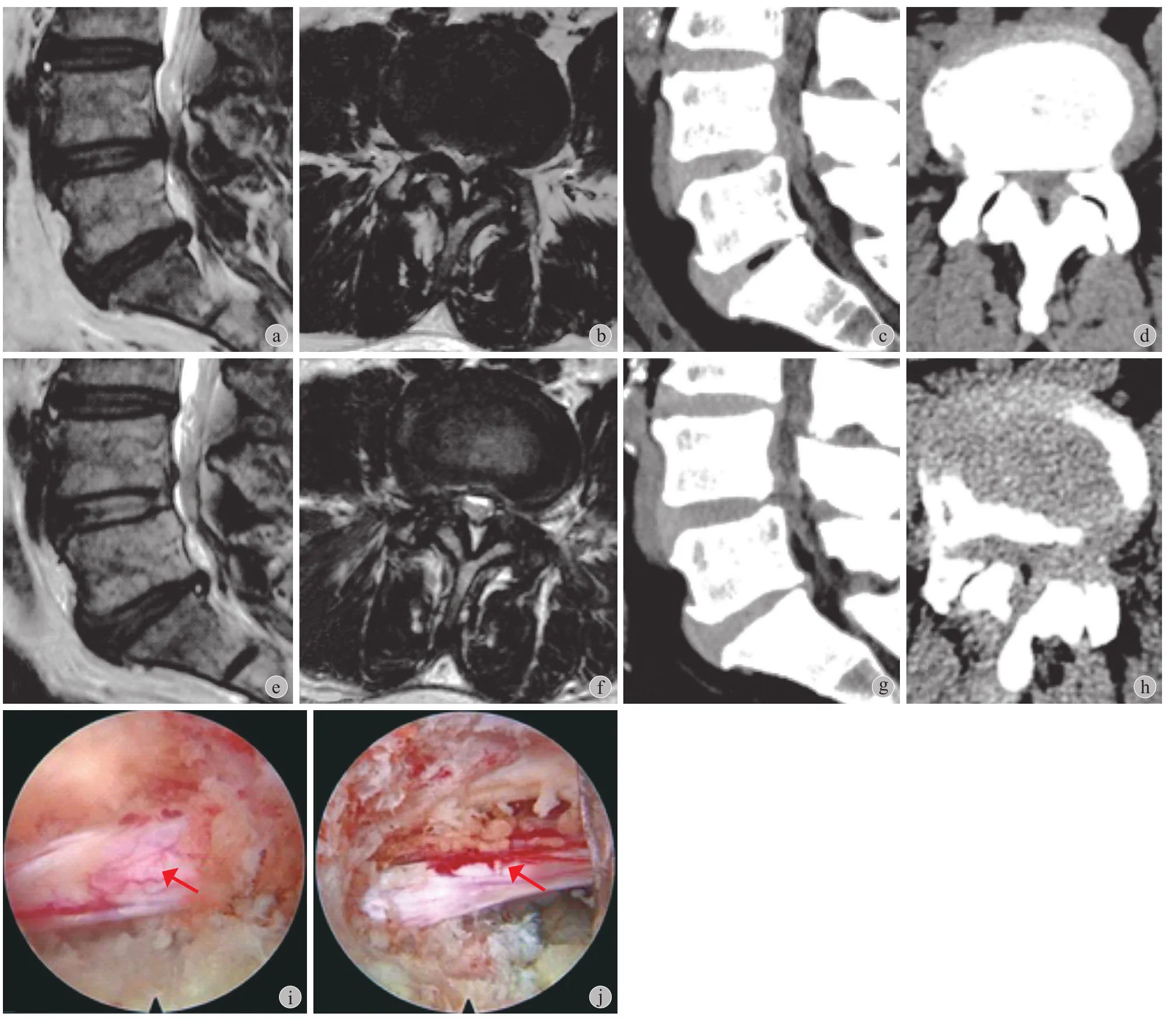
图2 B 组患者,男,49 岁,L4~5 重度中央型椎管狭窄,采用椎间孔镜双侧入路双侧减压 a、b:术前 MRI 示 L4~5 椎间盘突出,中央椎管重度狭窄伴黄韧带肥厚,关节突关节内聚;c、d:术前 CT 示关节突关节增生,黄韧带肥厚,双侧侧隐窝狭窄;e、f:术后 14 个月 MRI 示中央椎管区域明显减压、容积扩大;g、h:术后 14 个月 CT 示骨化黄韧带切除、中央椎管扩大,双侧侧隐窝减压,上关节突、下关节突均保留较好;i:术中减压后左侧神经根 ( 箭头 );j:术中减压后右侧神经根 ( 箭头 ),可见硬膜囊背侧脂肪组织Fig.2 A patient in group B, male, 49 years old, severe lumbar central spinal stenosis for L4-5, bilateral foramen microscopic bilateral decompression a - b: Preoperative MRI revealed L4-5 disc herniation, severe central spinal canal stenosis, ligamentum flavum hypertrophy and articular process cohesion; c - d: Preoperative CT images showed articular process hyperplasia, ligamentum flavum hypertrophy and bilateral lateral recess stenosis; e - f: 14 months after surgery, MRI showed remarkable decompression of central spinal canal; g - h: 14 months after surgery, CT showed that the ossified ligament flavum was removed,the central spinal canal was enlarged and decompressed, the bilateral lateral recess were decompressed and articular process was well preserved;i: The left nerve root after decompression ( arrow ); j: The right nerve root after decompression ( arrow ), adipose tissue on the dorsal side of the dural sac may be seen
二、两种手术方式的安全性
对于大通道下经椎板间单侧入路双侧减压技术,因后方经椎板间入路术式可获得良好的背侧结构视角,为脊柱外科医师所熟悉,更容易接受和掌握。与侧路镜相比,椎板间入路操作路径较短,更容易获得宽大的摆动角度和幅度,为套筒平移技术等提供了基本条件从而增加了减压范围,这有利于对侧减压技术的实施,从而为安全的单侧入路处理对侧狭窄椎管提供了技术条件。与椎间孔镜相比,大通道内镜无论是骨性结构还是软组织处理,全程均为可视性操作,因此进一步保证了大通道内镜的安全性。此外,内镜工作通道大,配套器械效率高,如椎板咬骨钳达 5.5 mm,大通道专用镜下骨刀 ( 4 mm )、镜下环锯处理效率高,可缩短手术时间。本研究中未出现硬膜囊撕裂、神经损伤等严重并发症。
对于经孔镜双侧入路双侧减压的安全性而言,目前主流麻醉方式为静脉麻醉 + 局部麻醉,术中患者清醒,患者可对神经刺激给予及时反馈从而进一步降低了术中操作损伤神经的可能性。此外限深环锯、镜外可视环锯、镜下磨钻、镜下骨刀的使用,不仅能更高效去除骨结构,还降低硬膜囊撕裂和神经损伤的风险。但仍需注意精细的操作和必要的预止血以确保手术区域清晰,从而有效减少手术过程中的并发症。有研究认为经皮椎间孔镜手术中由于部分盲视操作的存在,增加了硬膜囊撕裂、神经损伤等并发症的发生率。然而,与之前的内镜减压技术报道相比,本研究中手术相关并发症 ( 1 例硬膜囊撕裂 ) 发生率 ( 2% ) 并不高,低于既往研究结果,由于硬膜囊裂口小、无神经疝出及嵌顿,术后严密缝合,无其它特殊处理,术后未发生脑脊液漏等不良结果,患者未出现相关临床症状。
三、两种手术方式术中操作要点与技巧
对两种手术来说均需保证术中出血可控视野清晰,一方面,持续生理盐水灌注压力有助于椎管内止血,提高手术视野清晰度,进一步减少术中神经损伤的发生,笔者采用了电动输液架调节灌洗液的高度以保证术中水压的充分和稳定 ( 图 3 );另一方面:术前静脉使用 20~50 mg / kg 剂量的氨甲环酸,术前俯卧位腹部悬空降低腹压对椎管内出血的影响,合理地利用射频电极对局部小血管进行预止血,以上要点都对减少出血、维持术野清晰有帮助。
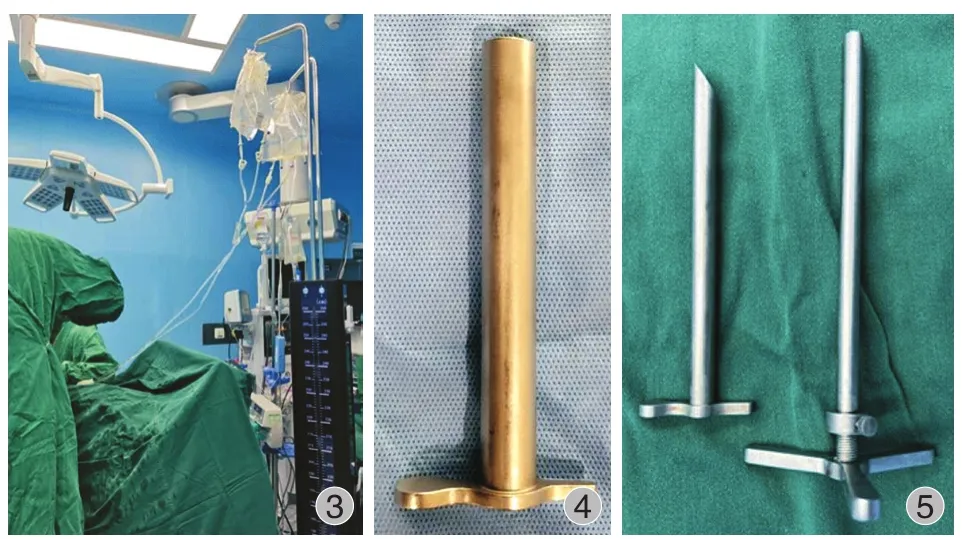
图3 电动输液架图4 大通道平口工作套管图5 镜外可视环锯及工作套管Fig.3 Electric infusion rackFig.4 Large channel flat mouth working sheathsFig.5 Endoscopic external visualization ring saw and working sheaths
大通道内镜:平口工作套管 ( 图 4 ) 与局部接触面积更大,可以高效地将软组织与骨性结构分离,减少周围软组织及出血对视野的影响,更便于后续使用镜下环锯处理骨性结构。术中减压顺序也有利于缩短手术时间,提高安全性,笔者建议先处理入路侧骨性结构 ( 部分下关节突、部分上关节突 ) 并使用椎板咬骨钳向头端和尾端咬除骨性结构至黄韧带止点,然后切除对侧部分下关节突。切除黄韧带后显露对侧上关节突内侧缘,使用镜下限深骨刀切除对侧上关节突内侧缘,显露对侧行走根,并减压扩大对侧侧隐窝空间。最后使用椎板咬骨钳咬除入路侧上关节突并暴露同侧行走根、减压侧隐窝。对于重度中央管狭窄症患者,黄韧带与硬膜囊常紧密粘连,术中先切除骨性结构暴露黄韧带止点,最后切除黄韧带进入椎管,这样的操作顺序不仅省去了高风险的破黄步骤,黄韧带间接起到保护神经结构作用从而增加了手术的安全性。先去除双侧骨性结构之后去除黄韧带,减少了椎管暴露的时间,从而减少了出血以及出血引起的盲视时间。在减压全过程利用平移技术平移工作套管,减小内镜倾角,便于镜下操作并且减少工作套筒对硬膜囊及神经的挤压。
双侧椎间孔镜:良好的成形是椎间孔镜手术顺利的前提,第一次成形时选用较大直径限深环锯( 8.5 mm ),在透视下和环锯深度限制下缓慢旋入,透视标准正位下环锯尖端位置接近但不超过椎弓根内缘,标准侧位下环锯腹侧不超过椎体后缘连线,注意以上事项才能保证安全的同时提高成形的效率。第一次成形后更换为可视环锯配套工作套管并置入镜外可视环锯 ( 图 5 ),在内镜监视下以初次环锯成形后的锯痕为参考,清理、止血、显露上关节突腹侧、外侧及与椎弓根移行处,在内镜监视下对骨性侧隐窝上部行第 2 次成形,充足且合理的骨性成形便于后续工作套管及内镜自如调节角度、调整位置,从而为椎管的彻底减压创造了先决条件。此外对于腹侧减压,笔者的经验是尽可能不破坏腹侧的纤维环以及后纵韧带结构,对于椎间盘膨出无破口的患者,在椎间盘的侧方开一小洞并将椎间盘内松散髓核从此处取出,从而减小复发概率;对于破口和椎间盘突出明显的患者则直接去除突出椎间盘并常规处理纤维环破口。减压范围要充分,骨性侧隐窝上出口 ( 行走根恢复正常形态,周围有清晰和充分的间隙 ),神经及硬膜囊背侧留有 3~5 mm 空间,腹侧无明显突出及神经致压因素。硬膜囊充盈良好,恢复正常搏动。
综上所述,对于重度中央型 LSS 的治疗,上述两种微创手术方式都是有效且安全的,相比之下椎板间大通道内镜单入路双侧减压具有手术时间更短,透视次数更少的优势,经孔镜双侧入路双侧减压虽然手术时间和透视次数不占优势,但是对于腹侧巨大突出、腹侧骨化、后纵韧带骨化的患者减压,神经牵拉张力更小、腹侧减压范围更广而更有优势。
