含钙矿物浮选过程中Ca-油酸胶体捕收剂的作用机理
2022-06-20孙文娟韩海生王舰程永彪王若林穆迎迎
孙文娟,韩海生,,王舰,程永彪,3,王若林,穆迎迎
1. 中南大学 资源加工与生物工程学院,湖南 长沙 410083;2. 湖南省伴生萤石综合利用氟化学工程技术研究中心,湖南 郴州 423037;3. 中化蓝天集团有限公司,浙江 杭州 310023
“高碱石灰法”[1-3]是典型的白钨矿浮选工艺,其特点在于在粗选段先加入大量的石灰和碳酸钠调整矿浆,然后加入抑制剂和捕收剂进行浮选。关于“高碱石灰法”的浮选机理,大多数研究是围绕石灰溶出的Ca2+影响和改变白钨矿和脉石矿物的表面电位的角度:石灰引入了大量的Ca2+到矿浆中,Ca2+选择性吸附在萤石、方解石等各种脉石矿物表面,使其表面荷正电,从而与随后加入的碳酸钠生成CaCO3沉淀覆盖在矿物表面。水玻璃吸附在脉石矿物表面形成的CaCO3覆盖层,从而增强脉石矿物的表面亲水性[1, 4-5]。“先碱后酸”工艺[6-7]是复杂伴生萤石浮选的常用工艺,其特点在于粗选过程在碱性条件下进行以保证回收率,精选过程在酸性条件下进行以提高精矿品位。研究表明,水玻璃在萤石表面的吸附产物在酸性条件下容易发生脱附,而在碱性条件下难以脱附[7]。此外,酸性条件下,方解石表面发生轻微溶解释放新表面,为水玻璃等抑制剂提供了新的吸附位点[6]。关于两种工艺机理研究一直以来都忽略了溶液中大量存在的钙离子与脂肪酸阴离子之间的作用。“高碱石灰法”工艺通过添加石灰向矿浆中引入了大量的钙离子,“先碱后酸”工艺中精选段的脉石矿物方解石表面发生溶解产生大量的钙离子。这些钙离子与脂肪酸捕收剂之间必然发生相互作用,影响矿浆组成和浮选行为。
从溶液化学角度分析,含钙矿物在溶液中溶出的钙离子非常容易与脂肪酸阴离子形成Ca-脂肪酸胶体[8]。研究表明,当钙离子浓度高于10-6mol/L时,油酸钙可以在溶液中生成,油酸钙的存在由溶液中钙离子浓度、油酸浓度和pH值三个条件共同决定[8-9]。在低浓度下,油酸钙可以通过化学吸附在矿物表面形成单层吸附,并随着离子浓度和药剂浓度增大逐渐形成多层吸附层[10]。在钙离子活化石英的浮选研究中发现,油酸钙可以在溶液中产生并迁移至石英表面,油酸钙在固/液界面发生吸附是石英可浮性增强的主要原因[11-14]。除此之外,油酸钙胶体在浮选中表现出优于油酸钠的选择性捕收能力,可以选择性吸附在萤石表面,实现萤石与方解石的选择性分离[15]。因此,研究含钙矿物浮选过程中钙离子与脂肪酸阴离子形成的Ca-脂肪酸胶体性质、在含钙矿物浮选过程中的行为及其吸附和作用机理,对于进一步完善浮选理论和指导含钙矿物浮选实践具有重要的现实意义。
本文以白钨矿、萤石和方解石为研究对象,以Ca(OL)2胶体为捕收剂,研究其在白钨矿、萤石和方解石浮选过程中的行为和作用机理。通过溶液化学计算和红外光谱分析研究了油酸钠浮选含钙矿物溶液体系中Ca(OL)2胶体存在的优势条件区间;通过纯矿物浮选试验研究Ca(OL)2胶体对白钨矿、萤石和方解石的浮选行为;通过红外光谱分析、动电位分析和接触角测试研究Ca(OL)2胶体在白钨矿、萤石和方解石表面的吸附和作用机理;基于上述试验和分析研究,提出了油酸钠浮选含钙矿物的作用新路径。
1 试验
1.1 试验样品及试样
试验所用的白钨矿、萤石和方解石纯矿物样品均取自湖南省柿竹园有色金属有限责任公司。纯度均大于95%,并进行X射线衍射(XRD)分析,结果如图1所示。矿物经手选后破碎,然后磨至-0.074 mm占100%,以供试验使用。试验所用氯化钙、油酸钠(C17H33COONa,简写为NaOL)、氢氧化钠和盐酸均为分析纯。Ca(OL)2胶体由氯化钙与油酸钠摩尔比11混合制备得到。试验用水均为去离子水。
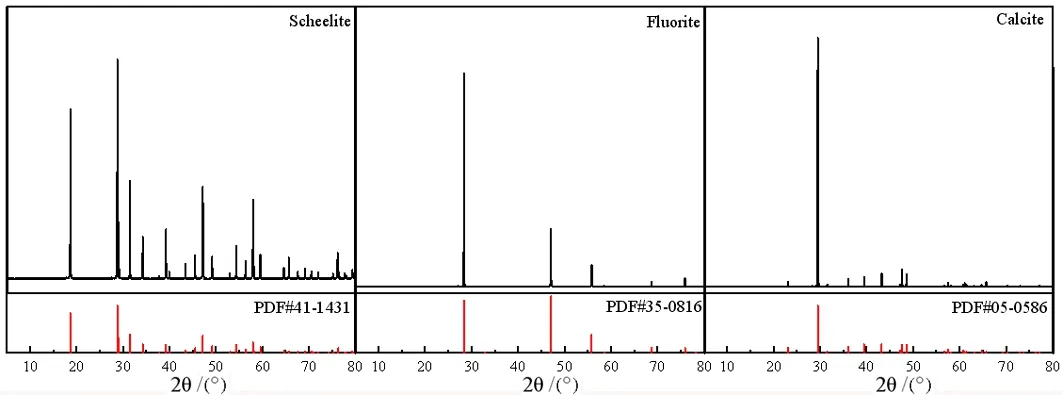
图1 白钨矿、萤石和方解石单矿物X射线衍射分析图
1.2 浮选试验方法
本试验采用XFG型挂槽式浮选机,配合使用50 mL单矿物浮选槽进行。试验前超声清洗浮选槽,称取2 g纯矿物与适量去离子水混合,控制总体积在40 mL以内。设置浮选机转速为1 750 r/min。如图2所示,依次调浆1 min、调整pH、调浆3 min、加入捕收剂作用3 mim后刮泡,刮泡时间控制在3 min。从浮选槽中刮得的上层泡沫产品即为精矿,而浮选槽中未上浮的底
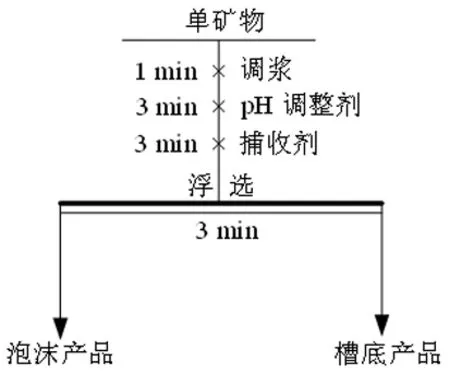
图2 单矿物浮选试验流程
部产品则为尾矿。将两种产品分别经过过滤、烘干、称重后按回收率公式计算回收率。
1.3 红外光谱测试
待测样品经玛瑙研钵磨细至-2 μm,按浮选流程与药剂作用后,采用溴化钾压片法进行压片处理,并使用740-FTIR型红外光谱仪对样品进行检测,分析波数范围为4 000~400 cm-1,记录试验数据。
1.4 Zeta电位测定
测试所用矿物样品经玛瑙研钵研磨1~2 h至粒度-2 μm。配制1×10-2mol/L 硝酸钾溶液作为电解质溶液。测试前称取20 mg待测样品,在烧杯中与40 mL 硝酸钾溶液混合后充分搅拌,并按单矿物浮选试验操作流程依次调节pH、添加药剂。长时间充分静置后,取澄清、无固体颗粒存在的上清液缓慢地注入Malvern Zetasizer Nano样品池,仔细检查没有气泡存在后测定Zeta电位。
1.5 接触角测定
接触角的测定采用ES-103HA型接触角测定仪。采用金相试样抛光机将矿物薄片磨平并抛光,参照单矿物浮选试验,将矿物表面放入盛有一定浓度浮选药剂的烧杯中,用磁力搅拌器搅拌2 min,然后用镊子取出矿物薄片,用滤纸吸干薄片上的液体,并用去离子水清洗两边,于温度为25 ℃的真空干燥箱烘干,然后将固体薄片固定在测定仪的载物台上,轻轻转动注射器滴出固定体积的水滴,测定水滴在矿样表面的接触角。每个条件重复测定5次,最终试验结果取测量平均值。测量完成后将矿物薄片用金相试样抛光机打磨抛光,使其产生新的表面,并用去离子水反复清洗,以备下次测量使用。
2 结果与讨论
2.1 Ca(OL)2胶体的溶液化学分析
白钨矿、萤石和方解石都具有一定的溶解性,在浮选过程中,矿物发生溶解反应,释放大量的钙离子进入矿浆中[9, 16-17]。这些钙离子容易与油酸阴离子反应,生成Ca(OL)2胶体,影响矿浆组成和矿物浮选行为[17]。表1列出了钙离子存在下油酸钠水溶液中存在的反应及反应平衡常数。根据以下反应,得到钙离子存在下的溶液组分浓度图,如图3所示。

表1 钙离子存在下,油酸钠溶液中的反应及反应平衡常数[9, 17]
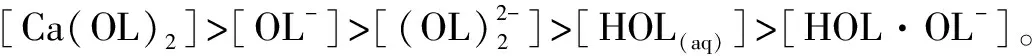
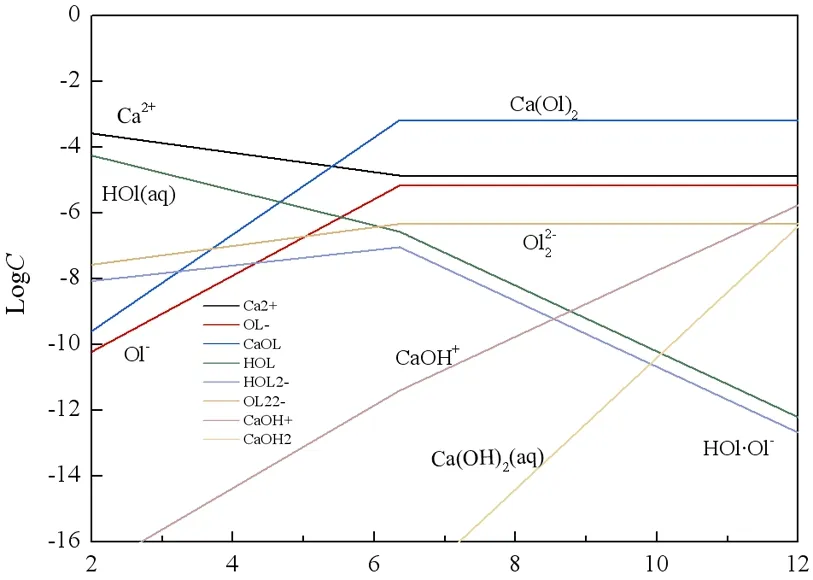
图3 加入钙离子后的油酸组分浓度图(CCa2+=1×10-3 mol/L,CHOl=1×10-3 mol/L)
2.2 Ca(OL)2胶体作用下的矿物浮选行为
分别使用油酸钠和Ca(OL)2胶体作为捕收剂浮选白钨矿、萤石和方解石三种含钙矿物,在不同pH条件下的浮选回收率结果如图4所示。Ca(OL)2胶体作用下白钨矿、萤石和方解石的浮选回收率随pH的变化规律与油酸钠相似,但Ca(OL)2胶体的浮选选择性较油酸钠更强。Ca(OL)2胶体对白钨矿和萤石的浮选效果优于油酸钠。随着pH增大,使用Ca(OL)2胶体浮选时白钨矿回收率不断升高,在pH=11时,白钨矿回收率达到73.38%,与使用油酸钠相比高了18.69百分点。当pH<10时,Ca(OL)2胶体浮选萤石的回收率始终高于油酸钠,pH=8时,Ca(OL)2胶体浮选萤石的回收率达到最高95.45%。当pH>10时,萤石浮选回收率明显降低,这是由于强碱性条件下萤石表面F-被OH-替代,从而影响捕收剂在表面的吸附[18-19]。对于方解石,使用Ca(OL)2胶体浮选时的回收率始终低于使用油酸钠,当pH=11时,Ca(OL)2胶体浮选方解石的回收率为54.17%,与使用油酸钠相比,回收率降低15.99百分点。
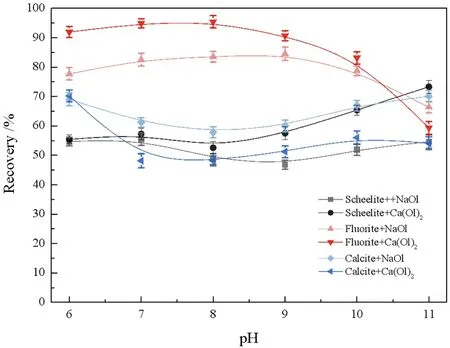
图4 Ca(OL)2胶体与油酸钠作捕收剂,三种含钙矿物浮选回收率与pH的关系(CCa(OL)2=CHOL=1×10-3 mol/L)
油酸钠和Ca(OL)2胶体作用后的白钨矿、萤石和方解石表面接触角测试结果如图5所示。油酸钠、Ca(OL)2胶体作用后三种矿物表面接触角都有所增加,且随着药剂浓度的升高而逐渐增大,这说明油酸钠与Ca(OL)2胶体在矿物的作用,增强了矿物表面疏水性。油酸钠浓度为5×10-4mol/L时,三种矿物表面接触角均在90°以上,表面疏水性相似。Ca(OL)2胶体作用后的白钨矿和萤石表面接触角大于油酸钠作用后的,而方解石表面接触角则低于油酸钠作用后的。Ca(OL)2胶浓度为5×10-4mol/L时,白钨矿和萤石表面接触角均在95°以上,而方解石接触角为83.14°,矿物表面疏水性差异明显增大。
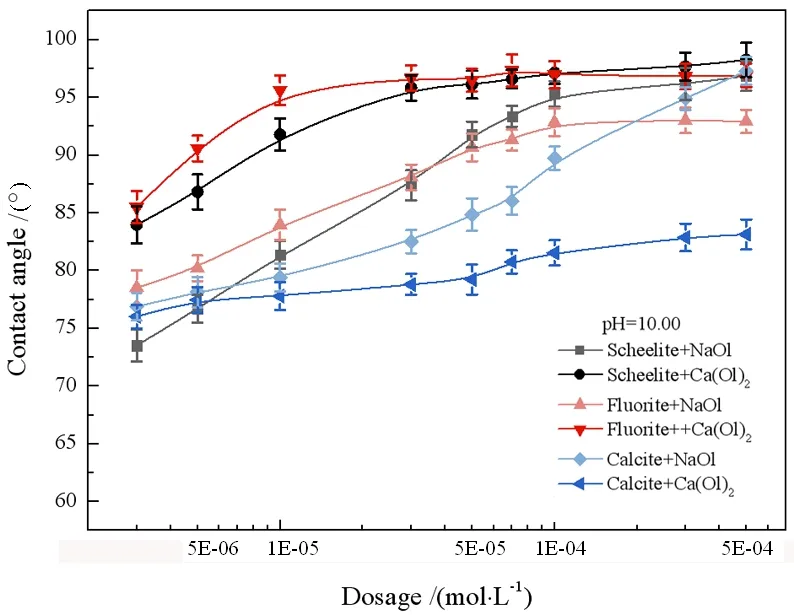
图5 油酸钠和Ca(OL)2胶体作用下白钨矿、萤石和方解石的表面接触角
2.3 Ca(OL)2胶体捕收剂的作用机理
2.3.1 Ca(OL)2胶体在矿物表面作用的红外光谱分析
图6为油酸钠和Ca(OL)2胶体作用前后,白钨矿、萤石和方解石的红外光谱分析结果。在Ca(OL)2的红外光谱图中,3 382.58 cm-1处为Ca(OL)2胶体的羟基振动吸收峰,2 923.61 cm-1和2 852.25 cm-1处分别为甲基、亚甲基伸缩振动吸收峰,1 737.58 cm-1处为羰基伸缩振动峰,1 577.51 cm-1和1 540.87 cm-1处为羧酸的反对称伸缩振动吸收峰,1 467.59 cm-1处为羧酸的反对称伸缩振动吸收峰,1 108.89 cm-1和1 104.32 cm-1处为羧酸负离子的对称伸缩振动吸收峰,721.26 cm-1处为Ca(OL)2胶体长链-(CH2)n-的吸收峰[20-22]。白钨矿纯矿物红外光谱中,W-O键的不对称伸缩振动吸收峰位于819.61 cm-1,W-O键面外弯曲振动吸收峰位于443.55 cm-1。与作用前相比,Ca(OL)2胶体作用后的白钨矿红外光谱图中在2 925.53 cm-1、2 854.18 cm-1、1 799.29 cm-1、1 697.08 cm-1、1 560.16 cm-1、1 461.80 cm-1处出现了新的吸收峰,这说明Ca(OL)2胶体在白钨矿表面发生了吸附。图谱中出现了Ca(OL)2胶体的甲基、亚甲基C-H伸缩振动吸收峰(偏移-1.92 cm-1、+1.93 cm-1)、羰基伸缩振动吸收峰(偏移+61.71 cm-1)、羧基反对称伸缩振动吸收峰(偏移+119.57 cm-1、+19.29 cm-1)和对称伸缩振动吸收峰(偏移-6.51 cm-1)。这说明,Ca(OL)2胶体在白钨矿表面发生了化学吸附。
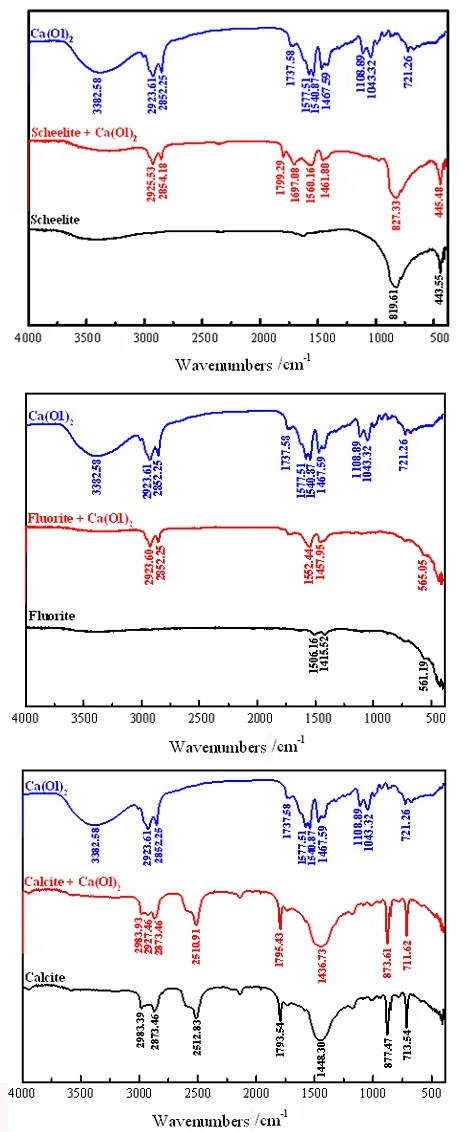
图6 Ca(OL)2胶体作用后的白钨矿、萤石和方解石红外光谱图
萤石的红外光谱图中,1 560.16 cm-1、1 415.52 cm-1、561.19 cm-1处吸收峰为萤石特征谱峰。Ca(OL)2胶体作用后的萤石红外光谱图中在2 925.53 cm-1、2 854.18 cm-1处出现了新的吸收峰,分别为Ca(OL)2胶体的甲基、亚甲基C-H伸缩振动吸收峰(偏移+1.92 cm-1、+1.93 cm-1)。此外,萤石在1 560.16 cm-1、1 415.52 cm-1处的特征吸收峰与Ca(OL)2胶体的吸收峰相互叠加、覆盖,强度变强。这说明Ca(OL)2胶体在萤石表面发生了化学吸附。方解石与Ca(OL)2胶体作用后的红外光谱图中,在2 927.46 cm-1处出现新的吸收峰,为Ca(OL)2胶体的甲基特征吸收峰偏移+3.85 cm-1所得。方解石在1 448.30 cm-1、877.47 cm-1、713.54 cm-1处的CO32-特征吸收峰峰位分别负移了11.57 cm-1、3.86 cm-1和1.93 cm-1,产生1 436.73 cm-1、873.61 cm-1和711.62 cm-1峰。这说明Ca(OL)2胶体在方解石表面发生了化学吸附。
2.2.2 Ca(OL)2胶体在矿物表面作用的动电位分析
图7为油酸钠和Ca(OL)2胶体表面电位及其作用后对白钨矿、萤石、方解石矿物表面动电位的影响。钙离子的动电位始终为负,且在测试pH范围内其动电位几乎不受pH影响。油酸钠动电位随着pH值增大而逐渐增大,最高值出现在pH=10.5。在测试pH范围内,Ca(OL)2胶体的电位曲线与Ca2+相似,介于 Ca2+与NaOL之间。随着pH的增大,Ca(OL)2胶体表面动电位与油酸钠表面动电位值差距逐渐减小。随着钙离子浓度增大,溶液中的Ca(OL)2胶体逐渐增多,动电位也逐渐正移。
Ca(OL)2胶体加入后的白钨矿、萤石和方解石表面动电位均发生了负移,说明Ca(OL)2胶体在白钨矿、萤石和方解石表面发生了吸附。白钨矿表面和Ca(OL)2胶体表面都荷负电,可以推测Ca(OL)2胶体在白钨矿表面发生了非静电吸附。当pH<9时,萤石和方解石表面都荷正电,此时荷负电的Ca(OL)2胶体可以通过静电吸附方式吸附于萤石、方解石表面。此外,Ca(OL)2胶体表面电位低于油酸钠,而Ca(OL)2胶体和油酸钠吸附后的萤石表面电位负移幅度相近,侧面说明Ca(OL)2胶体在萤石表面的吸附量要大于油酸钠。

图7 Ca(OL)2胶体和油酸钠对白钨矿、萤石和方解石表面动电位的影响
综合以上结果建立Ca(OL)2胶体在含钙矿物表面作用机理,如图8所示。油酸钠浮选体系中存在两种作用路径:一种是油酸阴离子直接与矿物表面钙质点作用,形成油酸钙沉淀;另一种是矿物表面溶解进入溶液中的钙离子与油酸阴离子生成稳定的Ca(OL)2胶体,然后迁移至矿物表面吸附。两种路径殊途同归,都在矿物表面最终形成油酸钙吸附层。浮选试验表明,第二种路径中的Ca(OL)2胶体对白钨矿和萤石的浮选效果较油酸钠更好,对方解石的浮选效果较油酸钠作用时差,可以增大矿物表面疏水性差异,增强浮选的选择性。
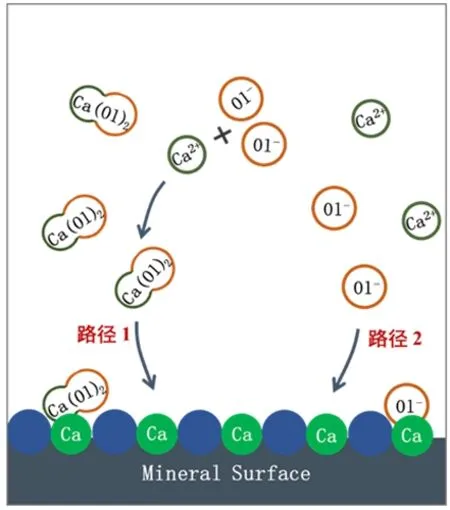
图8 油酸钠和Ca(OL)2胶体在含钙矿物表面作用机理
3 结论
(1)在碱性条件下,使用油酸钠浮选白钨矿、萤石和方解石时,矿物表面溶解产生的钙离子可以与油酸阴离子反应生成稳定存在的Ca(OL)2胶体,并作为油酸的主要溶液组分发挥作用。
(2)Ca(OL)2胶体对白钨矿和萤石的捕收能力较油酸钠强,对方解石的捕收能力较油酸钠弱。Ca(OL)2胶体吸附后的白钨矿、萤石表面疏水性强于油酸钠作用后的,而方解石表面疏水性弱于油酸钠作用后的。Ca(OL)2胶体在白钨矿表面发生化学吸附,在萤石和方解石表面以化学吸附为主,当pH<9时也存在一定的静电吸附作用。
(3)油酸钠浮选含钙矿物过程中除油酸阴离子直接作用于矿物表面的路径外,存在另外一种作用路径:钙离子与油酸阴离子在溶液中首先生成Ca(OL)2胶体,Ca(OL)2胶体在溶液中迁移至矿物表面发生吸附。
