超高效液相色谱-四极杆/静电场轨道阱高分辨质谱快速测定水果中17种对羟基苯甲酸酯
2022-06-18岑建斌周朗君方厚托林茵茵区硕俊何敏恒黄嘉乐李秀英
岑建斌,周朗君,方厚托,林茵茵,区硕俊,党 华,何敏恒,黄嘉乐,李秀英
(广州检验检测认证集团有限公司,国家加工食品质量监督检验中心(广东),广东 广州 511447)
对羟基苯甲酸酯(Parabens),又称尼泊金酯,因其具有酚羟基结构,属酚类防腐剂,其作用机制是破坏微生物的细胞膜,导致细胞内蛋白质变性,并可抑制微生物细胞的呼吸酶系与电子传递酶系的活性,具有良好的抑菌作用,是一种广谱型抗菌防腐剂[1]。对羟基苯甲酸酯的烷基碳链越长,菌体对尼泊金酯的吸附量越大,因而抗菌活性也越大[2]。有研究表明,对羟基苯甲酸酯具有雌激素活性[3-5],在人体中,从胃肠道和血液中迅速吸收,水解为对羟基苯甲酸,偶联并从尿液中排出[6]。接触对羟基苯甲酸酯可干扰人体的内分泌系统[7],且对人体细胞有一定毒性[8],从而对人类健康产生有害后果。我国允许部分该类物质(对羟基苯甲酸甲酯、对羟基苯甲酸乙酯)作为防腐剂在食品和药品的生产过程中使用[6]。其中GB 2760-2014 对经表面处理的鲜水果中的对羟基苯甲酸酯类(甲酯、乙酯)及其钠盐做出明确限量,要求以对羟基苯甲酸计不得大于0.012 g/kg[9]。而国际上欧洲经济共同体(EEC)规定,以对羟基苯甲酸计,食品中对羟基苯甲酸酯的最高允许含量为0.1%;当几种对羟基苯甲酸酯复配使用时,其总量不得超过0.1%[10]。因此,有必要对除甲酯、乙酯外的对羟基苯甲酸酯类物质进行定量研究。
目前测定对羟基苯甲酸酯的方法主要有液相色谱法[10-13]、薄层色谱法[14]、毛细管电泳法[15]、气相色谱法[16-18]、高效液相色谱-串联质谱法[19-20]、气相色谱-串联质谱法[21-22]、合相色谱-串联质谱法[23]等。其中,液相色谱法、薄层色谱法、毛细管电泳法、气相色谱法具有前处理步骤繁琐,分析图谱易受到杂质的影响,以及方法灵敏度较低的特点,对于ppb 级的目标化合物,难以准确测定,易出现假阳性现象。而高效液相色谱-串联质谱法、气相色谱-串联质谱法对目标物具有更高的选择性,灵敏度较高,且分析图谱受杂质的影响较小,对于同时测定多种化合物,具有高效定性定量的优点,且前处理无需过多净化或衍生即可准确测定,分析时间较短。近年来,相较于上述分析方法,高分辨质谱(HRMS)由于能测定精确质量数,因此具有更强的定性能力,在食品残留及污染物的快速检测和筛查中得到一定的应用[24-26]。本文以不同水果和17种对羟基苯甲酸酯为研究对象,借助超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UPLC-Q-Orbitrap HRMS),建立了快速测定不同水果中17 种对羟基苯甲酸酯类化合物的分析方法。
1 实验部分
1.1 仪器与试剂
Thermo Vanquish UHPLC 超高效液相色谱仪(美国Thermo Scientific 公司);Thermo Q-Exactive Orbitrap 高分辨质谱仪,配有电喷雾(H-ESI)离子源(美国Thermo Scientific 公司);KDC-40 低速离心机(安徽中科中佳科学仪器有限公司);IKA MS3 混匀振荡器(德国IKA 公司);ML204T 电子天平(瑞士Mettler Toledo 公司);Milli-Q 超纯水系统(美国Millipore 公司);KQ-500DE 型数控超声波清洗仪(昆山市超声仪器有限公司)。
3,5-二氯对羟基苯甲酸甲酯(纯度97%)、对羟基苯甲酸癸酯(纯度95%),上海源叶生物科技有限公司;对羟基苯甲酸甲酯(纯度99.7%)、对羟基苯甲酸乙酯(纯度99.0%)、对羟基苯甲酸丙酯(纯度>95%)、对羟基苯甲酸异丁酯(纯度>95%)、对羟基苯甲酸丁酯(纯度99.9%)、对羟基苯甲酸庚酯(纯度99.9%),德国Dr.Ehrenstorfer GmbH;对羟基苯甲酸异丙酯(纯度100%)、对羟基苯甲酸异辛酯(纯度≥98%),上海安谱实验科技股份有限公司;对羟基苯甲酸苯酯(纯度98%)、对羟基苯甲酸正戊酯(纯度97%),加拿大Toronto Research Chemicals 公司;对羟基苯甲酸苄酯(纯度100%,美国AccuStandard 公司);对羟基苯甲酸异戊酯(纯度99.6%,广州佳途科技股份有限公司);对羟基苯甲酸己酯(纯度≥98%)、对羟基苯甲酸壬酯(纯度≥98%),东京化成工业株式会社;对羟基苯甲酸正辛酯(纯度98%,阿法埃莎(中国)化学有限公司);甲醇(HPLC 级,德国Merck 公司);甲酸铵(色谱纯,美国Sigma-Aldrich公司)。
1.2 实验方法
1.2.1 样品前处理取适量水果,按照GB 2763-2021《食品安全国家标准食品中农药最大残留限量》附录A[27]测定部位要求制备试样,混合均匀,称取1.0 g(精确至0.001 g)样品于15 mL 离心管中,准确加入10 mL甲醇,涡旋振荡1 min,超声20 min。4 000 r/min离心2 min,上清液过0.22 μm尼龙膜,备用,待测。
1.2.2 标准溶液的配制标准储备液:分别准确称取适量17 种对羟基苯甲酸酯标准物质,用甲醇溶解后定容,折算浓度后,得到1 000 mg/L 标准储备液,于-20 ℃保存。标准中间液:分别取上述标准储备液100 μL于同一10 mL容量瓶中,甲醇定容,得到10 mg/L混合标准中间液。工作曲线:分别使用甲醇和空白基质液(选取阴性样品按“1.2.1”处理后得到),将标准中间液逐级稀释至2、3、4、5、10、50、100、200 μg/L。
1.2.3 液相色谱条件色谱柱:Agilent EclipsePlus C18RRHD(3.0 mm × 150 mm,1.8 μm,美国Agilent 公司);流动相:A 为5 mmol/L 甲酸铵水;B 为5 mmol/L 甲酸铵甲醇。梯度洗脱:-3 ~0 min,5%B;0 ~0.5 min,5%B;0.5 ~30 min,5%~80%B;30 ~32 min,80%~95%B;32 ~41 min,95%B。流速:0.3 mL/min;柱温:40 ℃;进样量:5 μL。
1.2.4 质谱条件电喷雾离子源(ESI);离子源电压:4.5 kV;透镜电压50 V;鞘气流速(Sheath gas)(氮气):45 unit;辅助气(Auxiliary gas)(氮气):8 unit;吹扫气(Sweep gas):1 unit;离子传输管温度(Capillary temperature):320 ℃;辅助气加热温度(Auxiliary gas heater temperature):400 ℃;扫描模式:Full MS/dd-MS2Confirmation,采集范围100 ~600m/z,负离子扫描模式;一级质谱分辨率(R):70 000;二级质谱分辨率为17 500;归一化碰撞能量(NCE):10、30、50 eV:测量数据采用赛默飞TraceFinder Software 4.1(美国Thermo Scientific公司)进行采集和处理。17种对羟基苯甲酸酯类化合物的质谱分析参数列于表1。
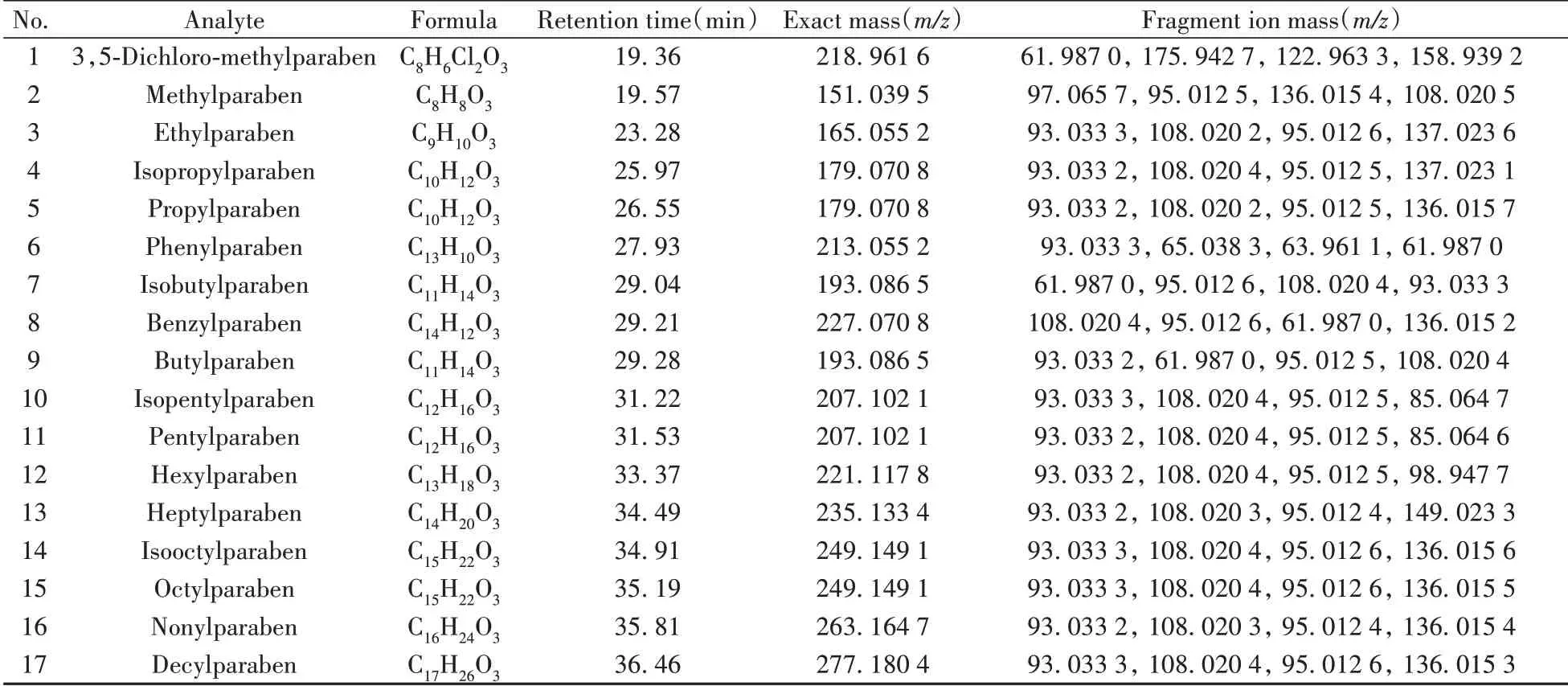
表1 17种对羟基苯甲酸酯标准物质及其方法参数Table 1 Method parameters of 17 parabens standards
2 结果与讨论
2.1 质谱-色谱条件的优化
通过对17种对羟基苯甲酸酯类化合物的结构进行研究,发现17种化合物均含有羟基和羰基,其在ESI 离子源电离时既可脱去氢离子显示电负性,又可带氢离子显示电正性。分别在电喷雾正、负模式下对17 种单标溶液(1 mg/L)进行质谱扫描,结果显示7 种分析物在负模式[M-H]-下响应较高,宜采用负模式进行测定。
分别对比了5 mmol/L 甲酸铵甲醇-5 mmol/L 甲酸铵溶液、5 mmol/L 甲酸铵乙腈-5 mmol/L 甲酸铵溶液作为流动相时的色谱分离效果。结果表明,使用5 mmol/L 甲酸铵甲醇-5 mmol/L 甲酸铵体系作流动相时,色谱峰形较好,17 种化合物均可达到基线分离;使用5 mmol/L 甲酸铵乙腈-5 mmol/L甲酸铵溶液体系时,部分色谱峰变形,影响定量分析。因此最终选择5 mmol/L 甲酸铵甲醇-5 mmol/L 甲酸铵溶液体系作为流动相。优化色谱条件后17 种化合物标准溶液的提取离子流图见图1。
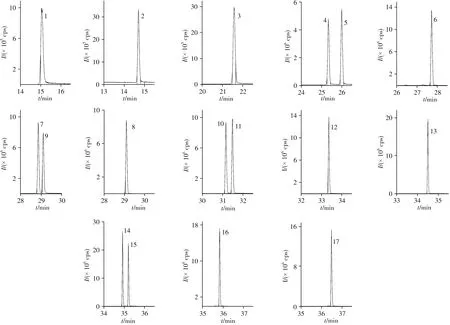
图1 17种对羟基苯甲酸酯标准溶液的提取离子流图(200 μg/L)Fig.1 XIC chromatograms of 17 parabens standard solutions(200 μg/L)the number denoted was the same as that in Table 1
2.2 提取溶剂种类的选择
分别称取1 g阴性苹果样品作为测试基质,加入500 μg/kg的17种对羟基苯甲酸酯,同时配制空白基质标准曲线用于定量分析。分别加入4种不同的提取溶剂(30%乙腈、乙腈、丙酮、甲醇)10 mL,超声20 min,实验重复6 次(n=6),以平均回收率作为参考指标,考察不同溶剂对回收率的影响,结果见图2。结果显示,甲醇的提取效率总体最好,回收率为88.1%~100%;采用30%乙腈水溶液提取时,由于对羟基苯甲酸酯类化合物的水溶性差,其回收率较低且沉淀效果差;使用乙腈提取时,对羟基苯甲酸酯类化合物的色谱峰形不佳,使用丙酮提取时,对羟基苯甲酸酯类化合物的回收率为62.3% ~88.3%。由于对羟基苯甲酸酯类化合物具有羟基,相比于乙腈、丙酮两种非质子溶剂,含有O—H键的质子性溶剂甲醇具有更强的提取效果,因此对羟基苯甲酸酯使用甲醇提取更适合。
2.3 提取溶剂用量的优化
由于水果的基质较复杂,目标物的提取效率易受水果中其他成分的影响,当提取溶剂用量低时,基质效应增强,提取溶剂用量大时,则方法的灵敏度降低,因此需对提取溶剂的用量进行优化。在同样条件下,考察了不同甲醇溶剂用量(5、10、15、20 mL)对17种化合物提取率(回收率)的影响。结果显示,当提取溶剂用量在10 mL 时,17 种化合物的整体提取率较高;当用量低于10 mL 时,整体提取率偏低,且以对羟基苯甲酸甲酯、丙酯、正戊酯、异戊酯、庚酯、正辛酯、异辛酯、癸酯以及3,5-二氯对羟基苯甲酸甲酯受影响最大,回收率较10 mL 低10%以上,可能由于基质在溶剂中的浓度较高,影响了对羟基苯甲酸酯类化合物的提取;当提取溶剂大于10 mL,对羟基苯甲酸酯类化合物的回收率随着溶剂量的增加呈下降趋势(见图2),且由于溶剂用量增加,稀释倍数增加,方法的灵敏度也随之下降。
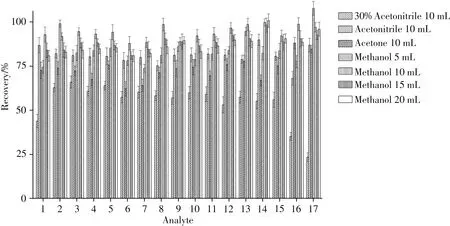
图2 不同溶剂及用量对目标物回收率的影响Fig.2 Influences of different solvents and dosages on recoveries of analytes the number denoted was the same as that in Table 1
2.4 化合物裂解途径分析
根据具体测得的化合物碎片,推断了17种对羟基苯甲酸酯的质谱裂解途径及主要碎片的具体结构(见图3)。17 种对羟基苯甲酸酯的分子式差异主要为R1、R2和R3基团的不同,除了3,5-二氯对羟基苯甲酸甲酯,其他化合物失去R1基团后,一般可产生m/z136 碎片,该碎片经过二次或三次碎裂,可得到m/z108 和m/z93,其余的碎片主要来源于[R1-O]-,但响应较低,因此在必要时,可考虑作为化合物自身的特征碎片进行匹配定性。另外,部分化合物m/z61的碎片响应较高,该碎片可能是通过苯环碎裂后生成的,同样,部分质荷比大于93 的碎片也可能存在苯环碎裂形成的情况,但响应均较低,因此不作深入探讨。

图3 化合物的质谱裂解途径分析图Fig.3 MS fragmentation pathways of analytes
2.5 基质效应的探究
考察了猕猴桃、葡萄、草莓、蓝莓、梨、苹果、油桃、枣、橙子、柑橘、柚子、荔枝、龙眼、火龙果、香蕉、芒果、菠萝、青橄榄、无花果、莲雾、西瓜、哈密瓜共22种水果基质效应的影响,覆盖了GB 2763-2021 对水果的所有分类,包括较具代表性的仁果类水果、核果类水果、浆果和其他小型类水果、热带和亚热带类水果、瓜果类水果[27]。采用“1.2.1”前处理方法,得到空白基质液,配制上机浓度为50 μg/L基质标准溶液,将基质标准溶液的峰面积与相应浓度甲醇配制的混合标准溶液所得峰面积相比,得到比值K。当K<0.8 时表示存在基质抑制现象,当K>1.2 时表示存在基质增强现象。结果表明,大部分对羟基苯甲酸酯类化合物K值在0.8 ~1.2之间,其中部分水果对应相关化合物呈基质抑制现象,如柚子中3,5-二氯对羟基苯甲酸甲酯的基质效应为0.758;无花果中对羟基苯甲酸甲酯的基质效应为0.660;菠萝、青橄榄、柚子中对羟基苯甲酸异丁酯的基质效应分别为0.742、0.717、0.751;青橄榄中对羟基苯甲酸正丁酯的基质效应为0.739。部分呈现基质增强作用,如油桃、橙子中对羟基苯甲酸异辛酯的基质效应分别为1.286、1.291;对羟基苯甲酸正辛酯、对羟基苯甲酸正壬酯、对羟基苯甲酸癸酯在大部分水果中存在基质增强现象,基质效应在0.871 ~3.150之间。结果显示,随着对羟基苯甲酸酯类化合物碳链增长或给电子能力变强,其基质增强效应整体呈上升趋势,可能原因为水果中普遍存在的成分协同使得给电子能力更强的化合物去质子效果更好,引起基质增强作用。因此当检出基质效应较强物质时,应使用基质标准曲线定量。
2.6 线性关系、检出限与定量下限
选取22 种不同水果经过本方法前处理后,配制混合标准基质曲线,以分析物的质量浓度为X,以其相应峰面积为Y,拟合线性方程,获得17种对羟基苯甲酸酯的线性范围(见表2)。取基质混合标准溶液,以本方法的仪器条件进行测定,由于部分对羟基苯甲酸酯类化合物在高分辨质谱无基线噪音,因此无法采用S/N计算方法检出限和定量下限。本方法采用阴性猕猴桃、葡萄、草莓、蓝莓、梨、苹果、油桃、枣、橙子、柑橘、柚子、荔枝、龙眼、火龙果、香蕉、芒果、菠萝、青橄榄、无花果、莲雾、西瓜、哈密瓜共22种水果基质,通过添加不同水平的17种对羟基苯甲酸酯类化合物,测得可获得碎片离子的最低质量浓度作为定量下限,并以定量下限最高的水果基质表示方法定量下限。确定定量下限后,以约1/3质量浓度对相对应的基质进样,当出现1个以上碎片,定义为检出限。测定结果见表2,17种对羟基苯甲酸酯的方法检出限为5 ~30 μg/kg,方法定量下限为20 ~100 μg/kg。
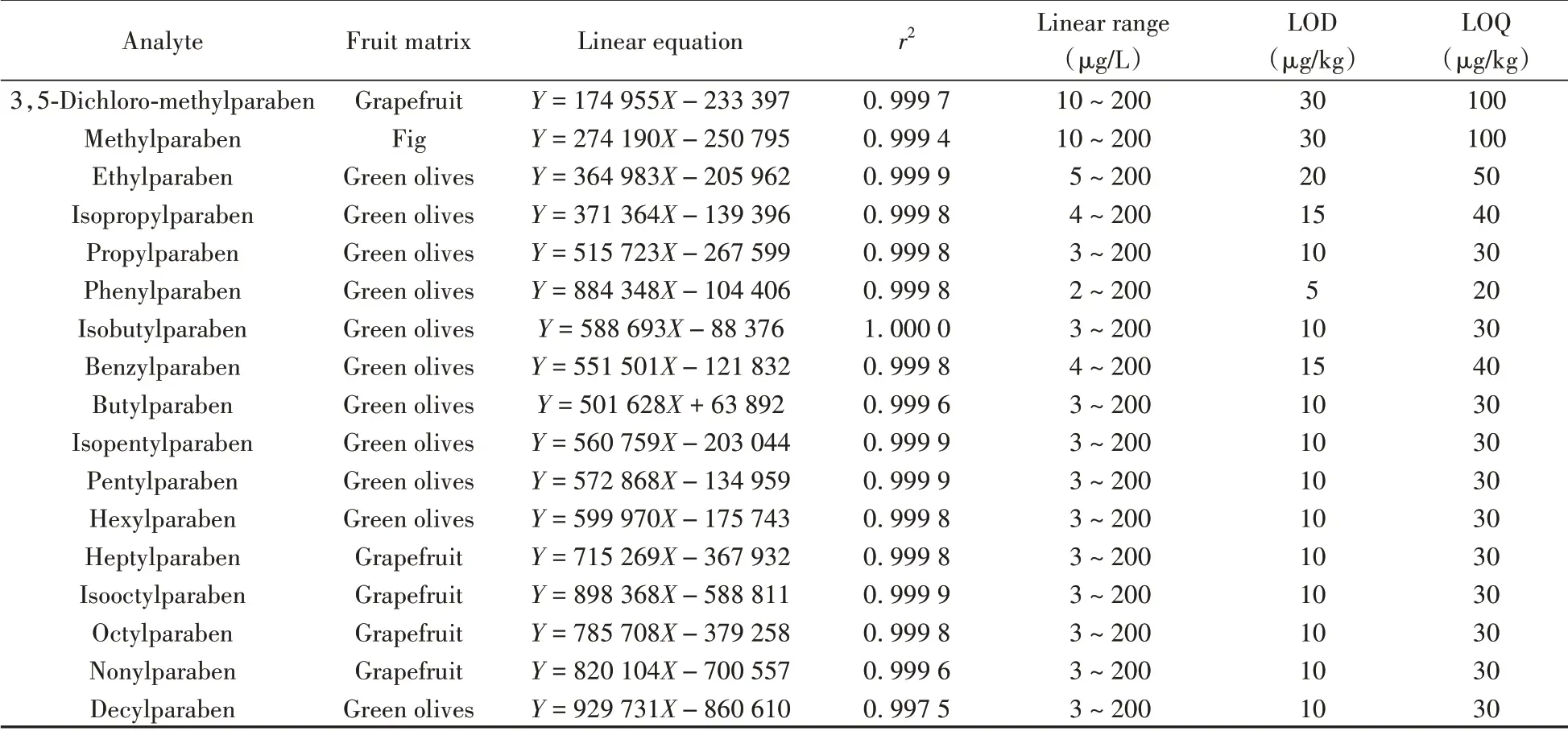
表2 17种对羟基苯甲酸酯的线性范围、相关系数(r2)、检出限(LOD)及定量下限(LOQ)Table 2 Linear ranges,correlation coefficients(r2),LODs and LOQs of 17 parabens
2.7 回收率与相对标准偏差
为验证方法的回收率和稳定性,选择17种目标物均呈阴性的22种水果为样品,添加标准溶液,最终样品中的加标浓度为1倍、2倍和5倍定量下限。按本方法对加标样品进行处理,并于同一日内进行6个平行样品测定(n=6),实验结果见表3。在22种水果中,17种对羟基苯甲酸酯的回收率为70.7%~117%,相对标准偏差(RSD)为1.5%~4.8%。除了个别基质或某一加标水平的结果存在偏差,以基质标准曲线定量,方法的回收率和RSD基本能满足方法学的验证要求,可用于日常实验室的批量测定。

表3 17种对羟基苯甲酸酯的回收率及相对标准偏差(n=6)Table 3 Recoveries and RSDs of 17 parabens(n=6)

(续表3)
2.8 实际样品的测定
为进一步验证方法可行性,随机选取实验室的上述22 种水果样品进行测定,每种水果10 个,共220 个。结果发现,包括1 个荔枝、1 个龙眼、1 个奇异果、1 个猕猴桃和2 个芒果在内的6 个样品中检出对羟基苯甲酸甲酯,含量分别为105、242、169、108、234、845 μg/kg。另外还有1个芒果样品,对羟基苯甲酸甲酯和对羟基苯甲酸乙酯均有检出,含量分别为233、220 μg/kg(如图4)。其余样品均未检出。
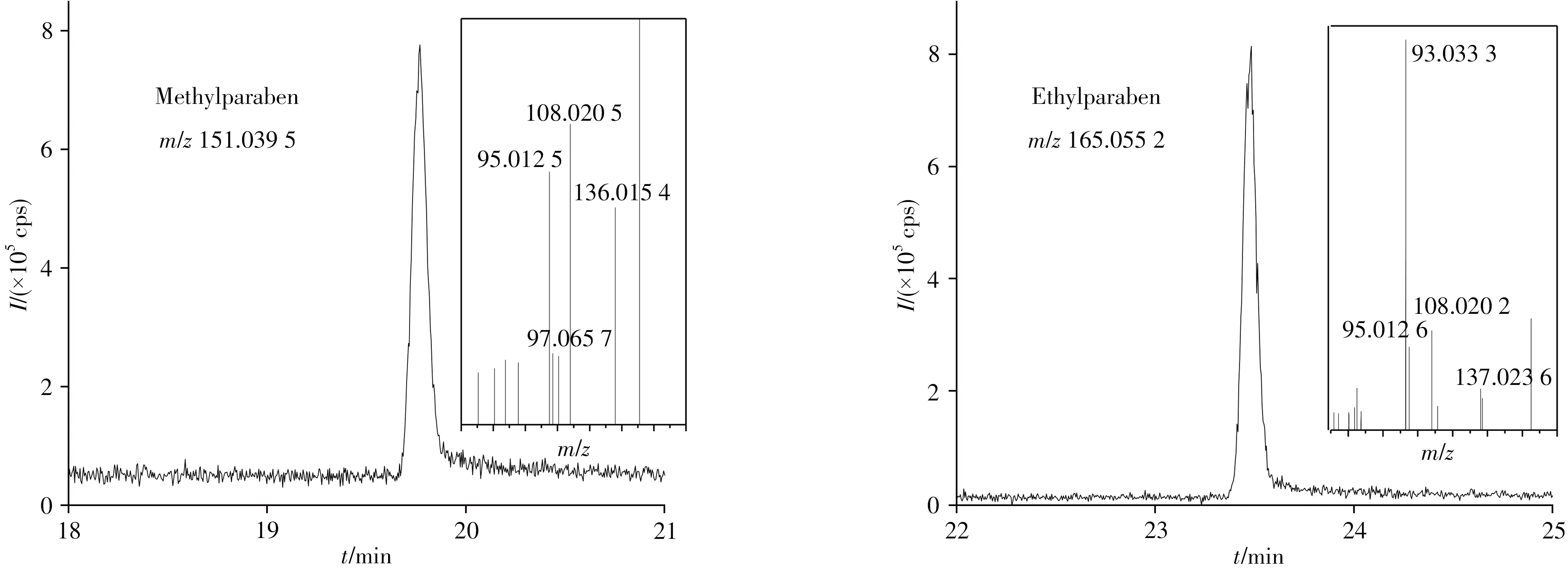
图4 阳性芒果样品中对羟基苯甲酸甲酯和对羟基苯甲酸乙酯的提取离子流图Fig.4 Selected ion chromatograms of methylparaben and ethylparaben in a mango positive sample
3 结 论
本文基于直接溶剂超声提取的方式,对不同水果中的17种对羟基苯甲酸酯进行快速测定;采用基质标准曲线校正结果,回收率满足分析测定要求;使用UPLC-Q-Orbitrap HRMS 进行分析测定,精确测得目标物母离子及子离子的分子量,大大降低了假阳性的可能,并通过碎片分子量推断出目标物的质谱裂解途径;该方法建立了17种对羟基苯甲酸酯的高分辨质谱数据库,可有效实现不同水果中对羟基苯甲酸酯类化合物的快速检测。方法操作简便,灵敏度高,回收率和精密度良好,可为水果中防腐剂的快速检测提供参考。
