2-氨基-5氯苯甲酸甲酯合成
2020-05-23关松健
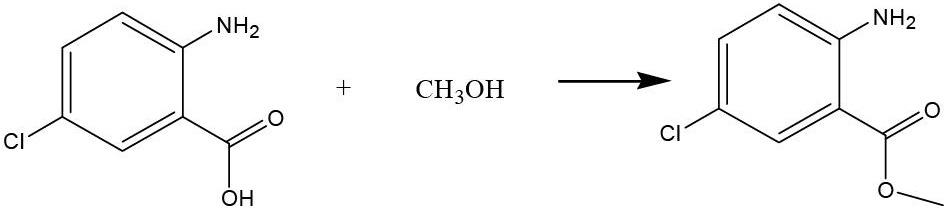

【摘 要】以邻氨基苯甲酸甲酯为原料,以冰醋酸为溶剂,以氯气、氯化氢为氯化剂进行氯化合成2-氨基-5-氯苯甲酸甲酯,本方法简单实用,收率高,经济性好,对环境污染性小,生产成本低,易工业化。在给定反应条件下,收率达到80%,产品经熔点测试,核磁确认结构,产品纯度≥99.5%
【关键词】2-氨基-5-氯苯甲酸甲酯;邻氨基苯甲酸甲酯;合成
2-氨基-5氯苯甲酸甲酯,英文名称:methyl 2-amino-5-chlorobenzoate,CAS:5202-89-1 分子式:C8H8ClNO2 分子量:185.61,熔点:66-68℃,密度:1.311g/cm3,类白至淡黄色结晶,广泛用于医药,染料、农药等中间体的合成。
1.合成路线
2-氨基-5-氯苯甲酸甲酯的主要合成路线主要有:
路线一:以邻氨基-5-氯苯甲酸为原料,与甲醇进行酯化【1,2】
路线二:以5-氯-2-硝基苯甲酸甲酯或5-氯-2-硝基苯甲酸为原料进行硝基还原。【3,4】
或者
路线三:以邻氨基苯甲酸甲酯为原料进行5位氯化
(1)以次氯酸钠或者次氯酸钙为氯化剂【5】
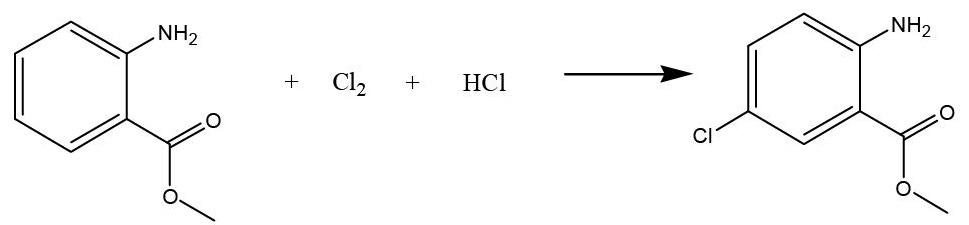
(2)以氯气、氯化氢为氯化剂【6】
本文以邻氨基苯甲酸甲酯为原料,以氯气、氯化氢为氯化剂进行5-位氯化来合成2-氨基-5氯苯甲酸甲酯,并对各反应条件进行试验优化,研究简单实用收率高的合成方法。
2.实验部分
2.1 试剂与仪器
试剂:邻氨基苯甲酸甲酯、冰醋酸、氯气为工业品,氯化氢为实验室自制
仪器:DF- 101集热式恒温加热磁力搅拌器,BILN-W-8007 低温恒温槽
SHB-Ⅲ循环水式多用真空泵,LC-10APL安捷伦液相色谱仪,
(一)实验步骤
邻氨基苯甲酸甲酯50.0g、冰乙酸250g入1000ml反应瓶,降温至15℃,通入自制的干燥氯化氢14.5g,通入氯化氢时控制温度15-20℃,通毕,搅拌20分钟,接着缓慢通氯气28.2g,控制通氯气时温度15-18℃,通毕,搅拌反应30分钟。取样液相,邻氨基苯甲酸甲酯≤5%
反应完毕,加水250g,搅拌,有白色固体析出,过滤,烘干得7.5 g,经核磁确认为2-氨基-3,5-二氯苯甲酸甲酯,液相纯度93.5%
滤液用浓氨水调PH值为4.0-4.5,析出类白至淡黄色结晶,室温搅拌30min,抽滤,水淋洗得产品粗品,液相纯度95.2%
粗品加正己烷200ml打浆3h,抽滤,烘干得类白至淡黄色固体49.1g,经核磁确认为2-氨基-5氯苯甲酸甲酯,液相纯度99.5%,熔点:66-68℃,收率约80%
3.产品表征
采用核磁共振谱图对产品和杂质进行了表征
产品核磁检测结果为:1HNMR(300M,CDCl3):δ(ppm)3.88(s,3H,CH3),5.01(s,2H,NH2),6.72(d,1H,ArH),7.16(d,1H,ArH),7.54(s,1H,ArH)
与标准样谱图进行比对,确认为2-氨基-5-氯苯甲酸甲酯。
杂质核磁检测结果为:1HNMR(300M,CDCl3):δ(ppm)3.88(s,3H,CH3),5.01(s,2H,NH2),7.16(d,1H,ArH),7.54(s,1H,ArH)
确认为2-氨基-3,5-二氯苯甲酸甲酯。
4.结果与讨论
4.1 氯气用量的选择
氯气用量的影响如表1
由于存在副反应,氯气用量1:1时,反应不够完全,而氯气用量增大,副反应产物2-氨基-3,5-二氯苯甲酸甲酯的生成也加大。由表1可见,氯气与邻氨基苯甲酸甲酯摩尔比为1:1.2时产品收率较理想,质量也最好。
4.2 反应时间
反应时间的影响如表2
随着反应时间的延长,2-氨基-3,5-二氯苯甲酸甲酯的生成量也加大,造成产品收率下降,质量变差。经实验监测,我们选择最优反应时间为30min。
4.3 反应温度
反应温度的影响如表3
我们分别实验了15℃,25℃,35℃,确定了邻氨基苯甲酸甲酯5-位氯化的最佳反应温度为15℃。
5.结论
本研究以邻氨基苯甲酸甲酯为原料,以冰醋酸为溶剂,以氯气、氯化氢为氯化剂进行氯化合成2-氨基-5氯苯甲酸甲酯,经过对各反应条件进行优化,收率达到80%,液相纯度99.5%以上,成本经济可行,适合工业化,对环境污染性小。
参考文献:
[1]Chen,Li;Feng,Lichun;Huang,Mengwei;Liu,Yongfu;Wu,Guolong;Wu,Jim Zhen;Zhou,Mingwei,Novel 3,3-dimethyl tetrahydroquinoline derivatives,Patent:US2011/257151A1,2011-10-20
[2]BARE THOMAS M [US];SPARKS RICHARD B[US]+,Pyridazinedione compounds useful in treating neurological disorders,Patent:US5599814A1,1997-02-04
[3]REDDY BANDI PARTHASARADHI[IN];REDDY KURA RATHNAKAR[IN];REDDY DASARI MURALIDHARA[IN];REDDY MARUTHI JANAKIRAM [IN];KRISHNA BANDI VAMSI [IN];HETERO RESEARCH FOUNDATION[IN]+,PROCESS FOR PREPARING TOLVAPTAN INTERMEDIATES,Patent:US2013/190490A1,2013-07-25
[4]HETERO RESEARCH FOUNDATION;PARTHASARADHI REDDY,Bandi;RATHNAKAR REDDY,Kura;MURALIDHARA REDDY,Dasari;JANAKIRAM REDDY,Maruthi;VAMSI KRISHNA,Bandi,PROCESS FOR PREPARING TOLVAPTAN INTERMEDIATES,Patent:WO2012/46244A1,2012-04-12
[5]Okabe;Sun Tetrahedron,1995,vol.51,# 7 p.1861 - 1866
[6]Freundler Comptes Rendus Hebdomadaires des Seances de l'Academie des Sciences,1910,vol.150,p.1179
[7]Pokhodylo,Nazariy T.;Matiychuk,Vasyl S. Journal of Heterocyclic Chemistry,2010,vol.47,# 2 p.415 - 420
[8]MERCK PATENT GMBH Patent:WO2006/122631 A1,2006
[9]Takeda Chemical Industries,Ltd. Patent:US5128356 A1,1992
[10]徐鳳波,张奉志,董建兰,金艳娟,一种2-氨基-5-氯苯甲酰胺的制备方法,[P]:CN101575301A,2009
作者简介:
关松健,女,从事有机合成研究,化工工程师,河北亚诺生物科技股份有限公司。
(作者单位:河北亚诺生物科技股份有限公司)
