紫甘蓝色素提取工艺优化及其酸碱指示剂性质
2022-06-14白晓菲梁东明张艳红闫心怡韩金龙弭永生
白晓菲,梁东明,张艳红,闫心怡,韩金龙,弭永生*
1. 德州学院生命科学学院(德州 253023);2. 德州市食品药品检验检测中心(德州 253015)
被广泛使用的食用色素分为两大类:人工合成色素和天然色素[1-2]。人工合成色素主要以苯、甲苯和苯胺等化工产品为原料,通过化学合成方法制备,通常色泽艳丽,呈色稳定。然而,伴随物质水平的提高和科学研究的发展,人工合成色素潜在的毒性、致癌和致畸风险越来越受到人们的关注[3-4]。天然色素主要来源于植物组织,某些动物和微生物也是天然色素的来源[5-7]。相对于人工合成色素,天然色素呈色自然,作为食用色素,其安全性可靠,并且具有一定的营养价值和药理保健功能[8-9]。近年来,人们对天然色素的需求逐渐增长,天然色素被广泛应用于医药、日化、纺织等行业[10-12]。花色苷是一类重要的天然色素物质,又称花青素,广泛存在于被子植物的花、果、叶、茎和根的细胞液中,受环境酸度和温度等因素的影响,能够呈现出红、紫、蓝等不同颜色。在生物体系中,花色苷具有吸收紫外光的功能,能够保护细胞分化等生命过程的正常进行。在生物医用方面,花色苷能够预防冠心病和心肌缺损,延缓癌细胞的生长[13-15],具有抗菌、抗炎和抗衰老等重要生理功能[16-18]。
紫甘蓝色素属于花色苷,是一种重要的水溶性天然色素,具有色调柔和、着色力强、安全性高的特点,对酸碱变化敏感,颜色变化明显,变色范围广[19-21]。另外,紫甘蓝色素还具有抑菌消炎、清除氧自由基、提高视觉灵敏度等生理功能[22-23]。紫甘蓝作为一种常见蔬菜,属于十字花科芸薹属,其生长周期短、产量高、适应性强、价格低、便于运输和贮藏,是提取花色苷天然色素的理想原料。国内外有关紫甘蓝色素的研究还不够系统,色素提取方法存在操作方法复杂、大规模生产成本高等问题,对于紫甘蓝色素的应用研究也难以实际转化。以市售新鲜紫甘蓝作为原料,设计单因素试验和正交试验优化紫甘蓝色素的水浴法提取工艺,具有操作简单易行的优势,便于实现天然色素的大规模提取,所提取天然色素经AB-8大孔吸附树脂纯化后,研究在不同酸碱性条件下的变色性能,开发在普通实验室能够应用的pH试纸,探索其作为酸碱滴定用指示剂的可行性。
1 材料与方法
1.1 材料与仪器
新鲜紫甘蓝(市售,使用前清洗干净);无水乙醇、盐酸、氢氧化钠(均为国产分析纯)。
FA224C分析天平(湖南力辰仪器科技有限公司);YP-B电子台秤(上海力辰仪器科技有限公司);HH-1恒温水浴锅(菏泽鑫源实验仪器设备有限公司);SHZ-D(III)循环水多用真空泵(上海力辰仪器科技有限公司);UV-5500紫外-可见分光光度计(上海元析仪器有限公司);Hei-Vap Value HL G3旋转蒸发仪(德国Heidolph公司);TDL-60B离心机(山东爱博科技贸易有限公司);DHG-9070A电热鼓风干燥箱(上海一恒科学仪器有限公司);PHS-3C酸度计(上海仪电科学);M150B粉碎机(浙江天喜网络科技有限公司)。
1.2 试验方法
1.2.1 紫甘蓝预处理
新鲜紫甘蓝切碎,在60 ℃电热鼓风干燥箱中干燥至恒重,转入粉碎机中粉碎,得紫甘蓝粉末,干燥避光条件下保存备用。
1.2.2 紫甘蓝色素提取单因素试验
通过测定紫甘蓝色素提取液的吸光度,考察不同条件下的提取效率。紫甘蓝色素在525 nm处有明显的特征吸收峰,其吸收强度随色素溶液pH变化,不同提取条件下的色素提取液需调整至相同pH后再测定其在525 nm处的吸光度,以免影响测定结果。分别考察提取剂pH、乙醇体积分数、提取时间和提取温度4个因素对紫甘蓝色素提取效率的影响。
1.2.2.1 提取剂pH对紫甘蓝色素提取的影响
分别称取5份0.5 g的紫甘蓝粉末放入小烧杯中,编号;以体积分数20%、pH分别为1,2,3,4和5的乙醇溶液作为提取剂,按料液比1∶20 g/mL加入到小烧杯中,在50 ℃下水浴提取1 h;浸提后立即离心,吸取上清液,用pH 2的缓冲溶液将上清液稀释10倍(取5 mL上清液到50 mL容量瓶中定容);测定稀释后的提取液在波长525 nm处的吸光度,选取最佳提取条件的pH。
1.2.2.2 乙醇体积分数对紫甘蓝色素提取的影响
分别称取8份0.5 g的紫甘蓝粉末放入小烧杯中,编号;以pH 1、体积分数分别为10%,15%,20%,25%,30%,35%,40%和45%的乙醇溶液作为提取剂,按照料液比1∶20 g/mL加入到小烧杯中,在50 ℃下水浴提取1 h;浸提后立即离心,吸取上清液,用pH 2的缓冲溶液将上清液稀释10倍(取5 mL上清液到50 mL容量瓶中定容);测定稀释后的提取液在波长525 nm处的吸光度,选取最佳提取条件的乙醇体积分数。
1.2.2.3 提取时间对紫甘蓝色素提取的影响
分别称取6份0.5 g的紫甘蓝粉末放入小烧杯中,编号;以pH 1、体积分数30%的乙醇溶液作为提取剂,按照料液比1∶20 g/mL加入到小烧杯中,分别在50 ℃下水浴提取不同时间(10,30,60,90,120和180 min);浸提后立即离心,吸取上清液,用pH 2的缓冲溶液将上清液稀释10倍(取5 mL上清液到50 mL容量瓶中定容);测定稀释后的提取液在波长525 nm处的吸光度,选取最佳提取条件的提取时间。
1.2.2.4 提取温度对紫甘蓝色素提取的影响
分别称取6份0.5 g的紫甘蓝粉末放入小烧杯中,编号;以pH 1、体积分数30%的乙醇溶液作为提取剂,按照料液比1∶20 g/mL加入到烧杯中,分别在不同温度(25,35,45,55,65和75 ℃)下水浴提取2 h;浸提后立即离心,吸取上清液,用pH 2的缓冲溶液将上清液稀释10倍(取5 mL上清液到50 mL容量瓶中定容);测定稀释后的提取液在波长525 nm处的吸光度,选取最佳提取条件的提取温度。
1.2.3 正交试验
在单因素试验基础上,设计四因素三水平的正交试验,以紫甘蓝色素的吸光度为指标,对提取剂pH、乙醇体积分数、提取温度、提取时间4个因素进行优选,各因素水平如表1所示,紫甘蓝粉末均为0.5 g,料液比均为1∶20 g/mL。

表1 正交试验因素水平
1.2.4 紫甘蓝色素的酸碱变色性质探究及pH试纸的制备
1.2.4.1 紫甘蓝色素在不同pH溶液中的颜色变化
用氢氧化钠溶液和稀盐酸溶液分别配制pH 1,3,5,6,7,8,10,12和14的溶液,分别取2 mL不同pH的溶液于试管中,向其中加入等量的紫甘蓝色素提取液,摇匀,观察溶液颜色变化。
1.2.4.2 紫甘蓝色素制备pH试纸
将滤纸剪成相等大小的滤纸条,放在浓缩后的紫甘蓝色素提取液中,充分浸泡,晾干,至色素在滤纸条上着色显著,制得紫甘蓝pH试纸,在紫甘蓝pH试纸上滴加不同pH的溶液,观察试纸颜色变化。
1.2.5 紫甘蓝色素作为指示剂在酸碱滴定中的应用
1.2.5.1 强碱滴定强酸
移取25.00 mL待测盐酸溶液于锥形瓶中,加入2~3滴浓缩后的紫甘蓝色素提取液作为指示剂,摇匀,此时溶液呈红色,用0.100 mol/L氢氧化钠溶液进行滴定,记录终点时消耗0.100 mol/L氢氧化钠溶液的体积,计算被测盐酸溶液浓度,使用酚酞作为指示剂进行滴定试验,将使用2种指示剂的测定结果进行对比。
1.2.5.2 强酸滴定强碱
移取25.00 mL待测氢氧化钠溶液于锥形瓶中,加入2~3滴浓缩后的紫甘蓝色素提取液作为指示剂,摇匀,此时溶液呈黄绿色,用0.100 mol/L盐酸溶液进行滴定,记录终点时消耗0.100 mol/L盐酸溶液的体积,计算被测氢氧化钠溶液浓度,使用酚酞作为指示剂进行滴定试验,将使用2种指示剂的测定结果进行对比。
1.3 数据处理
试验均为3次平行,试验结果用平均值±标准差表示,使用Excel 2010、Origin 8.0、SPSS 24.0等软件对试验数据进行处理和分析。
2 结果与分析
2.1 单因素试验结果与分析
2.1.1 提取剂pH对紫甘蓝色素提取的影响
如图1所示,在其他提取条件固定的情况下,考察提取剂pH对紫甘蓝色素提取的影响。提取液pH 1时,提取紫甘蓝色素效率最高,pH 2~4时,曲线变化较为平稳,提取效率变化不明显,pH大于4时,提取效率明显下降,因此,初步最佳提取条件的pH为1。
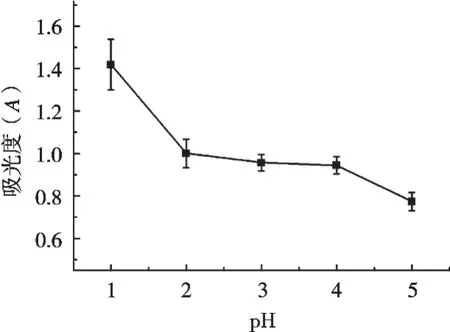
图1 提取剂pH对紫甘蓝色素提取的影响
2.1.2 乙醇体积分数对紫甘蓝色素提取的影响
如图2所示,在其他提取条件固定的情况下,考察乙醇体积分数对紫甘蓝色素提取的影响。乙醇体积分数10%~30%时,随着乙醇体积分数增加,提取率逐渐提高,乙醇体积分数30%时,紫甘蓝色素提取率最高,乙醇体积分数大于30%时,随着乙醇体积分数增加,提取率逐渐降低,因此,初步选择乙醇体积分数30%作为最佳条件,在此条件下,可尽量减少乙醇使用量,降低提取成本,同时保证较高的提取效果。
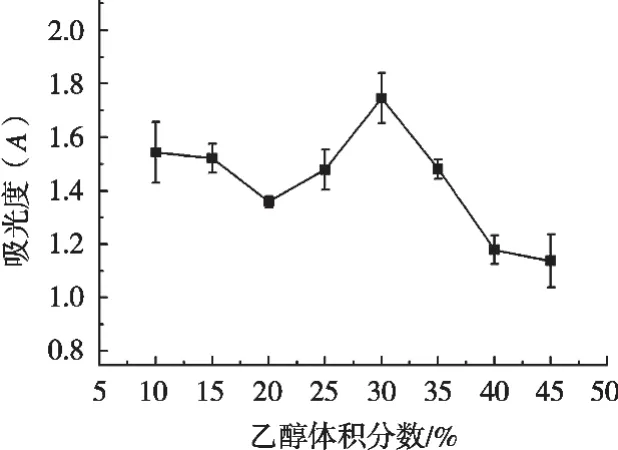
图2 乙醇体积分数对紫甘蓝色素提取的影响
2.1.3 提取时间对紫甘蓝色素提取的影响
如图3所示,在其他提取条件固定的情况下,考察不同提取时间对紫甘蓝色素提取效率的影响。随着提取时间延长,紫甘蓝色素的提取效率逐渐升高,说明延长时间能够提高溶剂浸提效果,提取时间达到120 min时,提取效率最高,超过120 min后,随着提取时间延长,提取效率有所降低,可能原因是长时间的热处理使紫甘蓝色素略有分解,因此,初步选择120 min为最佳提取时间。
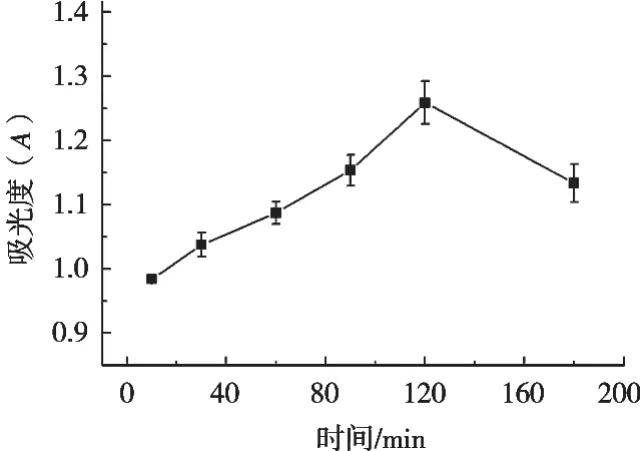
图3 提取时间对紫甘蓝色素提取的影响
2.1.4 提取温度对紫甘蓝色素提取的影响
如图4所示,在其他提取条件固定的情况下,考察不同提取温度对紫甘蓝色素提取效果的影响。提取温度在25~35 ℃时,紫甘蓝色素的提取效率几乎不变,在提取温度35~55 ℃时,随着温度升高,提取效率逐渐升高,说明提高提取温度有利于紫甘蓝色素的溶出,提取温度达到55 ℃时,提取效率最高,在提取温度55~75 ℃范围时,提取效率略有下降,可能原因是提取温度过高,导致少量紫甘蓝色素降解,同时,温度过高也不利于降低生产成本,因此,初步选择55 ℃为最佳提取温度。
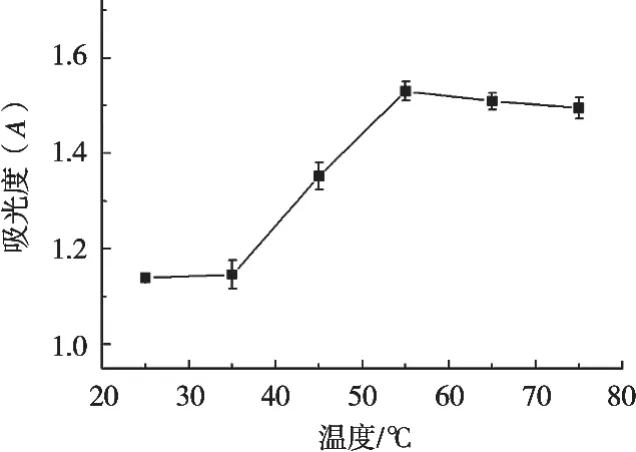
图4 提取温度对紫甘蓝色素提取的影响
2.2 正交试验结果与分析
提取工艺优化的正交试验结果如表2所示。由极差分析结果可以看出,影响紫甘蓝色素提取效果的因素主次顺序依次为提取剂pH>提取时间>乙醇体积分数>提取温度,即提取剂pH是最主要的影响因素,提取时间和乙醇体积分数是次要因素,提取温度的影响最不明显。根据正交试验分析得出的最佳组合是A1B2C2D1,即提取剂pH 1、乙醇体积分数30%、提取时间120 min(2 h)、提取温度45 ℃。
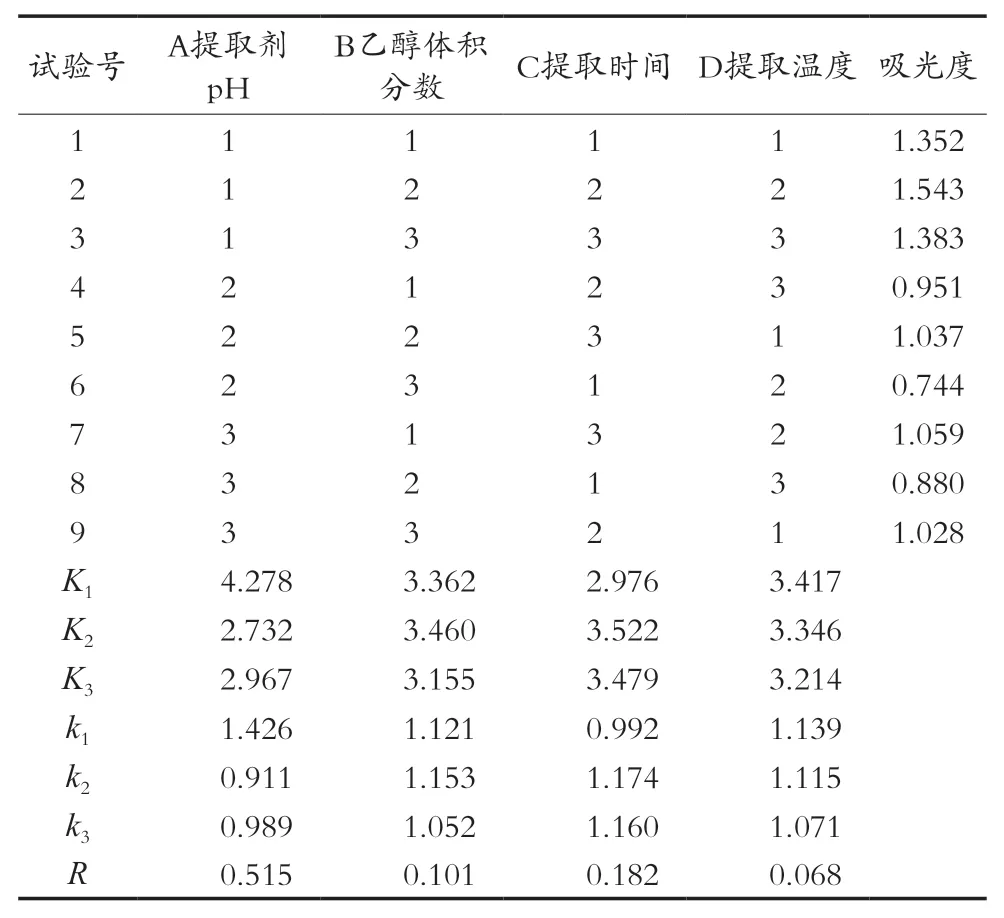
表2 正交试验设计及结果
2.3 紫甘蓝色素变色性质探究试验结果与分析
2.3.1 紫甘蓝色素在不同pH溶液中的显色情况
如表3和图5所示,将等量紫甘蓝色素加入到不同pH的溶液中时,溶液会呈现不同颜色,不同pH之间颜色区分明显,基于此,紫甘蓝色素可开发作为优良的酸碱指示剂。
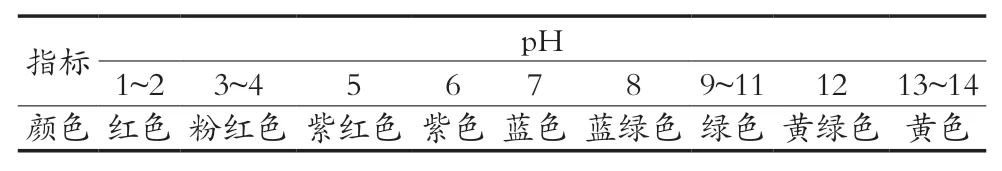
表3 紫甘蓝色素在不同pH溶液中的显色情况

图5 紫甘蓝色素在不同pH溶液中颜色变化
2.3.2 紫甘蓝色素pH试纸的制备
如图6所示,通过浸泡法制备紫甘蓝色素pH试纸,在试纸上分别滴加pH 1,2,5,7,10,11,12,13和14的水溶液,立即观察试纸变色情况,在不同pH条件下,试纸显色变化明显,与表3结果基本一致,说明所制备的紫甘蓝色素pH试纸有实际应用价值。
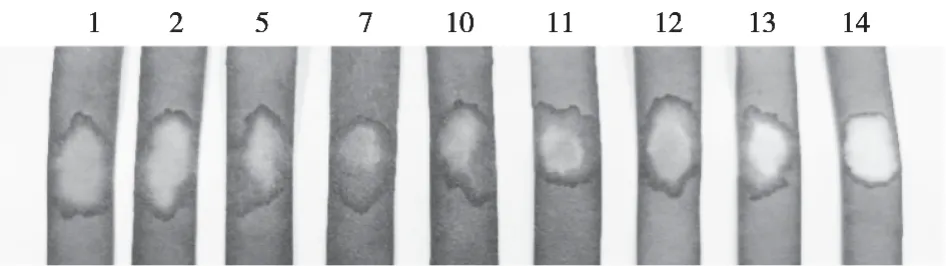
图6 紫甘蓝色素pH试纸变色结果
2.4 紫甘蓝色素作为指示剂在酸碱滴定中的应用效果
2.4.1 强碱滴定强酸
滴定终点判定方法:采用紫甘蓝色素作为指示剂时,滴定终点为滴至溶液变蓝色且半分钟内不变色;采用酚酞作为指示剂时,滴定终点为滴至溶液变红色且半分钟内不变色。如表4所示,以紫甘蓝色素作为指示剂时所测得盐酸浓度略低于以酚酞作为指示剂时测得的结果,分析原因可能是紫甘蓝色素指示剂的滴定终点约pH 7,而酚酞指示剂的滴定终点在pH 8~10,因此,采用紫甘蓝色素作为指示剂时消耗的氢氧化钠溶液体积相对较小,测得盐酸浓度也相应较小。

表4 氢氧化钠溶液滴定盐酸溶液测定结果
2.4.2 强酸滴定强碱
滴定终点判定方法:采用紫甘蓝色素作为指示剂时,滴定终点为滴至溶液变蓝色且半分钟内不变色;采用酚酞作为指示剂时,滴定终点为滴至溶液变无色且半分钟内不变色。如表5所示,以紫甘蓝色素作为指示剂时所测得氢氧化钠浓度略高于以酚酞作为指示剂时测得的结果,分析原因与碱滴定酸时类似,紫甘蓝色素作为指示剂时滴定终点约pH 7,而酚酞约pH 8~10。因此,采用紫甘蓝作为指示剂时消耗的盐酸体积相对较大,测得氢氧化钠浓度也相应较大。

表5 盐酸溶液滴定氢氧化钠溶液测定结果
3 结论
以紫甘蓝为原料,采用简便易行的水浴提取法提取紫甘蓝色素,在单因素试验基础上,进一步通过正交试验优化天然色素提取工艺,实验室中最佳提取条件为含30%乙醇溶剂体系、pH 1、温度45 ℃、时间2 h,提取方法具有生产成本低、操作简单的特点。对色素进行纯化后,进一步研究紫甘蓝色素的酸碱变色性质,研究表明紫甘蓝色素对酸碱环境敏感,在pH 1~14的宽范围内具有明显颜色变化,不同pH下的显色区分度高,成功制备紫甘蓝色素pH试纸用于溶液检测,并将紫甘蓝色素应用于酸碱滴定试验中,测试结果与传统酚酞指示剂相当。紫甘蓝色素作为一种优良的水溶性天然色素,在食品、保健和医药等领域展现潜在应用价值,研究其提取方法和性质具有重要参考价值。
