血液透析患者发生导管相关性血栓的危险因素
2022-06-08喻露卢亚飞章莉谭富媛
喻露 卢亚飞 章莉 谭富媛

[摘要] 目的 探讨血液透析患者发生导管相关性血栓(CRT)形成的危险因素,并提出相应对策。 方法 回顾性分析2017年1月至2020年12月在浙江省中西医结合医院行中心静脉置管(CVC)的412例血液透析患者的临床资料,根据彩超诊断结果,将其分为CRT组(n=103)和非CRT组(n=309);比较两组患者的性別、年龄、静脉血栓史、近期手术史、糖尿病、心脑血管疾病、肥胖、感染、生活自理能力障碍、置入静脉、穿刺方法、导管材料、置管前D-二聚体、APTT、使用抗凝药物、血栓传统预防等因素分布;再采用逐步logistic回归法筛选血液透析患者发生CRT的相关危险因素。 结果 血液透析患者CRT发生率为25.00%(103/412)。多因素结果显示,影响血液透析患者发生CRT的危险因素包括静脉血栓史(OR=3.732)、近期手术史(OR=2.869)、糖尿病(OR=3.600)、感染(OR=5.960)、生活自理能力障碍(OR=6.780)、传统穿刺法(OR=3.699)、置管前D-二聚体水平升高(OR=4.246)、无传统预防(OR=4.491)等。 结论 血液透析患者具有较高的CRT发生率,且多数是无症状性CRT患者;根据以上高危因素,进行早预防、早筛查、早诊断、早治疗CRT,可降低血液透析患者的CRT发生率,改善患者的预后。
[关键词] 血液透析;中心静脉导管;导管相关性血栓;危险因素;预防和控制
[中图分类号] R722.1 [文献标识码] B [文章编号] 1673-9701(2022)10-0099-04
[Abstract] Objective To explore the risk factors of catheter-related thrombosis (CRT) in hemodialysis patients, and put forward corresponding countermeasures. Methods The clinical data of 412 hemodialysis patients who underwent central venous catheterization(CVC) in Zhejiang Hospital of Integrated Traditional Chinese and Western Medicine from January 2017 to December 2020 were analyzed retrospectively. According to the results of color Doppler ultrasound diagnosis,they were divided into CRT group (n=103) and non-CRT group (n=309). The distribution of factors such as gender,age,history of venous thrombosis,recent operation history, diabetes mellitus,cardiovascular and cerebrovascular diseases,obesity,infection, disability of self-care ability,vein insertion,puncture method, catheter material,D-dimer before catheter insertion,APTT,use of anticoagulants and traditional prevention of thrombosis were compared between the two groups.Then stepwise Logistic regression was used to screen the risk factors of CRT in hemodialysis patients. Results The incidence of CRT in hemodialysis patients was 25.00%(103/412). The multivariate results showed that the risk factors of CRT in hemodialysis patients included venous thrombosis history(OR=3.732), recent operation history (OR=2.869),diabetes mellitus(OR=3.600),infection(OR=5.960),self-care disability (OR=6.780), and traditional puncture method(OR=3.699), elevated level of D-dimer before catheterization(OR=4.246),no traditional prevention(OR=4.491),etc. Conclusion Hemodialysis patients have a high incidence of CRT, and most of them are asymptomatic CRT patients. According to the above high-risk factors, early prevention, screening, diagnosis and treatment of CRT can reduce the incidence of CRT in hemodialysis patients and improve their prognosis.EF23B80C-863B-4283-8799-86D87399ABB5
[Key words] Hemodialysis; Central venous catheter; Catheter-associated thrombosis; Risk factors; Prevention and control
血液透析是终末期肾病患者进行肾脏替代治疗的重要手段,由于血液透析患者需要长期透析治疗,建立有效的、安全的静脉通道显得尤为必要,经中心静脉导管(central venous catheter,CVC)具有操作简便、避免反复穿刺、留置时间长、减少药物对皮肤血管刺激等优点[1],已广泛应用于血液透析、输血、输液治疗、肠外营养等[2]。然而,CVC也容易引起导管相关性感染、导管相关性血栓(catheter related,CRT)、导管堵塞、导管脱落等并发症,其中CRT被公认为CVC置管患者最为严重的并发症之一,增加导管非计划拔管率,溶栓治疗会增加血液透析患者出血的风险[3],而血栓脱落可导致大面积血栓或肺栓塞[4],危害患者的生命安全。因此,本研究对412例CVC置管的血液透析患者进行回顾性调查,分析CRT的发生率及其相关影响因素,探讨早期预防和治疗CRT的对策,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年1月至2020年12月浙江省中西医结合医院血透室收治的412例血液透析患者进行回顾性调查,纳入标准[3]:①均为血液透析患者;②均进行CVC置管(带涤纶套中心静脉长期导管),且置管时间≥1个月;③接受彩色超声筛查CRT;④临床资料较为完整。排除标准[3]:①年龄<18岁有生活自理能力障碍;②CVC置管时间<1个月生活自理能力障碍;③合并血液系统疾病、凝血功能障碍者;④未在医院内接受血液透析者。本回顾性调查研究得到医院医学伦理学委员会批准。412例CVC置管血透患者中,男239例,女173例;年龄30~85岁,平均(57.36±9.40)岁;糖尿病82例,心脑血管疾病181例,肥胖172例;依据血液透析患者是否发生CRT,将其分为CRT组103例与非CRT组309例。
1.2 方法
于CVC置管1周后、1个月后、拔管前分别进行IE33彩色多普勒超声诊断,若期间发生置管部位疼痛、红斑、肢体肿胀、胸闷胸痛等现象,应立即进行彩超检查。CRT诊断标准[5]:四肢静脉管腔没有被完全压扁,管腔内可探及低回声或中低回声,而受累静脉腔内无明显血流信号或仅能够探及到部分血流信号,脉冲多普勒显示的血流频谱以孤立型为主,不随呼吸变化而变化。查阅所有患者的病历资料,回顾性收集如下资料:性别、年龄、静脉血栓史、近期手术史、糖尿病、心脑血管疾病、身高、体重、感染、生活自理能力障碍、置入静脉、穿刺方法、导管材料、置管前D-二聚体、活化部分凝血活酶時间(activated partial thromboplastin time,APTT,<25 s)缩短、使用抗凝药物、血栓传统预防(弹力袜、间歇性充气加压装置、电刺激仪等)、超声诊断结果等。
1.3 统计学方法
使用SPSS 21.0统计学软件进行数据分析,单因素分析采用χ2检验,多因素分析则采用逐步logistic回归法;P<0.05为差异有统计学意义。
2 结果
2.1 影响血液透析患者发生CRT的单因素分析
对412例CVC置管的血液透析患者进行回顾性调查,经超声检查确诊有CRT的患者103例,发生率为25.00%(103/412)。单因素分析比较结果显示,两组间年龄、静脉血栓史、近期手术史、糖尿病、心脑血管疾病、感染、生活自理能力障碍、置入静脉、穿刺方法、导管材料、置管前D-二聚体、APTT低、使用抗凝药物、血栓传统预防等因素比较差异有统计学意义(P<0.05),而两组间性别、肥胖等因素比较,差异无统计学意义(P>0.05)。见表1。
2.2 影响血液透析患者发生CRT的多因素分析
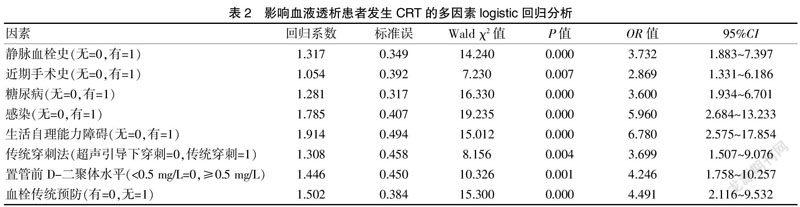
以血液透析患者是否发生CRT为因变量(非CRT组=0,CRT组=1),把单因素筛选有意义的14个因素作为自变量,进行多因素逐步回归logistic分析。影响血液透析患者发生CRT的危险因素包括静脉血栓史、近期手术史、糖尿病、感染、生活自理能力障碍、传统穿刺法、置管前D-二聚体水平升高、无血栓传统预防等。见表2。
3 讨论
3.1 血液透析患者CRT发生率及其危险因素分析
412例CVC置管的血液透析患者CRT发生率为25.00%,在张巧根等[6-7]报道的血液透析患者CRT发生率20%~70%范围内,这说明血液透析患者的CRT发生率较高,尤其是无症状性CRT,应引起临床医生对CRT的重视。
危险因素结果显示,①静脉血栓史:静脉血栓10年内的复发率高达30%~50%[8],这可能是由于此类患者存在一定程度的纤溶系统、凝血-抗凝功能障碍,而置管易引起血管内皮细胞损伤,激活凝血系统和抑制纤溶系统[9],从而引起CRT的发生。②近期手术史:手术引起CRT的原因较多,如损伤血管、破坏血管壁、操作压迫血管、抗凝或纤溶系统异常、应激性反应等[10],肺栓塞、血栓已成为手术后的一个重要并发症,一旦发生,若抢救不及时,患者死亡风险较高。③糖尿病:透析患者若合并糖尿病,其血管内皮细胞易受到损伤、血小板活性较强、血黏度增加,引起微循环瘀滞、局部组织缺氧等[11],这些均会加速患者血栓的形成。④感染:该因素是MHC患者发生CRT的重要危险因素,手术、置管、化疗、放疗等使得患者感染率增加,感染所引起的机体炎症反应,这会激活机体凝血系统、降低纤溶系统的活性[12],一定程度上直接或间接导致CRT的发生。⑤生活自理能力障碍:患者若存在生活自理能力障碍,一般需要长期卧床或静坐,其活动量明显减少,可引起患者肢体肌力下降、血流速度缓慢,激活内源性的凝血系统,促使血小板聚集[13-14],这会增加下肢深静脉血栓的发生风险。⑥传统穿刺法:这可能与进针送管前需要把套管针芯抽离,而导管质软不容易固定,这会引起导管移位并且损伤皮下组织[15],从而导致CRT的形成。⑦置管前D-二聚体水平升高:正常的凝血系统和纤溶系统处于动态平衡,D-二聚体是纤溶系统中的纤维蛋白降解物,可作为血液高凝状态的分子标志物[16],当平衡失调后,D-二聚体水平升高,在凝血酶的一系列作用下形成CRT[17]。⑧无传统预防:未采取传统预防措施如弹力袜、间歇性充气加压装置、电刺激仪等,CRT发生的风险系数高达4.49,抗凝药物过量使用容易引起出血,而传统物理疗法可减轻血液瘀滞、加快静脉血流回流速度、促进血液循环等[18],预防血栓发生。EF23B80C-863B-4283-8799-86D87399ABB5
3.2 血液透析置管患者预防CRT的对策分析
①做好CRT高危因素筛查和彩超检查:置管前应进行静脉血栓史、近期手术史、糖尿病、生活自理能力障碍、D-二聚体、血小板、纤维蛋白原等高危因素筛查,评估置管患者的CRT易感性,以便定期进行彩超筛查和诊断CRT,也便于早期采取预防措施。②加强CVC置管操作和管理:严格实施CVC穿刺操作人员准入制度,掌握CVC置管的适应证和禁忌证,操作由经验丰富和技术娴熟的人员来完成;尽量选择颈内静脉进行置管,实行无菌置管操作;定期对导管进行维护管理,减少导管相关性感染、脱落、移动等并发症。③药物预防:目前对于预防性使用抗凝药物的结论争议较大,对于有较多危险因素的高危患者,预防性使用抗凝剂是一种较为合理的选择,但西方国家对置管患者不强调预防性使用抗凝剂[19],而建议加强肢体功能锻炼,定期彩超检查来达到预防和及时治疗CRT的目的。④物理预防:由于预防性使用抗凝药物容易给患者带来出血风险,空气波压力治疗、穿弹力袜、间歇性充气加压装置、电刺激仪等传统物理疗法可促进血液循环[20-22],预防CRT的形成。⑤加强健康教育:MHC患者置管后应进行健康教育,提高患者对导管的自我管理能力[23-24];嘱咐患者适当活动置管侧肢体,避免该肢体过度上举、外展、提重、长时间压迫等,避免导管脱落、移动、非计划性拔管等;若出现疼痛、红肿、酸胀、胸闷胸痛等,应及时报告医生。
[参考文献]
[1] 郭晓明,熊飞.中心静脉导管封管液渗漏原因及对凝血功能影响的研究进展[J].临床肾脏病杂志,2018,18(3):188-190.
[2] 羅杏英,李佩球,肖菲娜,等.血液透析中心静脉导管相关性血流感染患者医院感染特点及影响因素[J].中华医院感染学杂志,2019,29(22):3431-3434.
[3] 李明霞,向秋芬,符琰,等.经外周静脉置入中心静脉导管相关性静脉血栓防治体系的构建与应用[J].广西医学,2020,42(6):776-778,785.
[4] 应丽,朱云霞.肿瘤患者PICC相关性上肢深静脉血栓影响因素研究进展[J].重庆医学,2017,46(9):1283-1285.
[5] 侯玉芬,刘政.下肢深静脉血栓形成诊断及疗效标准(2015年修订稿)[J].中国中西医结合外科杂志,2016,22(5):520-521.
[6] 张巧根.血液透析患者中心静脉导管血栓形成的相关因素分析[J].泰州职业技术学院学报,2017,17(2):62-64.
[7] 李颂婷,洪银钗.血液透析尿毒症患者中心静脉导管感染的高危因素及细菌分布特点[J].现代实用医学,2018, 30(6):812-813.
[8] 王沙沙,马志芳,龙玲玲,等.分隔膜无针密闭式输液接头在血液透析中心静脉导管中的应用及临床观察[J].中国血液净化,2019,18(11):780-782.
[9] 王俭苗,赵锐祎,刘震杰,等.经外周静脉置入中心静脉导管相关性血栓的危险因素及预防策略进展[J].中华血管外科杂志,2018,3(4):258-260,封3.
[10] 梁涛,黄艳秋.血液透析患者中心静脉导管相关性感染的影响因素分析[J].广西医科大学学报,2019,36(8):1292-1295.
[11] 郝传明,张敏.糖尿病肾病的防治策略—三级预防一体化治疗[J].中国实用内科杂志,2017,37(3):195-198.
[12] 郭晓燕,冯晓楠,王革,等.血液透析患者中心静脉临时导管感染危险因素分析[J].宁夏医学杂志,2018,40(3):280-282.
[13] 张东亮.基于抗组织纤维化的慢性肾脏病治疗新进展[J].首都医科大学学报,2015,36(3):333-337.
[14] 覃燕,高文,韦义萍,等.血液透析患者发生中心静脉导管相关性深静脉血栓的危险因素[J].广西医学,2018, 40(13):1410-1413.
[15] 阳新星.不同穿刺方法对血液透析患者动静脉内瘘并发症的影响分析[J].中国现代药物应用,2020,14(8):202-203.
[16] 白红晓,邓群,罗景怡.D-二聚体和C-反应蛋白预测肿瘤患者静脉血栓栓塞症复发的价值[J].中华航海医学与高气压医学杂志,2019,26(3):251-254.
[17] 杨敏,谢俊英,谭培昭,等.动态监测D-二聚体在肿瘤患者导管相关性血栓的临床意义[J].实用肿瘤学杂志,2019,33(5):425-430.
[18] 昌晓,李力,金婷.血液肿瘤儿童导管相关性血栓预防和治疗研究现状[J].数理医药学杂志,2018,31(12):1853-1854.
[19] 孙淑芬,蓝志明,王建,等.桃红四物汤结合物理疗法预防人工全髋关节置换术后下肢深静脉血栓的临床观察[J].广州中医药大学学报,2019,36(6):805-809.
[20] 胡英芳,郭晓玲.物理干预在预防血液肿瘤患者中心静脉置管相关性血栓中的应用[J].重庆医学,2017,46(13):1867-1868.
[21] 关毅标,黄胜,李丽波,等.尿毒症患者应用高通量血液透析与常规血液透析两种治疗方案的效果[J].中国医药科学,2021,11(15):193-196.
[22] 汪启龙.血液透析治疗尿毒症并发症的疗效探讨[J].中国医药科学,2021,11(3):215-217.
[23] 刘伟,肖萍.高通量血液透析治疗老年尿毒症患者钙磷代谢异常的效果[J].中国当代医药,2021,28(22):139-142.
[24] 林芷珊,黄白茹,郑秀玲,等.不同护理干预在无肝素血液透析中的应用效果研究[J].中国医药科学,2020,10(3):131-133.
(收稿日期:2021-10-09)EF23B80C-863B-4283-8799-86D87399ABB5
