CO还原氧化铁实验装置的改进
2022-06-07闫相友
闫相友


摘要: 针对教材实验存在的一些问题,组织学生兴趣小组进行一氧化碳还原氧化铁实验装置的改进探索,有助于学生加深了解一氧化碳的制取、验纯、干燥、收集及排出方法等知识。通过改进可以直观判断装置中的空气是否排尽,并对实验尾气进行检验和回收。改进后的实验药品用量少、效果好、安全性高,既环保又节能,并推广为学生分组实验。
关键词: 一氧化碳还原氧化铁; 装置改进; 实验探究; 学生兴趣小组
文章编号: 1005-6629(2022)05-0068-04
中图分类号: G633.8
文献标识码: B
化学是一门以实验为基础的学科,科学探究是学习化学的重要而有效的方式,科学探究始于问题,问题的解决可以提升学生的学科素养[1]。实验可以培养学生的规范意识和小组合作能力。但目前许多教师在实验教学中以课本设计好的实验为主导,利用准备好的仪器和药品让学生开展实验探究。这与其说是实验探究还不如说是实验验证更为合适,实验的设计和教师的设定很大程度上限制了学生的想象力。如何在实验中进一步挖掘其育人价值,有效落实“三思而后行”与“行后而三思”的实验理念,是每一位化学教师都应认真探讨的问题。笔者认为,在实验教学中应引导学生多提几个为什么,明确提出问题的模式:因为……所以……,我认为怎样处理效果会更好,等等。从方案、药品、装置等角度进行分析,在改进中提升对实验的认知。
鲁教版九年级化学第四单元第一节“常见的金属材料”中设置了“金属矿物及其冶炼”的知识模块,让学生了解常见的金属矿产资源以及在自然界中的存在形式,知道矿产资源不可再生,从而形成保护和合理开采矿产资源的意识。教材中设计了探究“工业炼铁的化学原理”实验,学生通过实验探究了解工业冶炼金属的一般原理和方法,理解氧化反应和还原反应的概念。不同版本的教材中均设计了类似的实验探究,铁矿石通过一系列复杂的化学变化冶炼成铁,充分体现了通过化学变化可以改造和创造物质的化学基本观念[2]。鲁教版课本设置了简单的关于炼铁原理的实验探究,体现了化繁为简的思想以及实验指导化工生产的理念。
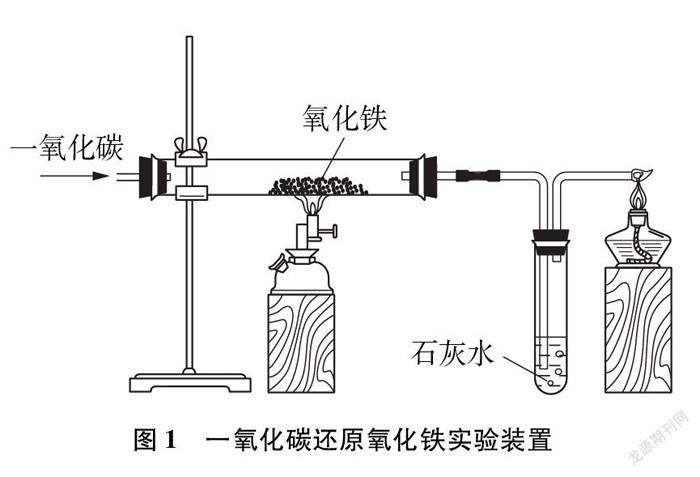
教材采用如图1所示的实验装置[3],旨在模拟工业炼铁的原理,但没有给出整套的实验装置。由于实验中用的一氧化碳气体有毒、不纯会发生爆炸,所以实验前教师一般会采用观看视频或口述的方法对一氧化碳的有关知识和实验注意事项进行反复强调。通过调查发现,由于该实验操作繁琐,危险系数很高等诸多因素,許多教师均采用视频方法代替演示实验,把“做”实验变成“看”实验,剥夺了学生对实验的直观感知,将“多感官”联动的实验教学缩减为一般的视觉认知,大大降低了实验教学的有效性和应有价值。
也有教师为了便于学生记忆实验的先后顺序,采用如图2所示的顺序轴。
并在分析的过程中逐一明确实验中各步骤、各注意事项的原因:
实验前,先检验一氧化碳气体的纯度。
实验开始时,要先通入一氧化碳,再加热。目的是用一氧化碳排净玻璃管中的空气,以免加热时,玻璃管中的一氧化碳和空气的混合气体受热发生爆炸(一氧化碳要“早出晚归”,即先通气,再点灯;先熄灯,再停气)。
实验结束时,要先撤离酒精喷灯,继续通入CO,待玻璃管冷却后,再停止通入一氧化碳,并撤掉酒精灯。目的是防止空气进入,与高温的铁反应(或防止灼热的铁被空气中的氧气氧化)。
尾气处理: 由于CO气体有毒,直接排放到空气中会污染空气,故在装置末端放一个燃着的酒精灯,用于点燃未反应的一氧化碳,防止污染空气(也可用气球收集后再处理,但是气球胀大后压力增大,不利于气体流通)。
石灰水的作用: 检验及吸收二氧化碳气体。
这样的授课方式将实验探究变成了讲实验、背实验,失去了实验教学的魅力。为了最大程度地让学生参与到探究中来,笔者在讲授本节内容前一周,采用“兴趣小组实验探究法”,利用课外活动时间,将教材实验进行逐一探寻。将知识清单发给各个兴趣小组,开展组内讨论,将实验中的问题找出来,进行实验解密。在原理探知、装置改进的过程中加深学生对本实验的认知。通过此环节,授课时多了一些“小老师”,变老师讲为学生分享,提高了学生的积极性和表达能力。
1 一氧化碳的制取和储存
教材中的装置(见图1)只是展示了反应及尾气处理装置,没有明确CO的来源,很多学校的条件也难以储备一氧化碳。学生在实验中就产生了疑问: 一氧化碳是如何制取的?实验中所用的一氧化碳用什么仪器储存?此装置能否持续稳定地给反应提供一氧化碳?……
学生通过查阅资料,知道实验室制取一氧化碳的反应药品是甲酸和浓硫酸[4]。其反应原理是:
HCOOH浓H2SO480—90℃CO↑+H2O
根据反应物的状态和反应条件,可以选择“液液加热型”发生装置。该反应所需温度不高,可选择水浴加热来代替酒精灯直接加热,优点是受热面积大,比较稳定安全。学生设计了如图3所示的气体发生和收集装置。
所用仪器: 铁架台、分液漏斗、圆底烧瓶、温度计、双孔塞、导气管、T型管、弹簧夹、水槽、集气瓶、烧杯。
操作: 组装仪器,检查装置的气密性;向圆底烧瓶中加入适量浓硫酸,用水浴给浓硫酸加热,从分液漏斗中滴加甲酸;打开弹簧夹a,用排水法收集一小试管气体,检验纯度,待气体纯净后,打开止水夹b,关闭止水夹a,收集气体。
该实验中有以下几个改进点:
(1) 一氧化碳吹肥皂泡,检验气体的纯度。
有几个兴趣小组借用前面探究氢气可燃性时所采用的检验方法: 将气体通入肥皂水中产生大量的肥皂泡,再用火柴点燃肥皂泡。刚开始听到尖锐的爆鸣声,说明气体不纯,后面听到“噗”的声音,然后安静地燃烧,说明一氧化碳比较纯净了。
此方法改变传统的验纯方法,使实验趣味性增强了,既节约了药品,又提高了实验的可视性与安全系数。
(2) 一氧化碳的收集与排出。
一氧化碳的收集及实验中怎样将一氧化碳排出,一直是学生热烈讨论的焦点问题。
有学生建议直接将发生装置连入教材所示装置(见图1)中进行实验,但很多学生提出了质疑: 一是装置仪器多,不便于携带,在每个班进行实验时都要重新组装、检查气密性等,比较浪费时间;二是所用的药品浓硫酸有强烈的腐蚀性,甲酸也易挥发,携带使用时存在安全隐患。
有学生设计了如图3所示的方法: 先收集一瓶一氧化碳气体,实验时再从长管中慢慢注入水,将一氧化碳排入反应装置中。此方法的问题在于若是实验室中有水龙头,此法操作还算方便;若是在教室(无水龙头)中进行演示,
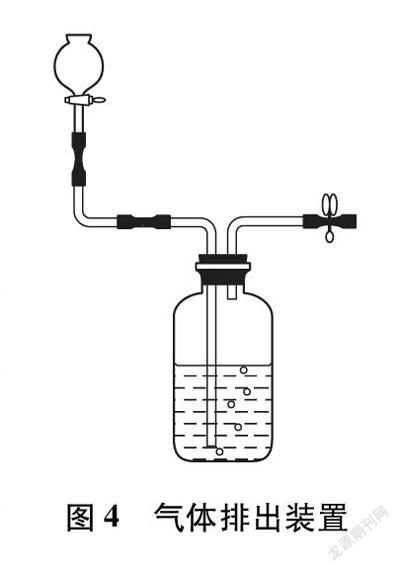
用水排出的方法就显得不易操作,也不易控制水速。有学生建议在长管上连一个分液漏斗(如图4所示),通过控制水的滴加速率来控制排出一氧化碳气体的速率。不过虽然方便了实验,但实验中又多了一个固定装置,还需有专人负责加水,反应时间较长,显然不太合适,还需作进一步优化。
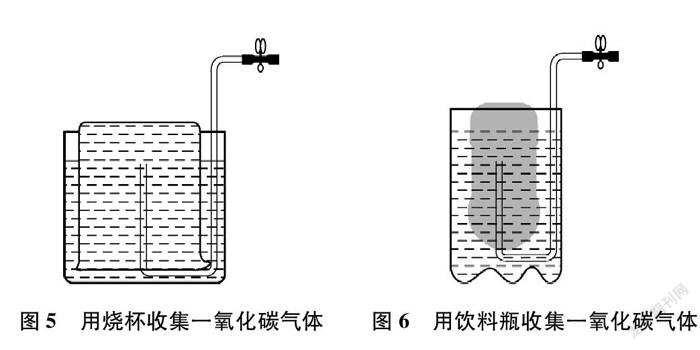
有学生通过反复实验又提出了一个新方法: 用烧杯收集一氧化碳(如图5所示)。将两个容积相近的烧杯倒扣并装满水,先用排水法收集一氧化碳。因两个烧杯容积相近,里面的烧杯收集气体后不会侧翻。使用时,因烧杯重力作用,会慢慢地将气体排入反应装置中;又因为浮力存在,烧杯不会下降太快,保证了气体排出的速率。此装置的改进,克服了图4装置的不足,既便于携带,装配简单,增强了实验的可视性,又始终处于液封状态,保证了装置的气密性。
还有学生受此装置的启发,改用两个矿泉水瓶(如图6所示)收集一氧化碳气体,改进后的装置更加容易装配,且轻便易携带。将废旧物品引入实验,体现了实验绿色化的理念。
(3) 一氧化碳气体的干燥。
在实验过程中,学生发现硬质玻璃管中有水雾,这是一氧化碳气体没有干燥的缘故。学生讨论决定,在一氧化碳进入反应装置前需作干燥处理,但需要什么干燥剂时,学生展开了讨论。
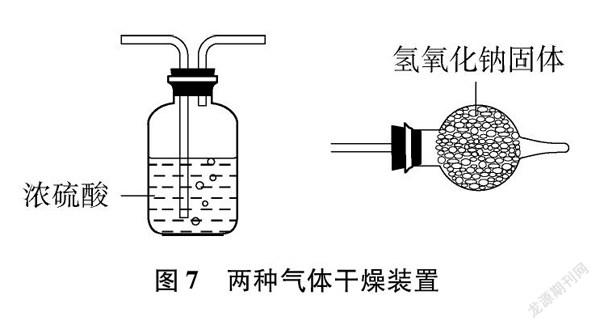
初中阶段常见的干燥剂有浓硫酸和氢氧化钠固体。一氧化碳是一种不成盐氧化物,既不和浓硫酸反应,也不与氢氧化钠反应,所以两种干燥剂都可用。若用浓硫酸做干燥剂,采用的是洗气瓶,若用氢氧化钠做干燥剂,采用的是干燥管(如图7所示)。两套装置各有利弊: 用浓硫酸来干燥气体,可以通过观察气泡快慢得知一氧化碳的产生速率,洗气瓶能放置在实验台上,不用固定;用氢氧化钠做干燥剂便于携带,但需要多一个铁架台来固定。
2 何时知道装置中的空气排净
实验前要先通入一氧化碳,排净装置中的空气,防止加热时发生爆炸,但是如何知道装置中的空气排干净了呢?
部分学生采用类似氢气验纯的方法: 在装置末尾连接一导气管,用排水法收集一小试管气体,用拇指堵住试管口,移向酒精灯火焰处进行检验,如果听到尖锐的爆鸣声则证明没有排净,如果听到“噗”的一声,则证明排干净了。此方法容易想到,也便于学生理解,但是整个过程中缺乏直观感知,存在猜的成分,需要多次检验,比较浪费时间,若操作不当,还会产生误判,造成危险。
有学生根据前面学习测定空气成分的实验,提出可以用“水量法”测出实验装置中硬质玻璃管的容积,然后粗略估算导气管的容积。用“水量法”找出集气瓶相应容积的位置,套上一个彩色橡皮筋作为标记(如图8所示)[5]。实验开始时,打开弹簧夹,一氧化碳缓缓地进入反应装置,集气瓶中的水位逐渐下降,当液面下降到刻度线时,说明装置中的空气已基本排净,可以点燃酒精喷灯进行加热。
部分学生为了对产生的气体进行检验,将集气瓶中的水换成了澄清石灰水,实验中可以明显地看到石灰水变浑浊。因为氢氧化钙微溶于水,吸收二氧化碳的能力较弱,学生为了将混合气体除杂并回收一氧化碳气体,将集气瓶中的溶液又换成氢氧化钠和氢氧化钙的混合溶液,既看到了明顯的现象,又进行了尾气处理。
应注意此装置中进气管要略短于排液管,防止气泡进入排液管,为了让气体中的二氧化碳充分吸收,进气管也不能过短,应尽可能地靠近集气瓶底部。
装置改进后既可以直观地显示装置中的空气是否排净,又可以检验并吸收产生的二氧化碳气体,还能收集未反应的一氧化碳气体,实现尾气处理。实验结束后,还可以将这部分气体导入储气装置中实现循环使用,从而节约药品。
3 为什么要冷却到室温才停止通入CO
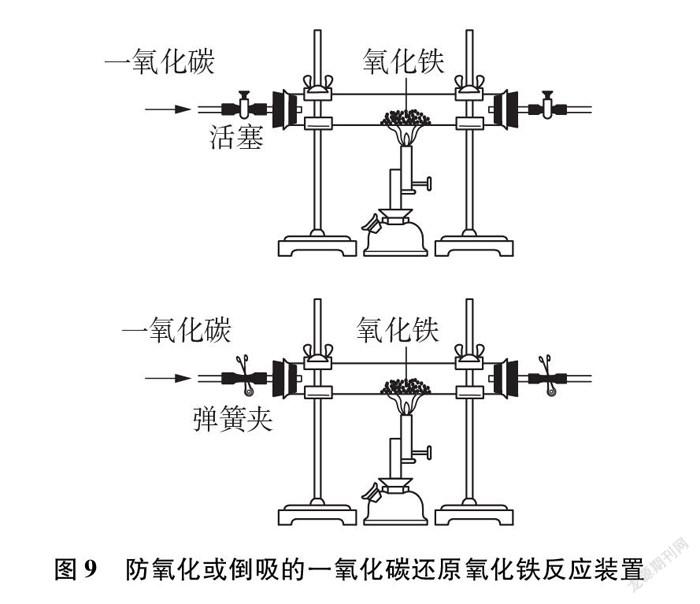
教材所示的实验中,反应结束后应继续通入CO直到冷却到室温。很多资料给出的解释是防止灼热的Fe被氧气氧化。有的学生提出了疑问: 装置拆开了,会有氧气进入,若没有拆开哪来的氧气呢?用图1装置时,熄灭酒精喷灯后,继续通入一氧化碳,作用不应该仅仅是防止铁被氧化?可以设想,若装置未拆开,熄灭了酒精喷灯,反应装置的温度降低,压强会减小,澄清石灰水会倒吸到硬质玻璃管中,所以继续通入一氧化碳应该还起到防止水倒吸的作用!
学生经过讨论和分析,又对装置进行了改进(见图9): 一部分学生在反应装置的两端,分别加上一个活塞;还有一些学生在反应装置两端分别连接一小段橡胶管,夹上弹簧夹。反应结束后,关闭两端的活塞或夹上弹簧夹,停止通入一氧化碳,冷却到室温后,经过检验,发现铁粉没有被氧化,还有效防止了水倒吸。这样的改进既节约药品、节省能源,又增加了实验的安全性和可靠性。
4 结束语
每一个化学实验的设计,总会有一些潜在的问题。教学中,应引导学生在实验中随时发现问题、分析问题,进而解决问题。一氧化碳还原氧化铁实验中学生所提出的几个问题的探究和解决,培养了学生大胆质疑的科学精神;对实验装置的改进,培养了学生的实验创新能力;通过挖掘实验教学的育人价值,提升了学生的化学素养。改进后的实验装置安全、方便、可视性强,绿色环保理念渗透其中,有效降低了课前准备的负担,解决了该实验在课堂教学中的难题,并成功地将一般的演示实验推广为学生分组实验,促进了化学实验教学的真正落实。
参考文献:
[1][2]卢巍. 鲁教版化学九年级教师教学用书[M]. 济南: 山东教育出版社, 2019: 145~150.
[3]毕华林, 卢巍. 义务教育教科书·化学(八年级全一册)[M]. 济南: 山东教育出版社, 2019: 9~13.
[4]吴晓颖, 王振, 张明月. 一氧化碳还原氧化铁实验的改进[J]. 化学教学, 2020, (3): 72~75.
[5]马逸群, 张晓敏. “CO还原氧化铁实验”改进装置的优化[J]. 实验教学与仪器, 2020, (7/8): 49~50.
