三维超声斑点追踪成像预测急性心肌梗死患者介入术后主要心脏不良事件的价值
2022-06-06程建中王佩佩周海霞刘学森
程建中,王佩佩,周海霞,闫 卫,张 娜,刘学森
1)驻马店市中心医院超声科 河南驻马店 463000 2)郑州大学第一附属医院超声科 郑州 450052 3)驻马店市中心医院心血管内科 河南驻马店 463000
急性心肌梗死(acute myocardial infarction,AMI)是冠状动脉粥样硬化严重狭窄性疾病,有较高的致死率。经皮冠状动脉介入(percutaneous coronary intervention,PCI)具有创伤小、效果确切的优点,是治疗AMI的主要方法。但有研究[1]显示,PCI术后部分患者仍不可避免地出现节段性心肌运动障碍,是主要心脏不良事件(major adverse cardiac events,MACEs)发生的主要原因。因此,准确测量AMI患者心肌舒缩功能以及整体运动协调性对评估心室重构进程,预测预后具有十分重要的意义。研究[2-3]显示,三维超声斑点追踪成像(three dimensional speckle tracking imaging,3D-STI)在2D-STI基础上实现了实时、连续性心脏全容积成像,在三维立体结构中能够更加真实、准确测量心脏整体和局部心肌运动情况,更加客观反映AMI靶血管缺血导致的区域性支配心肌运动障碍;同时具有无创性、重复性好、变异性小等优点,已经在冠心病[4]、心肌病[5]、心脏再同步化治疗[6]、心力衰竭[7]等多个领域有重要应用。该研究主要评价3D-STI预测AMI患者PCI术后MACEs的价值。
1 对象与方法
1.1 研究对象选择2019年1月至2020年5月在驻马店市中心医院首次确诊为AMI、接受PCI治疗的患者作为研究对象。纳入标准:①年龄大于18岁。②符合AMI诊断标准,有PCI应用指征,根据指南推荐进行药物和PCI治疗。③在患者康复出院前(PCI术后5~7 d)完成常规超声和3D-STI检查。④取得患者知情同意,临床和随访资料完整。排除标准:①合并先天性心脏病、心肌病、心肌炎,出院前已经诊断心力衰竭。②严重肝肾功能障碍。③出院后未按医嘱要求继续药物治疗。④合并恶性肿瘤、自身免疫性疾病、营养代谢性疾病。该研究获医学伦理委员会批准。该研究采用临床前瞻性横断面观察法,最终筛选符合纳排标准的124例患者完成治疗和随访,住院期间根据病情特点和指南推荐进行合理的药物和PCI治疗,出院前评估心脏功能,制定个性化心脏康复策略,指导定期复查。
1.2 3D-STI检查患者出院前采用GE Vivid E95型多功能彩色多普勒超声诊断仪,线性探头频率为4~6 MHz,首先经胸二维模式测量心室、心房、室间隔大小以及心脏瓣膜是否返流等,以左心室为测量重点,采用双平面Simpson法测量左室射血分数(left ventricular ejection fraction,LVEF)和左室舒张末容积(left ventricular end diastolic volume,LVEDV)。结束后切换至三维模式,更换为V5矩阵探头,调整各项参数并开启谐波至最优化模式,保证三维图像高清状态;选取心尖四腔切面,帧频>24帧/s,指导患者呼气后屏住呼吸,立即启动4D模式,连续采集4个心动周期的三维动态图像。保存图像后脱机状态下使用三维应变斑点追踪分析软件,手动或者自动勾画左心室内外膜曲线,调整心内膜边缘曲线、感兴趣区域的宽度以及3个平面的间距,与室壁厚度一致,确保回声斑点在心肌内,运行程序自动计算左心室心肌整体纵向峰值应变(global longitudinal peak strain,GLS)、环向峰值应变(global circumferential peak strain,GCS)、径向峰值应变(global radial peak strain,GRS)、面积应变(global area strain,GAS)、旋转和扭转角度[8]。每例患者分别由两名经验丰富的超声科医师独立完成检查,结果取均值。
1.3 血浆N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)水平测定出院前采用放射免疫法检测血浆NT-proBNP水平,试剂盒购自美国Sigma公司,根据说明书步骤进行。
1.4 随访出院后常规随访1 a,根据是否发生MACEs将其分为MACEs组和无MACEs组。其中MACEs定义为新发心力衰竭、再发心肌梗死、靶血管重建以及心源性死亡[3]。
1.5 统计学处理采用SPSS 20.0处理数据。采用两独立样本t检验或χ2检验比较MACEs组和无MACEs组患者一般及临床资料的差异;采用Pearson相关分析GLS、GCS、GRS和GAS与LVEF、NT-proBNP水平的关系。采用ROC曲线分析GLS、GCS、GRS和GAS单独预测MACEs的效能。检验水准α=0.05。
2 结果
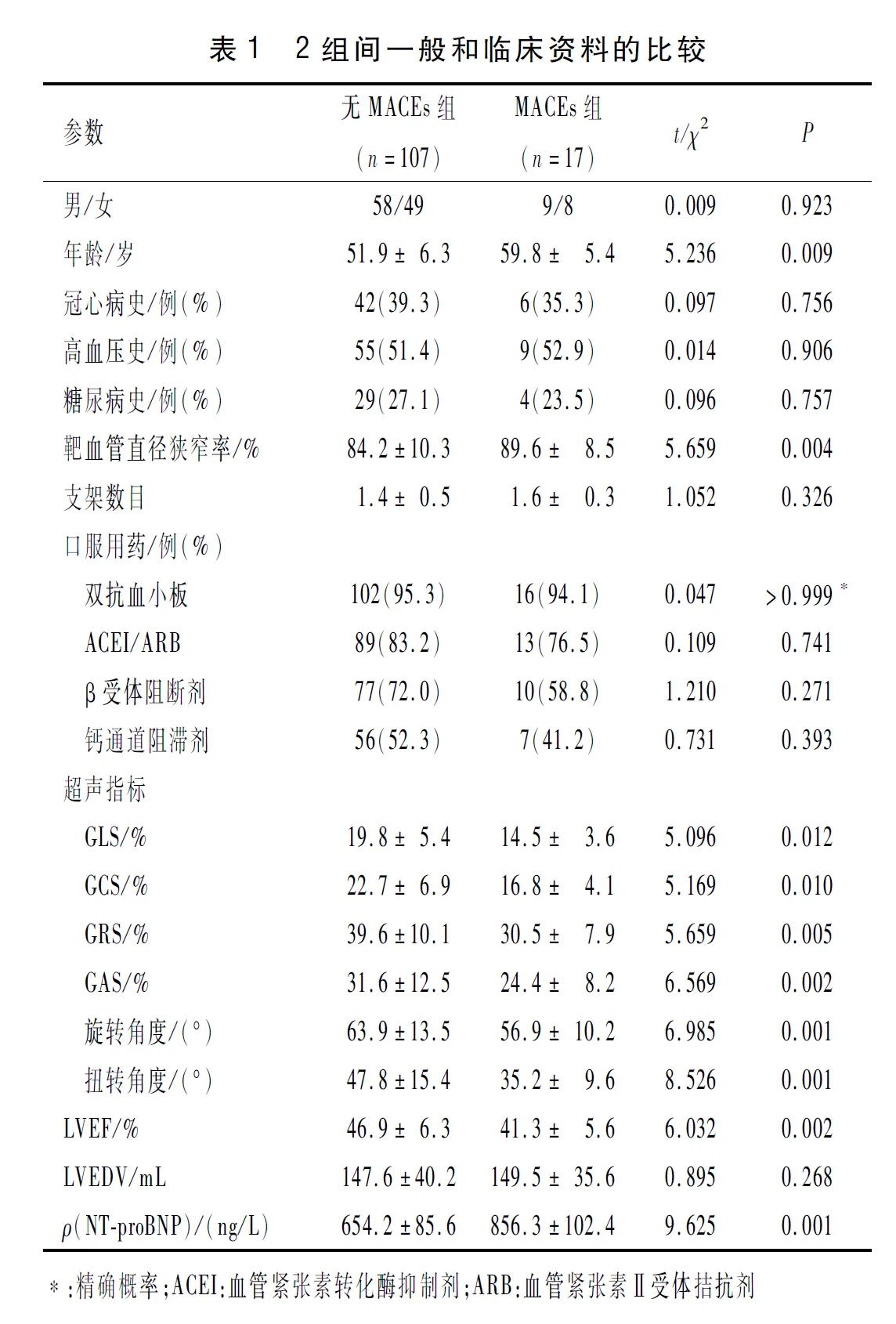
2.1 MACEs和无MACEs患者一般和临床资料的比较17例发生MACEs,其中新发心力衰竭7例,再发心肌梗死3例,靶血管重建6例,心源性死亡1例。与无MACEs组相比,MACEs组患者年龄较高,靶血管直径狭窄率更高,GLS、GCS、GRS、GAS、旋转和扭转角度降低,LVEF降低,血浆NT-proBNP水平升高(P<0.05),见表1。
2.2 相关性分析Pearson检验显示,GLS、GCS、GRS和GAS与LVEF呈正相关,与NT-proBNP水平呈负相关(P<0.05),见表2。

表2 相关性分析(n=124)
2.3 GLS、GCS、GRS和GAS对MACEs的预测效能ROC分析显示,GLS、GCS、GRS和GAS单独预测MACEs均有较高应用价值(P<0.05),见表3。

3 讨论
研究[8]已经证实,AMI主要导致供血功能支配区域的心肌节段性运动障碍。常规超声仅能整体测量心腔大小和运动是否协调,而3D-STI则可以通过心肌运动的斑点回声进行重建,在三维空间再现心肌的运动轨迹[9]。心脏内外膜心肌的不同排列方式决定了心脏的运动形式,最终量化为GLS、GCS、GRS、GAS、旋转和扭转6种指标,较全面反映了心肌运动与心脏舒缩功能的关系[10-11]。
该研究显示,与无MACEs患者相比,MACEs患者年龄更高、靶血管直径狭窄率升高,术后GLS、GCS、GRS、GAS、旋转和扭转角度降低,LVEF值降低,血浆NT-proBNP水平升高。Bastawy等[12]指出,早期AMI PCI术后GLS和左室扭转是前壁心肌梗死后左室重构的独立预测指标,可用于预测6个月后左室重构的发生;并且提出GLS最佳临界值>12.5(敏感度87%,特异度85%)和左室扭转的最佳临界值<9.5°(敏感度91%,特异度85%)。正常心脏收缩期GLS为负值,表示心肌在长轴上缩短;GCS为负值,表示心室在短轴切面上周长减小;GRS为正值,表示室壁增厚;GAS表示心内膜表面积的变化率[13]。多项研究[14-15]发现,心肌缺血导致局部心肌舒缩能力下降,表现为GLS、GCS、GRS、GAS、旋转和扭转角度降低,经血运重建后可恢复部分心肌运动能力,表现为GLS、GCS、GRS、GAS、旋转和扭转角度增加,但与健康群体相比可能仍然存在较大差异。
Pearson相关分析显示,GLS、GCS、GRS和GAS与LVEF呈正相关,与NT-proBNP水平呈负相关。LVEF和NT-proBNP是目前评估心室舒缩功能和临床预后的主要客观指标,具有较好的准确性。研究[16-17]发现,冠心病的不同阶段,心肌的累及范围也有所不同,早期主要集中在心内膜,以GLS降低居多;中晚期主要集中在中层和心外膜,以GCS和GRS降低居多。ROC曲线分析显示,GLS、GCS、GRS和GAS值在预测PCI术后MACEs发生方面具有较好的效能,为指导临床早期识别预后不良患者提供了参考。
综上所述,3D-STI作为评估心脏整体和局部舒缩功能的新技术,对AMI患者PCI术后MACEs的发生有较高的预测效能,其中GLS、GCS、GRS和GAS有望成为指导临床早期评估预后不良的辅助指标。当然,3D-STI还有一定的局限性,如需要患者屏气和有规律的心律来实现ECG门控图像采集;与三维应变参数有关的测量值、正常值和截断值高度依赖于所使用的三维超声设备,可能导致不同研究结果之间存在一定偏差。但是,我们相信随着分辨率的提高以及三维应变测量标准化技术的进步,3D-STI有望在临床和研究领域得到广泛应用。
