包埋提高异常威克汉姆酵母醛脱氢酶的稳定性
2022-06-02倪育军徐莉娜郭薇丹
陈 耕 倪育军 钟 敏 徐莉娜 郭薇丹
(1. 湖南省产商品评审中心,湖南 长沙 410111;2. 湘潭市食品药品检验所,湖南 湘潭 411101;3. 中南林业科技大学食品科学与工程学院,湖南 长沙 410004)
研究[1-3]表明,食品中的不饱和醛对人体健康有负面影响。例如,食品中的糖基化反应、蛋白质氧化和脂肪氧化所产生的丙酮醛与一些口腔疾病如牙周病有关[4];二羰基醛类化合物与慢性糖尿病有关[5];丙烯醛、巴豆醛可诱导基因突变以及抑制DNA修复[6]。醛脱氢酶(ALDH,EC l.2.1)是一种可催化内源和外源性醛类化合物脱氢的胞内酶[7],常用于消减食品中的不饱和醛从而减轻因摄入不饱和醛而给机体带来的危害。目前,ALDH主要来源于动物肝脏,存在稳定性差、成本高、催化效率低等问题[8],因此其应用受到限制。大量微生物具有较高的ALDH活性,如酵母[8-9]、醋酸菌[10]、乳酸菌[11]以及深海细菌[12],利用微生物提取ALDH并采用固定化的方式来稳定酶活是一种有效解决上述问题的方法。付湘晋[13]研究发现,用葡萄酒酵母细胞处理鱼糜2 h后,鱼糜中丙二醛含量下降了70%,2,4-庚-二烯醛和2,4-癸-二烯醛的含量低于检出限。刘薇丛[14]从传统发酵食品中筛选出的6株具有耐冷冻特性的异常威克汉姆酵母(Wickerhamomycesanomalus)菌株J3、J7、J8、J9、J12、J18可消减鱼肉中的脂肪氧化产物丙二醛,是潜在的鱼肉、肉类生物保鲜剂。研究拟测定上述6株(J3、J7、J8、J9、J12、J18)酵母菌株的ALDH活性,并采用海藻酸钠—氯化钙法对ALDH进行包埋,分析游离ALDH及包埋ALDH在冷藏、模拟胃肠道环境中的稳定性,以期为开发可用于消减胃肠道内活性醛的产品提供依据。
1 材料与方法
1.1 菌种
异常威克汉姆酵母(Wickerhamomycesanomalus)菌株J3、J7、J8、J9、J12、J18:中南林业科技大学食品科学与工程学院实验室。
1.2 材料与试剂
二硫苏糖醇:分析纯,上海如吉生物科技有限公司;
氯化钙、葡萄糖:分析纯,国药集团化学试剂有限公司;
NAD+:上海如吉生物科技有限公司;
海藻酸钠、蛋白胨、酵母浸粉、琼脂:国药集团化学试剂有限公司;
胃蛋白酶:1 200 U/g,国药集团化学试剂有限公司;
胰蛋白酶:500 U/g,国药集团化学试剂有限公司;
液体培养基:2%葡萄糖,2%蛋白胨,1%酵母浸粉;
固体培养基:在液体培养基的基础上加入2%琼脂。
1.3 仪器与设备
微生物培养箱:SPK-150BⅢ型,北京中兴伟业仪器有限公司;
立式自动压力蒸汽灭菌锅:G154DWS型,厦口致微仪器有限公司;
超净工作台:SW-CJ-IFD型,苏州安泰空气技术有限公司;
紫外可见分光光度计:BluestarB型,北京莱伯泰科仪器股份有限公司;
超声波细胞破碎仪:JY92-ⅡN型,宁波新芝有限公司;
离心机:TG25KR型,长沙东旺实验仪器有限公司。
1.4 方法
1.4.1 酵母菌活化和扩大培养 参照刘薇丛[14]的方法并稍作修改,将斜面培养基的酵母接种于液体培养基,在28 ℃,150 r/min条件下培养24 h进行活化,再以5%的接种量进行扩大培养得到酵母菌悬液。
1.4.2 酵母菌粗酶液制备与检测
(1) 酵母菌粗酶液制备:参照衣海龙[15]的方法并稍作修改,取1.4.1中培养好的菌液100 mL,在4 ℃下以8 000 r/min 离心15 min,弃上清液,并用0.05 mol/L、pH 8.0的磷酸钾缓冲溶液30 mL洗涤酵母菌细胞泥1次,然后在4 ℃下以10 000 r/min离心10 min 收集得到酵母泥。将湿酵母按m湿酵母∶m缓冲液=1∶30重悬浮于0.05 mol/L PBS (pH 8.0)缓冲液中,于冰水浴中超声波破碎。超声参数:超声功率300 W、超声时间7 s、间歇5 s、全程时间15 min。将细胞破碎物于4 ℃下以12 000 r/min 离心15 min,取上清液进行醛脱氢酶活性和蛋白浓度测定。
(2) 醛脱氢酶活性检测:参照Okibe等[16]的方法。酶活反应体系组成:2.52 mL Tris-HCl缓冲液(0.05 mol/L,pH 8.0)、0.1 mL 3 mol/L KCl溶液、0.1 mL 0.02 mol/L NAD+溶液、0.1 mL 0.05 mol/L EDTA溶液、0.03 mL 0.05 mol/L 二硫苏糖醇溶液、0.05 mL 0.1 mol/L乙醛溶液、0.1 mL粗酶液。酶活性测定体系和待测酶液分别在25 ℃下恒温水浴5 min,将待测酶液迅速加入酶活反应体系中混匀,立即放入分光光度计中,每隔l min读取340 nm 处的吸光度值,持续5 min。定义每分钟转化1 μmol 的底物所需酶量为一个酶活力单位(U)。
(3) 粗蛋白含量检测:参照万茵等[11]的方法。用缓冲液的吸光度作为空白值,分别测定蛋白溶液在260 nm及280 nm处的吸光度,按式(1)计算蛋白质质量浓度。
(1)
式中:
C——蛋白质质量浓度,mg/mL;
A280 nm——蛋白溶液在280 nm处的吸光度;
A260 nm——蛋白溶液在260 nm处的吸光度。
1.4.3 比活力计算 按式(2)计算比活力。
(2)
式中:
A——比活力,U/mg;
式(2)就是输送臂关节1,2的运动学方程,它表明了输送臂的末端在空间的位置和姿态。用4×1的位置向量表示为
E——酶活力,U;
P——蛋白质含量,mg。
1.4.4 酶的包埋 参照刘天龙[17]的海藻酸钠—氯化钙包埋法,将10 mL海藻酸钠溶液加热溶解,冷却后与5 mL 的游离酶液混合均匀,用一次性的注射器将海藻酸钠与酶液混合液匀速滴入氯化钙溶液中,形成大小均一的光滑颗粒,固化1 h后过滤取出,用蒸馏水洗涤,4 ℃下静置硬化2 h。
1.4.5 包埋酶的活性测定 称取1 g包埋酶的海藻酸钠—氯化钙颗粒,加入0.05 mol/L、pH 8.0的PBS缓冲液4 mL,充分碾磨,于4 ℃下以12 000 r/min离心15 min,取上清液0.1 mL按1.4.2中方法测定醛脱氢酶活性。
1.4.6 包埋酶冷藏稳定性 分别取包埋酶和游离酶保存于4 ℃冰箱中,连续5 d内每天定时定量取出测定两者的残余酶活。
1.4.7 包埋酶在模拟胃肠液中的酶活变化 参考万茵等[11]的方法制备模拟胃液、模拟肠液。
在模拟胃液中加入粗酶液或包埋酶,置于37 ℃、160 r/min 的摇床振180 min,于0,10,20,30,40,50,60,90,180 min 时,测定消化液中ALDH酶活。以未经消化的粗酶液和包埋酶活性视作100%酶活,计算酶活性保留率。
在模拟肠液中加入粗酶液或包埋酶,于0,10,20,30,40,50,60 min时测定ALDH酶活。以未经消化的粗酶液和包埋酶活性视作100%酶活,计算酶活性保留率。
1.5 数据统计与分析
所有试验均重复3次,结果用平均值±标准差表示,采用Excel软件进行数据统计、绘图,采用SPSS软件进行数据分析。
2 结果与分析
2.1 异常威克汉姆酵母菌ALDH活性
6株W.anomalus菌株J3、J7、J8、J9、J12、J18的ALDH酶测定结果见图1。J9的比活力[(482.14±14.62) U/mg]显著高于其他5株的,选用酶活最高的J9进行后续试验。9号菌株与干酵母0.465 U/mg[8]、酿酒酵母120 U/mg[9]、醋酸菌20.25 U/mg[10]、醋化醋杆菌0.893 U/mL[18]、深海细菌52.44 U/mg[12]相比也具有明显的优势。
2.2 海藻酸钠添加量对ALDH酶活性的影响
设定氯化钙的添加量为3%(质量分数),分别与2.0%,2.5%,3.0%,3.5%,4.0%的海藻酸钠对ALDH酶进行包埋,得到的酶活见图2。
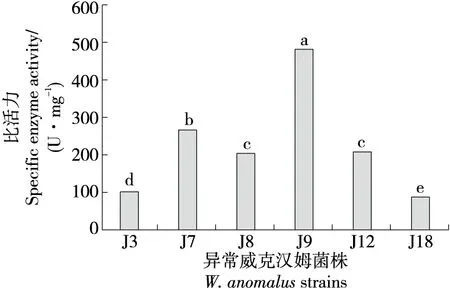
小写字母不同表示差异显著(P<0.05)图1 6株异常威克汉姆酵母ALDH活性Figure 1 ALDH activity of 6 Wickerhamomyces anomalus strains

小写字母不同表示差异显著(P<0.05)图2 海藻酸钠添加量对包埋酶酶活的影响Figure 2 Effect of sodium alginate concentration on enzyme activity
由图2可知,当海藻酸钠添加量为3%时,包埋效果显著高于其他添加量的。随着海藻酸钠添加量的增加,包埋酶酶活呈上升趋势,当海藻酸钠添加量高于3.0%时,随着海藻酸钠添加量的增加,酶活呈下降趋势。可能是因为海藻酸钠含量较低时包埋的凝胶结构不够紧密导致包埋率低,随着海藻酸钠含量的增加,形成的凝胶强度增加,内部结构更加稳定从而提高了包埋率。但是高含量的海藻酸钠形成的凝胶强度过大,硬度上升,导致注射器挤压出的颗粒呈不规则的圆形并有拖尾的现象,影响了酶的包埋和释放效果从而影响酶活[19]。
2.3 氯化钙添加量对ALDH酶活性的影响
设定海藻酸钠添加量为3.0%,分别与2.0%,2.5%,3.0%,3.5%,4.0%的氯化钙对ALDH酶进行包埋,得到的酶活见图3。由图3可知,不同氯化钙添加量下的包埋酶酶活差异显著。其中,添加3.0%的氯化钙包埋效果显著优于其他添加量的。随着氯化钙添加量的增加,包埋效果提高,当氯化钙添加量高于3.0%时,包埋效果下降。可能是低含量的氯化钙与海藻酸钠形成的海藻酸钙凝胶强度较小,会导致酶流失[12]。氯化钙添加量过高可能使海藻酸钙凝胶的内部网状结构发生变化,从而影响底物分子与酶分子的相互结合与作用,使酶活受到影响[19]。

小写字母不同表示差异显著(P<0.05)图3 氯化钙添加量对包埋酶酶活的影响Figure 3 Effect of calcium chloride concentration on enzyme activity
2.4 包埋酶的冷藏稳定性
由图4可知,未进行包埋的游离酶在5 d内相对酶活下降至44.13%,而包埋酶的相对酶活仅下降了6.69%,游离酶的酶活下降速率明显快于包埋酶的,说明用海藻酸钠和氯化钙进行包埋对酶起到了较好的保护效果。

图4 游离酶与包埋酶稳定性的比较Figure 4 Comparison of the stability of free enzyme and embedding enzyme
2.5 模拟胃肠道环境下酶活变化
未进行包埋的游离酶经胃液消化10 min后已检测不出酶活,说明该酶在胃液环境中极不稳定。而利用海藻酸钠与氯化钙进行包埋后的酶在模拟胃液消化环境下表现出较好的稳定性,包埋酶经胃液消化3 h后,酶活仍然保留了56.39%(图5)。在模拟肠液消化环境下,包埋酶在前30 min表现出良好的稳定性,相对酶活保持在90%以上,之后酶活下降速度加快,降至60%以下(图6),与万茵等[11]的研究结果一致。可能是因为海藻酸钙颗粒的结构受到了破坏,导致内部包埋的酶渗出,但是酶活仍然被较好保留,说明海藻酸钠与氯化钙的包埋起到了较好的保护效果,有效增加了ALDH在胃肠道环境下的稳定性。

图5 包埋酶在模拟胃液消化环境下的酶活变化Figure 5 Enzyme activity changes of embedding enzymes in simulated gastric juice digestion
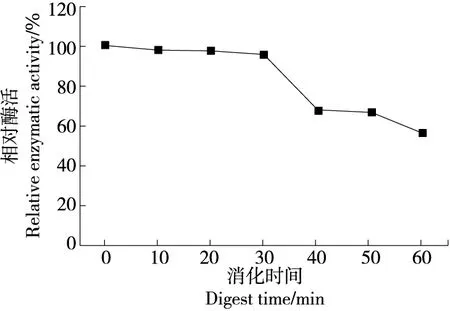
图6 包埋酶在模拟肠液消化环境下的酶活变化Figure 6 Enzyme ativity changes of embedding enzyme in simulated intestinal juice dig
3 结论
对6株W.anomalus酵母的ALDH酶活进行测定,发现J9酵母菌株的ALDH酶活最高。选取J9作为研究对象,优化ALDH酶包埋工艺,最终结果显示3.0%海藻酸钠与3.0%氯化钙的包埋效果最佳,包埋酶在冷藏及在胃肠道环境下有很好的稳定性。可促进酵母菌醛脱氢酶在食品领域的广泛应用,对于降低加工类食品中的一些有害醛类从而降低食品中的风险具有深远意义。后续可进一步研究ALDH酶体内活性及清除活性醛的效果。
